Введение
Несмотря на то, что 5 мая 2023 г. Всемирная организация здравоохранения (ВОЗ) отменила глобальную чрезвычайную ситуацию, связанную с пандемией COVID-19, последствия ее до сих пор оказывают влияние на многие аспекты жизни населения планеты. По обновленным данным ВОЗ, с 5 января 2020 г. по март 2025 г. было зарегистрировано 777 637 340 случаев заболевания COVID-19, в том числе 70 90 480 смертельных случаев1.
С момента начала пандемии COVID-19 разработка вакцин стала ключевой стратегией в борьбе с распространением вируса и его осложнениями. С начала пандемии 174 вакцины были на стадии доклинических испытаний, лишь 64 из них — на стадии клинических испытаний (по состоянию на 20 января 2021 г.). Первым препаратом, одобренным ВОЗ уже 31 декабря 2020 г., стала вакцина тозинамеран (Pfizer-BioNTech, США) [1].
На сегодняшний день проведено множество исследований по изучению эффективности вакцин против COVID-19, их влияния на заболеваемость, предотвращения тяжелых форм заболевания и возможных долгосрочных последствий.
Основная причина летального исхода при COVID-19 — тяжелый острый респираторный синдром (ТОРС), с этиологическим агентом Severe acute respiratory syndrome-related coronavirus-2 (SARS-CoV-2), вызывающим атипичную инфекцию, при котором главным клиническим признаком является лихорадка с последующим развитием пневмонии2.
Вакцинация показала высокую эффективность в предотвращении не только самой инфекции COVID-19, но и ее тяжелых форм, включая ТОРС. Исследование HDR UK COALESCE Consortium [2], в котором анализировалась вероятность развития тяжелых форм коронавирусной инфекции среди населения Великобритании, подтвердило, что вакцинированные пациенты реже переносят тяжелые формы COVID-19, что снижает частоту госпитализации и смертности. Безусловно, определенную роль играли социально-экономические факторы, момент введения (до заболевания или во время заболевания) компонентов вакцин, однако решающую роль играл сам факт вакцинации.
Особенно важен бустерный эффект вакцин, позволяющий поддерживать уровень антител на высоком уровне в течение длительного срока. Наиболее высокую эффективность продемонстрировали вакцины на основе мРНК, такие как тозинамеран (Pfizer-BioNTech, США) и Spikevax (Moderna, США), которые обеспечивают до 95% защиты при корректном введении двух доз с последующим бустером. мРНК инкапсулирована в липидные наночастицы, которые после проникновения в организм активно выделяют антиген-мишень в клетки организма человека, на основе мРНК синтезируется Spike-белок, ответственный за образование шипов на оболочке вируса. С помощью антигенпрезентирующих клеток происходит представление этого антигена (Spike-белка) T-helper (Th) 0, дифференцирующимся в Th2. Th2 обеспечивают активацию B-лимфоцитов, становящихся плазматическими клетками и синтезирующими защитные антитела (IgM, IgG) [3].
Бустерный эффект заключается в усилении активирования Т- и В-лимфоцитов для восстановления иммунной защиты, которая уже не является эффективной. Происходит воздействие иммунизирующего антигена после первоначальной иммунизации. Это отличает их от других вакцин, у которых стимулирование иммунного ответа медленнее. На данный момент к этой группе относятся тозинамеран (Pfizer-BioNTech, США), Spikevax (Moderna, США), Oxford/AstraZeneca (Великобритания, Швеция), вакцина для профилактики новой коронавирусной инфекции (COVID-19) (Россия), VeroCell (Sinopharm, Китай) и BBV152 (Covaxin, Индия) [4]. Таким образом, целью исследования стал сравнительный анализ вышеуказанных вакцин, а также CoronaVac (Sinovac Biotech Ltd, Китай); вакцины для профилактики COVID-19 (ЭпиВакКорона, Россия) и вакцины для профилактики COVID-19 (КовиВак, Россия).
Содержание статьи
Влияние вакцинации на риск развития постковидных осложнений
Для обозначения отсроченных эффектов заболевания был введен термин long COVID, который определяет состояние в течение 14–110 дней после перенесенного заболевания. Наиболее распространенными симптомами long COVID являются усталость (58%), головная боль (44%), нарушение внимания (27%), выпадение волос (25%) и одышка (24%) [5].
Впервые об эффекте вакцинации по отношению к long COVID начали говорить в 2022 г. P. Gao et al. [6] сообщают, что вероятность развития постковидного синдрома у вакцинированных пациентов по сравнению с контрольной группой на 29% ниже. По результатам исследования L. Lundberg-Morris et al. [7], частота выявленного long COVID в вакцинированной группе составила 0,4% по сравнению с 1,4% среди лиц без вакцинации.
Также A. Watanabe et al. [8] указывают, что двухкомпонентная вакцинация до инфицирования вирусом SARS-CoV-2 связана с более низким риском развития таких симптомов long COVID, как длительная усталость, одышка, по сравнению с невакцинированными пациентами. Среди пациентов, прошедших вакцинацию уже после инфицирования вирусом, 20,3% отмечали улучшение симптомов long COVID в течение 2 нед. — 6 мес. после вакцинации. Однако в данном случае невозможно утверждать, что положительная динамика связана именно с вакцинацией, а не с регрессом симптоматики по прошествии времени.
Вопрос профилактики постковидного синдрома при помощи вакцинации остается предметом активных исследований. В метаанализе A.R. Marra et al. [9] были оценены данные различных исследований, демонстрирующие, что пациенты, получившие полную серию вакцинации, реже сталкиваются с долгосрочными последствиями инфекции. Таким образом, вакцинация приводит как к снижению риска инфицирования вирусом, так и к более быстрому регрессу симптомов long COVID. Эта информация особенно важна для врачей и пациентов, так как постковидные осложнения могут существенно повлиять на качество жизни пациентов. Кроме того, исследование Multidisciplinary Digital Publishing Institute (MDPI) описывает необходимость наблюдения за пациентами, перенесшими COVID-19, особенно с ослабленным иммунитетом, и подчеркивает роль вакцинации в улучшении качества их жизни после выздоровления. Таким образом, эти выводы доказывают безопасность применения вакцин на основе мРНК для иммунокомпрометированных пациентов в плане предотвращения не только первичного инфицирования, но и возможных долговременных последствий [10].
Сравнительная эффективность различных вакцин
Различные типы вакцин, такие как мРНК-вакцины, векторные вакцины и инактивированные вакцины, имеют разную эффективность и профиль безопасности. При сравнении эффективности мРНК-вакцин (тозинамеран (Pfizer-BioNTech, США) и Spikevax (Moderna, США)) с векторными вакцинами (AstraZeneca) обнаружен более высокий уровень антител и продолжительная защита у пациентов, привитых мРНК-вакцинами, особенно при применении бустерных доз [10] (табл. 1)3.
![Таблица 1. Классификация вакцин от COVID-19 [11] Таблица 1. Классификация вакцин от COVID-19 [11]](https://medblog.su/wp-content/uploads/2025/04/Effektivnost-i-bezopasnost-vaktsin-protiv-COVID-19-sravnitelnyj-analiz-Reznik.png)
A. Watanabe et al. [8] уделяют особое внимание бустерным дозам мРНК-вакцин, таким как тозинамеран (Pfizer-BioNTech, США) и Spikevax (Moderna, США), и их способности поддерживать иммунную защиту у пациентов. Авторы отмечают, что с течением времени уровень антител может снижаться, однако повторные дозы вакцин значительно усиливают иммунный ответ, обеспечивая более эффективную защиту от новых штаммов вируса.
Исследование показало, что введение бустера в значительной степени повышает защиту от тяжелых форм COVID-19, снижает частоту госпитализаций и обеспечивает стойкий иммунный ответ даже к мутантным формам вируса. Таким образом, пациентам уязвимых групп (пожилые, с хроническими заболеваниями) предпочтительнее вводить бустерные дозы. Исследователи также акцентируют внимание на снижении риска осложнений у вакцинированных, что подтверждает ценность вакцинации как меры не только для предотвращения инфицирования, но и для смягчения потенциальных долгосрочных последствий [12].
Вакцинация пациентов с коморбидными состояниями и уязвимых групп населения
Пациенты с хроническими заболеваниями и люди пожилого возраста особенно подвержены риску тяжелых форм COVID-19, а вакцинация для них становится критически важной мерой профилактики. В исследовании BioMed Central Infectious Diseases изучалось влияние вакцинации на пациентов с коморбидными состояниями [13]. Описаны результаты нескольких исследований эффективности вакцинации у пациентов с сахарным диабетом (СД): S. Dispinseri et al. [14] сообщают о том, что наличие СД 2 типа никак не влияет на формирование иммунного ответа, в то же время, согласно данным I. Yelin et al. [15], СД 2 типа в анамнезе может снижать эффективность вакцины. В России исследований по охвату вакцинацией пациентов с СД не проводилось. По данным H. Li et al. [16], в Китае более 83% больных СД получили минимум 1 дозу вакцины, более 65% прошли ревакцинацию, эти данные подтверждают, что в группе пациентов с коморбидной патологией рекомендовано проводить вакцинацию, которая не только предотвращает тяжелые формы заболевания, но и снижает частоту госпитализаций и необходимость в интенсивной терапии.
Группой риска по развитию вторичных осложнений и тяжелого течения коронавирусной инфекции являются пациенты с вирусом иммунодефицита человека (ВИЧ). В этой группе пациентов наблюдался достаточно низкий охват вакцинацией — 71% по всему миру в 2022 г. Поэтому большое значение имеет пропаганда необходимости вакцинации для предотвращения возможных неблагоприятных исходов [17].
Нежелательные реакции и безопасность вакцин против COVID-19
Несмотря на высокую эффективность, вакцины против COVID-19 связаны с некоторыми нежелательными реакциями, что требует постоянного мониторинга и оценки их безопасности. К группе осложнений легкой и средней степени тяжести, по данным K.S. Medeiros et al. [1], относят местные воспалительные реакции при введении препарата, лихорадку, мышечные боли, головные боли и усталость.
Миокардит, ассоциированный с вакцинацией, встречается достаточно редко: 2,7 на 100 000 человек в Израиле, 1,4 на 100 000 человек в Дании [18]. В 2021 г. было описано 62 случая тромбоза церебрального венозного синуса и 24 случая тромбоза висцеральных вен у пациентов после вакцинации Oxford/AstraZeneca4. К более редким осложнениям относят развитие синдрома Гийена — Барре (60 описанных случаев) при вакцинации ДНК-вакцинами (Oxford/AstraZeneca). Патогенетической связи между вакцинацией и этими осложнениями, однако, найти не удалось, взаимосвязь объясняется временным осложненным характером течения заболевания после введения препарата [19].
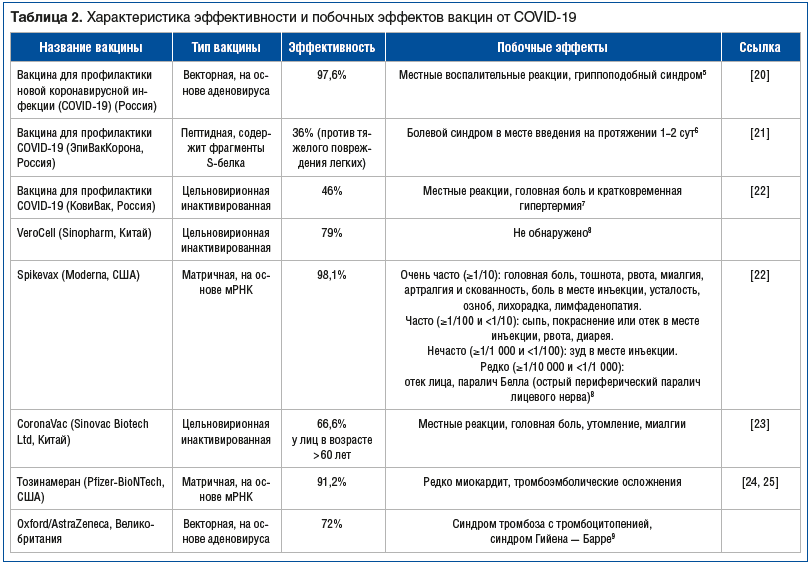
Однако частота серьезных осложнений остается крайне низкой по сравнению с риском тяжелых последствий самого COVID-19. Это подчеркивает необходимость регулярного наблюдения за пациентами после вакцинации и проведения просветительской работы с населением о безопасности и преимуществах вакцин. Наиболее часто используемые вакцины и специфические осложнения, характерные для них, представлены в таблице 2.5-9
Заключение
Ряд исследований демонстрирует высокую эффективность вакцинации против COVID-19 в предотвращении инфекции, ее тяжелых форм и постковидного синдрома. Вакцины также оказываются эффективными для уязвимых групп населения и помогают снизить общую нагрузку на систему здравоохранения. Именно уменьшение процента невакцинированных людей способствует снижению заболеваемости, так как эта группа является резервуаром для репликации и мутационных изменений вируса [26]. Несмотря на редкие побочные эффекты, вакцинация остается безопасной и необходимой профилактической мерой борьбы с COVID-19. Важно продолжать исследования для выявления долгосрочных эффектов вакцинации и разработки новых стратегий защиты от коронавирусной инфекции.
Последние исследования подтверждают, что бустерные дозы вакцин мРНК значительно усиливают иммунную защиту и снижают вероятность развития тяжелых форм COVID-19. Вакцинация также оказывает положительное влияние на профилактику долгосрочных осложнений COVID-19, что особенно важно для уязвимых групп населения. Таким образом, вакцинация остается ключевым инструментом борьбы с COVID-19 и важной мерой по снижению влияния постковидного синдрома на качество жизни пациентов.
1World Health Organization Data. (Электронный ресурс.) URL: https://data.who.int/dashboards/covid19/cases?n=o (дата обращения:12 .03.2025).
2Отслеживание вариантов вируса SARS-CoV-2 (2024). (Электронный ресурс.) URL: https://www.who.int/ru/activities/tracking-SARS-CoV-2-variants (дата обращения: 12.03.2025).
3The different types of COVID-19 vaccines (2021). (Электронный ресурс.) URL: https://www.who.int/ru/news-room/feature-stories/detail/the-race-for-a-covid-19-vaccine-explained (дата обращения: 12.03.2025).
4AstraZeneca’s COVID-19 vaccine: EMA finds possible link to very rare cases of unusual blood clots with low blood (2021). (Электронный ресурс.) URL: https://www.ema.europa.eu/en/news/astrazenecas-covid-19-vaccine-ema-finds-possible-link-very-rare-ca… (дата обращения: 27.11.2024).
5Спутник V. (2021) (Электронный ресурс.) URL: https://sputnikvaccine.com/rus/newsroom/pressreleases/effektivnost-vaktsiny-sputnik-v-sostavila-97-6… (дата обращения: 12.03.2025).
6Сравнительные характеристики вакцин Гам-Ковид-Вак, Спутник Лайт, ЭпиВакКорона и КовиВак (2021). (Электронный ресурс.) URL: https://vakcina.ru/files/tmpfiles/upload-documents/COVID-19/2021/sravnenie-vakcin-2021.pdf?ysclid=m2… (дата обращения: 12.03.2025).
7Что необходимо знать о вакцине против COVID-19 Sinopharm (2022). (Электронный ресурс.) URL: https://www.who.int/ru/news-room/feature-stories/detail/the-sinopharm-covid-19-vaccine-what-you-need… (дата обращения: 12.03.2025).
8Пояснительная записка по вакцине от COVID-19 (2021). (Электронный ресурс.) URL: https://www.who.int/docs/default-source/coronaviruse/act-accelerator/covax/21100_russian_moderna-vac… (дата обращения: 12.03.2025).
9Что необходимо знать о вакцине против COVID-19 Oxford/AstraZeneca ([рекомбинантной] вакцине ChAdOx1 S) (2022). (Электронный ресурс.) URL: https://www.who.int/ru/news-room/feature-stories/detail/the-oxford-astrazeneca-covid-19-vaccine-what… (дата обращения: 12.03.2025).
Информация с rmj.ru






