Содержание статьи
Введение
Согласно данным Всемирной организации здравоохранения1 в мире по меньшей мере 2,2 млрд человек имеют нарушения зрительных функций, а в 1 млрд случаев снижение зрения можно было предотвратить. Среди этого 1 млрд человек основным заболеванием, вызывающим ухудшение зрения, является катаракта (94 млн человек). Вследствие высокой распространенности и заболеваемости катаракта является не только медицинской, но и социальной проблемой [1].
В настоящее время это заболевание выявляется у пациентов не только средней (у лиц старше 50 лет) и старшей возрастной категории (пик заболеваемости приходится на 70–80 лет), но и у пациентов зрелого (40 лет) и молодого возраста (20 лет) [2].
Этиология и классификация
Существует разделение катаракты по времени возникновения на врожденную и приобретенную.
Наиболее часто встречаются приобретенные возрастные (инволюционные) катаракты. К приобретенным катарактам относятся также осложненные катаракты.
К факторам риска приобретенных осложненных катаракт можно отнести:
-
заболевания органа зрения: осложненная миопия, глаукома, пигментная дегенерация сетчатки, воспаление сосудистой оболочки глаза (увеит, увеопатии), травмы глаза, предшествующая витрэктомия;
-
общие заболевания: различные виды метаболических нарушений (врожденные и приобретенные болезни обмена веществ, включая сахарный диабет), сердечно-сосудистые (артериальная гипертония, дислипидемия), аутоиммунные, системные заболевания соединительной ткани, острые и хронические инфекционные и паразитарные заболевания, гипотиреоз, миотонические дистрофии, гипопаратиреоз, аллергический дерматит, ожирение и т. д.;
-
алиментарные факторы: высокоуглеводная диета, длительное обезвоживание из-за недоедания, несбалансированное питание и др.;
-
воздействие радиационных факторов, лучистой энергии (опасным для хрусталика является ультрафиолетовый свет с длиной волны 280–315 нм, В-диапазон), рентгеновского, инфракрасного, излучения микроволн от СВЧ и электромагнитного излучения, удара молнии и других видов проникающей радиации;
-
общее отравление (нафталином, спорыньей, талием, динитрофенолом и др.), а также результат побочного действия при длительном приеме ряда лекарственных препаратов: кортикостероидов, антималярийных препаратов, амиодарона, аспирина, β-блокаторов и др.;
-
травматические воздействия механических и химических факторов (проникающие ранения, контузии, ожоги, металлозы).
Так, хроническая гипокальциемия, вызванная гипопаратиреозом, приводит к двухсторонней катаракте. Ранняя диагностика первичного гипопаратиреоза, сахарного диабета и других эндокринных заболеваний может уберечь пациентов от многих осложнений, в том числе от раннего развития катаракты [3]. Более 70 лекарственных средств способствуют образованию катаракты [4]. Употребление алкоголя и наркотических веществ (в частности, дым каннабиса, как и табачный дым, содержит различные канцерогенные и токсичные соединения), табакокурение являются факторами риска развития катаракты и других заболеваний [5].
Патогенез
Помутнение хрусталика — это мультифакторное и полиэтиологическое заболевание, развивающееся в результате оксидативного стресса [6]. На развитие катаракты влияют генетические факторы, возрастные изменения, радиация, дефицит питательных веществ, метаболические нарушения, травма и определенные химические агенты [7].
В течение жизни человека хрусталик подвергается окислительному стрессу как эндогенными путями, включающими митохондриальное дыхание и окислительный взрыв макрофагов, так и экзогенными, включающими воздействие ультрафиолетовой части спектра, табачного дыма, металлов и лекарств.
В клинических исследованиях была показана связь между лазерными рефракционными операциями и ранней катарактой2.
Доказанными механизмами, вызывающими появление и прогрессирование катаракты, являются неферментативное гликирование, окислительный стресс, полиольный путь метаболизма глюкозы, избыток хиноидных субстанций и активация альдозоредуктазы.
При воздействии активных форм кислорода в клетках происходит обширное повреждение белков и перекисное окисление мембранных липидов, что вызывает внутриклеточную агрегацию и осаждение белков, приводящее к помутнению хрусталика [6].
Симптоматика
Катаракта разнообразна в своих проявлениях. Известно, что незначительные возрастные помутнения хрусталика могут приводить к зрительным расстройствам даже при нормальной остроте зрения [1]. Начальные симптомы катаракты у всех примерно одинаковы. Основные жалобы — на изменение зрения:
-
постепенное безболезненное снижение остроты зрения вдаль;
-
временное улучшение остроты зрения вблизи;
-
ощущение тумана перед глазами, нечеткость изображения, двоение и изменение цветоощущения, контрастности и яркости, в сумерках видно лучше, чем днем;
-
появление ореолов, лучей светорассеяния от источников света, двоение светящихся предметов;
-
частая смена очков.
Катаракта при осложненной миопии
Одним из факторов риска развития приобретенных катаракт является осложненная миопия, ставшая серьезной проблемой здравоохранения во всем мире. Более 80% подростков в странах Восточной Азии и одна треть в Европе и США страдают близорукостью [8]. Ожидается, что со временем эта распространенность будет увеличиваться из-за особенностей современного образа жизни, а пандемия COVID-19 усугубила возникновение и прогрессирование близорукости [9–11]. Миопия является причиной инвалидности по зрению в 20–28% случаев, и, по прогнозам, при отсутствии принятия превентивных мер во всем мире к 2050 г. ожидаемое число пациентов с миопией составит 4,9 млрд [12, 13].
С возрастом у пациентов с близорукостью, особенно высокой степени, возникают различные сопутствующие заболевания глаз, такие как катаракта и макулопатия, которые могут привести к серьезным нарушениям зрения [14]. Хотя катаракта является обратимой причиной слепоты, ее лечение у пациентов с близорукостью может оказаться затруднительным [15–17].
Связь между близорукостью и возникновением или прогрессированием катаракты изучалась в 3 проспективных и 8 перекрестных исследованиях. В 9 из 11 исследований была выявлена сильная связь между миопией и задней субкапсулярной катарактой [18]. Метаанализ, проведенный A.E.G. Haarman et al. [18], выявил сильную связь между развитием ядерной катаракты и миопией любой степени (отношение шансов (ОШ) 2,51, 95% доверительный интервал (ДИ) 1,53–4,13, гетерогенности нет); миопией низкой степени (ОШ 1,79, 95% ДИ 1,08–2,97, гетерогенности нет); миопией средней степени (ОШ 2,39, 95% ДИ 1,03–5,55, гетерогенности нет); миопией высокой степени (ОШ 2,86, 95% ДИ 1,43–5,73, гетерогенности нет). Что касается кортикальной катаракты, то данный метаанализ показал суммарное ОШ 1,15 (95% ДИ 0,94–1,40, отсутствие гетерогенности) для миопии любой степени; ОШ 0,99 (95% ДИ 0,85–1,15, гетерогенности нет) для миопии низкой степени; ОШ 1,06 (95% ДИ 0,83–1,35, гетерогенности нет) для миопии средней степени; ОШ 1,07 (95% ДИ 0,81–1,40, низкая гетерогенность) для миопии высокой степени.
Типичными проявлениями неблагоприятного течения миопии является развитие дистрофических изменений в хрусталике, стекловидном теле, в центральных и периферических отделах глазного дна с возникновением отслойки сетчатки, поражением зрительного нерва [19]. Осложненная катаракта при высокой близорукости формируется у пациентов на 10 лет раньше, чем сенильная.
Для объяснения взаимосвязи между близорукостью и катарактой наиболее доказаны 2 механизма. Во-первых, при миопии более высокий уровень оксидативного стресса, вызванный быстрым разжижением стекловидного тела и снижением уровня глутатиона (антиоксидантного агента) в хрусталике близоруких глаз (рис. 1). Во-вторых, более высокий уровень побочных продуктов перекисного окисления липидов при близорукости может приводить к образованию катаракты [21].
![Рис. 1. Патогенез осложненной миопии: роль оксидативного стресса [20] Fig. 1. Pathogenesis of degenerative myopia: the role of oxidative stress [20] Рис. 1. Патогенез осложненной миопии: роль оксидативного стресса [20] Fig. 1. Pathogenesis of degenerative myopia: the role of oxidative stress [20]](https://medblog.su/wp-content/uploads/2023/11/Izmeneniya-hrustalika-pri-oslozhnennoj-miopii-Vozmozhnosti-lecheniya-Rabadanova-MG.png)
Снижение прозрачности хрусталика при миопии проявляется в виде уплотнения его швов и развития факосклероза, затем процесс затрагивает субкапсулярные и кортикальные слои (рис. 2).
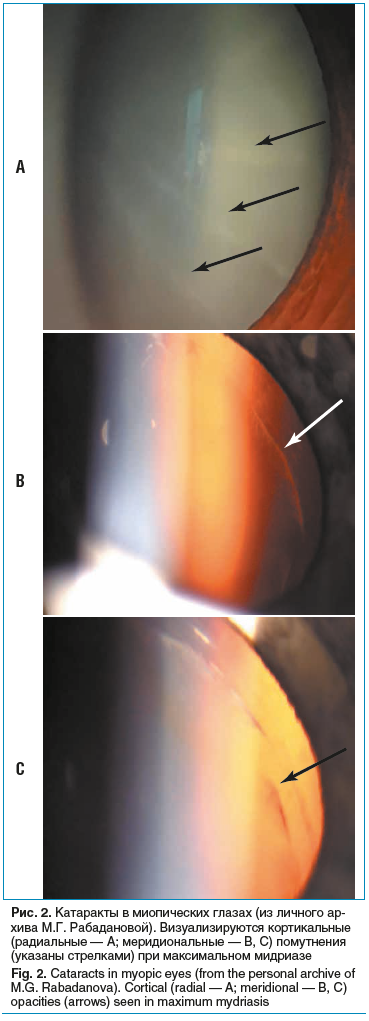
Собственный опыт
Нами было проведено исследование по оценке изменения прозрачности хрусталика у 60 пациентов (120 глаз) в возрасте от 19 до 65 лет и с диагнозом «периферические витреохориоретинальные дистрофии» (ПВХРД) (опасные формы — разрыв сетчатки, решетчатая дистрофия, «след улитки») на фоне осложненной миопии, направленных для проведения лазерной коагуляции сетчатки.
Пациентов разделили на 3 группы по степени миопии: слабая (n=21), средняя (n=21), высокая (n=18). Офтальмологическое обследование включало визометрию с помощью электрического проектора, измерение внутриглазного давления, авторефрактометрию в условиях циклоплегии, компьютерную периметрию, офтальмометрию с обязательной биомикроофтальмоскопией переднего и заднего отделов глаза в условиях максимального мидриаза и фоторегистрацию изменений в хрусталике.
При сборе анамнеза у пациентов обращали внимание на наличие осложненной миопии у родственников, другой офтальмопатологии, дисплазии соединительной ткани, хронических соматических заболеваний, вредных привычек, профессиональных вредностей, интенсивность зрительной нагрузки (в том числе наличие компьютерного зрительного синдрома), перенесенные травмы (общие и органа зрения). У всех пациентов с изменением прозрачности хрусталика наблюдался отягощенный анамнез, т. е. имелись сопутствующие хронические заболевания на фоне наследственной предрасположенности.
Нами было выявлено, что изменения структуры хрусталика сопровождают прогрессирование осложненной мио-пии и часто встречающимся изменением у пациентов со слабой степенью миопии является уплотнение швов хрусталика. Частота встречаемости начальной катаракты у пациентов с осложненной миопией увеличивалась в зависимости от степени миопии [19].
Лечение
В случае прогрессирования помутнений в хрусталике с развитием незрелой катаракты однозначно показано хирургическое лечение — факоэмульсификация с имплантацией интраокулярной линзы.
В то же время на начальной стадии заболевания пациенту может быть предложено местное медикаментозное лечение катаракты. Особенно назначение такого лечения актуально для тех больных, у которых есть временные противопоказания к оперативному лечению из-за глазной или соматической патологии, и пациентов с повышенным риском послеоперационных осложнений (послеоперационные экссудативные реакции, отек роговицы, кистозный макулярный отек и др.), к которым относятся в том числе пациенты с миопией [21–23]. Фармакологическое лечение для таких пациентов доступно, удобно, безопасно и замедляет (а в ряде случаев и останавливает) прогрессирование помутнений хрусталика [6, 7].
В настоящее время продолжают вестись научные исследования потенциальных лекарственных веществ, способных замедлить катарактогенез, разрабатываются стратегии, направленные на предотвращение развития катаракты с использованием антиоксидантов, ингибиторов альдозоредуктазы и сульфгидрильных ингибиторов хиноидных соединений [6].
Медикаментозное лечение направлено на улучшение обменных процессов в хрусталике, коррекцию биохимических сдвигов, восполнение недостатка различных веществ, нормализацию метаболизма и окислительно-восстановительного баланса. Такая терапия предупреждает прогрессирование помутнений преимущественно в начальной стадии развития катаракты, возможно, на длительный период, но не вызывает обратного развития процесса. Что касается результатов воздействия на катарактогенез системного применения биологически активных добавок, то, согласно данным литературы, они неоднозначны, так же как и попытки лечения катаракты с помощью перорального приема аспирина, альдоредуктазы и местной терапии N-ацетилкарнозином [24].
Действенным и хорошо переносимым средством, применяемым для профилактики прогрессирования катаракты и ее лечения, является препарат Каталин, действующим веществом которого служит пиреноксин. Препарат впервые был зарегистрирован в Японии в 1958 г. и используется в настоящее время более чем в 20 странах мира, имея обширную доказательную базу в виде результатов клинических исследований. Каталин представлен в Государственном реестре лекарственных средств РФ3 как единственный антикатарактальный лекарственный препарат.
Действие пиреноксина патогенетически обосновано, большинство имеющихся данных свидетельствуют о его антиоксидантных свойствах, выражающихся в защите белков хрусталика от денатурации, что сохраняет прозрачность структуры хрусталика и замедляет развитие катаракты [7]. Пиреноксин также является хелатором Se2+ и Ca2+, ингибитором окисления НАДФН и протектором тиоловой группы.
Согласно результатам отечественных и зарубежных исследований Каталин является эффективным препаратом для лечения возрастной катаракты, хорошо переносится пациентами всех возрастных групп и продемонстрировал положительный клинический эффект в профилактике и лечении диабетической катаракты [7, 25].
Так, у 30 пациентов основной группы через 3 мес. инстилляций Каталина было зафиксировано достоверное снижение денситометрических показателей оптической плотности хрусталика в передних и задних кортикальных слоях и задней капсуле. В то же время в контрольной группе показатели оптической плотности практически не изменились. Эффект сохранялся на протяжении 12 мес., не было выявлено каких-либо побочных эффектов [26].
В другом исследовании было доказано влияние глазных капель пиреноксина на эластичность хрусталика. В группе контроля через 6 мес. объективная амплитуда аккомодации снизилась на 0,16 дптр, что означало прогрессирование пресбиопии, а в группе пациентов в возрасте до 50 лет, получающих пиреноксин, амплитуда не изменилась, пресбиопия не прогрессировала. Авторы сделали вывод о том, что пиреноксин перспективен для изучения не только с целью профилактики прогрессирования начальных проявлений катаракты, но и как средство ранней терапии пресбиопии [27].
В отечественном исследовании, включившем 822 пациента, ожидающих хирургического лечения катаракты, при применении Каталина пациентами основной группы с начальной катарактой (65 человек) зафиксировано уменьшение образования новых помутнений в кортикальных слоях хрусталика и существенное замедление изменений рефракции. У пациентов с незрелой катарактой препарат не стабилизировал развитие катарактального процесса, но замедлял развитие рефракционных изменений, что существенно отражалось на качестве жизни пациентов, так как они продолжали пользоваться привычной очковой коррекцией [28].
Заключение
Высокая распространенность катаракты и прогнозируемое увеличение числа пациентов молодого и среднего возраста с помутнением хрусталика, обусловленным различными факторами, являются важной медико-социальной проблемой. Старение населения планеты в ряде случаев снижает доступность хирургического лечения и требует поиска новых и применения известных терапевтических методов замедления развития катаракты и профилактики ее возникновения. Важна не только ранняя диагностика катаракты, но и медикаментозная коррекция на начальных стадиях помутнений хрусталика, когда она наиболее эффективна. Особое внимание следует уделить пациентам с осложненной миопией, исследуя их хрусталик при максимальном медикаментозном мидриазе. Обнаружение начальных изменений в хрусталике у данной группы больных будет свидетельствовать о наличии процессов в глазу, связанных с оксидативным стрессом, который впоследствии может вызвать и другие, более серьезные, осложнения со стороны сетчатки. То есть ранняя диагностика катаракты у пациентов с миопией с последующим назначением патогенетически обоснованного лечения способствует уменьшению риска развития осложнений миопии и снижению показателей инвалидности по зрению, особенно у лиц молодого и среднего возраста. Использование местной и общей фармакотерапии, направленной на уменьшение прогрессирования осложнений миопии, с возможным включением антикатарактальных капель будет способствовать снижению скорости образования помутнений хрусталика, что особенно актуально для миопических больных, катарактальная хирургия у которых сопряжена с повышенными интра- и послеоперационными рисками.
Также для профилактики развития и прогрессирования катаракты важно рекомендовать пациентам вести здоровый образ жизни: исключить табакокурение, изменить рацион питания, ограничить употребление алкоголя, снизить воздействие ультрафиолетового излучения и профессиональных вредностей, использовать оптимальную очковую коррекцию, провести санацию очагов хронической инфекции, коррекцию сосудистых, метаболических и аутоиммунных нарушений, т. е. провести коррекцию модифицируемых факторов риска, что повышает физическую и социальную адаптацию. Данные рекомендации могут стать наиболее эффективными и наименее затратными направлениями для предотвращения возникновения возрастной катаракты. Литература / References
1 Blindness and vision impairment. (Electronic resource.) URL: https://www.who.int/news-room/fact-sheets/detail/blindness-and-visual-impairment (30.08.2023).
2 Катаракта старческая. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/recomend/284_1 (дата обращения: 30.08.2023).
3 Каталин, инструкция по медицинскому применению. (Электронный ресурс.) URL: https://grls.rosminzdrav.ru/GRLS.aspx?RegNumber=&MnnR=&lf=&TradeNmR=Каталин&OwnerName=&MnfOrg=&Mnf OrgCountry=&isfs=0®type=1%2c2%2c3%2c4%2c5%2c6%2c7%2c8&pageSize=10&order=Registered&orderType=desc&pageNum=1 (дата обращения: 30.08.2023).
Сведения об авторах:
Рабаданова Мадина Гусейновна — к.м.н., доцент кафедры офтальмологии им. акад. А.П. Нестерова лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; врач-офтальмолог лазерного отделения ГБУЗ «ГКБ № 15 ДЗМ»; 111539, Россия, г. Москва, ул. Вешняковская, д. 23; ORCID iD 0000-0003-2847-3670.
Оганезова Жанна Григорьевна — к.м.н., доцент кафедры офтальмологии им. акад. А.П. Нестерова лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-4437-9070.
Кремкова Елена Витальевна — д.м.н., профессор, профессор кафедры офтальмологии им. акад. А.П. Нестерова лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1.
Яхъяева Марьяна Магомедсаидовна — студентка 5-го курса педиатрического факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1.
Контактная информация: Оганезова Жанна Григорьевна, e-mail: jannaogan@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 31.08.2023.
Поступила после рецензирования 21.09.2023.
Принята в печать 12.10.2023.
About the authors:
Madina G. Rabadanova — C. Sc. (Med.), associate professor of the Academician A.P. Nesterov Department of Ophthalmology, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ophthalmologist in the Laser Department, O.M. Filatov City Clinical Hospital No. 15; 23, Veshnyakovskaya str., Moscow, 111539, Russian Federation; ORCID iD 0000-0003-2847-3670.
Janna G. Oganezova — C. Sc. (Med.), associate professor of the Academician A.P. Nesterov Department of Ophthalmology, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-4437-9070.
Elena V. Kremkova — Dr. Sc. (Med.), Professor, professor of the Academician A.P. Nesterov Department of Ophthalmology, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation.
Mar’yana M. Yakh”yaeva — student of the 5th course of the Pediatric Faculty, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation.
Contact information: Janna G. Oganezova, e-mail: jannaogan@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 31.08.2023.
Revised 21.09.2023.
Accepted 12.10.2023.
материал rmj.ru
