Врожденный стеноз и атрезия наружного слухового прохода (НСП) являются наиболее встречаемыми пороками развития наружного уха. По данным различных исследователей, данная патология встречается с частотой 1 случай на 10 000–20 000 новорожденных [1–3]. Обычно наблюдается одностороннее поражение, и преимущественно у пациентов мужского пола [3–5]. Врожденный стеноз и атрезия НСП часто сочетаются с микротией, аномалиями развития среднего уха, лицевого скелета, однако могут наблюдаться и изолированно [1, 6, 7].
Помимо визуального дефекта (деформации ушной раковины) и функциональных нарушений (кондуктивной тугоухости) данная группа пациентов имеет повышенный риск
развития холестеатомы височной кости (ХВК) [7–9].
В литературе ХВК представлена как кистоподобное образование, состоящее из ороговевающего плоскоклеточного эпителия, расположенное в полостях височной кости и способное вызывать в процессе своего роста воспалительную реакцию и резорбтивные процессы в прилежащих костных тканях [10–12]. В настоящее время ХВК принято классифицировать на врожденную, приобретенную и ятрогенную [11, 12].
По данным ряда авторов, приобретенная холестеатома НСП считается потенциальным осложнением врожденного стеноза НСП [7–9]. В данном случае холестеатома образуется из кожи НСП вследствие нарушения процессов элиминации слущенного эпидермиса через стенозированный участок НСП [7, 9, 13]. При этом наибольший риск развития холестеатомного процесса наблюдается у пациентов с диаметром НСП 2 мм и менее, при этом вероятность образования холестеатомы НСП достигает 90% [9].
Полная атрезия НСП исключает приобретенный механизм холестеатомы вследствие отсутствия клеток эпидермиса за костной атретической пластинкой (АП) [9, 14]. В зарубежной литературе мы встретили 3 статьи с описанием единичных клинических случаев врожденной холестеатомы, располагающейся медиальнее АП [15–17].
В период с 2014 по 2019 г. в ФГБУ «СПб НИИ ЛОР» Минздрава России у 7 пациентов с врожденной аномалией развития наружного и среднего уха было проведено хирургическое лечение врожденной ХВК. Из них у 4 пациентов (9,5%) холестеатома располагалась медиальнее АП, в 3 случаях (7,1%) — за неповрежденной барабанной перепонкой.
В данной статье описаны наиболее показательные клинические наблюдения врожденной ХВК, сочетанной с аномалиями развития наружного и среднего уха.
Содержание статьи
Клиническое наблюдение № 1
Пациент и результаты обследования
Пациентка Ф., 6 лет, поступила на обследование в ФГБУ «СПб НИИ ЛОР» Минздрава России с диагнозом «рецидивирующий левосторонний экссудативный средний отит». Врожденная атрезия НСП справа. Синдром Шерешевского — Тернера. До развития левостороннего экссудативного отита слуховая функция левого уха была в пределах нормы, поэтому операция по устранению врожденной атрезии НСП справа была запланирована на более поздние сроки.
Отомикроскопия. Левое ухо: ушная раковина без особенностей, НСП широкий, свободный; барабанная перепонка серая, мутная, без дефектов, в барабанной полости уровень жидкости. Правое ухо: микротия, полная атрезия НСП.
Мультиспиральная компьютерная томография (МСКТ) височных костей: выявлены мягкотканное образование, заполняющее костную часть правого слухового прохода, и костно-деструктивные изменения в области АП.
Магнитно-резонансная томография (МРТ) среднего уха в DWI-режиме: идентифицирована холестеатома НСП правой височной кости (рис. 1).
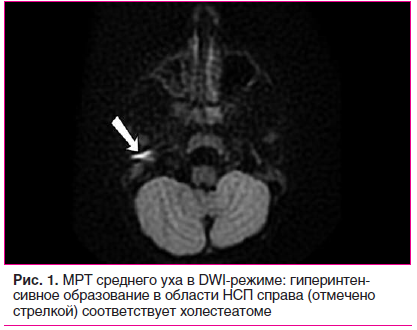
На основании проведенного обследования было принято решение о проведении одномоментной операции по устранению врожденной костной атрезии правого НСП и удалению холестеатомы в кратчайшие сроки.
Интраоперационные находки
Хирургическое вмешательство проведено в условиях многокомпонентной анестезии с интубацией трахеи. Операция проводилась трансмастоидальным доступом.
После отсепаровки мягких тканей был визуализирован щелевидный дефект в костной АП, заполненный холестеатомными массами. Борами была удалена АП, расширена костная часть НСП, сформирована антромастоидальная полость. Холестеатома тотально заполняла пространство между барабанной перепонкой и АП (рис. 2).
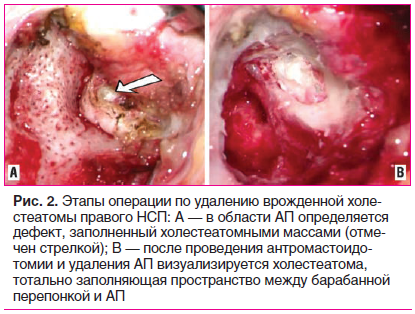
Холестеатома выделена одним блоком и удалена вместе с капсулой. Барабанная перепонка гиперемирована, отечна, без дефектов. Выполнена тимпанотомия с ревизией барабанной полости. Структуры среднего уха располагались типично. Aditus ad antrum свободен, проходим. Цепь слуховых косточек окутана спайками, длинный отросток наковальни не контактировал с головкой стремени. Наковальня резецирована. Тимпанальное устье слуховой трубы широкое, свободное. Патологической ткани при контрольной ревизии барабанной и антромастоидальной полостей не обнаружено. Симптом передачи давления перелимфы с окна преддверия на окно улитки положительный. Выполнена оссикулопластика титановым протезом PORP 2,0 мм, установленным на головку стремени. На шляпку протеза уложена аутохрящевая пластинка. Аутофасциальный лоскут уложен под заднюю часть барабанной перепонки и на область аттика и антрума. Произведена пластика НСП. Сохраненная кожа низведена на костные стенки НСП и зафиксирована бумажными протекторами, силиконовыми полосками и гемостатическими губками. Заушную рану послойно ушили. Патологическая ткань отправлена на гистологическое исследование.
Клиническое наблюдение № 2
Пациент и результаты обследования
Родители пациентки М., возраст которой на момент операции составлял 1 год 3 мес., обратились в ФГБУ «СПб НИИ ЛОР» Минздрава России по поводу двустороннего снижения слуха, задержки речевого развития и косметического дефекта ушных раковин в виде микротии. В анамнезе заболевания отсутствовали оторея и отохирургические процедуры.
Отомикроскопия. Слева в барабанной полости за неповрежденной барабанной перепонкой визуализировалось перламутрово-белое образование.
МСКТ височных костей. В барабанной полости слева определялось мягкотканное образование, занимающее мезотимпанум, гипотимпанум и частично аттик, костно-деструктивных изменений не отмечено.
МРТ среднего уха в DWI-режиме. Подтверждена холестеатомная природа образования (рис. 3).
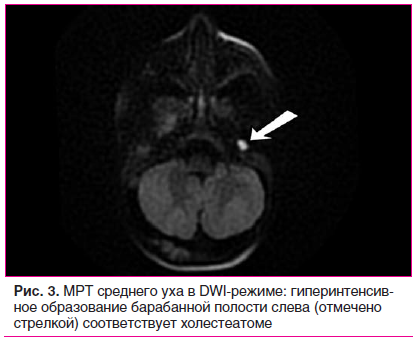
По данным регистрации коротколатентных слуховых вызванных потенциалов диагностирована двусторонняя кондуктивная тугоухость: справа — III степени, слева —
IV степени.
На основании полученных данных было принято решение о проведении санирующей операции с удалением холестеатомы.
Интраоперационные находки
Хирургическое вмешательство проведено в условиях многокомпонентной анестезии с интубацией трахеи. Произведен заушный разрез слева. Мягкие ткани отсепарованы до planum mastoideum, кожа задней стенки НСП — до фиброзного кольца. Борами расширена костная часть НСП. Визуализирована интактная барабанная перепонка с пролабированием ее задних отделов белесоватым образованием. После проведения тимпанотомии обнаружено, что образование (холестеатома) тотально заполняло мезотимпанум, частично — гипотимпанум, протимпанум и аттик и имело плотную, хорошо васкуляризированную капсулу. Из-за размеров холестеатомы и степени ее охвата структур среднего уха резецирована сhorda timpanу и выполнено ее опорожнение, при этом получены творожистые эпидермальные хлопья (холестеатомные массы). Образование выделено вместе с капсулой, удалено и отправлено на гистологическое исследование (рис. 4).
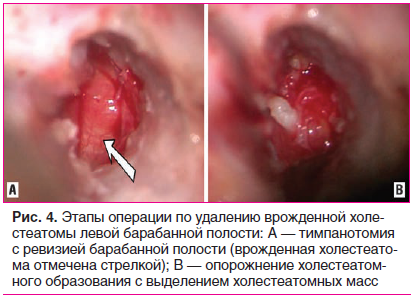
При дальнейшей ревизии барабанной полости были выявлены сопутствующие аномалии развития среднего уха: горизонтальный отдел канала лицевого нерва четко не прослеживался и располагался латеральнее, ближе к аттику; головка молоточка была фиксирована костной балкой к передней стенке барабанной полости, наковальня и стремя четко не определялись. Костная балка, фиксирующая молоточек, была удалена. Патологической ткани при контрольной ревизии барабанной полости не выявлено. Меатотимпанальный лоскут низведен на прежнее место. Слуховой проход тампонирован силиконовыми полосками и гемостатическими губками. Заушную рану послойно ушили.
Результаты
Послеоперационный период в обоих случаях протекал без осложнений.
По результатам гистологического исследования операционного материала верифицирована холестеатома. Пациенткам рекомендовано динамичное наблюдение. Контрольная МРТ среднего уха в DWI-режиме запланирована через 6 мес. с момента операции.
Обсуждение
Принятыми клиническими критериями верификации врожденной ХВК являются: новообразование перламутрово-белого цвета, располагающееся медиальнее неизмененной барабанной перепонки с интактной натянутой и ненатянутой ее частями; отсутствие в анамнезе у пациента отореи, перфорации барабанной перепонки и предыдущих отологических хирургических процедур [18]. В первом клиническом наблюдении холестеатома располагалась за пределами барабанной полости, между неповрежденной барабанной перепонкой и АП. Данная холестеатома была отнесена к врожденной по причине отсутствия у нее прямого контакта с кожным покровом, что исключало возможность миграции эпидермиса с образованием холестеатомы.
На сегодняшний день существует множество теорий развития врожденной холестеатомы. Наиболее признанной является теория остаточного эпидермального образования в височной кости. Данное образование в среднем ухе впервые обнаружил R.W. Teed в 1936 г. при исследовании кадаверного материала [19]. В последующем, в 1986 г., L. Michaels подтвердил наличие данного образования в височных костях плодов, отметив, что оно расположено в передневерхнем отделе барабанной полости и исчезает, в подавляющем большинстве случаев, к 33-й нед. гестации [20]. Позже J. Liang et al. выявили данное образование и в других отделах височной кости [21]. На основании этого можно сделать предположение, что подобное образование, находясь в закрытом пространстве медиальнее АП, может дать начало врожденной ХВК.
Врожденная ХВК сама по себе трудно диагностируется вследствие ряда факторов: отсутствия активных жалоб пациента ввиду его юного возраста; скрытого течения до развития интра- и экстратемпоральных осложнений; низкой информированности и отсутствия настороженности у многих специалистов в отношении данного заболевания [22]. Развитие холестеатомы на фоне врожденной аномалии НСП еще сильнее усложняет ее диагностику [7, 15]. В случае стеноза или атрезии НСП визуализация барабанной перепонки становится невозможной, что исключает вероятность диагностирования врожденной холестеатомы на этапе оториноларингологического осмотра. Данный факт указывает на необходимость проведения инструментальных методов исследования.
МСКТ височных костей позволяет оценить протяженность стенозированного участка НСП, объем барабанной полости и антрума, состояние структур среднего уха, исключить или подтвердить наличие деструктивных процессов в височной кости [2, 8, 14]. Данная информация необходима при планировании оперативного вмешательства, однако не позволяет достоверно исключить ХВК, которая будет выглядеть на срезах МСКТ как неоднородное мягкотканное образование, трудноотличимое от фиброзной ткани [7, 8]. Единственным на сегодняшний день неинвазивным высокочувствительным способом диагностики ХВК служит МРТ среднего уха в режиме DWI [23, 24]. В описанных клинических наблюдениях данная методика позволила выявить врожденную холестеатому и в ранние сроки провести оперативное вмешательство.
Принятым алгоритмом ведения пациентов с врожденной аномалией развития НСП является проведение реконструктивной операции на ухе в возрасте старше 5 лет. При билатеральном поражении показаны максимально раннее слухопротезирование с применением слуховых аппаратов костной проводимости или имплантация систем костного звукопроведения для предотвращения задержки психического и социального развития [3, 6]. При врожденной холестеатоме, сочетанной с врожденной аномалией развития уха, оперативное лечение должно проводиться независимо от возраста ребенка. В литературе имеются описания случаев комбинации данных патологий с выраженными деструктивными изменениями височной кости. Так, K. Bhavana описал врожденную холестеатому, располагающуюся медиальнее АП, которая в процессе своего роста разрушила заднюю стенку слухового прохода с распространением в сосцевидный отросток и барабанную полость [16]; в работе M. Abdel-Aziz врожденная холестеатома, сочетанная с врожденной атрезией НСП, тотально заполнила барабанную полость, распространилась в подвисочную ямку вследствие деструкции капсулы височно-нижнечелюстного сустава [17].
В описанных клинических наблюдениях врожденная ХВК была диагностирована до развития выраженных деструктивных процессов, что позволило минимизировать объем оперативного вмешательства. Такой подход в дальнейшем сократит сроки реабилитации пациентов и упростит последующие реконструктивные операции, связанные с врожденной аномалией развития наружного и среднего уха.
Заключение
Представленные клинические наблюдения акцентируют внимание на бессимптомном развитии и течении холестеатомы у детей с врожденной аномалией развития наружного и среднего уха. Отсутствие выраженных жалоб и невозможность диагностировать холестеатому на этапе базового оториноларингологического обследования подчеркивает необходимость настороженного отношения врачей при врожденных аномалиях развития наружного и среднего уха и проведения дополнительных инструментальных визуализирующих методов исследования, наиболее достоверным из которых является МРТ среднего уха в DWI-режиме.
Оперативное лечение при врожденной холестеатоме, сочетанной с атрезией/стенозом НСП, должно проводиться в кратчайшие сроки независимо от возраста ребенка для предупреждения развития внутричерепных осложнений.
материал rmj.ru
