Введение
В связи с ростом резистентности микроорганизмов, мутациями патогенов, приводящих к развитию пандемий, актуальной является разработка новых лекарственных препаратов, в том числе неспецифических противовирусных средств широкого спектра действия, для неспецифической активации врожденного иммунитета[1]
[1–3].
Создаются как специфические высокотехнологичные таргетные лекарства и вакцины против современных пандемических инфекций, так и противовирусные средства широкого спектра действия для неспецифической активации врожденного иммунитета.
К таким средствам можно отнести спрей для полости рта Панавир Инлайт®, обладающий широким спектром противовирусного и антибактериального действия. Активный компонент препарата является высокомолекулярной фракцией полисахаридов, экстрагированных из побегов Solanum tuberosum. Препараты Панавир® проявляют активность против многих типов вирусов, включая коронавирус животных, а также против бактериальных инфекций [4]. По данным литературы, препараты линейки Панавир® довольно давно и успешно применяются в клинической практике. Их противовирусная активность подтверждена при лечении различных вирусных инфекций, таких как рецидивирующий генитальный герпес [5], вирус папилломы человека [6, 7], грипп [8], клещевой энцефалит [9].
Цель исследования: оценка клинической эффективности, переносимости и безопасности использования спрея для полости рта Панавир Инлайт® в терапии острого тонзиллофарингита (ОТФ) нестрептококковой этиологии.
Материал и методы
Задачи исследования:
Определить по клиническим данным и субъективной оценке пациента с ОТФ нестрептококковой этиологии эффективность местной терапии средствами разных групп.
Установить сроки наступления эффекта (скорость купирования объективных и субъективных симптомов) при применении различных топических препаратов в лечении больных с ОТФ нестрептококковой этиологии.
Проанализировать скорость восстановления слизистой оболочки глотки при применении различных топических средств путем проведения цитоморфометрии (оценка ряда показателей деструкции эпителия и наличия клеток воспаления).
Оценить переносимость и удовлетворенность пациентов лечением.
Было проведено простое открытое наблюдательное сравнительное исследование.
Критерии включения:
возраст от 18 до 65 лет;
установленные диагнозы по МКБ-10:
J02.9 Острый фарингит неуточненный,
J03.9 Острый тонзиллит неуточненный;
отрицательный результат экспресс-диагностической системы для определения in vitro В-гемолитического стрептококка группы А (БГСА);
подписанное пациентом информированное согласие.
Критерии невключения:
инфекционно-воспалительные заболевания, требующие назначения системной антибактериальной терапии или госпитализации;
аксиллярная температура тела >38,0°С на визите скрининга;
положительный результат экспресс-диагностической системы для определения in vitro БГСА;
наличие признаков дифтерии, включая наличие пленок и налетов на слизистой оболочке задней стенки глотки и гортани;
осложненное течение основного заболевания: паратонзиллярный абсцесс, паратонзиллит, парафарингит, гнойный медиастинит, тонзиллярный сепсис;
наличие признаков хронического фарингита / хронического тонзиллита, включая кардиотонзиллярный синдром в анамнезе и/или на момент включения в наблюдение;
травма и/или ожог ротоглотки, в том числе свежие раны в полости рта и горла, в том числе сразу после челюстно-лицевой операции, стоматологических процедур на момент включения в исследование и не ранее 3 мес. до включения в исследование;
наличие признаков поражения гортани, включая стеноз, а также эпиглоттит;
наличие налетов в области гортани;
лечение любым из антибактериальных препаратов системного действия или топических антибактериальных и/или антисептических препаратов в течение 14 дней до момента включения в исследование;
применение глюкокортикостероидных препаратов;
указание на наличие аллергических заболеваний, отягощенный аллергологический анамнез, повышенную чувствительность или непереносимость компонентов исследуемых препаратов;
участие пациента в любом другом клиническом исследовании в течение 3 мес. до включения в исследование;
вакцинация больного за 14 дней до включения в исследование;
беременность или период грудного вскармливания;
наличие подозрений или указаний на диагностированные острые, хронические (включая обострение, нестабильность течения и декомпенсацию) заболевания, выраженность проявлений которых препятствует участию в клиническом исследовании, влияет на проявление и течение ОТФ, затрудняет правильную верификацию и интерпретацию данных, оцениваемых в настоящем исследовании, приводит к невозможности проведения процедур в рамках настоящего исследования или представляет опасность для пациента при его участии в наблюдательном исследовании;
прочие условия, которые, по мнению врача-исследователя, препятствуют включению пациента в исследование.
Критерии исключения из исследования:
невозможность или отказ (отзыв согласия) пациента продолжать участие в исследовании;
желание пациента досрочно завершить исследование по причине неэффективности терапии или любой иной причине;
случаи, не оговоренные протоколом, когда исследователь считает, что дальнейшее участие пациента в исследовании наносит ему вред;
ошибочное включение непригодного к участию в исследовании пациента.
Пациентов рандомизировали в 2 группы наблюдения поочередно по мере включения в исследование. В основной группе (n=30) пациенты орошали слизистую оболочку ротоглотки спреем для полости рта Панавир Инлайт® по 4 дозы 5 раз в день в течение 7 дней. При стихании воспалительных явлений пациентам разрешалось после 5-го дня прекращать лечение. Жаропонижающие и обезболивающие препараты — по необходимости.
В контрольной группе (n=30) больные орошали слизистую оболочку ротоглотки бензидамином в форме спрея по 4 дозы 5 раз в день в течение 7 дней. При стихании воспалительных явлений пациентам также разрешалось после 5-го дня прекращать лечение. Жаропонижающие и обезболивающие препараты — по необходимости.
Дизайн исследования
Визит 1. Первичное обследование. 0(1) день. Первичный осмотр. Сбор анамнеза и жалоб больного. Оценка клинических проявлений заболевания, лабораторных и инструментальных методов исследования с учетом критериев включения и невключения в исследование. Подпись согласия на участие в исследовании, распределение пациентов по группам терапии. Анализ субъективной оценки пациентом своего самочувствия (шкала боли, шкала общего самочувствия). Забор биоматериала (мазок-отпечаток с поверхности слизистой оболочки задней стенки ротоглотки).
Визит 2. 3±1 день лечения. Промежуточный осмотр. Анализ клинических показателей течения заболевания. Анализ объективной оценки состояния (отек, гиперемия) и субъективной оценки пациентом своего самочувствия (шкала боли, шкала общего самочувствия). Оценка переносимости исследуемого средства, описание характера побочных явлений при их наличии.
Визит 3. 7±1 день лечения. Контрольное обследование. Анализ клинических показателей течения заболевания. Анализ объективной оценки состояния (отек, гиперемия) и субъективной оценки пациентом своего самочувствия (шкала боли, шкала общего самочувствия). Забор биоматериала (мазок-отпечаток с поверхности слизистой оболочки задней стенки ротоглотки). Оценка переносимости исследуемого средства, описание характера побочных явлений при их наличии.
Визит 4. 14±2 день лечения. Заключительный день. Телефонный контакт.
Объективный осмотр включал в себя оценку общего состояния пациента и подробный специализированный осмотр ЛОР-органов. Врачебный осмотр проводился в полном объеме на всех очных визитах. При объективном осмотре пациента (мезофарингоскопия) врач отмечал наличие изменений по балльной системе. Гиперемия слизистой оболочки ротоглотки оценивалась от 0 баллов (отсутствие) до 3 баллов (сильно выраженная). Отечность слизистой оболочки ротоглотки оценивалась от 0 баллов (отсутствие) до 3 баллов (сильно выраженная).
В соответствии с протоколом проводимого наблюдательного исследования дневник пациента выдавался участнику на визите 1 вместе с инструкцией по его заполнению. На визите 2 врач-исследователь проводил проверку правильности заполнения дневника. На визите 3 участник исследования возвращал врачу-исследователю заполненный дневник. Для оценки самочувствия пациенты заполняли визуально-аналоговые шкалы (ВАШ) по оценке боли в горле в покое / при глотании: от 0 баллов — отсутствие боли до 10 баллов — очень сильная боль. Внесение пациентом данных в дневник самонаблюдения проводилось в 08:00 до применения препарата в этот день.
Проведение дополнительных методов обследования: цитоморфометрия мазков-отпечатков из очага воспаления. Для оценки степени деструкции эпителия слизистой оболочки в очаге воспаления в ротоглотке и на небных миндалинах, а также выраженности воспаления на каждом очном визите осуществлялся забор биоматериала (мазок-отпечаток), который наносился на предметные стекла, в дальнейшем в лаборатории специальным образом окрашивался. Специалистом-цитологом проводилась цитоморфометрия с определением: морфологических критериев деструкции эпителиальных клеток по классам, среднего показателя деструкции клеток.
Критерии эффективности
Первичные критерии:
Доли пациентов, у которых наблюдали терапевтический ответ на визитах 2 и 3 (исчезновение всех исходных и отсутствие появления новых признаков, оцениваемых по данным мезофарингоскопии и дневникам самонаблюдения).
Вторичные критерии:
среднее изменение суммарного показателя жалоб, специфических для ОТФ, на визитах 2 и 3 по сравнению с исходным уровнем;
среднее изменение суммарного показателя местных признаков воспаления, в том числе по данным мезофарингоскопии, на визитах 2 и 3 по сравнению с исходным уровнем;
среднее изменение суммарного показателя жалоб, специфических для ОТФ, на 3, 5, 7-й день лечения по данным дневника самонаблюдения по сравнению с исходным уровнем;
средние изменения цитоморфометрических показателей на визите 3 по сравнению с исходным уровнем.
Таким образом, клиническая эффективность оценивалась по изменениям суммарного значения субъективных и объективных критериев.
Переносимость терапии оценивали и врач, и пациент.
Для оценки безопасности выявляли наличие у больного любых нежелательных или непредвиденных симптомов, жалоб, заболеваний, возникших на фоне применения исследуемых средств. Побочные реакции фиксировались пациентом при ведении дневника самоконтроля и лечащим врачом при очередных обследованиях.
Данные представлены в виде среднего и стандартного отклонения или n (%).
Результаты и обсуждение
Распределение больных по полу и возрасту в группах представлено в таблице 1.

Возраст пациентов варьировал в диапазоне от 18 до 53 лет, преобладали женщины. Распределение больных по полу и возрасту в клинических группах было сопоставимым. Все пациенты завершили участие в исследовании в соответствии с протоколом.
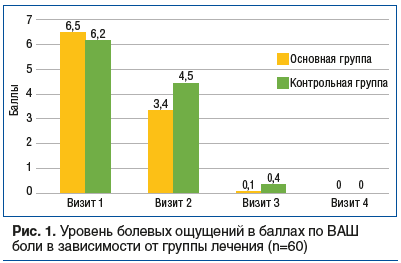
На визите 1 в день 0(1) в обеих группах все пациенты отметили по ВАШ ощущение боли и/или дискомфорта в горле разной степени выраженности — от 3 до 8 баллов. В основной группе в среднем 6,5±1,5 балла, в контрольной группе в среднем 6,2±1,4 балла.
На визите 2 на 3±1 сутки все пациенты отметили улучшение состояния по сравнению с первым визитом: в основной группе по ВАШ в среднем 3,4±1,3 балла, в контрольной группе — 4,5±1,4 балла.
На визите 3 в день 7±1 во всех группах наблюдалась положительная динамика и купирование болевых ощущений. Но часть пациентов отмечала остаточные явления дискомфорта в горле (ВАШ не более 2 баллов): в основной группе таких больных было 3 (10%), в контрольной группе — 8 (26,7%) человек (рис. 1).
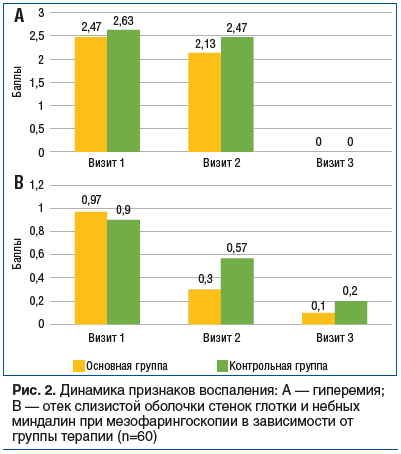
В основной группе на визите 1 у всех 30 пациентов отмечена гиперемия слизистой оболочки задней стенки глотки и небных миндалин (2–3 балла); у 19 человек — отечность слизистой оболочки задней стенки глотки и небных миндалин (1–2 балла). Во время второго визита у 11 пациентов отмечалась гиперемия слизистой оболочки задней стенки глотки и небных миндалин, которую мы оценили в 3 балла; у 12 пациентов сохранялась незначительная гиперемия (2 балла); минимальные изменения (1 балл) отмечены у 7 больных. У 8 человек сохранялась отечность слизистой оболочки задней стенки глотки и небных миндалин (1–2 балла). К визиту 3 гиперемия слизистой оболочки задней стенки глотки и небных миндалин отсутствовала у всех пациентов; у 3 пациентов сохранялась незначительная отечность слизистой оболочки задней стенки глотки и небных миндалин (1 балл).
В контрольной группе на визите 1 у всех пациентов отмечена гиперемия слизистой оболочки задней стенки глотки и небных миндалин (2–3 балла); у 17 — отечность слизистой оболочки задней стенки глотки и небных миндалин (1–2 балла). На визите 2 у 19 пациентов отмечалась гиперемия слизистой оболочки задней стенки глотки и небных миндалин, которую мы оценили в 3 балла, у 6 пациентов сохранялась умеренная гиперемия слизистой оболочки задней стенки глотки и небных миндалин (2 балла), у остальных наблюдалась незначительная гиперемия (1 балл); у 11 пациентов сохранялась отечность слизистой оболочки задней стенки глотки и небных миндалин (1–2 балла). К визиту 3 симптомы воспаления в глотке при мезофарингоскопии отсутствовали у 26 пациентов, у 4 больных сохранялась незначительная отечность слизистой оболочки задней стенки глотки и небных миндалин (1 балл) (рис. 2).
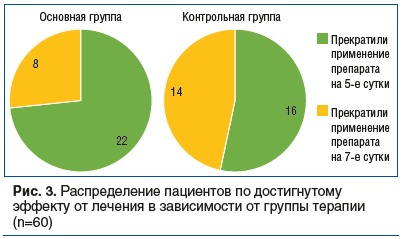
В основной группе 22 (73,3%) пациента прекратили прием препарата после 5 дней лечения в связи с отсутствием болевого синдрома и уменьшением воспаления, 8 (26,7%) пациентов продолжили прием препарата до 7 дней. Средняя длительность лечения составила 5,53±0,90 дня.
В контрольной группе 16 (53,3%) пациентов прекратили прием препарата после 5 дней лечения в связи с уменьшением воспаления и отсутствием болевого синдрома, 14 (46,7%) пациентов продолжили прием препарата до 7 дней. Средняя длительность лечения составила 5,93±1,01 дня.
Использование спрея для полости рта Панавир Инлайт® позволило сократить продолжительность курсового лечения по сравнению с контрольной группой: почти у 1/3 пациентов длительность применения средства была на 2 сут меньше. У 22 (73%) больных из 30 в основной группе к 5-му дню от начала лечения отмечено клиническое выздоровление.
Результаты лечения в исследуемых группах больных представлены на рисунке 3.
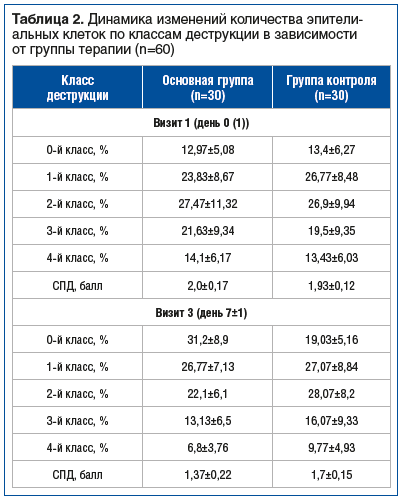
Результаты цитоморфометрии продемонстрировали, что при первичном обследовании на визите в день 0(1) наблюдалась повышенная частота выявления эпителиальных клеток, имеющих признаки деструкции, что соответствует воспалительным изменениям. Затем во время процесса выздоровления, стихания воспалительных явлений и репарации поврежденной слизистой закономерно снижалось количество клеток, имеющих признаки повреждения, параллельно с увеличением доли неповрежденных клеток. При этом в основной группе отмечалось более значительное снижение доли поврежденных клеток и преобладание клеток, полностью лишенных признаков повреждения. Процессы репарации в основной группе происходили быстрее по сравнению с группой контроля. Таким образом, можно считать, что в основной группе к 7-му дню от начала терапии завершались репаративные процессы и восстановление слизистой оболочки задней стенки глотки.
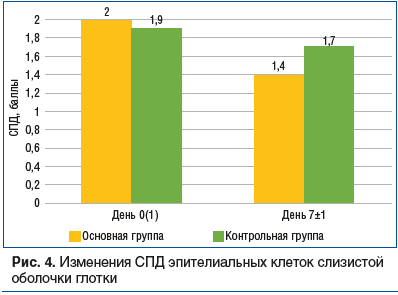
Распределение эпителиальных клеток в зависимости от класса деструкции [10] представлено в таблице 2. Значения среднего показателя деструкции (СПД) также снижались на фоне проводимой терапии, динамика между визитами и сравнительная характеристика в зависимости от группы терапии отражена на рисунке 4.
Для большей наглядности продемонстрируем варианты мазков-отпечатков пациентов на 7-й день лечения (рис. 5).

В основной группе нежелательных явлений и аллергических реакций не отмечено. В контрольной группе 8 (26,7%) пациентов отмечали незначительное ощущение сухости при использовании препарата. В основной группе назначение дополнительных препаратов, в том числе системных антибиотиков, не понадобилось. Переносимость препарата исследования была хорошей.
Преимуществом данного исследования является адаптирование опыта применения анализа воспалительных изменений с помощью цитологического исследования (цитоморфометрии) слизистой оболочки полости рта [10] к слизистой оболочке ротоглотки. Это позволяет более комплексно оценивать динамику воспалительного процесса (субъективно и объективно), а значит, и эффективность назначенной терапии. Для того чтобы избавиться от ряда ограничений проведенного исследования и повысить его научную значимость, в будущем можно увеличить размер выборки и провести статистический анализ полученных данных.
Заключение
Применение спрея для полости рта Панавир Инлайт® продемонстрировало высокую эффективность в лечении острых воспалительных заболеваний глотки. Все пациенты отмечали улучшение самочувствия и снижение болевых ощущений уже после начала терапии. Нежелательных явлений и аллергических реакций отмечено не было. Применение данного препарата в остром периоде заболевания позволяет достичь более быстрого и выраженного восстановления поврежденной воспалением слизистой оболочки глотки, что доказано проведением цитоморфометрии и динамическим снижением среднего показателя деструкции эпителия. К 7-му дню от начала лечения практически у всех пациентов основной группы отмечено полное восстановление слизистой оболочки после перенесенного эпизода вирусной инфекции.
[1] Устойчивость к антибиотикам. (Электронный ресурс.) URL: https://www.who.int/ru/news-room/fact-sheets/detail/antibiotic-resistance (дата обращения: 24.12.2024).
материал rmj.ru
