Содержание статьи
Введение
На сегодняшний день проблема нарушения сердечного ритма продолжает оставаться актуальной для современной медицинской науки в целом и фармакологии в частности. В первую очередь это связано с рядом факторов:
высокий процент аритмий как причин внезапной сердечной смерти (ВСС) у больных сердечно-сосудистыми заболеваниями (ССЗ) [1];
трудность контроля наступления жизнеугрожающих эпизодов аритмии без имплантационных пособий (дефибриллятор, кардиовертер и т. д.);
сложность оценки соотношения риск/польза при назначении антиаритмических препаратов, высокая цена «терапевтической ошибки».
Одна из наиболее частых причин жизнеугрожающих аритмий у взрослых — ишемическая болезнь сердца (ИБС). Несмотря на то, что в структуре причин ВСС доля ИБС составляет около 80% [1, 2], до сих пор нет однозначно эффективного решения проблемы предотвращения аритмий ишемического генеза.
При этом именно желудочковые аритмии ишемического генеза наиболее опасны в отношении развития фатальных событий — летальность в группе больных ИБС с нагрузочными аритмиями в 3 раза выше в сравнении с теми, у кого аритмий при физической нагрузке не было [3].
Компенсация энергодефицита миокарда как возможный компонент антиаритмической терапии
Формирование аритмогенного очага при ИБС — крайне сложный процесс. Примечательно, что в ходе исследований, изучающих электрофизиологические механизмы нарушений ритма ишемического генеза, применение антиаритмических препаратов I и III класса не сопровождалось снижением как общей смертности, так и частоты ВСС. Вероятно, это объясняется тем, что антиаритмическая терапия в данном случае является симптоматической, не воздействующей на патогенетическую основу аритмии [4]. Очевидно, что помимо сдвигов в нервной и гуморальной регуляции развитие желудочковых аритмий обусловлено каскадом нарушений энергетического обмена в миокарде. Гипоксические и метаболические нарушения, возникающие в лишенном доступа кислорода миокарде, запускают цепь аритмического механизма: гипоксия → снижение уровня синтеза АТФ → торможение активности внутриклеточных ферментов → нарушение трансмембранного переноса электролитов (K, Са, Na) → нарушение процессов активации и проведения электрического импульса в миокарде → возникновение атипичных очагов возникновения сердечного импульса → аритмия. В этой связи оптимизация метаболизма в кардиомиоцитах, функционирующих в условиях дефицита кислорода и образующих очаг ишемических аритмий, выглядит перспективным решением с точки зрения нормализации их электрофизиологического состояния и, соответственно, клинического течения нарушений сердечного ритма.
Важнейшим аргументом в пользу доказательства прямой зависимости степени тяжести аритмий от энергодефицита в кардиомиоцитах стало исследование, проведенное учеными Университета Джона Хопкинса [5]. Оригинальная методика, разработанная ими (магнитно-резонансная томография с магнитно-резонансной спектроскопией фосфора (31 P)) позволила неинвазивным путем определять уровень АТФ в сердечной мышце. В ходе 10-летнего наблюдения за пациентами с установленными кардиовертерами-дефибрилляторами было выявлено, что люди с низким содержанием внутрисердечного АТФ имели примерно в 3 раза более высокий риск ВСС.
Чаще всего при ишемии миокарда возникают желудочковые аритмии по типу экстрасистолии, в зависимости от группировки и числа которых определяется тяжесть аритмии (так называемая Lown-Wolf классификация) [6].
Возможность фармакологически повлиять на предотвращение атипичных импульсов появилась с применением нескольких классов антиаритмических препаратов, различных по механизму действия. Принципиальное их действие оценивается как антиаритмическая эффективность, показывающая, во сколько раз снижается число аритмий на фоне приема отдельного препарата. Главная трудность применения антиаритмических препаратов — оптимальный подбор дозы таким образом, чтобы, с одной стороны, снизить число аритмий до минимально возможного предела (в идеале купировать полностью), с другой — избежать серьезных побочных реакций (наиболее часто это возникновение блока проведения сердечного импульса). В итоге антиаритмические препараты должны максимально подавлять аритмии, увеличивать продолжительность и улучшать качество жизни пациентов, поэтому и в настоящее время продолжается активный поиск безопасных и лишенных побочного действия препаратов и их комбинаций для лечения аритмий.
Включение в терапию цитопротективных препаратов (в том числе этилметилгидроксипиридина сукцината — ЭМГПС) позволяет расширить возможности современных антиаритмических средств. Связано это, главным образом, с уменьшением влияния на сердечную проводимость патологических факторов гипоксии и свободнорадикального окисления.
Данные клинических исследований
В клинических исследованиях, проведенных в НМИЦ им. В.А. Алмазова в период с 2008 по 2016 г., оценили возможность ЭМГПС влиять на электрическую стабильность ишемизированного миокарда и, соответственно, на частоту и градацию нарушений ритма. Для определения ишемического генеза нарушений ритма использовали суточное ЭКГ-мониторирование и тредмил-тест. Специализированные методики эмиссионной кардиотомографии позволили исследователям топологически соотнести ишемический очаг с зоной аритмической активности [2, 4, 7, 8].
Проведенная 2-месячная терапия капсульной формой ЭМГПС (Мексикор®, ООО «ЭкоФармИнвест») показала, что его антиаритмическая эффективность в отношении ишемических аритмий оказалась выше, чем в отношении неишемических, практически на порядок (рис. 1) [2].
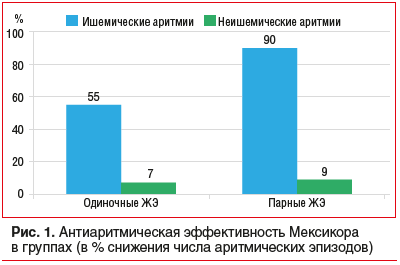
В абсолютном выражении количество одиночных желудочковых экстрасистолий (ЖЭ) в группе пациентов, получавших ЭМГПС, снизилось в среднем в 2,8 раза, а парных — в 3 раза (р<0,05), при отсутствии статистически значимых изменений в контрольной группе (рис. 2) [7].
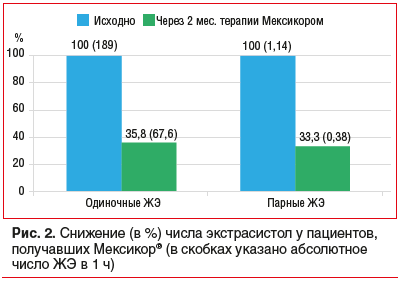
У всех пациентов, получавших ЭМГПС, в динамике по данным позитронной эмиссионной томографии (ПЭТ) в зонах миокарда с транзиторной ишемией наблюдался статистически значимый прирост процента выведения 11С-бутирата натрия (11С-БН), свидетельствующий о повышении эффективности энергетического метаболизма в участках гипоксии миокарда. У 5 из них профиль выведения 11C-БН из миокарда достиг значений, соответствующих значениям в интактных сегментах сердечной мышцы [2].
Ниже представлены сканограммы теста у пациента 56 лет с ЖЭ и эпизодами неустойчивой желудочковой тахикардии (рис. 3). Через 2 мес. после начала терапии ЭМГПС при холтеровском мониторировании наблюдалось значимое уменьшение количества и комплексности ЖЭ, в том числе одиночных полиморфных ЖЭ, с 16 453 до 1528 в сутки (на 91%); парных полиморфных — с 172 до 17 в сутки (на 90%). Антиаритмический эффект в виде снижения числа эпизодов нарушений ритма высокой комплексности также подтверждался результатами велоэргометрии при достижении субмаксимальной частоты сердечных сокращений [8].
![Рис. 3. Визуализация улучшения метаболизма жирных кислот в миокарде методом ПЭТ с 11С-БН [8] Рис. 3. Визуализация улучшения метаболизма жирных кислот в миокарде методом ПЭТ с 11С-БН [8]](https://medblog.su/wp-content/uploads/2023/12/1703033138_490_Sovremennyj-podhod-k-optimizatsii-antiaritmicheskoj-terapii-Vozmozhnosti-etilmetilgidroksipiridina-suktsinata.png)
Как показали исследования О.А. Котлярова [9], нормализация метаболического баланса миокарда позитивным образом влияет не только на процесс формирования (проявляющийся снижением эктопической активности), но и на проведение внутрисердечного импульса. Установлено, что прием ЭМГПС (внутривенно в дозе 300 мг в течение 10 сут) пациентами с брадиаритмиями достоверно улучшает автоматическую активность синусового узла и проводимость в атриовентрикулярном узле. Так, к 10-му дню лечения время восстановления функции синусового узла уменьшилось на 14% (p=0,005), корригированное время восстановления функции синусового узла — на 25% (p=0,0008), а точка Венкебаха, характеризующая проводимость в атриовентрикулярном узле, увеличилась на 7% (p=0,06).
Эффект, достигаемый при назначении ЭМГПС при ишемических аритмиях, в полной мере реализуется и при совместном назначении с β-адреноблокаторами, в частности метопрололом. Проведенные исследования позволили установить наиболее характерные аспекты этого взаимодействия [10, 11].
В нашем исследовании, проведенном на базе ОБУЗ «КГКБСМП», было установлено, что после проведенного в течение 1 мес. лечения больных ИБС, стенокардией напряжения III–IV ФК в группе, получавшей ЭМГПС в дополнение к основной терапии метопрололом, в сравнении с контрольной группой, получавшей только метопролол, частота одиночных ЖЭ статистически значимо уменьшилась соответственно на 90 и 60%, парных ЖЭ — на 96,5 и 75%, групповых ЖЭ — на 94 и 56% (р<0,05) (рис. 4). Выявлено, что наибольшее антиаритмическое воздействие ЭМГПС в данной комбинации оказывает в предутренние и дневные часы.
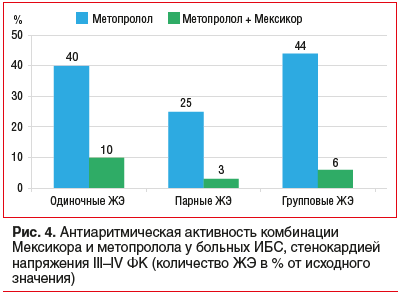
В группе пациентов со стабильной стенокардией в сочетании с постинфарктным кардиосклерозом также выявлено значительное усиление антиаритмического эффекта β-адреноблокатора при добавлении к лечению ЭМГПС, что проявлялось в купировании парных, групповых ЖЭ, а также пароксизмов неустойчивой желудочковой тахикардии. В контрольной группе данный вид аритмии сохранялся на протяжении всего исследования.
Для оценки антиаритмического эффекта также была проведена оценка показателя SDNN (Standart deviation NN — квадратный корень из разброса интервалов RR). Этот показатель зависит от баланса активности симпатического и парасимпатического отделов вегетативной нервной системы и является интервальным показателем, характеризующим вариабельность ритма сердца, его низкие (менее 30 мс) значения прогностически неблагоприятны в плане развития внезапных фатальных нарушений ритма. Присоединение к базовой терапии метопрололом ЭМГПС в течение 1 мес. привело к достоверному увеличению параметра SDNN в группе ЭМГПС + мексикор на 56% (р<0,05), тогда как в группе, получавшей только метопролол, статистически значимых изменений не было (по отношению к исходным данным).
Снижение эктопической активности в миокарде при лечении пациентов с ИБС с применением ЭМГПС коррелирует со снижением патологической активности компонентов перекисного окисления липидов. На фоне терапии ЭМГПС в течение 1 мес. отмечалось снижение концентрации диеновых конъюгатов на 37% (р<0,05), содержание маркера оксидативного стресса — малонового диальдегида уменьшилось на 30% (р<0,05). Низкий уровень диеновых конъюгатов сохранялся в течение 2 мес. после отмены препарата [10, 11].
Выраженное антиоксидантное действие ЭМГПС играет значительную роль в профилактике аритмических нарушений и при острых формах кардиальной ишемии. Так, по данным С.А. Бойцова [12], применение ЭМГПС в остром периоде инфаркта миокарда позволило к 14-м суткам терапии снизить общее число ЖЭ в 3,8 раза, тогда как в контрольной группе (не получавшей ЭМГПС) показатель снизился только в 2 раза. Количество наджелудочковых экстрасистолий (НЖЭ) также существенно сократилось в основной группе — в 3,1 раза, в то время как в контрольной выросло на 14,7% (рис. 5).
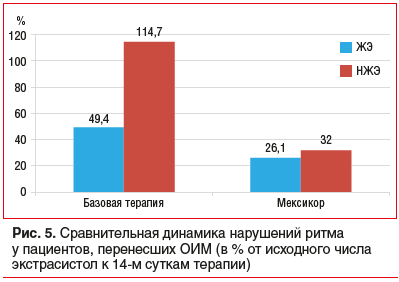
Аспект применения ЭМГПС для профилактики нарушений ритма при лечении инфаркта миокарда, очевидно, имеет важнейшее значение в плане защиты от реперфузионных нарушений после реканализации инфаркт-ответственной артерии в связи с выраженным антиоксидантным и кардиопротективным действием препарата [13].
Применительно к кардиоинвазивным пособиям интересен опыт Н.В. Лапшиной, применявшей ЭМГПС для профилактики рецидивов фибрилляции предсердий (ФП) после радиочастотной изоляции устьев легочных вен (РЧИ УЛВ) [14]. В исследование были включены 76 пациентов (разделенных на две группы) с пароксизмальной и длительно персистирующей ФП после успешно проведенной РЧИ УЛВ. В первой группе наблюдались 38 пациентов, получавших Мексикор® в/в капельно по 400 мг в течение 2 сут после операции, затем в течение 1 мес. перорально в капсулах по 100 мг 3 р/сут. Антиаритмическая терапия у 10 (26,3%) пациентов проводилась амиодароном с β-адреноблокаторами, у 12 (31,6%) — пропафеноном в дозе 450 мг/сут, у 16 (42,1%) — сотагексалом по 160 мг/сут. Вторая (контрольная) группа состояла также из 38 пациентов. В ней 12 (31,6%) человек в течение 6-месячного периода наблюдения получали амиодарон и β-адреноблокаторы, 14 (36,8%) — пропафенон, 12 (31,6%) — сотагексал. Применение ЭМГПС позволило значимо уменьшить количество рецидивов ФП. Так, рецидивы ФП в первой группе были зарегистрированы только у 10 пациентов в течение 1 мес. после РЧИ УЛВ, во второй группе — у 27 пациентов (р=0,001). После 3 мес. наблюдения в первой группе рецидивы ФП были отмечены у 8 человек, во второй группе — у 16 (р<0,05). Спустя полгода после оперативного вмешательства тенденция сохранилась: рецидивы ФП зафиксировали у 8 и 13 человек из первой и второй групп соответственно, хотя это различие и не было статистически значимым (р>0,05). Достоверно определяемое снижение количества рецидивов ФП после РЧИ УЛВ позволило исследователям рекомендовать ЭМГПС в качестве вспомогательной терапии для повышения эффективности данной методики.
Отдельного внимания заслуживает возможность применения Мексикора в комплексе профилактики аритмических эпизодов у больных ССЗ, перенесших новую коронавирусную инфекцию.
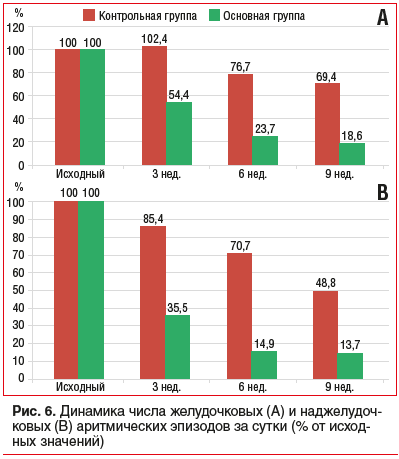
В 2021 г. на базе ОБУЗ «КГКБСМП» нами было проведено рандомизированное контролируемое исследование эффективности ЭМГПС в периоде реабилитации 48 пациентов с артериальной гипертензией (АГ) II стадии, перенесших новую коронавирусную инфекцию средней степени тяжести с явлениями вегетативной дистонии, у которых в доковидный период по данным анамнеза и амбулаторной карты значимых нарушений сердечного ритма не отмечалось. Пациенты были рандомизированы в 2 группы по 24 человека. В основной группе базовое лечение АГ и постковидного синдрома было дополнено цитопротектором в течение 9 нед. — ЭМГПС (Мексикор®) 400 мг/сут, контрольная группа получала только базовую терапию (рамиприл 5–10 мг/сут, индапамид ретард 1,5 мг/сут, апиксабан 5 мг/сут). Применение ЭМГПС в значительно большей степени позволило лучше контролировать аритмические нарушения, как желудочковые, так и суправентрикулярные. Сокращение общего числа желудочковых нарушений ритма в основной группе было более выраженным (больше чем в 2 раза), чем в контрольной группе (к концу наблюдения число ЖЭ сократилось на 81,4 и 30,6% соответственно р<0,05) (рис. 6А). Кроме того, применение ЭМГПС позволило более чем в 24 раза сократить число угрожающих парных и групповых аритмий (в контрольной группе — в 14,4 раза, р<0,05). Сходная динамика наблюдалась и в отношении наджелудочковых аритмических эпизодов, число которых у пациентов, принимавших ЭМГПС, сократилось в 7,3 раза от исходного, тогда как в контрольной группе — только в 2,04 раза (р<0,05) (рис. 6B).
Применение ЭМГПС, таким образом, обеспечило лучшее восстановление электрической стабильности миокарда при постковидной реабилитации кардиологических пациентов по сравнению с контрольной группой. По данным объективных методов исследования, это выразилось в кратной разнице уменьшения числа эпизодов нарушений ритма в сравниваемых группах.
Заключение
Сочетание двухкомпонентного (антиоксидантного и антигипоксантного) действия ЭМГПС делает его высокоэффективным элементом фармакотерапии при нарушениях сердечного ритма. Определяющим фактором для его применения является ишемический генез аритмии, который может быть объективно установлен современными методами диагностики.
Имеющиеся исследовательские данные свидетельствуют о существенном влиянии ЭМГПС на частоту аритмических эпизодов (прежде всего ЖЭ) и их градацию при ИБС, что прогностически благоприятно как при острых, так и при хронических формах ИБС. Примечательно, что при приеме ЭМГПС значимые нежелательные явления не регистрировались.
В этой связи ЭМГПС может оказать позитивное влияние на течение и исход кардиологической патологии, сопровождающейся нарушениями сердечного ритма, в том числе как компонент вспомогательной терапии при проведении кардиоинвазивных манипуляций (реканализация инфаркт-ответственной артерии при инфаркте миокарда, РЧИ УЛВ при ФП), реабилитации пациентов с ССЗ, перенесших новую коронавирусную инфекцию.
Конфликт интересов
Статья подготовлена при поддержке ООО «ЭкоФармИнвест».
Информация с rmj.ru






