Введение
Хронический тонзиллит (ХТ) — инфекционно-аллергическое заболевание с локализацией хронического очага инфекции в небных миндалинах [1]. Анатомически и топографически небные миндалины взаимодействуют с жизнеобеспечивающими органами. [2] Особенности анатомического строения небных миндалин предрасполагают к развитию в них хронического воспаления, способствуют нарушению иммунной функции, что делает миндалины источником хронической инфекции, тонзиллогенной интоксикации и аллергизации организма [2, 3]. В связи с этим неоднократно была доказана важнейшая роль ХТ в развитии многих заболеваний органов и систем. Кроме того, ХТ может осложнять течение хронических заболеваний, особенно в период его обострения [4]. В первой классификации ХТ, предложенной Л.А. Луковским, были выделены компенсированная, субкомпенсированная и декомпенсированная формы ХТ. Авторы многих последующих классификаций ХТ повторили аналогичное деление в разных интерпретациях, исходя из симптомов заболевания, но не оценивая при этом патогенетическую связь реактивности организма и тонзиллогенных токсико-аллергических процессов, а также связь этиологических и патогенетических факторов ХТ и протекающих одновременно с ним заболеваний. В практике врача-оториноларинголога в последнее время используются 2 классификации ХТ. В классификации И.Б. Солдатова выделяют компенсированную и декомпенсированную формы. Компенсированная форма проявляется лишь местными воспалительными признаками, а декомпенсированная, кроме местных признаков, сопровождается явлениями декомпенсации и распространения патологического процесса за пределы ткани небных миндалин в виде паратонзиллитов, паратонзиллярных абсцессов, частых повторных обострений (ангин), а также различных метатонзиллярных осложнений (эндокардит, миокардит, гломерулонефрит (ГН), заболевания щитовидной железы и кожи, полиартрит и др.). В классификации Б.С. Преображенского, дополненной В.Т. Пальчуном, выделяют простую форму ХТ и токсико-
аллергическую (ТАФ), которую делят на ТАФ I и ТАФ II. У 96% больных обострения ХТ проявляются в виде ангин, однако у 4% пациентов встречается безангинная
форма ХТ [1, 5, 6]. К сожалению, зачастую многие оториноларингологи для выбора тактики ведения больных с хронической тонзиллярной патологией руководствуются исключительно признаками фарингоскопической картины. ТАФ I проявляется местными признаками простой формы ХТ (казеозное отделяемое, жидкий или густой гной в лакунах миндалин, признаки Зака, Гизе и Преображенского, рубцовые изменения миндалин и окружающих тканей, увеличение регионарных лимфоузлов) и общими умеренно выраженными токсико-аллергическими реакциями (ТАР). Тонзиллогенные ТАР выражаются в периодических недомогании, слабости, быстрой утомляемости, сниженной трудоспособности, субфебрилитете, функциональных нарушениях сердечно-сосудистой системы, могут наблюдаться при нагрузке и в покое, в период обострения ХТ. Кроме этого, при периодических суставных болях и ломоте в лабораторных показателях могут появляться изменения, указывающие на воспаление. Форма ТАФ II характеризуется как местными, так и общими признаками простой формы ХТ и ТАФ I, а также выраженными ТАР. При выявлении заболеваний, объединенных с ХТ единым инфекционным фактором, диагностируется II степень. При II степени ХТ является постоянным активным очагом инфекции, а небные миндалины — источником токсинов, вызывающих интоксикацию организма. Наиболее целесообразной тактикой при ТАФ II служит тонзиллэктомия. Основанием для консервативного, а не хирургического лечения при этой форме ХТ могут быть только абсолютные противопоказания к операции (тяжелые соматические заболевания, в т. ч. заболевания системы крови) [1, 7–10]. При этом в отношении общей, сопряженной с ХТ патологии до настоящего времени нет полной определенности в понимании проблемы и ее оценке. А между тем именно диагностика сопряженной с ХТ патологии лежит в основе определения формы ХТ и, следовательно, выбора адекватной тактики ведения пациента, выбора между возможностью консервативной терапии и необходимостью хирургического лечения [11, 12]. Стоит отметить, что общие, сопряженные с ХТ заболевания могут проявиться всего лишь после одного случая ангины. Как правило, диагностика ХТ не вызывает затруднений. Однако необходимо отметить, что в случаях с сопряженными заболеваниями фарингоскопические признаки ХТ могут быть выражены минимально. По данным ВОЗ, около 100 заболеваний могут быть сопряжены с ХТ [5, 13].
При оценке патологии мочевыделительной системы как осложнения хронического воспаления небных миндалин возникают некоторые диагностические трудности, т. к. нет единого взгляда на патогенез поражения почек при ХТ. Кроме того, врачи терапевтических специальностей, за исключением нефрологов, зачастую не связывают выявленные изменения в анализах мочи с хронической тонзиллярной патологией. Поражение почек в виде ГН является наиболее сложным, резистентным к терапии, склонным к хронизации и частым исходам в терминальную стадию хронической почечной недостаточности (ХПН). ГН развивается в связи с хроническим или острым инфекционным процессом стрептококковой этиологии. В патогенезе ГН выделяют, как правило, иммунопатогенетический механизм воспаления в ответ на развитие стрептококковой инфекции, в т. ч. в небных миндалинах. Кроме этого, ГН может развиваться в результате воздействия на гломерулярный аппарат неполноценных по структуре иммуноглобулинов класса А1 (IgA-нефропатия). Если пост-стрептококковый ГН развивается остро и относительно редко приводит к тяжелым исходам, то при IgA-нефропатии у 20–30% больных через 10 лет развивается ХПН [12]. IgA-нефропатия является вариантом мезангиопролиферативного ГН, который впервые описал Berger в 1968 г. после исследования биоптатов почек при помощи метода иммунофлюоресцентного анализа, после чего IgA-нефропатию стали называть болезнью Берже [14–16]. В настоящее время IgA-нефропатия выделяется в самостоятельную нозологию и является наиболее распространенной в мире формой первичного (идиопатического) ГН. Заболевание клинически проявляется протеинурией и гематурией и подтверждается при биопсии почки. По данным различных авторов, распространенность IgA-нефропатии варьирует в зависимости от географического региона и составляет от 10–20% в США и Европе до 40–45% в странах Азии [17–20]. Однако заболеваемость IgA-нефропатией может быть намного выше, т. к. не всем пациентам с характерной клинической картиной данного заболевания выполняется биопсия почки [15–17]. Дебют IgA-нефропатии может наблюдаться в любом возрасте, в основном пик заболеваемости приходится на второе и третье десятилетия жизни. В среднем мужчины заболевают в 2 раза чаще женщин. Доказано, что 50% первичных ГН и 40% из всех заболеваний, приводящих к терминальной почечной недостаточности, — это IgA-нефропатия. В США и Западной Европе эти показатели составляют 10% и 30% соответственно [17–19]. Известно, что ХТ может способствовать прогрессированию IgA-нефропатии, усиливая иммунопатогенетический ответ [20].
Цель исследования — оценка особенностей клинического течения ХТ у пациентов с IgA-нефропатией.
Материал и методы
На кафедре оториноларингологии с клиникой ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России обследованы 111 пациентов с ХТ, обратившихся к оториноларингологу по рекомендации нефролога с целью исключения очагов хронической инфекции. Среди пациентов было 46 женщин и 65 мужчин в возрасте от 18 до 58 лет, средний возраст составил 34,5±9,3 года. У всех пациентов были проанализированы жалобы, данные анамнеза, фарингоскопическая картина с применением шкал от 0 до 3 баллов или от 0 до 1 балла. Полученные данные были занесены в таблицу, было подсчитано число пациентов по каждому балльному значению для всех исследуемых показателей и их процентное соотношение.
Результаты исследования
Пациенты оценивали выраженность жалоб по шкале от 0 до 3, где 0 — отсутствие жалобы, 1 — редкая жалоба, 2 — частая жалоба, 3 — очень частая жалоба. Среди жалоб отдельно выделялись: боль в горле, наличие казеозных пробок в миндалинах, субфебрилитет, общая слабость и неприятный запах изо рта (рис. 1).
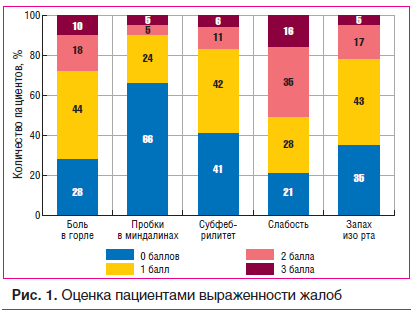
В большинстве случаев пациенты оценивали периодическую боль в горле в 1 балл (44% пациентов), казеозные пробки в миндалинах — в 0 баллов (66%), субфебрилитет — в 0 баллов (41%) и в 1 балл (42%). Почти равное число пациентов указывали на слабость и утомляемость. Выраженный запах изо рта отметили всего 0,5% пациентов, не отмечали его вовсе 35%. Таким образом, выраженные жалобы пациенты отмечали крайне редко.
С помощью анкеты и качественного анализа показателей оценен предшествующий анамнез пациентов, особое внимание уделено:
частоте ангин или обострений ХТ (0 баллов — пациент ни разу в жизни не болел ангиной, 1 балл — ангины были только в детстве или бывают менее 1 раза в год, 2 балла — ангины бывают 1–2 раза в год, 3 балла — ангины бывают более 2 раз в год);
частоте боли в горле (0 баллов — нет боли и першения в горле в течение года, 1 балл — боли бывают 1–2 раза в течение года, 2 балла — боли бывают 2–5 раз в течение года, 3 балла — постоянные боли или першение в горле);
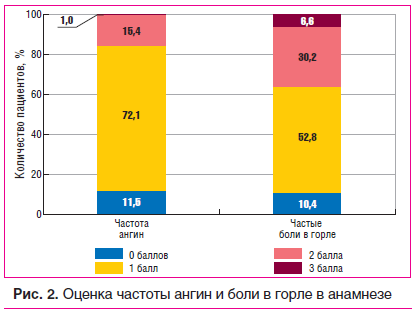
наличию в анамнезе местных осложнений ангин (паратонзиллярный абсцесс), консервативного лечения ХТ в виде промывания лакун миндалин, изменений в анализах мочи при боли в горле, периодического увеличения регионарных лимфоузлов, боли и ломоты в суставах (положительные ответы оценивались в 1 балл, отрицательные — в 0 баллов). Большинство пациентов оценили частоту ангин и болей в горле в 1 балл (72,1% и 52,8% соответственно), что указывает на минимальную выраженность местной симптоматики (рис. 2).
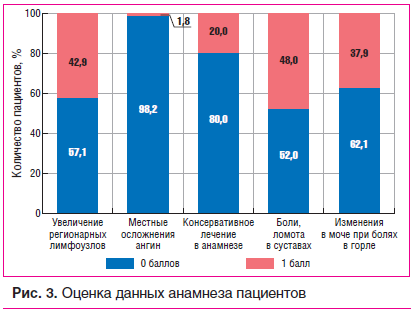
Всего 42,9% пациентов отмечали периодическое увеличение регионарных лимфоузлов; у 1 пациента в анамнезе наблюдалось осложнение ангины в виде паратонзиллярного абсцесса; 80% пациентов никогда не проводили лечение ХТ в виде промывания миндалин; 48% пациентов отмечали боль или ломоту в суставах. При расспросе выявлено, что 37,9% пациентов отмечали изменения цвета мочи или показателей в анализах мочи при болях в горле или ангинах (рис. 3).
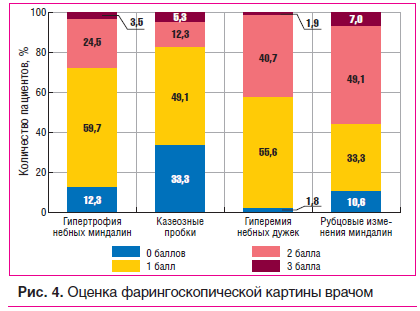
Фарингоскопическую картину мы оценивали с помощью шкалы от 0 до 3 баллов. Гипертрофия небных миндалин оценивалась в 0 баллов, если миндалины были атрофичными и не выходили за пределы небных дужек, 1 балл — гипертрофия I степени, 2 балла — гипертрофия II степени, 3 балла — гипертрофия III степени. Наличие казеозных пробок оценивалось в 3 балла, если на поверхности миндалины определялось большое количество пробок, 2 балла — единичные казеозные массы, 1 балл — если казеозные массы выявлялись только при надавливании шпателем на миндалину, 0 баллов — пробки отсутствовали. Гиперемия небных дужек оценивалась в 1 балл, если при фарингоскопии была выявлена гиперемия передних небных дужек, 2 балла — гиперемия и валикообразные утолщения передней и задней небных дужек, 3 балла — если гиперемия и утолщение дужек переходили на небный язычок. Рубцовые изменения оценивались в 1 балл, если были незначительные сращения с капсулой миндалины, 2 балла — сращение с передней или задней дужкой, 3 балла — значительные рубцовые сращения с капсулой и дужками.
При оценке фарингоскопической картины гипертрофия небных миндалин редко превышала I степень, казеозное отделяемое из лакун миндалин также было минимальным, у большинства пациентов гиперемия небных дужек соответствовала 1 и 2 баллам (55,6% и 40,7% соответственно), у многих пациентов наблюдались рубцовые изменения между капсулой миндалины и окружающими тканями (у 49,1% пациентов они оценены в 2 балла) (рис. 4).
Выводы
Таким образом, ХТ при IgA-нефропатии характеризуется стертой клинической картиной, безангинной формой, минимальными проявлениями и скудными анамнестическими данными, что зачастую затрудняет лечебную тактику.
Своевременная диагностика ХТ, особенно безангинной формы, помогает предупредить осложнения со стороны различных органов и систем.
Врачи должны проявлять настороженность по отношению к тонзиллярной инфекции у пациентов с такой патологией почек, как IgA-нефропатия, и своевременно направлять на консультацию к оториноларингологу.
материал rmj.ru
