Введение
Остеопоротические переломы костей скелета представляют собой серьезную проблему для лиц пожилого возраста. По данным отечественной литературы, патологические переломы костей среди лиц старше 50 лет встречались у 33,8% женщин и 26,9% мужчин [1]. Остеопоротические переломы тел позвонков и костей периферического скелета, как известно, приводят к длительной потере трудоспособности, а показатели смертности в течение первого года после перелома шейки бедренной кости составляют от 12 до 40%, при этом данный показатель выше у мужчин [2]. Частота переломов костей периферического скелета у мужчин значительно ниже по сравнению с женщинами, что объясняется более продолжительным пубертатным периодом, более высокой мышечной массой, низким уровнем эндокортикального ремоделирования, особенностями гормонального регулирования [3]. Однако имеются данные, что риск повторного перелома костей периферического скелета у мужчин значительно выше, чем у женщин [4], что, вероятно, обусловлено повышенной концентрацией провоспалительных цитокинов [5].
Особый интерес вызывает изучение патогенеза системного снижения костной массы и, в особенности, факторов, лежащих в его основе, что может привести к повышению риска перелома как на фоне остеопороза, так и при нормальных показателях минеральной плотности костной ткани (МПК). Как известно, снижение МПК развивается вследствие дисбаланса между костеобразованием и резорб-цией костной ткани в течение жизни [6], поэтому важно определить механизмы, поддерживающие относительный баланс этих процессов.
В данной статье обобщены сведения о системной потере костной ткани после перелома, потенциальные механизмы, вызывающие это явление, и рассмотрены отдельные факторы, влияющие на величину системной потери костной массы после перелома.
Ремоделирование кости после перелома
Несмотря на то, что костная ткань является жесткой и прочной, она биологически очень активна и постоянно модифицируется для приспособления к изменяющимся механическим нагрузкам и восстановления структуры после случившихся переломов за счет сбалансированной активности остеокластов (ОК), остеобластов (ОБ) и остеоцитов (ОЦ), образующих кость.
Ремоделирование кости — непрерывный процесс образования и резорбции костной ткани, который продолжается всю жизнь. После достижения максимальной костной массы (к 20–30 годам) устанавливаются равновесные процессы остеогенеза и резорбции, обеспечивающие постоянное обновление отдельных участков кости по всему скелету. Период обновления костной ткани в губчатых костях составляет 200 дней, из них три четверти времени — это период формирования и одна четверть — резорбция костной ткани [7].
Регенерация кости после перелома представляет собой сложный процесс. Известно, что кость — одна из немногих тканей, которые могут зажить без образования фиброзного рубца. Процессы репарации переломов традиционно протекают в определенном хронологическом порядке. Вследствие перелома и нарушения целостности сосудов образуется локальная гематома, содержащая костные и иммунные клетки, характеризующиеся высокой остео-генной активностью. Тромботическая масса, формирующая фибриновую сетку, необходима для изоляции области перелома и образования каркаса для осаждения клеток, участвующих в регенерации костной ткани. Основная роль в заживлении перелома приписывается клеткам, описанным в 1962 г. как неспециализированные клетки-остеохондропрогениторы (ОХПГ), происходящие от мезенхимальных стволовых клеток (МСК). Временное местное нарушение кровотока в зоне перелома вызывает некроз тканей, высвобождение провоспалительных цитокинов. Провоспалительные цитокины, такие как интерлейкин (ИЛ) 1β и фактор некроза опухоли альфа (ФНО-α), достигают пика концентрации в первые 4 ч после перелома, в последующие 12 ч нарастает активность ИЛ-6, а второй пик концентрации ФНО-α наблюдается через 24 ч [8]. Дефицит ИЛ-6, ФНО-α приводит к снижению остеокластогенеза и, как следствие, вызывает замедление минерализации каллуса и прочности костной мозоли через 2 нед. после перелома [9].
Параллельно с первой фазой происходит образование грануляционной ткани. МСК дифференцируются в фибробласты и остеогенные клетки, необходимые для поддержания механической стабильности. Процесс оссификации осуществляется путем интрамембранозной и энхондральной оссификации, вследствие чего регенерация костной ткани может проходить одновременно в разных участках перелома. Первичная оссификация протекает в условиях компенсированных посттравматических циркуляторных расстройств кровоснабжения и характерна в первую очередь для репарации плоских костей, а также трубчатых костей с минимальным диастазом отломков, без формирования обширных гематом и переломов по типу «зеленой ветки» в детском возрасте. При интрамембранозной оссификации МСК проходят последовательный путь трансформации в остеопрогениторные клетки, далее в ОБ и ОЦ. Энхондральная оссификация развивается при субкомпенсированных или декомпенсированных нарушениях кровоснабжения и встречается при повреждениях трубчатых костей. Для энхондральной оссификации характерно наличие промежуточного звена — хондрогенеза, при котором хондробласты, дифференцированные из МСК, формируют хрящевую ткань, которая в дальнейшем оссифицируется [10].
На молекулярном уровне эти репаративные процессы опосредуются определенными факторами роста [11]:
Трансформирующий фактор роста β (TGF-β), стимулирующий недифференцированную пролиферацию МСК.
Костный морфогенетический белок (BMP), способствующий дифференцировке МСК в хондроциты и ОБ.
Фактор роста фибробластов (FGF), участвующий в ангиогенезе.
Тромбоцитарные факторы роста (PDGF), усиливающие пролиферацию МСК, макрофагов и ОБ.
Инсулиноподобный фактор роста (IGF), стимулирующий пролиферацию и дифференцировку ОХПГ.
Хотя при исследовании процессов костеобразования после перелома вопросы системной потери костной ткани, как правило, не рассматриваются, ускоренное ремоделирование приводит к длительному системному снижению костной массы [12].
Патогенетические механизмы системной потери костной массы на фоне перелома
Несмотря на обилие факторов риска, позволивших создать модель расчета риска переломов — FRAX, предшествующий перелом является наиболее надежным предиктором развития повторного перелома любой локализации [6]. Даже незначительные переломы увеличивают риск последующих более серьезных переломов (позвоночника, шейки бедренной кости). Так, после возникновения первого перелома костей риск повторного перелома любой локализации увеличивается в 2–10 раз, а последующие переломы еще больше увеличивают предполагаемый риск развития такой патологии [13]. У женщин с переломами в возрасте от 20 до 50 лет наблюдался повышенный риск развития в последующем остеопоротических переломов в возрасте старше 70 лет, а у мужчин в возрасте до 18 лет — более высокий риск перелома после 35 лет [14]. Таким образом, предшествующий перелом костей остается фактором риска развития перелома даже в случае нормальной МПК, что свидетельствует о том, что низкоэнергетические переломы не являются исключительной «привилегией» лиц с низкими показателями МПК.
Для более детального понимания системной потери костной массы необходимо рассмотреть патогенетические механизмы, приводящие к ее снижению, а также отдельные факторы, влияющие на данный процесс. Длительное ограничение физической активности, наличие воспалительного процесса и метаболические изменения, действующие на фосфорно-кальциевый обмен, несомненно, являются основными механизмами посттравматического снижения костной плотности, однако их относительный вклад в костное ремоделирование и то, как они изменяют активность костных клеток, изучены недостаточно.
Резорбция и образование кости, вызванные переломом, являются результатом изменений активности костных клеток, находящихся в базовой многоклеточной единице: ОБ, ОК и ОЦ. При оптимальном балансе процессов ремоделирования кость полностью замещается новой. Известно, что процессы резорбции превалируют над формированием костной ткани. Ключевая роль в поддержании костного метаболизма принадлежит цитокиновой системе рецептора активатора ядерного фактора kB (RANK), лиганда рецептора активатора ядерного фактора kB (RANKL) и остеопротегерина (OPG) [15, 16], отвечающих за синтез костной ткани (рис. 1).
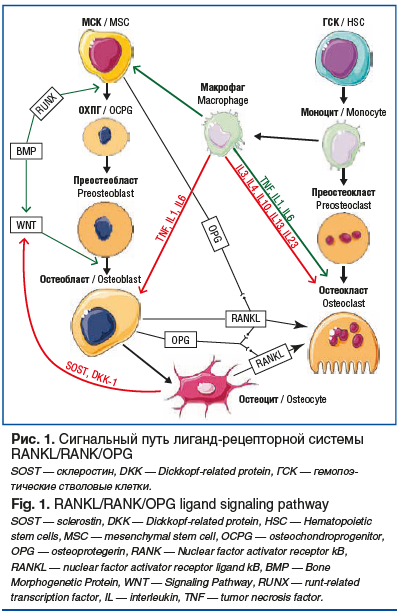
Регуляция ремоделирования осуществляется RANKL, который относится к цитокинам суперсемейства ФНО и OPG, продуцируемым дендритными клетками, МСК и преостеобластами. Основным стимулятором дифференцировки ОК является RANKL, экспрессия которого регулируется цитокинами (ИЛ-1, -6, -11, ФНО), глюкокортикостероидами и паратиреоидным гормоном [17]. Слияние RANKL с рецептором RANK на мембранах клеток — предшественников ОК вызывает активацию факторов транскрипции (NK-kB, c-fos и NFATC1), что приводит к дифференцировке в зрелый ОК. В свою очередь OPG, синтезируемый ОБ, блокирует связывание RANKL с RANK. Экспрессия и продукция OPG модулируются различными цитокинами, пептидами, гормонами и препаратами. Рецепторы к OPG расположены на ОБ, иммунных клетках и преостеокластах. Также ОБ продуцируют макрофагальный колониестимулирующий фактор (M-CSF), участвующий в пролиферации и дифференцировке клеток — предшественников ОК [18].
Определенное место в регуляции остеобластогенеза отводится микроРНК (мкРНК). По данным литературы, именно мкРНК играют ведущую роль в регуляции костного ремоделирования среди других типов эпигенетического контроля экспрессии генов. Группа мкРНК (мкРНК23а, мкРНК30а-d, мкРНК135а, мкРНК204, мкРНК335, мкРНК433, мкРНК34с, мкРНК133а, мкРНК137, мкРНК205, мкРНК211, мкРНК217 и мкРНК93), блокируя траскрипционный фактор остеобластогенеза (Runx2) и остерикс (OSX), ингибирует костеобразование. С другой стороны, мкРНК155 может угнетать синтез ассоциированного с микроофтальмией фактора транскрипции (MITF), приостанавливая образование клеток — предшественников ОК, и приводит к усилению остеобластогенеза путем снижения активности ОК [19].
Хотя максимальный риск повторного перелома приходится на первые несколько лет после него, возможность нарушения целостности кости может сохраняться в течение нескольких десятилетий [20]. Причина повышенного риска переломов костей скелета после первичного перелома долгое время оставалась неясна. Однако более двух десятилетий назад A.J. Silman выявил потенциальные механизмы, которые способствовали после первоначального перелома кости увеличению его риска в дальнейшем [21]:
продолжающееся воздействие факторов риска, приведших к перелому;
системное снижение костной массы, вызванное переломом;
неполное восстановление костной ткани после случившегося перелома.
Впервые повышенная способность к костному ремоделированию, которое приводило к снижению плотности кости вблизи перелома, была описана ортопедом H.M. Frost (1981 г.), который применил термин «феномен ускоренного метаболизма» [22]. Данный феномен характеризовался преобладанием процессов резорбции костной ткани над остегенезом. Пик данного феномена приходится на первые 2 мес. после травмы, при этом отмечалось увеличение скорости костного метаболизма в 2–20 раз, сохраняющееся в течение последующих 6–24 мес. [23]. Рядом авторов также был выделен «феномен системного ускорения» после повреждения костной ткани. Так, на моделях мышей показано, что остеотомия большеберцовой кости увеличила скорость формирования и минерализации костной ткани у мышей и крыс в 3–3,5 раза в контралатеральных голенях и поясничных позвонках [24]. В других исследованиях выявлено увеличение активности ОК в поясничных позвонках после остеотомии бедра или перелома у мышей [25]. Имеются работы, в которых показано, что уровни маркеров резорбции увеличивались в течение 2 нед. после перелома, тогда как маркеры костеобразования нарастали только к 24-й неделе [26]. Скорость костеобразования и скорость резорбции могут оставаться несбалансированными в течение многих лет после перелома [27]: например, у женщин, перенесших перелом в последние 6 лет, наблюдалось снижение синтеза костной ткани, при этом уровень резорбции кости оставался неизменным по сравнению с контрольной группой.
Развитие системной потери костной массы после случившегося перелома обусловлено и воспалительным процессом, играющим ключевую роль в регуляции процесса репарации [28]. Имеется тесная связь между хроническим воспалением и снижением костной массы. Так, например, у пациентов с ревматоидным артритом, воспалительными заболеваниями кишечника и анкилозирующим спондилитом наблюдаются системная потеря костной ткани и повышенный риск остеопении или остеопороза [29]. Известно, что при воспалении иммунными клетками и ОБ высвобождаются провоспалительные цитокины (в частности, ФНО-α, ИЛ-1 и ИЛ-6), оказывающие катаболическое воздействие на костную ткань. Данные цитокины могут индуцировать продукцию RANKL в ОБ и ОЦ, увеличивая дифференцировку ОК [30]. Воспалительные цитокины также уменьшают образование ОБ посредством прямого взаимодействия либо путем увеличения выработки ОЦ склеростина (SOST) и белка DKK1, которые снижают активность ОБ путем ингибирования сигнального пути Wnt/β-катенина [31]. В определенной степени BMP-2, относящийся к суперсемейству TGF-β, индуцирует остеогенез через активацию канонического Wnt сигнала и увеличение экспрессии гена Runx2.
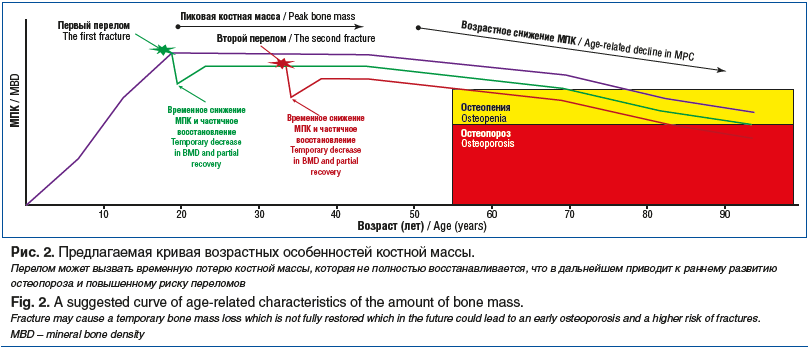
В многочисленных исследованиях продемонстрировано, что при исходной низкой физической активности наблюдался более высокий риск падений [32]. Наличие перелома может отрицательно влиять на физическую активность вследствие нарушения подвижности суставов и дискоординации. Однако эти механизмы не могут полностью объяснить повышенный риск последующего перелома. Вероятно, перелом вызывает системную потерю костной массы и снижение качества костной ткани, что уменьшает МПК, и, как следствие, процесс восстановления костной ткани занимает более длительное время. Также посттравматическая потеря костной массы может сопровождать естественный процесс снижения МПК скелета, в результате чего риск развития остеопороза и последующих переломов возрастает (рис. 2).
В моделях на животных показано, что после перелома уровень физической активности снижался, что приводило к системной потере костной массы [33]. В настоящее время роль функциональной нагрузки декларируется практически всеми травматологами. Ранние циклические движения способствуют восстановлению как кости, так и суставного хряща, что снижает риск развития остеопороза [34]. Отмечено, что в группе больных, ограничивающих двигательную активность после перелома нижней конечности, не только существенно снижена сила мышц, но и замедлен процесс регенерации кости [35]. В результате снижения активности повышается продукция ОБ RANKL и ОЦ — SOST, уровень которых сохранялся высоким в течение 8 нед. и выявлялся в течение 1 года после перелома, что усиливало костную резорбцию и снижение репаративных процессов [36].
Несомненно, регулирует активность процессов костного ремоделирования эндокринная система, причем речь идет не только о гендерных и возрастных гормональных изменениях. Изменения после перелома в первую очередь касаются увеличения активности гипофизарно-адреналовой системы, обеспечивающей системную стрессовую реакцию (адренокортикотропный гормон и кортизол), и паращитовидных желез, активизирующих реабсорбцию кальция (паратгормон). Значительный рост уровня паратгормона в первые 2 нед. с последующим снижением до нормы через 1,5 мес. после травмы способствует активной резорбции органического матрикса, формированию фона для пролиферации костномозговых элементов и инициации превращения клеток-предшественников в ОБ. Избыточная адреналовая активность проявляется в том числе и повышением уровня альдостерона, поддерживающего асептическое воспаление в месте перелома. Было показано, что существенно повышается продукция циклических нуклеотидов: повышение концентрации цАМФ (максимально через 4–5 ч с дальнейшей нормализацией в течение 3 нед.) обеспечивает не только роль вторичного посредника при реализации действия пептидных гормонов на мембрану клеток-мишеней, но и активное участие в процессах кальциевого обмена, регулировании активности ряда протеинкиназ. Увеличение концентрации цГМФ (с 3-го дня после травмы) и изменение соотношения цАМФ/цГМФ взаимосвязано с процессами клеточной пролиферации и образования костного регенерата. От уровня кальция крови зависит и концентрация других гормонов — регуляторов кальциево-фосфорного обмена, таких как кальцитонин (постепенный прирост с максимальным уровнем через 1,5 мес. после травмы) и кальцитриол (активный метаболит — 1,25-дигидроксивитамин D (1,25(ОН)2D), играющих существенную роль в процессах минерализации. Несомненно участие в регуляции анаболических процессов (к которым относятся в том числе прирост костной ткани и ее минерализация) и соматотропного гормона: постепенный прирост его концентрации отмечен в течение первых 1,5 мес. после травмы [37].
Алиментарные дефициты (в первую очередь белковый, кальциевый и дефицит витамина D) могут существенно влиять на репаративные процессы в кости. Известно, что при переломе на фоне недостаточного содержания микро-, макроэлементов, а также гиповитаминоза витамина D развивается феномен ускоренного метаболизма, приводящий к повышению биодоступности минералов, депонирующихся в неизмененных костях скелета. Следовательно, дефицит кальция может модулировать системную потерю костной массы после перелома. M. Haffner-Luntzer et al. обнаружили, что добавление кальция после остеотомии бедренной кости у мышей снижало активность ОК и увеличивало костную массу в поясничных позвонках [38].
Профилактика и лечение
Важнейшим направлением в борьбе с повторными переломами является их профилактика, что приводит к снижению риска развития остеопороза, смертности и, как следствие, экономических затрат и для государства, и для больного [39]. Как известно, при лечении остеопороза в настоящее время используются бисфосфонаты, моноклональное антитело к RANKL — деносумаб, рекомбинантный человеческий паратиреоидный гормон — терипаратид, стронция ранелат и активные метаболиты витамина D (колекальциферол и др.). Данные препараты назначаются при показаниях денситометрического исследования, соответствующих Т-критерию менее -2,5, а также при наличии низкоэнергетических переломов крупных костей (бедра, тел позвонков, множественных переломов) независимо от результатов денситометрии или оценки 10-летнего риска низкотравматического перелома (FRAX) [40].
В свою очередь у лиц с нормальными значениями МПК, а также моложе 40 лет, которым невозможно провести расчет FRAX, данные препараты не применяются. В таком случае основным направлением профилактики являются мероприятия, изложенные в российских клинических рекомендациях по ревматологии и направленные на оптимальный набор пика костной массы и его поддержание: увеличение физической активности, коррекция питания, отказ от вредных привычек, ношение жестких и полужестких корсетов, комплекс мер, направленных на снижение риска падения, таких как коррекция зрения, обучение правильному стереотипу движений, использование трости, обуви на низком каблуке [40]. Тем не менее влияние мероприятий по профилактике переломов и воздействие на системное снижение костной ткани, в особенности у лиц моложе 40 лет с нормальными показателями МПК, требуют дальнейшего изучения.
Заключение
Случившийся перелом инициирует системную потерю костной массы, что приводит к увеличению риска низкоэнергетических переломов в течение нескольких лет после травмы, причем любой локализации. Неполноценное восстановление качества и количества костной ткани сохраняется на протяжении длительного времени, что свидетельствует о том, что системная потеря костной массы является механизмом развития последующего перелома.
Развитие системной потери костной массы на фоне перелома обусловлено, прежде всего, воспалительными реакциями, которые играют ведущую роль в регуляции костеобразования. В частности, гиперпродукция воспалительных цитокинов, регулирующих системную резорбцию кости на фоне низкой физической активности, гормонального дисбаланса, а также меньшее, чем в норме, содержание минеральных веществ в рационе способствуют снижению костной массы вскоре после перелома, однако их относительный вклад в процессы репарации костной ткани до конца не изучен.
Необходимо дальнейшее изучение механизма системного снижения костной массы у лиц моложе 40 лет с нормальными показателями МПК. Понимание данного процесса позволит определить методы профилактики и лечения посттравматической потери костной массы с целью снижения риска переломов в будущем.
Сведения об авторах:
Аганов Дмитрий Сергеевич — к.м.н., преподаватель кафедры факультетской терапии Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0002-5082-9332.
Топорков Михаил Михайлович — к.м.н., старший преподаватель кафедры факультетской терапии Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0002-7417-7509.
Свинцицкая Ирина Сергеевна — к.м.н., доцент кафедры факультетской терапии Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0002-1317-8276.
Тыренко Вадим Витальевич — д.м.н., профессор, начальник кафедры факультетской терапии Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0002-0470-1109.
Максим Оксана Владимировна — к.м.н., преподаватель 1-й кафедры терапии усовершенствования врачей Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0003-0808-3325.
Нуршакирова Ирина Евгеньевна — курсант 6-го курса 4-го факультета Военно-медицинской академии имени С.М. Кирова; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, литера Ж; ORCID iD 0000-0003-3659-6515.
Контактная информация: Свинцицкая Ирина Сергеевна, e-mail: sonirinadoc@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 05.02.2023.
Поступила после рецензирования 02.03.2023.
Принята в печать 28.03.2023.
About the authors:
Dmitry S. Aganov — C. Sc. (Med.), lecturer of the Department of Faculty Therapy, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0002-5082-9332.
Mikhail M. Toporkov — C. Sc. (Med.), senior lecturer of the Department of Faculty Therapy, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0002-7417-7509.
Irina S. Svintsitskaya — C. Sc. (Med.), associate professor of the Department of Faculty Therapy, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0002-1317-8276.
Vadim V. Tyrenko — Dr. Sc. (Med.), Professor, Head of the Department of Faculty Therapy, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0002-0470-1109.
Oksana V. Maksim — C. Sc. (Med.), lecturer of the 1st Department of Therapy, Continuing Medical Education, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0003-0808-3325.
Irina E. Nurshakirova — 6-grade student of the 4th Faculty, S.M. Kirov Military Medical Academy; 6Zh, Academician Lebedev str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0003-3659-6515.
Contact information: Irina S. Svintsitskaya, e-mail: sonirinadoc@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 05.02.2023.
Revised 02.03.2023.
Accepted 28.03.2023.
Информация с rmj.ru