Введение
Текущая ситуация в отечественной клинической практике, касающаяся использования терапевтических стратегий лечения пациентов с первичной открытоугольной глаукомой (ПОУГ), постепенно трансформируется. Это связано с рядом очевидных причин и, в частности, определяется формированием новых общепринятых подходов к лечению (ведению) пациентов с ПОУГ [1, 2]. Вместе с тем врачи, применяющие подходы, сталкиваются со сложностями, к которым следует отнести крайне медленное увеличение доли назначений препаратов группы аналогов простагландинов (АПГ) в монотерапии на старте лечения у пациентов с ПОУГ и такое же медленное снижение количества назначений β-адреноблокаторов (БАБ) [3–6]. Насыщение рынка большим количеством различных фиксированных комбинаций (ФК) [7–9] антиглаукомных препаратов, включая преобладающее количество препаратов-дженериков, не привело пока еще к их оптимальному использованию [10, 11], например, при применении в процессе лечения у пациентов с разными стадиями глаукомы [12–15]. Отмечаются многочисленные случаи неоправданного назначения медикаментозной терапии в максимальном объеме, зачастую в ущерб использованию рациональных подходов, что, в свою очередь, связано с увеличением доли пациентов, длительно получающих гипотензивные препараты [10]. Однако следует отметить и ряд положительных тенденций [16–19]. В частности, во врачебной среде активно обсуждается такой ориентир лечения, как приверженность [20, 21]. На практике используют для лечения все больше бесконсервантных форм антиглаукомных препаратов, обладающих повышенным профилем безопасности [19, 22, 23]. Наконец, все заметнее влияние актуальных клинических рекомендаций и стандартов лечения1 [2].
Цель исследования: оценить клинический эффект и переносимость терапии биматопростом/тимололом (Бимикомби Антиглау ЭКО)2 и бримонидином (Брим Антиглау ЭКО)3 (производитель — АО «АКРИХИН») у пациентов с разными стадиями ПОУГ по сравнению с предшествующей терапией.
Материал и методы
В итоговый протокол многоцентрового комбинированного (ретроспективный анализ и проспективное наблюдение) научно-клинического исследования, проведенного с января по октябрь 2022 г., были включены данные 1036 пациентов из 19 городов Российской Федерации.
Исследование было проведено в соответствии с признанными этическими стандартами. На проведение исследования было получено разрешение этического комитета.
Участие в исследовании было добровольным и подтверждалось письменными решениями респондентов в виде информированного согласия и врачами-исследователями в виде согласия на обработку персональных данных на основании Федерального закона «О персональных данных» от 27.07.2006 № 152-ФЗ4. Вся обезличенная информация вносилась несколькими врачами-исследователями в электронную индивидуальную регистрационную карту.
Критерии включения: наличие подписанного информированного согласия, возраст от 18 до 80 лет включительно, I–III стадии ПОУГ или подозрение на глаукому (ПГ), сопровождающееся повышением уровня ВГД (сроки верификации диагнозов составили от 6 мес. до 2 лет).
Критерии невключения: наличие в анамнезе вторичной глаукомы (врожденной, воспалительной, неоваскулярной, закрытоугольной или открытоугольной с узким углом), глаукомы низкого давления, возрастной макулодистрофии и системных заболеваний, требующих постоянного применения гормональной терапии; выраженные помутнения оптических сред, возникающие вследствие заболеваний или травм глаза, затрудняющие проведение офтальмоскопии и тонометрии; проведение оперативного лечения катаракты либо за 6 мес. до включения в исследование, либо более чем за 6 мес. до включения в исследование, но с осложнениями; оперированные по поводу заболеваний сетчатки; отсутствие доступных ретроспективных данных (медицинской документации); одновременное применение препаратов Бимикомби Антиглау Эко и Брим Антиглау Эко; участие в текущий момент в других клинических или эпидемиологических исследованиях.
В исследование включали респондентов, имеющих в анамнезе указанные в медицинской документации данные уровня ВГД. Проводили анализ антиглаукомной терапии, которую получали пациенты до включения в исследование.
Пациенты на момент начала терапии препаратом биматопрост/тимолол (Бимикомби Антиглау Эко) не использовали дополнительные антиглаукомные препараты или препарат бримонидин (Брим Антиглау Эко) в монотерапии или в свободной комбинации с другими гипотензивными препаратами (АПГ, ингибиторами карбоангидразы (ИКА), БАБ или их ФК).
Всем пациентам выполняли комплексное офтальмологическое обследование, которое включало сбор жалоб, демографические и антропометрические данные, данные о наличии сопутствующей патологии и коморбидных состояний, оценку стадии ПОУГ, офтальмоскопию, контактный метод измерения уровня офтальмотонуса (во всех случаях использовали метод измерения по Маклакову, грузом 10 г), анамнестические данные по основным показателям уровня ВГД и данные о предшествующей терапии (международные непатентованные наименования лекарственных средств и причины замены), фиксацию оценки эффективности, переносимости и приверженности назначенной терапии. Сбор отдельных данных осуществлялся на основании данных медицинских карт и опроса мнения врачей и пациентов на основании психометрической шкалы — опросника Лайкерта5 и с использованием специально разработанной электронной анкеты. Дополнительно все испытуемые заполняли опросник «Индекс патологии глазной поверхности» (Ocular Surface Disease Index, OSDI) [24]. Для заполнения базы данных и проведения анкетирования по опроснику OSDI были использованы лицензированные персонализированные возможности технологии Google и Microsoft (обе — США) с предварительной кодировкой результатов для исключения нарушения норм локального законодательства.
Одной из задач работы стал анализ предшествующей антиглаукомной терапии, которую получали пациенты до включения в исследование.
Терапия препаратами исследования должна была продолжаться в течение 2–4 мес., а ее выбор стал следствием недостаточной эффективности, неэффективности или непереносимости предыдущих схем лечения. Контрольное исследование проводилось однократно, не менее чем через 1 мес. после включения пациента в исследование.
Статистический анализ. Обработка полученных данных была проведена одним исследователем с использованием программы Statistica (версия 10,0, StatSoft Inc., США) с последующей выборочной проверкой полученных результатов и обсуждением с коллегами. Приводимые параметры, имеющие нормальное распределение, представлены в формате М±m, где М — среднее значение, m — стандартная ошибка среднего значения. При нормальном распределении параметров для сравнения двух независимых групп или повторных внутригрупповых изменений использовался t-критерий Стьюдента; при отличном от нормального распределении параметров для сравнения нескольких независимых выборок — для попарного сравнения двух независимых выборок — Z-аппроксимация U-критерия Манна — Уитни, для повторных внутригрупповых сравнений — Z-аппроксимация T-критерия Уилкоксона. Использование непараметрического критерия было обосновано несоответствием распределения по шкалам нормальному распределению. Критический уровень значимости при проверке статистических гипотез принимался равным 0,05.
Результаты и обсуждение
Среди участников исследования было 596 (57,5%) женщин и 440 (42,5%) мужчин. Средний возраст пациентов составил 64,9±10,12 года. На 1-м месте по численности обследуемых были пациенты из Санкт-Петербурга — 228 (22%) человек, на 2-м месте — из Москвы — 160 (15,4%) человек, 3-е место заняла Самара — 135 (13%) человек. Далее следовали Ростов-на-Дону — 99 (9,6%), Челябинск — 69 (6,7%), Казань — 61 (5,9%), Красноярск — 60 (5,8%), Таганрог — 43 (4,2%), Тюмень — 25 (2,4%), Краснодар — 21 (2%), Екатеринбург — 20 (1,9%), Омск — 20 (1,9%), Пермь — 20 (1,9%), Иркутск — 15 (1,4%), Уфа — 15 (1,4%), Химки — 15 (1,4%), Новосибирск — 1 (1%), Мытищи — 10 (1%) и Подольск — 10 (1%).
Первичная открытоугольная глаукома (все стадии) была диагностирована у 982 (94,8%) пациентов, а ПГ, сопровождающееся офтальмогипертензией, — у 54 (5,2%) человек. Начальная стадия ПОУГ была зарегистрирована у 342 (34,8%) пациентов, развитая — у 491 (50%) пациента, далеко зашедшая стадия — у 149 (15,2%) пациентов.
Больше всего пациентов, болеющих ПОУГ, были со II стадией — 491 (50%) человек, далее по численности — I стадия (342; 34,8%) и III стадия (149; 15,2%). Исследователями изучены сопутствующие заболевания у пациентов. Было установлено, что среди сопутствующих заболеваний превалировала гипертоническая болезнь — 752 (78,3%) наблюдения, далее следовала ишемическая болезнь сердца — 361 (37,6%), сахарный диабет — 273 (28,4%), гипотония — 71 (7,4%) и бронхиальная астма — 22 (2,3%).
При обработке данных было выявлено, что гипотензивная терапия включала в себя АПГ (508 случаев), которые применялись как в монотерапии, так и при назначении различных ФК. В этой группе препаратов наиболее распространенным стал латанопрост (279; 55,0%), далее следовали тафлупрост (102; 20,1%), травопрост (101; 19,9%) и биматопрост (26; 5,1%). Препараты группы БАБ применяли в 374 случаях (тимолол — в 276 (73,8%) случаях, бетаксолол — в 98 (26,2%) случаях. Местные и общие ИКА применялись у 340 пациентов (дорзоламид — у 290 (85,3%), бринзоламид — у 42 (12,3%), ацетазоламид — у 8 (2,4%)). Терапия селективными α2-адреномиметиками (АМ, бримонидин) применялась у 105 пациентов, а еще 51 пациент инстиллировал пилокарпин. В целом ФК в предшествующей гипотензивной терапии применялись только у 182 (17,6%) пациентов, а в остальных случаях приоритет был отдан раздельному применению различных схем антиглаукомных топических препаратов — у 854 (82,4%), включая максимально возможные схемы лечения. Наиболее применяемым видом ФК была комбинация ИКА и БАБ (дорзоламид/тимолол) — у 59 пациентов (32,4% от всех случаев назначения ФК), затем следовала ФК, включающая АПГ и БАБ (латанопрост/тимолол), — у 40 (22%), далее в порядке уменьшения: бринзоламид/тимолол — у 26 (14,3%), тафлупрост/тимолол — у 17 (9,3%), биматопрост/тимолол — у 16 (8,8%), травопрост/тимолол — у 12 (6,6%), бримонидин/тимолол — у 8 (4,4%) и, крайне редко, пилокарпин/тимолол — у 2 (1,1%), бринзоламид/бримонидин — у 2 (1,1%).
Следует подчеркнуть, что часть пациентов до включения их в исследование уже получала исследуемые препараты — Бимикомби Антиглау ЭКО (53; 5,1%) или Брим Антиглау ЭКО (105; 10,1%), что было определено ретроспективно по данным изучения медицинской документации.
По данным проведенного анализа было установлено, что большинство пациентов при использовании предшествующей гипотензивной терапии (не включающей анализируемые в исследовании препараты) (n=878) жаловались на чувство «инородного тела» — 410 (46,7%) человек, чувство «сухости глаз» — 382 (43,5%), «слезотечение» — 336 (38,2%), покраснение глаз — 323 (36,7%), «жжение» глаз — 307 (34,5%). В свою очередь при проведении биомикроскопии врачами-офтальмологами были выявлены следующие симптомы и синдромы: синдром «сухого» глаза (ССГ) — у 277 (31,5%), дисфункция мейбомиевых желез — у 135 (15,3%), блефарит — у 87 (9,9%), повреждения роговицы — у 23 (2,6%).
Главной причиной смены схемы лечения стала недостаточная клиническая эффективность (217 (36,6%) пациентов), что подтвердило опубликованные нами ранее данные о неэффективности и непродолжительности стартового лечения при использовании нерациональных схем терапии [6] и принятых во внимание актуальных версий клинических рекомендаций1. Другими причинами стали жалобы на «дискомфорт» во время выполнения предыдущих назначений — у 158 (26,6%) пациентов, неудовлетворительную переносимость терапии — у 142 (23,9%), дороговизну препарата — у 32 (5,4%), ухудшение зрения при инстилляции препаратов — у 26 (4,4%) и неудобство использования флакона с ранее назначенным препаратом — у 18 (3,0%).
Изучение гипотензивной эффективности наряду с переносимостью препаратов является приоритетом современной терапии глаукомы. В этой связи был проведен сравнительный анализ показателей ВГД (правый и левый глаза исследовались отдельно) до и после начала применения препаратов Брим Антиглау ЭКО и Бимикомби Антиглау ЭКО. По данным тонометрии были выявлены значимые различия между исходными значениями и текущими показателями (табл. 1).

Исходный уровень ВГД правого глаза составил 23,2 мм рт. ст., на фоне лечения он статистически значимо снизился (T=38,07; p<0,001). Значения уровня офтальмотонуса левого глаза были сопоставимыми с таковыми для правого глаза и статистически значимо уменьшались после лечения (T=38,81; p=0,001), при этом не было установлено различий между парными глазами как до момента смены схемы лечения, так и при финальном обследовании.
Неоспоримое преимущество препаратов Брим Антиглау ЭКО и Бимикомби Антиглау ЭКО заключается в отсутствии консервантов в их составе. Такое преимущество было подтверждено при изучении субъективных жалоб пациентов и данных клинического обследования на фоне проводимого лечения с использованием вышеуказанных препаратов (табл. 2).
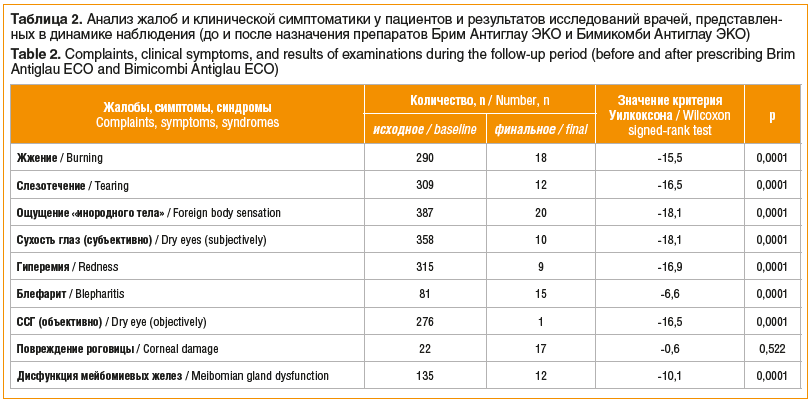
Результаты исследования, касающиеся жалоб пациентов и данных обследования, представленных врачами-офтальмологами, свидетельствуют, что их доля до назначения новой схемы лечения статистически значимо отличается от количества таковых, установленных во время текущего визита, практически по всем показателям.
Объединение субъективных подходов (например, анализ жалоб, связанных с объемом терапии) с объективными данными обследования, выполненными профессионалами, несомненно, является современной тенденцией медицины, что позволяет увеличивать показатель приверженности пациентов проводимому лечению. В этой работе была использована психометрическая шкала Лайкерта, которая применялась для анализа оценок удовлетворенности врачей и пациентов применяемой гипотензивной терапией (см. рисунок).
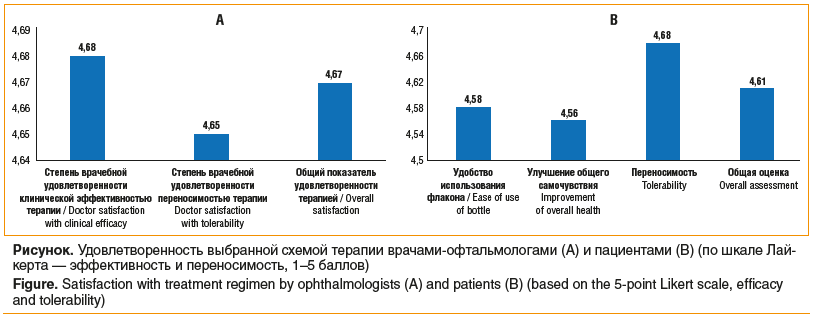
Следует отметить, что общий показатель врачебной оценки удовлетворенности клиническим эффектом и переносимости терапии был высоким, составив 4,67±0,49 балла. При этом у подавляющего большинства пациентов также была определена высокая оценка переносимости лечения препаратами Брим Антиглау ЭКО и Бимикомби Антиглау ЭКО (4,68±0,58 балла). Касаясь отдельных составляющих данной шкалы, следует отметить высокую степень врачебной удовлетворенности клинической эффективностью выбранной терапии (4,68±0,52 балла) и аналогичную оценку пациентами удобства использования флакона (4,58±0,58 балла). В целом по результатам субъективной оценки приверженности лечению, пациенты продемонстрировали крайне высокую степень в 58,8% наблюдений, в 19,9% — высокую, в 7,4% — среднюю и в 13,9% — низкую. Такое распределение высокой доли приверженности лечению было подтверждено данными подсчета сохранявшихся или впервые развившихся нежелательных реакций, которые при использовании Брим Антиглау ЭКО и Бимикомби Антиглау ЭКО составили около 1% (9 случаев в течение всего срока наблюдения), и при этом ни у одного пациента эти побочные локальные эффекты не явились причиной отмены препарата.
Завершением исследования стало заполнение всеми респондентами специализированного опросника «Индекс патологии глазной поверхности», который был ранее валидирован в качестве международной системы оценки состояния глазной поверхности согласно жалобам пациента и предназначен для быстрого выявления симптомов раздражения глаз и их влияния на зрительные функции. При заполнении международного опросника OSDI по каждому вопросу превалировал вариант «норма» или «редкие проявления симптоматики ССГ». Среднее значение этого показателя составило 14,4±5,53 балла, что соответствует нормальным значениям.
Ограничения исследования
Ограничением данной работы стало исключение анализа результатов назначений лекарственных препаратов у лиц, поменявших лечение. Также был размыт срок назначений исследуемой группы препаратов и ограничен срок проспективного наблюдения. Помимо этого, в исследование были включены пациенты, уже получающие ранее (срок от 2 до 4 мес.) гипотензивную терапию, включающую подвергнутые анализу препараты. Для корректного завершения исследования и с целью сравнения полученных результатов имеет смысл увеличить сроки проспективного наблюдения, а также включить в исследование анализ результатов назначений предыдущих гипотензивных лекарственных препаратов.
Заключение
Результаты проведенного исследования свидетельствуют о том, что смена режимов лечения (в плановом порядке) помогает обойти возможное развитие тахифилаксии и предупреждает развитие толерантности к ранее назначенным лекарственным препаратам, что подтверждается тонометрическими данными (понижение уровня ВГД составило около 20% от предшествующих значений офтальмотонуса).
В случае смены режима по разным причинам (в целом проанализированы 6 причин) первые 3 позиции последовательно занимают: недостаточная клиническая эффективность (36,6%), дискомфорт (26,6%) и плохая переносимость (23,9%). Назначение бесконсервантной гипотензивной антиглаукомной терапии с использованием препаратов Бимикомби Антиглау ЭКО или Брим Антиглау ЭКО (после применения периода вымывания и в течение 1 мес. инстилляций) способствует статистически значимому уменьшению количества таких жалоб (в 19 раз). Применение препаратов без консервантов значительно повышает максимальную удовлетворенность пациентов назначенными схемами лечения (58,8%, или 4,61 балла из 5 по шкале Лайкерта), а также в значительной мере удовлетворяет ожидания врачей, касающиеся эффективности и переносимости препаратов (4,67 балла из 5 по шкале Лайкерта).
Полученные данные имеют особую актуальность и практическую значимость для обоснования необходимости разработки специфических мер профилактики развития ССГ у пациентов с глаукомой, постоянно инстиллирующих гипотензивные капли. Возможными мерами могут быть более активное применение в условиях рутинной клинической практики бесконсервантных форм антиглаукомных лекарственных препаратов и превентивное использование препаратов «искусственной слезы» у соответствующих категорий пациентов.
1. Клинические рекомендации. Глаукома первичная открытоугольная. 2020. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/schema/96_1 (дата обращения: 22.06.2023).
2. Инструкция по медицинскому применению лекарственного препарата для медицинского применения Бимикомби Антиглау ЭКО. (Электронный ресурс.) URL: https://grls.rosminzdrav.ru/Grls_Viewv2.aspx?routingGuid=ff64a075-63f9-4003-a4aa-6ff053cb9418. (дата обращения: 22.06.2023).
3. Инструкция по медицинскому применению лекарственного препарата для медицинского применения Брим Антиглау ЭКО. (Электронный ресурс.) URL: https://grls.rosminzdrav.ru/Grls_Viewv2.aspx?routingGuid=ab6958db-9b17-487e-acbd-70f234d9e7ac (дата обращения: 22.06.2023).
4. Федеральный закон «О персональных данных» от 27.07.2006 No 152-ФЗ. (Электронный ресурс.) URL: https://fstec.ru/tekhnicheskaya-zashchita-informatsii/dokumenty/107-zakony/365-federalnyj-zakon-ot-27-iyulya-2006-g-n-152-fz (дата обращения: 21.01.2023).
5. Шкала Лайкерта. (Электронный ресурс.) URL: https://ru.abcdef.wiki/wiki/Likert_Scale (дата обращения: 22.06.2023).
Благодарность
Авторы благодарят коллег, принимавших участие в сборе первичной информации для исследования (список доступен по запросу).
Acknowledgment
The authors are grateful to colleagues involved in primary data collection (list available upon request).
Сведения об авторах:
Куроедов Александр Владимирович — д.м.н., начальник офтальмологического центра (с дневным стационаром) ФКУ «ЦВКГ им. П.В. Мандрыка»; 107014, Россия, г. Москва, ул. Большая Оленья, вл. 8А; профессор кафедры офтальмологии РНИМУ им. Н.И. Пирогова Минздрава России; 117437, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0001-9606-0566.
Косаковская Мария Владимировна — врач-ординатор РНИМУ им. Н.И. Пирогова Минздрава России; 117437, Россия, г. Москва, ул. Островитянова, д. 1; врач-офтальмолог 3АО «Группа компаний «Медси»; 123056, Россия, г. Москва, Грузинский пер., д. 3А; ORCID iD 0000-0002-3541-8891.
Гапонько Олеся Владимировна — к.м.н., заведующая дневным стационаром офтальмологического центра ФКУ «ЦВКГ им. П.В. Мандрыка»; 107014, Россия, г. Москва, ул. Большая Оленья, вл. 8А; ассистент кафедры офтальмологии РНИМУ им. Н.И. Пирогова Минздрава России; 117437, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 000-0001-5893-7371.
Городничий Виталий Владимирович — врач-офтальмолог офтальмологического отделения ФКУ «ЦВКГ им. П.В. Мандрыка»; 107014, Россия, г. Москва, ул. Большая Оленья, вл. 8А; ORCID iD 0000-0002-7276-5753.
Ловпаче Джамиля Нурийдиновна — к.м.н., доцент кафедры офтальмологии РНИМУ им. Н.И. Пирогова Минздрава России; 117437, Россия, г. Москва, ул. Островитянова, д. 1; врач-офтальмолог офтальмологической клиники «3Z»; 129301, Россия, г. Москва, ул. Б. Галушкина, д. 3; ORCID iD 0000-0002-4287-4502.
Булах Илья Алексеевич — врач-офтальмолог ООО МЦ «Ивастрамед»; 153021, Россия, г. Иваново, ул. Рабфаковская, д. 30; ORCID iD 0000-0003-2348-4880.
Контактная информация: Куроедов Александр Владимирович, e-mail: akuroyedov@hotmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 15.06.2023.
Поступила после рецензирования 06.07.2023.
Принята в печать 27.07.2023.
About the authors:
Aleksandr V. Kuroyedov — Dr. Sc. (Med.), Head of the Ophthalmological Center (with Day Hospital), Mandryka Central Military Clinical Hospital; 8A, Bolshaya Olenya str., Moscow, 107014, Russian Federation; Professor of the Department of Ophthalmology, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0001-9606-0566.
Mariya V. Kosakovskaya — resident, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ophthalmologist, JSC «Group of Companies MEDSI»; 3A, Gruzinskiy lane, Moscow, 123056, Russian Federation; ORCID iD 0000-0002-3541-8891.
Olesya V. Gapon’ko — C. Sc. (Med.), Head of the Day Hospital of the Ophthalmological Center, Mandryka Central Military Clinical Hospital; 8A, Bolshaya Olenya str., Moscow, 107014, Russian Federation; assistant of the Department of Ophthalmology, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0001-5893-7371.
Vitaliy V. Gorodnichiy — ophthalmologist of the Department of Ophthalmology, Mandryka Central Military Clinical Hospital; 8A, Bolshaya Olenya str., Moscow, 107014, Russian Federation; ORCID iD 0000-0002-7276-5753.
Dzhamilya N. Lovpache — C. Sc. (Med.), associate professor of the Department of Ophthalmology, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ophthalmologist, Ophthalmological Clinic «3Z»; 3, Boris Galushkin str., 129301, Russian Federation; ORCID iD 0000-0002-4287-4502.
Il’ya A. Bulakh — ophthalmologist, LLC Medical Center «Ivastramed»; 30, Rabfakovskaya str., Ivanovo, 153021, Russian Federation; ORCID iD 0000-0003-2348-4880.
Contact information: Aleksandr V. Kuroyedov, e-mail: akuroyedov@hotmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 15.06.2023.
Revised 06.07.2023.
Accepted 27.07.2023.
Информация с rmj.ru