Введение
Аллергический ринит (АР), являясь одним из наиболее распространенных заболеваний у детей, представляет собой важную медико-социальную и экономическую проблему [1, 2]. Во всем мире распространенность АР продолжает расти, особенно в странах с низким и средним уровнем дохода, и колеблется от 1 до 54,5% [3]. Распространенность АР составляет примерно 5% среди детей в возрасте до 3 лет, увеличивается с 8,5% в возрасте 6–7 лет до 14,6% в возрасте 13–14 лет и достигает 11,8–46% в возрастной группе от 20 до 44 лет [4].
Аллергический ринит предшествует бронхиальной астме (БА) в 45,3–83,3% случаев, дебютом для АР может являться и сама БА — в 1,1–20% случаев, а в 5,3–6,6% случаев оба заболевания развиваются одновременно [5]. В свою очередь как АР может являться триггером для реализации БА, так и острая респираторная инфекция (ОРИ) может быть триггером для АР [6]. Известно, что слизистая оболочка верхних дыхательных путей покрыта однослойным многорядным мерцательным эпителием, который образует тонкий и весьма чувствительный барьер, на который постоянно оказывает воздействие большое количество антигенного материала. Иммунитет слизистых является многоуровневой системой, его состояние и нарушение функции могут привести к развитию аллергопатологии.
В последнее время отмечается неуклонный рост в популяции вирусных инфекций и аллергопатологии с резистентностью и торпидностью к проводимой терапии. Взаимосвязь течения ОРИ и аллергических заболеваний респираторного тракта обусловлена тем, что сами вирусные агенты могут являться причинно-значимыми аллергенами, инфекция может формировать аллергическое заболевание у предрасположенного к этому человека, также инфекция выступает в качестве триггера обострения аллергического заболевания и вызывает прогрессирование болезни, что подтверждается увеличением количества госпитализаций с БА и АР в период ОРИ.
Взаимосвязь АР и ОРИ также не вызывает сомнений, ведь на фоне аллергии создаются условия для присоединения вторичной инфекции или возникновения инфекционного заболевания, персистирования минимального аллергического воспаления, особенно длительно текущего, порождает склонность к персистенции инфекционного агента. Кроме того, аллергия влияет на клиническую картину инфекционного заболевания и может видоизменять его течение [2, 7].
С учетом разнообразия форм и гетерогенной природы АР основным направлением в диагностике и контроле за ним является разработка новых подходов к верификации диагноза и превентивной терапии, учитывающей социальные, клинические и биологические особенности заболевания [8].
Цель исследования: оценка эффективности каскадного алгоритма диагностики и превентивного медикаментозного подхода к профилактике АР у детей из групп высокого риска.
Содержание статьи
Материал и методы
Исследование было проведено в соответствии с Кокрейновскими рекомендациями [9] на базах ГБУЗ МО «Одинцовская ОБ» (г. Одинцово), ГБУЗ ЯО «Областная детская клиническая больницы» (г. Ярославль), ГБУЗ ТО «Городская детская клиническая больница» (г. Тверь), ГБУЗ ВО «ОДКБ» (г. Владимир), БУЗ ВО «ВДГП» (г. Вологда). В условиях поликлиник был проведен ретроспективный статистический и эпидемиологический анализ распространенности и заболеваемости АР, выполнены оценки абсолютных и относительных рисков за 2017–2021 гг. на основании годовых статистических отчетов по форме № 030-ПО/о-17.
Протокол исследования одобрен на заседании локального этического комитета при ГБУЗ «Морозовская ДГКБ ДЗМ» (23.12.2021). Все пациенты, участвующие в проспективном исследовании, подписывали информированное согласие, одобренное этическим комитетом.
В каждом регионе, включенном в исследование, последовательно определялись и анализировались все имеющиеся факторы риска АР за исследуемый период с расчетом инцидентности, превалентности, добавочного риска, добавочного популяционного риска, добавочной доли популяционного риска, атрибутивной фракции, относительного риска (ОР) и оценки шанса (ОШ) реализации риска. В ходе работы была разработана модель скринингового каскада для выявления управляемых факторов риска, которая является частью маршрута оказания медицинской помощи детям с выявленными факторами риска на этапе ранней диагностики АР.
В 2021 г. в условиях поликлиники на базе ГБУЗ МО «Одинцовская ОБ» было проведено сравнительное исследование стандартной модели диагностики АР и предложенного скрининг-диагностического каскада, который включает скрининг, трехэтапную модель диагностики и превентивный подход к медикаментозной терапии пациентов, имеющих высокий риск развития АР, но без сформировавшегося АР на данном этапе.
По результатам проведенного скрининга пациенты, имеющие факторы риска развития АР, маршрутизируются на этап ранней диагностики, который является частью трех-этапной модели диагностики АР. Дети, прошедшие скрининг, у которых факторы риска АР не были выявлены, направляются на проведение скрининга в следующем возрастном периоде.
Диагностика АР проводилась согласно каскадному алгоритму (см. рисунок). Основной целью предложенного алгоритма поэтапной диагностики является внедрение итерационной модели персонифицированного подхода к диагностике АР у детей, согласно которой дети, включенные по результатам скрининга в исследование, не исключаются из него даже при полностью отрицательных результатах исследования, а постоянно возвращаются на первый этап диагностики в следующем возрастном периоде, а часть пациентов, с высоким риском реализации АР, получают превентивное медикаментозное лечение в период ОРИ. Оценка риска развития АР осуществляется при помощи компьютерной капилляроскопии ногтевого ложа (патент РФ RU 2760395 C1 от 05.02.2021. Бережанский П.В., Бережанская Ю.С.). В итоге проведенного исследования, в зависимости от риска развития АР, все дети были распределены на 2 группы — с высоким или низким риском развития АР. Детям, имеющим высокий риск развития АР, были рекомендованы превентивные лечебные мероприятия, направленные на снижение риска реализации АР.
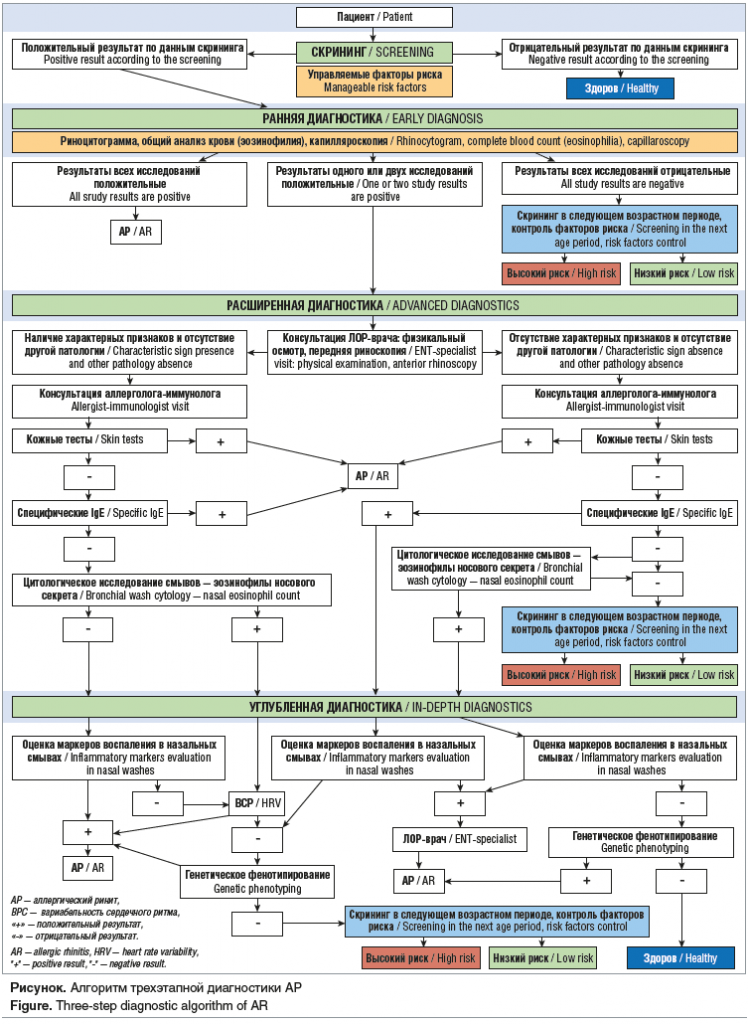
Определение риска развития АР осуществлялось на каждом из последующих этапов диагностики (расширенной и углубленной), в следующем возрастном периоде.
Оценка эффективности скринингового каскада была проведена на базе ГБУЗ МО «Одинцовская ОБ» в 2021 г. Учитывая динамический характер популяции и широкую территориальную разрозненность, основным методом проведения скрининга выбрали анкетирование родителей или законных представителей ребенка. Все участники получали приглашение на тест, используя активную ссылку или QR-код.
На базе ГБУЗ МО «Одинцовская ОБ» в 2022 г. для оценки эффективности предложенной модели превентивной медикаментозной профилактики было проведено катамнестическое наблюдение за детьми из группы высокого риска реализации АР: в 1-й группе дети (n=50) не получали превентивную терапию, во 2-й группе дети (n=50) получали превентивную терапию.
Статистическая и эпидемиологическая обработка материалов проводилась посредством программ: MedCalc®, эпидемиологического пакета EpiInfo, ReviewManager 5.3.5 и пакета компьютерных программ Stata/MP 14.0.
Результаты и обсуждение
В 2017 г. общая изучаемая популяция составляла 345 222 ребенка (размер эффекта), из них у 1,728% (95% доверительный интервал (ДИ) 1,685–1,772) детей был выставлен диагноз АР. По результатам проведенного анализа выявлен постоянный рост общей детской популяции во всех изучаемых регионах и количества пациентов от рождения до 17 лет с диагнозом АР, с истинно установленной по статистической отчетности медицинских организаций частотой встречаемости в 2021 г. от 1,472% в Твери до 2,684% в Вологде. При оценке распространенности и заболеваемости в различные возрастные периоды было выявлено увеличение заболеваемости АР по мере взросления населения, что говорит о гиподиагностике, недостаточности оказания лечебно-профилактической помощи пациентам с минимальными проявлениями АР в период развития ОРИ и отсутствии утвержденного алгоритма диагностики АР у участковых врачей-педиатров и врачей общей практики.
На основании полученных данных в пяти независимых регионах были определены и проанализированы все 28 выявленных факторов риска за исследуемый период времени. В ходе работы была сформирована база данных факторов риска (свидетельство о регистрации № 2022620939 от 13.04.2022). Все факторы риска были распределены на 3 группы. Критериями распределения на группы являлась возможность воздействия на факторы риска и снижение эффекта их воздействия на реализацию АР: неуправляемые (6 факторов), частично управляемые (10 факторов) и управляемые (12 факторов).
По результатам проведенного эпидемиологического анализа установлено, что факторы риска воздействуют неравномерно в различные возрастные периоды. По наибольшему шансу реализации конкретных факторов риска была проведена возрастная дифференцировка популяции на 4 возрастные группы: дети с рождения до 5 лет, дети 6–7 лет, 8–12 лет и дети 13 лет и старше.
В группе детей до 5 лет достоверно оказывают эффект на реализацию АР 10 факторов риска (2 неуправляемых, 6 частично управляемых, 2 управляемых) и 11 однозначно не оказывают эффекта (р<0,05). Среди управляемых факторов риска были выявлены прием парацетамола и антибиотиков в первые 12 мес. жизни (ОР 3,020, 95% ДИ 2,399–5,746; ОШ 4,325, 95% ДИ 2,770–8,752) и материнская депрессия (ОР 2,652, 95% ДИ 1,254–6,764; ОШ 3,797, 95% ДИ 2,403–10,302).
В группе детей 6–7 лет достоверно оказывают эффект на реализацию АР 9 факторов риска (3 неуправляемых, 2 частично управляемых, 4 управляемых) и 11 не оказывают никакого воздействия (р<0,05). Наиболее значимыми управляемыми факторами риска в данной группе являются проживание около автомагистралей (ОШ 5,245, 95% ДИ 3,739–7,273) и позднее введение прикормов (ОШ 4,593, 95% ДИ 1,375–14,552).
В группе детей 8–12 лет среди неуправляемых факторов риска наибольший достоверный эффект на реализацию АР оказывает отягощенный собственный аллергоанамнез (ОР 1,811, 95%, ДИ 1,036–2,752; ОШ 2,192, 95% ДИ 1,134–3,693). Среди управляемых факторов риска значимыми являются низкий уровень витамина D — ниже 30 нг/мл (ОР 2,688, 95% ДИ 1,619–4,060; ОШ 2,418, 95% ДИ 1,520–6,184), проживание в городской среде (ОР 3,184, 95% ДИ 2,155–5,664; ОШ 3,560, 95% ДИ 2,692–8,626) и пассивное курение (ОР 5,664, 95% ДИ 2,414–11,585; ОШ 5,247, 95% ДИ 1,096–11,645).
В подростковой группе (13 лет и старше) достоверными управляемыми факторами риска являются использование компьютера более 2 ч в день (ОР 3,047, 95% ДИ 1,360–6,942; ОШ 4,364, 95% ДИ 1,078–7,526), избыток массы тела и ожирение (ОР 4,078, 95% ДИ 2,990–5,950; ОШ 5,840, 95% ДИ 3,960–9,062), вредные привычки (ОР 3,672, 95% ДИ 1,246–8,129; ОШ 2,395, 95% ДИ 1,400–6,381).
Скрининговый каскад в первую очередь направлен на выявление случаев изменений в бессимптомной стадии, свойственных конкретному заболеванию в бессимптомной стадии. Бессимптомные лица с ранней стадией заболевания имеют значительно лучший ответ на лечение, чем те, кому впервые был выставлен диагноз при обращении к врачу с жалобами. Таким образом, профилактическая служба может дать больший положительный результат, чем медикаментозная терапия самого заболевания.
В результате проведенного анализа было выявлено, что на IV квартал 2021 г. 984 пациента находились на учете с диагнозом АР в г. Одинцово, из них 709/984 (72,1%), по данным амбулаторных карт, имели управляемые факторы риска в различные возрастные периоды до верификации диагноза АР. При ретроспективной оценке управляемых факторов риска выявлено, что данные факторы риска в анамнезе в возрасте до 5 лет имели 28/58 (48,3%) детей, в возрасте 6–7 лет — 74/152 (48,7%), 8–12 лет — 202/465 (43,4%), 13 лет и старше — 168/308 (54,6%).
В г. Одинцово в 2021 г. скрининг факторов риска был проведен 39 852 (63,81%) детям от 0 до 17 лет из 62 458 детей, прикрепленных к ГБУЗ МО «Одинцовская ОБ». У 35 576/62 458 (57%) детей были получены отрицательные результаты скрининга. Всем детям до 5 лет (9361/35 576 (26,3%)), 6–7 лет (4713/35 576 (13,3%)), 8–12 лет (12 058/35 576 (33,9%)), 13 лет и старше (9444/35 576 (26,5%)) с отрицательными результатами скрининга было рекомендовано уменьшение воздействия управляемых факторов риска развития АР и прохождение скрининга в следующем возрастном периоде.
В настоящее время профилактика АР представлена первичной (исключение факторов риска), вторичной (устранение контакта с аллергеном) и третичной (профилактика тяжелого АР) профилактикой [10]. Первичную профилактику АР проводят в общей популяции детского населения без дифференциации на группы высокого и низкого риска реализации АР, что делает ее менее эффективной. Скрининг позволяет ограничить популяцию детей, нуждающихся в адресной профилактике, так как из всей популяции детского населения на следующий этап попадают только те, которые относятся к группе риска, что позволит подойти персонифицированно, избирательно и экономически целесообразно.
Все пациенты, имеющие по результатам скрининга факторы риска, были включены в диагностический каскад. На рисунке отражено сочетание диагностических методов исследования для верификации диагноза АР и маршрутизации.
Из всех детей, прошедших скрининг, 4276 детей были маршрутизированы на этап ранней диагностики: 952/4276 (22,3%) в возрасте до 5 лет, 783/4276 (18,3%) — 6–7 лет, 1476/4276 (34,5%) — 8–12 лет и 1065/4276 (24,9%) — 13 лет и старше. При оценке полового состава группы выявлено, что 2907/4276 (68%) детей были мужского пола и 1369/4276 (32%) — женского.
На данном этапе диагноз АР был верифицирован у 22 детей: у 2/952 (0,2%) в возрасте до 5 лет, у 4/783 (0,5%) — 6–7 лет, у 7/1476 (0,47%) — 8–12 лет и у 9/1065 (0,85%) — 13 лет и старше.
Имели 3 отрицательных результата исследования на раннем этапе диагностики в группе детей в возрасте до 5 лет 74/952 (7,8%), 6–7 лет — 38/783 (4,9%), 8–12 лет — 89/1476 (6%), 13 лет и старше — 102/1065 (9,58%) детей. Всем пациентам было рекомендовано проведение скрининга в следующем возрастном периоде и исследование, направленное на оценку риска реализации АР запатентованным методом оценки прогностических критериев на основании изменений в микроциркуляторном русле. Высокая степень риска развития АР имеет в своей основе не только воздействие факторов риска, но и определенные патоморфологические изменения в микроциркуляторном русле, которые предрасполагают к реализации АР. С точки зрения нашего подхода данная группа пациентов может относиться к группе со «скрытой патологией» или с минимальными проявлениями АР, реализующимися на фоне течения ОРИ, которые являются триггерами запуска каскада минимального персистирующего воспаления и АР. По результатам обследования в группе детей до 5 лет имели высокий риск 27/74 (36,5%), до 2 лет — 11/74 (14,5%), с 2 до 5 лет — 16/74 (21,6%), а 47/74 (63,5%) детей имели низкий риск реализации АР. В группе детей 6–7 лет имели высокий риск и низкий риск развития АР 14/38 (36,8%) и 24/38 (63,2%) детей соответственно; в группе детей 8–12 лет — 31/89 (34,8%) и 58/89 (65,2%), а в группе 13 лет и старше — 26/102 (25,5%) и 76/102 (74,5%) детей имели высокий риск и низкий риск развития АР соответственно. Всем детям с низким риском развития АР было рекомендовано проведение скрининга в следующих возрастных категориях с обязательной профилактикой и снижением воздействия управляемых факторов риска.
Всем пациентам с высоким риском реализации АР по данным обследования была рекомендована превентивная фармакологическая терапия в период начала ОРИ, включающая в себя базисные препараты для лечения АР в зависимости от степени выраженности симптомов [8, 11]. Превентивная терапия АР в группах высокого риска была назначена согласно стандартным клиническим рекомендациям и в зависимости от возраста пациента (табл. 1).

На этапе расширенной диагностики, согласно нашему алгоритму, часть пациентов (n=50, с отсутствием характерных изменений на слизистой носа, с отрицательными кожными тестами, sIgE и отрицательными результатами цитологических исследований смывов) были маршрутизированы на проведение скрининга в следующем возрастном периоде, им проведена оценка риска реализации АР. По результатам исследования 32/50 (64%) детей имели высокий риск формирования АР, 18/50 (36%) — низкий. Группе пациентов с высоким риском реализации АР было рекомендовано проведение превентивной медикаментозной терапии в соответствии с возрастом в период течения ОРИ.
На этапе углубленной диагностики выставлен диагноз АР у 4/50 (8%) детей в возрасте до 5 лет, у 3/50 (6%) — 6–7 лет, у 1/50 (2%) — 8–12 лет и у 1/50 (2%) — 13 лет и старше. Таким образом, на этапе углубленной диагностики диагноз АР был установлен детям, которые, согласно стандартным методам диагностики, не имели диагноза АР. Диагноз в этом случае был установлен в более раннем возрасте. По результатам проведенного диагностического каскада было получено свидетельство о регистрации базы данных (свидетельство о регистрации № 20236620321 от 20.01.2023).
По данным статистических форм в 2022 г. к ГБУЗ МО «Одинцовская ОБ» было прикреплено 63 108 человек в возрасте от 0 до 17 лет. В г. Одинцово Московской области с 2017 по 2021 г. отмечен значительный рост численности детского населения, при этом также отмечалось ежегодное увеличение частоты встречаемости АР. В 2022 г. выявлен прирост детского населения по отношению к 2021 г. на 650 человек и увеличение количества пациентов с диагнозом АР, но при этом выявлено снижение количества детей с впервые выставленным диагнозом АР (табл. 2).
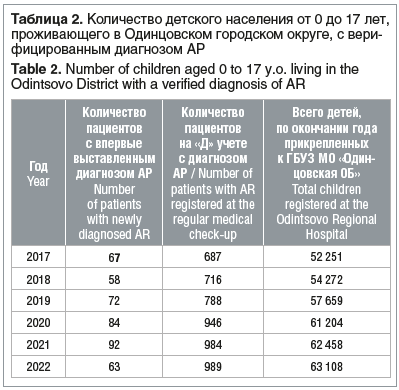
При анализе возрастных периодов впервые выставленных диагнозов АР выявлено, что сохраняется тенденция постановки диагноза АР в более старшем возрасте, но при этом частота верификации диагноза в группе детей до 5 лет увеличилась в 2 раза в 2022 г. В группе детей от 0 до 5 лет диагноз АР был выставлен у 15/63 (23,8%), 6–7 лет — у 14/63 (22,2%), 8–12 лет — у 24/63 (38,1%), 13 лет и старше — у 10/63 (15,9%) детей. В подростковом возрасте АР чаще выявляется у девочек, тогда как в младшей возрастной группе он чаще встречается у мальчиков.
При проведении катамнестического сравнительного анализа групп пациентов с высоким риском реализации АР было выявлено, что за 2022 г. в группе детей, не получавших превентивную терапию, у 12/50 (24%) был верифицирован диагноз АР, что составляет 12/63 (19%) от всех впервые выставленных диагнозов АР в 2022 г., а в группе детей, получавших превентивную терапию, диагноз АР был верифицирован у 6/50 (12%), что составило 6/63 (9,5%) от всех впервые верифицированных диагнозов. У детей, получавших терапию, уровень комплаентности был определен как высокий на основании приверженности лечению и поведенческих действий в период высокой заболеваемости и аллергонагрузки, что было подтверждено клиническими результатами.
Таким образом, в группе пациентов высокого риска реализации АР по результатам проведенного скринингово-диагностического каскада назначение превентивного лечения происходит в более раннем возрасте, что имеет прогностически более благоприятный результат. В группе пациентов, не получавших превентивную терапию, АР реализуется в 2 раза чаще в течение первого года катамнестического наблюдения.
Предложенный алгоритм диагностики снижает количество впервые выставленных диагнозов АР в более старшем возрасте и с более выраженной клинической картиной проявления заболевания, что обеспечивается персонифицированной превентивной профилактикой в группе пациентов, имеющих высокий риск развития АР.
Задержка с превентивной терапией и постановкой диагноза АР приводит к ухудшению клинического состояния пациента, дополнительным затратам на лечение, снижению качества жизни как самого пациента, так и его семьи. По результатам проведенного исследования в г. Одинцово выявлено, что применение каскадного подхода к диагностике и превентивному лечению в группе пациентов с высоким риском реализации АР позволяет сократить количество пациентов с впервые установленным диагнозом.
Заключение
Концепция скоординированного единого подхода скрининго-диагностического каскада и превентивно-профилактической терапии АР у пациентов из групп высокого риска реализации АР является эффективной, обоснованной и социально значимой. Предложено обоснование превентивной терапии, применяемой у пациентов с высоким риском реализации АР в период развития ОРИ, которая может создавать условия для развития местной сенсибилизации, запуска каскада минимального персистирующего воспаления и дальнейшего развития нарушения общего и местного гомеостаза. Данную группу пациентов можно отнести к группе с минимальными проявлениями АР на фоне ОРИ, у которых в ближайшем катамнестическом наблюдении может реализоваться АР с выраженными клиническими проявлениями. В настоящее время построение непрерывной каскадной модели «скрининг — диагностика — лечение» является доступным и простым в применении алгоритмом персонифицированного подхода к лечению и превентивной профилактике АР у детей, что также может оказать прямой эффект и на снижение риска реализации БА у детей. Разработанная итерационная модель является частью маршрута оказания медицинской помощи детям с высоким риском реализации АР и может быть применима во всех регионах, включенных в исследование.
Сведения об авторах:
Бережанский Павел Вячеславович — к.м.н., доцент кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ассистент кафедры клинической иммунологии, аллергологии и адаптологии ФНМО МИ РУДН; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 6; врач-пульмонолог ГБУЗ «Морозовская ДГКБ ДЗМ»; 119049, Россия, г. Москва, 4-й Добрынинский пер., д. 1/9; старший научный сотрудник отдела педиатрии ГБУЗ МО «НИКИ детства МЗ МО»; 115093, Россия, г. Москва, ул. Большая Серпуховская, д. 62; ORCID iD 0000-0001-5235-5303.
Малахов Александр Борисович — д.м.н., профессор кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; главный внештатный детский специалист-пульмонолог Департамента здравоохранения г. Москвы, врач-пульмонолог ГБУЗ «Морозовская ДГКБ ДЗМ»; 119049, Россия, г. Москва, 4-й Добрынинский пер., д. 1/9; руководитель отдела педиатрии ГБУЗ МО «НИКИ детства МЗ МО»; 115093, Россия, г. Москва, ул. Большая Серпуховская, д. 62; ORCID iD 0000-0002-2686-8284.
Геппе Наталья Анатольевна — д.м.н., профессор, заслуженный врач РФ, заведующая кафедрой детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0003-0547-3686.
Колосова Наталья Георгиевна — к.м.н., доцент кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-5071-9302.
Татаурщикова Наталья Станиславовна — д.м.н., профессор, заведующий кафедрой клинической иммунологии, аллергологии и адаптологии РУДН; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 6; ORCID iD 0000-0002-3486-8188.
Контактная информация: Бережанский Павел Вячеславович, e-mail: p.berezhanskiy@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 30.06.2023.
Поступила после рецензирования 21.07.2023.
Принята в печать 11.08.2023.
About the authors:
Pavel V. Berezhanskiy — C. Sc. (Med.), Associate Professor of the Department of Children’s Diseases, N.F. Filatov Clinical Institute of Children’s Health, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; Assistant Professor of Clinical Immunology and Allergology, RUDN University; 6, Miklukho-Maklaya str., Moscow, 117198, Russian Federation; pulmonologist, Morozov Children’s City Clinical Hospital; 1/9, 4th Dobryninskiy pass., Moscow, 119049, Russian Federation; Senior Researcher of the Department of Pediatrics, Research Clinical Institute of Childhood of the Moscow Region; 62, Bolshaya Serpukhovskaya str., Moscow, 115093, Russian Federation; ORCID iD 0000-0001-5235-5303.
Alexander B. Malakhov — Dr. Sc. (Med.), Professor of the Department of Children’s Diseases, N.F. Filatov Clinical Institute of Children’s Health, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; Chief Consultant Children Pulmonologist, Morozov Children’s City Clinical Hospital; 1/9, 4th Dobryninskiy pass., Moscow, 119049, Russian Federation; Head of the Department of Pediatrics, Research Clinical Institute of Childhood of the Moscow Region; 62, Bolshaya Serpukhovskaya str., Moscow, 115093, Russian Federation; ORCID iD 0000-0002-2686-8284.
Natalia A. Geppe — Dr. Sc. (Med), Professor, Honored Doctor of the Russian Federation, Head of the Department of Children’s Diseases, N.F. Filatov Clinical Institute of Children’s Health, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0003-0547-3686.
Natalia G. Kolosova — C. Sc. (Med.), Associate Professor of the Department of Children’s Diseases, N.F. Filatov Clinical Institute of Children’s Health, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0001-5071-9302.
Natalia S. Tataurshchikova — Dr. Sc. (Med.), Professor, Head of the Department of Clinical Immunology and Allergology, RUDN University; 6, Miklukho-Maklaya str., Moscow, 117198, Russian Federation; ORCID iD 0000-0002-3486-8188.
Contact information: Pavel V. Berezhanskiy, e-mail: p.berezhanskiy@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 30.06.2023.
Revised 21.07.2023.
Accepted 11.08.2023.
Информация с rmj.ru






