Содержание статьи
Клинико-лабораторные критерии в оценке эффективности терапии
пациентов с синдромом раздраженного кишечника
И. В. Козлова*, доктор медицинских наук, профессор
Ю. Н. Мялина*, кандидат медицинских наук
О. Е. Бадиева*
Т. А. Тихонова*
М. А. Осадчук**, доктор медицинских наук, профессор
* ГБОУ ВПО СГМУ им. В. И. Разумовского МЗ РФ, Саратов
** ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Синдром раздраженного кишечника (СРК) является одним из наиболее частых
диагнозов в практике врача-гастроэнтеролога. На долю этой патологии приходится
от 25% до 50% всех посещений врача данной специальности. Заболевание широко
распространено в промышленно развитых странах, где частота СРК составляет 15–23%
в популяции, при этом установлено, что 2/3 лиц, испытывающих симптомы СРК, к
врачам не обращаются. Пик заболеваемости приходится на молодой, трудоспособный
возраст — 30–40 лет [1, 2]. Медико-социальная значимость СРК определяется
высоким уровнем затрат в первичном звене оказания медицинской помощи, сниженным
качеством жизни пациентов, сравнимым с таковым при сахарном диабете, хронической
сердечной и почечной недостаточности, циррозе печени [3–5].
Гетерогенность триггеров, механизмов возникновения, вариабельность симптомов
затрудняют поиск надежных критериев ранней диагностики СРК. Значимую роль в
развитии СРК играют генетические, средовые, психосоциальные факторы, влияющие на
висцеральную гиперчувствительность, нарушение связей по оси «мозг–кишечник» и
двигательной активности кишечника [6, 7].
Психосоматическая концепция считается одной из наиболее доказанных при СРК.
Хронические стрессы являются триггерами возникновения и обострения заболевания
[8]. В условиях стресса повышается экспрессия нейропептидов (мотилин,
вазоинтестинальный пептид, субстанции Р), которая инициирует и поддерживает
воспалительные изменения в слизистой оболочке кишки [9, 10]. Установлена связь
между состоянием тревоги, депрессии у больных СРК и дисбалансом цитокинов в
плазме крови и слизистой оболочке сигмовидной кишки [11].
Значимую роль в регуляции иммунной системы кишечника играют тучные клетки,
продуцирующие гистамин, триптазу и другие биологически активные вещества [12].
При этом выявляется повышенная количественная плотность нейроэндокринных клеток
и мастоцитов, что предполагает участие нейроиммунных механизмов в патогенезе СРК.
Гистамин и триптаза обнаружены в биоптатах слизистой оболочки кишки пациентов с
СРК, что вызывает повышенную мезентериальную сенсорную активацию, активирует
гистамин-1-рецепторы и рецепторы к протеиназе-2, потенцируя развитие
висцеральной гиперчувствительности [13].
В литературе приводятся убедительные доказательства относительно роли
иммунной системы кишечника в развитии постинфекционного СРК (пСРК) [14, 15].
Так, примерно один из десяти пациентов с СРК отмечал эпизод острой кишечной
инфекции перед развитием заболевания [16]. Проспективные исследования показали,
что у 3–36% пациентов, перенесших острую кишечную инфекцию, в дальнейшем
формируются стойкие симптомы пСРК [17]. Механизмы, которые вызывают пСРК, могут
включать остаточные воспалительные проявления в кишечнике, изменения
функционирования, энтерохромаффинных и тучных клеток, нервов и микробиоты
желудочно-кишечного тракта [18]. Следствием перенесенной в прошлом кишечной
инфекции становятся стойкие изменения слизистой кишечника с инфильтрацией
иммунными клетками и увеличением синтеза различных цитокинов [19]. Проведенные
исследования продемонстрировали наличие врожденных изменений иммунного ответа с
активацией toll-подобных рецепторов у этих пациентов [20].
В последние годы активно обсуждаются вопросы, связанные с тесным
взаимодействием центральной и местной нейроэндокринной регуляции
желудочно-кишечного тракта (ЖКТ) и микробиоты кишечника. Полагают, что
освобождение сигнальных молекул микробиоты кишечника стимулирует
нейроэндокринную активность, обеспечивая продукцию катехоламинов, серотонина,
эндорфинов и цитокинов. С другой стороны, центральная нервная система играет
важную роль в регуляции продукции этих молекул [21].
Таким образом, СРК в настоящее время рассматривается как многофакторное по
происхождению и клинически неоднородное заболевание, что затрудняет
стандартизацию терапии. Заслуживают внимания данные о том, что со временем у 75%
пациентов с СРК возможен переход от одного варианта болезни к другому. При этом
частота перехода СРК с диареей в СРК с запором достигает 29% [22, 23].
Перспективным направлением в лечении СРК представляется применение препарата
Колофорт®. Это единственный препарат комплексного действия, влияющий не на
отдельные симптомы, а на основные звенья патогенеза СРК, что обеспечивает
универсальный эффект в терапии СРК вне зависимости от клинического варианта
заболевания. Препарат Колофорт представляет собой комбинацию действующих веществ
в релиз-активной форме: антител к мозгоспецифическому белку S-100 (РА-АТ S100),
антител к гистамину (РА-АТ Гис) и антител к человеческому фактору некроза
опухоли-альфа (ФНО-α) (РА-АТ ФНО). Молекулярной мишенью РА-АТ S100 является
белок S100, который участвует в регуляции разнообразных внутриклеточных
процессов, включая передачу внутриклеточного сигнала, рост, дифференцировку,
апоптоз нейронов и глии. РА-АТ S100 способствует устранению беспокойства,
чувства тревоги и страха, уменьшению внутреннего напряжения, повышенной
раздражительности. РА-АТ Гис восстанавливает нарушенную моторно-эвакуаторную и
секреторную функции ЖКТ, обладает противовоспалительным, спазмолитическим и
анальгетическим действием. Механизм действия РА-АТ ФНО заключается во влиянии на
продукцию ФНО-α и сопряженных с ним цитокинов. Под влиянием РА-АТ ФНО
происходили достоверные изменения в системной продукции (содержание в сыворотке)
исследованных цитокинов — ФНО-α, интерлейкинов (ИЛ-1, ИЛ-6, ИЛ-4, ИЛ-10),
гамма-интерферона. Таким образом, противовоспалительный эффект РА-АТ ФНО
обусловлен подавлением продукции провоспалительных цитокинов. Полученные данные
были подтверждены в клинических исследованиях [24].
Целью настоящего исследования было оценить клинические и микробиологические
эффекты препарата Колофорт® при разных клинических вариантах СРК.
Материалы и методы исследования
В исследование включены 53 пациента (39 женщин и 14 мужчин).
Критерии включения: верифицированный СРК с диареей и смешанный вариант
заболевания, подписанное информированное согласие на участие в исследовании.
Критериями исключения служили возраст старше 50 лет, наличие сопутствующей
органической патологии ЖКТ в фазе обострения, в анамнезе — оперативные
вмешательства, острые кишечные инфекции и паразитарные инвазии, изменения
статуса курения в течение последнего месяца, кормление грудью или беременность,
аллергическая предрасположенность к препарату или его компонентам, прием
препаратов, которые, по мнению исследователей, могли бы влиять на результаты.
Включенные в исследование пациенты были рандомизированы на группы: 1-я — 32
пациента (8 мужчин и 24 женщины) с СРК с диареей (СРК-Д); 2-я — 21 пациент (6
мужчин, 15 женщин) со смешанным вариантом СРК (СРК-С). Средний возраст
исследуемых составил 37,2 ± 1,3 года. Пациентам назначен Колофорт® по 2 таблетки
2 раза в сутки сублингвально вне приема пищи в течение 12 недель. Отдельные
пациенты при выраженных симптомах заболевания на начальных этапах лечения
принимали симптоматическую терапию (дротаверин, Смекту). Потребность в
симптоматической терапии дротаверином, Смектой возникла на 1-й неделе нашего
исследования у 5 пациентов с СРК-С и у 3 пациентов с СРК-Д.
Диагноз СРК верифицирован в соответствии с Римскими критериями III (2006 г.)
[22]. Проводилось комплексное клинико-лабораторное и инструментальное
обследование; дополнительно исключался острый инфекционный процесс
(бактериологический анализ кала на кишечные патогены, копроовоскопия,
определение АТ к кишечным гельминтам).
Мониторинг клинических проявлений СРК оценивался результатами шкал и
опросников: визуально-аналоговой шкалой (ВАШ) оценки выраженности симптомов СРК
(Visual Analog Scale — Irritable Bowel Syndrome — VAS-IBS), индексом
висцеральной чувствительности (Visceral Sensitivity Index — VSI), опросником
качества жизни при СРК (Irritable Bowel Syndrome — Quality of Life — IBS-QoL),
дневником дефекации.
В работе использованы методы диагностики дисбактериоза кишечника в
соответствии с отраслевым стандартом «Протокол ведения больных. Дисбактериоз
кишечника» (ОСТ 91500.11.0004–2003, утвержден Приказом МЗ РФ № 231 от
09.06.2003). Включенным в исследование пациентам в начале наблюдения были
выполнены бактериологические исследования кала с выделением степеней
дисбактериоза. Повторная оценка степени дисбиоза проводилась через 4 недели
после окончания терапии препаратом Колофорт®. Бактериологические исследования
выполнялись в Медицинской лаборатории KDL.
Динамическое наблюдение пациентов осуществлялось в течение 5 визитов на
протяжении 12 недель. Проведение дополнительных визитов в ходе исследования не
потребовалось. Статистическую обработку результатов производили в пакете
компьютерных программ Excel и Statistica 6.0 с последующим анализом полученных
материалов, с использованием критерия Стьюдента. Анализ корреляционных связей
изученных параметров определяли по Спирмену с оценкой статистической значимости
каждой корреляционной связи, анализ взаимосвязи параметров — кластерным анализом
с использованием критерия Пирсона.
Исследование одобрено Локальным этическим комитетом на базе ГУЗ «Саратовская
городская клиническая больница № 5».
Результаты исследования
Средняя продолжительность болезни в группах СРК-Д и СРК-С составила 24,3 ±
0,34 и 21,4 ± 0,64 месяца соответственно.
До включения в исследование пациенты получали симптоматическую терапию без
стойкого и продолжительного эффекта. 74,5% обследованных пациентов развитие
обострения СРК связывали со стрессами.
Абдоминальная боль в группах СРК-Д до начала лечения по 10-балльной ВАШ
составила 0,6 ± 0,3 балла (рис. 1). После 12 недель терапии препаратом Колофорт®
показатель ВАШ в группе СРК-Д не превышал 0,4 балла.
В группе СРК-С до начала лечения отмечался выраженный абдоминальный болевой
синдром: интенсивность боли по ВАШ достигала 5,3 ± 0,18 балла. По окончании
терапии отмечена значимая положительная динамика со снижением показателя до 0,2
балла (p < 0,05).
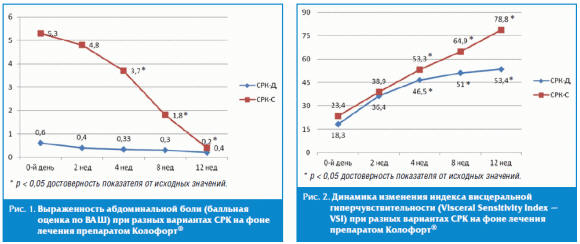
Динамика индекса висцеральной гиперчувствительности (Visceral Sensitivity
Index — VSI) отражена в рис. 2. Максимальные изменения по завершении курса
терапии наблюдались в группе пациентов с СРК-С, когда суммарный балл индекса
висцеральной гиперчувствительности повышался со значений 23,4 до 78,8 (p <
0,05). В группе СРК-Д отмечалась аналогичная динамика, с достоверными отличиями
от исходных значений. Индекс висцеральной гиперчувствительности напрямую зависел
от интенсивности болевого синдрома у пациентов с СРК-С (r = 0,57; р < 0,05).
Таким образом, на фоне терапии препаратом Колофорт® у пациентов выявлено
существенное повышение болевого порога и снижение висцеральной
гиперчувствительности.
Значимым критерием оценки эффективности препарата Колофорт® явилось
исследование частоты и формы стула. Форма стула оценивалась по Бристольской
шкале [22], его частота отмечалась пациентами в дневниках самонаблюдения. До
включения в исследование у пациентов с СРК-Д частота стула составила 3–7 раз в
сутки, диарея регистрировалась преимущественно в утренние часы и первой половине
дня. У пациентов этой группы выявлены 6-й и 7-й типы по Бристольской шкале. На
фоне приема препарата Колофорт® у пациентов изменения формы стула стали
соответствовать 3–5 типам, а частота стула не превышала 2 раз (в среднем 1,1) в
сутки (рис. 3).
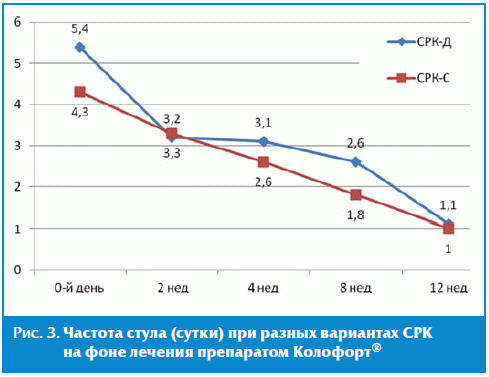
У пациентов с СРК-С до лечения частота дефекации достигала 3–5 раз в сутки (в
среднем 4,3 раза). После курса терапии варьировала от 1 раза в сутки до 1 раза в
2 суток (в среднем 1 раз в сутки). Форма стула также изменилась: с 6–7 типов на
4-й по Бристольской шкале.
Исследование качества жизни (КЖ) в динамике разных вариантов СРК проводилось
с помощью опросника Irritable Bowel Syndrome — Quality of Life (IBS-QoL). На
старте исследования у пациентов с СРК были изменены все параметры КЖ. Балльная
оценка по каждому из показателей варьировала от 24,6 до 66,6. Пациенты обеих
групп отмечали хроническую усталость, неспособность из-за симптомов болезни
качественно выполнять повседневные профессиональные обязанности, включая учебу.
В ходе тестирования на старте исследования были выявлены снижение
работоспособности, ограничение объема нагрузок, боязнь возвращения или усиления
симптомов в связи с физической активностью. До включения в исследование в группе
пациентов с СРК-Д снижались общий тонус и физическая активность, значимо
страдали эмоциональная и психическая сферы. В группе СРК-С изменения
эмоциональной и психической сферы были выражены более ярко по сравнению с
соответствующими показателями в группе СРК-Д.
После 12-недельного курса терапии наблюдался эффект препарата Колофорт® в
виде влияния на различные параметры физического и психического здоровья
пациентов: выявлены положительные изменения в повседневной, общественной и
личной, в том числе сексуальной, жизни пациентов. Установлена связь между
снижением выраженности абдоминальной боли (r1 = 0,4 при p < 0,05),
нормализацией стула (r2 = 0,3 при p < 0,05) и позитивными изменениями
в психическом статусе пациентов с СРК.
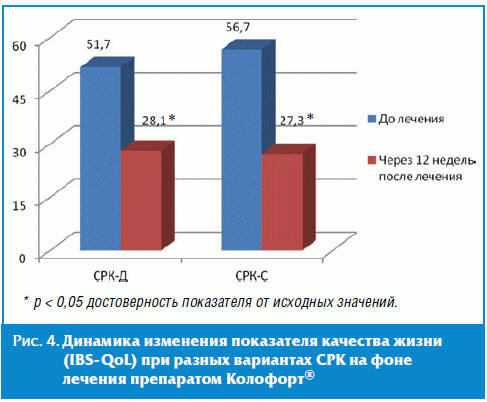
В целом качество жизни пациентов с СРК к окончанию терапии препаратом
существенно повышалось (рис. 4).
Вероятно, анальгетический эффект препарата Колофорт®, его позитивное влияние
на висцеральную гиперчувствительность, нормализация моторики кишечника
обеспечивали устранение внутреннего напряжения и тревоги при СРК; в свою
очередь, улучшение психологического состояния поддерживало нормальное
функционирование кишечника, создавая условия для дальнейшей мотивации пациентов
к продолжению терапии.
Дисорганизации регуляции и моторики при СРК, появление висцеральной
гиперчувствительности оказывают влияние на постоянный состав кишечной микробиоты.
В силу дисбиотических изменений микробиоты (отсутствие или дефицит основных
бактериальных симбионтов — бифидобактерий, уменьшение количества молочнокислых
палочек) редуцируются процессы пищеварения (в основном нарушается гидролиз
клетчатки) и всасывания. Следствием этих изменений могут стать нарушения
двигательной, секреторной, пищеварительной и других функций кишечника [25].
Накопление микробных эндотоксинов в химусе способствует разрушению слизистого
барьера кишечника, увеличению проницаемости слизистой и может являться предтечей
воспалительных процессов в стенке кишечника. Нами проведена оценка влияния
препарата Колофорт® на состояние биоценоза толстой кишки. Оценка показателей
биоценоза проводилась до включения в исследование и после окончания проводимой
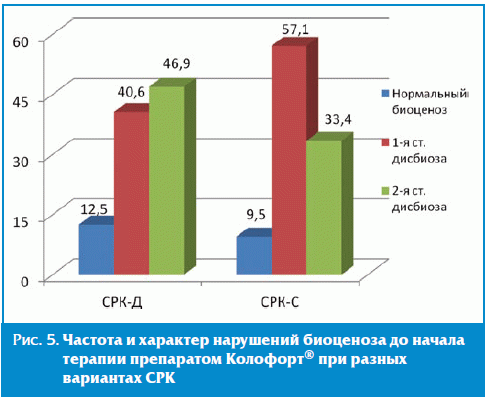
терапии. При бактериологическом исследовании кала на старте исследования у 84,5%
всех пациентов с СРК были обнаружены нарушения микробного пейзажа с
количественными и видовыми изменениями состава кишечной микрофлоры. При этом в
группе СРК-Д 1-я степень дисбиоза выявлена у 40,6% обследованных, 2-я степень
дисбиоза — у 46,9%. В группе СРК-С нарушения биоценоза 1-й степени выявлены у
57,1%, 2-я степень дисбиотических расстройств регистрировались у 33,4%.
Нормальные показатели микробного пейзажа регистрировались практически одинаково
часто в обеих группах пациентов — у 12,5% и 9,5% пациентов соответственно (рис.
5).
При исследовании состава кишечной флоры отмечались изменения количественных
показателей облигатных представителей анаэробной (бифидобактерии и лактобактерии)
и аэробной флоры (E. coli, Enterococcus spp., Streptococcus spp., Proteus
spp., грибы рода Candida).
После окончания терапии препаратом Колофорт® количественные показатели
биоценоза толстой кишки значительно улучшились, дисбиоз 1-й и 2-й степени
определялся значимо реже (рис. 6).
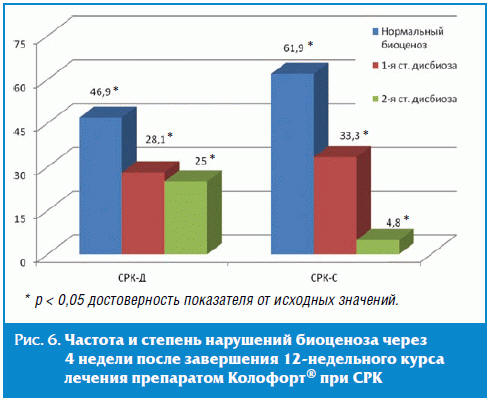
Результаты проведенных исследований показали, что терапия препаратом Колофорт®
по схеме 4 таблетки в сутки на два приема на протяжении 12 недель обеспечивала
редукцию клинических проявлений СРК с диареей и при смешанном варианте болезни,
улучшала состояние биоценоза толстой кишки и способствовала повышению качества
жизни по психологическим и физическим шкалам. Полученные нами результаты
клинической оценки эффектов препарата Колофорт® во многом схожи с
опубликованными в литературе. Так, в многоцентровом двойном слепом
рандомизированном плацебо-контролируемом исследовании, в котором приняли участие
128 пациентов с разными вариантами СРК, были продемонстрированы анальгетический
и анксиолитические эффекты препарата, улучшение показателей физического и
психического здоровья пациентов [26].
Выявленные позитивные изменения могут быть связаны с восстановлением
регуляторного баланса в иммунной системе кишечника, обусловленным нормализацией
соотношения про- и противоспалительных цитокинов за счет модулирующих эффектов
антител к ФНО-α в составе препарата Колофорт®. Оптимальное сочетание РА-АТ S100,
РА-АТ Гис и РА-АТ ФНО позволяет нормализовать нейрогуморальную регуляцию
деятельности кишечника, снизить висцеральную гиперчувствительность рецепторов
кишки, уменьшить болевой синдром, восстановить нарушенную моторику ЖКТ, улучшить
состояние кишечного биоценоза и повысить качество жизни пациентов с СРК в целом.
Результаты, демонстрирующие эффект препарата Колофорт® при СРК, сходный с
пребиотическим, определяют перспективы дальнейших исследований.
Выводы
- При синдроме раздраженного кишечника терапия препаратом Колофорт® в
течение 12 недель оказывает положительное влияние на состояние пациентов с
диареей и при смешанным варианте заболевания: повышается порог висцеральной
чувствительности, уменьшается абдоминальная боль, нормализуется паттерн стула. - Колофорт® улучшает психоэмоциональное состояние пациентов при разных
вариантах течения СРК, значимо повышает качество жизни по шкалам физического и
психического здоровья, что, в свою очередь, мотивирует пациентов к продолжению
терапии. - Через 4 недели после 12-недельной терапии препаратом Колофорт® выявлено
улучшение показателей микробиоценоза кишечника. С 12,5% до лечения до 47%
пациентов при СРК-Д и от 9,5% до лечения до 62% с СРК-С возросло количество
пациентов с эубиозом. Представляется целесообразным дальнейшее изучение
пребиотических эффектов препарата. - При курсовом лечении препаратом Колофорт® не зарегистрировано
нежелательных реакций, связанных с приемом препарата.
Литература
-
Бурулова О. Е., Козлова И. В., Мялина Ю. Н. Синдром раздраженного
кишечника как биопсихосоциальное заболевание // Саратовский научно-медицинский
журнал. 2012; 2: 232–237. -
Козлова И. В., Пахомова А. Л. Современный пациент
гастроэнтерологического профиля: штрихи к клиническому портрету //
Экспериментальная и клиническая гастроэнтерология. 2015; 6: 4–10. -
Canavan C., West J., Card T. Review article: the economic impact
of the irritable bowel syndrome // Aliment. Pharmacol. Ther. 2014; 40:
1023–1034. -
Koloski N., Boyce P., Jones M., Talley N. What level of IBS
symptoms drives impairment in health-related quality of life in community
subjects with irritable bowel syndrome? // Qual Life Res. 2012; 21: 829–836. -
Monnikes H. Quality of life in patients with irritable bowel
syndrome // J. Clin. Gastroenterol. 2011; 45 (Suppl.): 98–101. -
Bindels L. B., Dewulf E. M., Delzenne N. M. GPR43/FFA2:
physiopathological relevance and therapeutic prospects // Trends Pharmacol Sci.
2013; 34: 226–232. -
Muscatello M. R., Bruno A., Scimeca G., Pandolfo G., Zoccali R. A.
Role of negative affects in pathophysiology and clinical expression of
irritable bowel syndrome // World J. Gastroenterol. 2014; 20: 7570–7586. -
Berman S., Suyenobu B., Naliboff B. D. et al. Evidence for
alterations in central noradrenergic signaling in irritable bowel syndrome //
Neuroimage. 2012; 63: 1854–1863. -
Ohman L., Stridsberg M., Isaksson S., Jerlstad P., Simren M.
Altered levels of fecal chromogranins and secretogranins in IBS: relevance for
pathophysiology and symptoms? // Am. J. Gastroenterol. 2012; 107: 440–447. -
Козлова И. В., Мялина Ю. Н., Бадиева О. Е.
Клинико-диагностическое значение содержания нейротрансмиттеров при
функциональных и воспалительных заболеваниях кишечника // Молекулярная
медицина. 2015; 3: 8–13. -
Macsharry J., O’Mahony L., Fanning A., Bairead E., Sherlock G.,
Tiesman J., Fulmer A., Kiely B., Dinan T. G., Shanahan F. et al. Mucosal
cytokine imbalance in irritable bowel syndrome // Scand J Gastroenterol. 2008;
43: 1467–1476. -
Barbara G., Wang B., Stranghellini V. et al. Mast cell-dependent
excitation of visceral-nociceptive sensory neurons in irritable bowel syndrome
// Gastroenterol. 2007; 132: 26–37. -
Guilarte M., Santos J., de Torres I., Alonso C., Vicario M.., Ramos L.
et al. Diarrhoea-predominant IBS patients show mast cell activation and
hyperplasia in the jejunum // Gut. 2007; 56: 203–209. -
Simren M., Barbara G., Flint H. J., Spiegel B. M., Spiller R. C.,
Vanner S. et al. Intestinal microbiota in functional bowel disorders: a
Rome foundation report // Gut. 2013; 62: 159–166. -
Natividad J. M., Verdu E. F. Modulation of intestinal barrier by
intestinal microbiota: pathological and therapeutic implications // Pharmacol
Res. 2013; 69: 42–51. -
Mearin F., Perez-Oliveras M., Perello A., Vinyet J., Ibanez A.,
Coderch J. et al. Dyspepsia and irritable bowel syndrome after a
Salmonella gastroenteritis outbreak: one-year follow-up cohort study //
Gastroenterology. 2005; 129: 98–104. -
Thabane M., Kottachchi D. T., Marshall J. K. Systematic review
and meta-analysis: The incidence and prognosis of post-infectious irritable
bowel syndrome // Aliment Pharmacol Ther. 2007; 26: 535–544. -
Natividad J. M., Verdu E. F. Modulation of intestinal barrier by
intestinal microbiota: pathological and therapeutic implications // Pharmacol
Res. 2013; 69: 42–51. -
Tana C., Umesaki Y., Imaoka A., Handa T., Kanazawa M., Fukudo S.
Altered profiles of intestinal microbiota and organic acids may be the origin
of symptoms in irritable bowel syndrome // Neurogastroenterol Motil. 2010; 22:
512–519. -
Brint E. K., MacSharry J., Fanning A., Shanahan F., Quigley E. M.
Differential expression of toll-like receptors in patients with irritable
bowel syndrome // Am J Gastroenterol. 2011; 106: 329–336. -
Hyland N. P., Quigley E. M., Brint E. Microbiota host
interactions in irritable bowel syndrome: epithelial barrier, immune
regulation and brain-gut interactions // World journal of gastroenterology:
WJG. 2014; 20 (27): 8859–8866. -
Drossman D. A., Dumitrascu D. L. Rome III: New standard for
functional gastrointestinal disorders // J. Gastrointestin. Liver Dis. 2006;
15: 237–241. -
Quigley E. M., Abdel-Hamid H., Barbara G., Bhatia S. J., Boeckxstaens
G., de Giorgio R., Delvaux M., Drossman D. A., Foxx-Orenstein A. E., Guarner
F. et al. A global perspective on irritable bowel syndrome: a consensus
statement of the World Gastroenterology Organisation Summit Task Force on
irritable bowel syndrome // J Clin Gastroenterol. 2012; 46: 356–366. -
Осадчук М. А. Колофорт — новый препарат в терапии функциональных
расстройств кишечника // Медицинский альманах. 2015; 1: 57–59. -
Григорьев П. Я., Яковенко Э. П. Синдром раздраженной кишки,
ассоциированный с дисбактериозом // Consilium Medicum. 2000, 2 (7). http://www.con-med.ru/magazines/consilium_medicum/consilium_medicum-07–2000/. -
Авалуева Е. Б., Адашева Т. В., Бабаева А. Р., Бурдина Е. Г., Киреева
Н. В., Ленская Л. Г. и др. Эффективность и безопасность применения
Колофорта при синдроме раздраженного кишечника: итоги многоцентрового двойного
слепого плацебо-контролируемого рандомизированного клинического исследования
// Приложение Сonsilium Medicum (Гастроэнтерология). 2014; 1: 36–43.
Статья опубликована в журнале
Лечащий Врач
материал MedLinks.ru







