
Введение
Коррекция отсроченных осложнений при введении инъекционных тканевых наполнителей (ИТН) в эстетической медицине не требует экстренного медицинского вмешательства, однако остается актуальной темой не только ввиду отсутствия принятых клинических протоколов и рекомендаций по лечению и устранению данных осложнений, но и в связи с постоянным обновлением каталога ИТН как уже известных химических групп, так и вновь изобретенных1. В большей степени это связано с увеличением числа медицинских изделий из разряда тканевых наполнителей сложного состава, не имеющего полного биоидентичного аналога в матриксе соединительной ткани. Одной из таких групп дермальных ИТН являются наполнители на основе энантиомеров полимолочной кислоты, не имеющих прямой тождественности с элементами дермального матрикса [1]. Сложный многокомпонентный состав таких наполнителей представлен как преобладанием образца энантиомера одного типа (к примеру, L-форма полимолочной кислоты), так и рацемической смесью обоих вариантов стереоизомеров — L- и D-формы полимолочной кислоты. Несмотря на то, что продукты биодеградации данных субстанций, представленные многоступенчатым и многоэтапным переходом полимолочной кислоты в мономер молочной и к окончательным продуктам в виде углекислого газа и воды, являются аналоговыми и биосовместимыми с дермальными компонентами, тем не менее возникновение отсроченных осложнений в виде появления локальных узелков после проведения эстетических манипуляций с использованием ИТН остается малопрогнозируемым и малопрофилактируемым процессом [2].
Цель исследования: разработка и изучение эффективности коррекции гранулемы как отсроченного осложнения при использовании ИТН на основе полимолочной кислоты с применением аутологичной плазмы крови человека (АПКЧ).
Содержание статьи
Материал и методы
Проведено интервенционное продольное проспективное исследование на клинической базе кафедры кожных болезней и косметологии факультета дополнительного профессионального образования РНИМУ им. Н.И. Пирогова Минздрава России, а также в двух медицинских центрах г. Москвы (одобрено локальным этическим комитетом РНИМУ им. Н.И. Пирогова Минздрава России, протокол № 224 от 19 декабря 2022 г.). После первичного скрининга (длительность от 1 до 10 нед.) были получены результаты ультразвукового исследования (аппарат для УЗИ Canon Aplio i800 (Canon, Япония), высокочастотный датчик: i24LX8 с частотным диапазоном 8,8–24,0 МГц) для фиксации изначальных размеров и количества гранулем. Далее было выполнено патоморфологическое исследование (рис. 1) с помощью панч-биопсии (DERMO PUNCH®, SteryLab, Италия), подтвердившее диагноз: гранулемы инородного тела кожи шеи (L92.3).
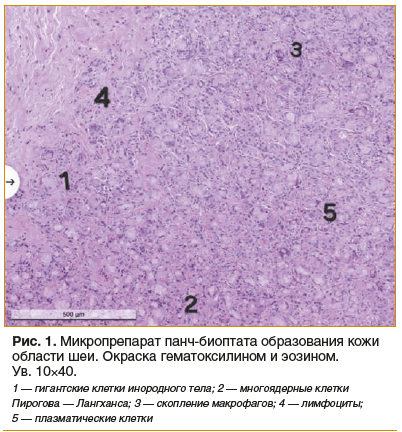
Исследование проводилось с 14 августа 2023 г. по 20 мая 2024 г., включая периоды отбора, скрининга, лечения (5 нед.) и последующего наблюдения в течение 24 нед. Двумя основными конечными точками были количество недель ремиссии за весь период наблюдения.
Участницы исследования (n=27), женщины в возрасте от 46 до 62 лет, были отобраны согласно следующим критериям включения:
-
наличие введенного ИТН на основе полимолочной кислоты;
-
отсутствие косметологических процедур (кроме введения изучаемого ИТН) в течение предшествующего года;
-
отсутствие приема изотретионина в течение предшествующих 6 мес.;
-
отсутствие резкого снижения массы тела (более 5 кг) в течение предшествующего года;
-
подписанное информированное согласие на участие в исследовании;
-
подписанное информированное согласие на фотодокументацию области лица и шеи (рис. 2).
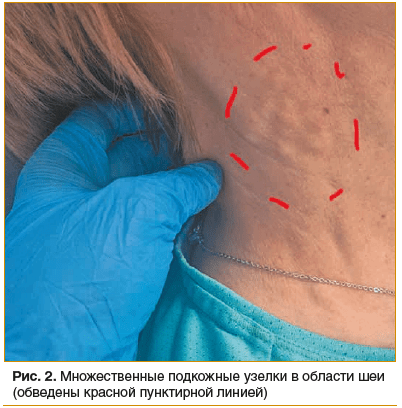
Предлагаемый протокол и схема (рис. 3) введения АПКЧ предполагают первичное введение в центральную часть каждой гранулемы 0,1 мл АПКЧ, а затем, вторым этапом, широкое веероподобное обкалывание границ гранулемы с отступом 2–5 мм от ее пальпируемых границ с введением 0,1–0,2 мл АПКЧ на каждый вкол [3].
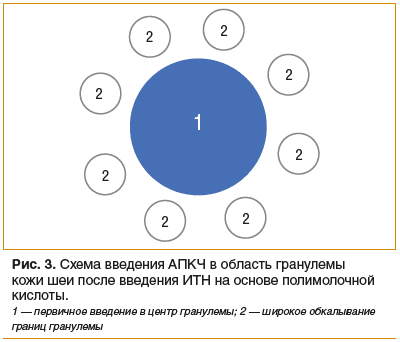
В связи с наличием публикаций о самопроизвольном разрешении гранулем, возникших после применения ИТН, было принято решение в качестве условной контрольной группы выбрать противоположную сторону области шеи тех же пациенток, также имеющую отсроченное осложнение в виде гранулем, однако не получающих терапию не только по предложенному протоколу и схеме, но и в какой-либо другой форме [4].
Результаты и обсуждение
Выбор метода лечения основывался на предположительном механизме позитивного изменения рН-показателей зоны скопления клеточных ростков, способных к фагоцитозу, за счет введения АПКЧ, что способствует разобщению плотных клеточных контактов внутри самой гранулемы и, как следствие, уменьшению ее размеров и выраженности вплоть до полного регресса. Согласно дизайну исследования повтор процедуры лечения проводили каждые 10 дней в течение 5 нед. (3 инъекции).
Применение АПКЧ уже к 5-й неделе от начала лечения привело к значительному уменьшению размеров и выраженности гранулем (64% по сравнению с контрольной группой, р<0,001), оцениваемых по результатам двух измерений (максимальные поперечный и продольный размеры) с помощью ультразвукового исследования. Доля пациенток, достигших частичного регресса гранулем к 4-й неделе, составила 32%, а к 25-й — 87,3%.
Хотя между группой с гранулемами, получающей лечение АПКЧ, и группой без лечения не было существенной разницы в процентном соотношении имеющихся нежелательных явлений (НЯ), в течение периода исследования наблюдался дисбаланс НЯ, связанных с инъекцией АПКЧ (у 32% в группе с лечением и у 0% в группе без лечения). В целом наиболее частыми НЯ, о которых сообщалось, были подкожные гематомы в местах инъекций (у 32% участниц в группе лечения), отек (у 18% пациенток в группе лечения). После первой инъекции 6 (22,2%) пациенток отмечали значительное уплощение гранулем, но при этом увеличение их площади. Однако данное явление полностью проходило после повторного введения АПКЧ на следующем этапе лечения. Системных реакций во всех случаях отмечено не было.
Также стоит отметить, что на образование отсроченных осложнений (гранулемы) при использовании ИТН на основе полимолочной кислоты влияют многие факторы, такие как: химический состав ИТН, объем инъекции, примеси, присутствующие в наполнителях, физические свойства наполнителей, соблюдение протокола и слоя введения и др. [5, 6]. Несмотря на одинаковые химические свойства энантиомеров как таковых, у ИТН на основе полимолочной кислоты эти химические свойства будут сохраняться, только если остальные задействованные вещества (реагенты, катализатор, растворитель) имеют симметричные молекулы, что крайне редко встречается в суспензиальной форме наполнителя. Возможно, это может послужить основой для уточнения разницы в частоте встречаемости НЯ различных по составу и разных производителей ИТН на основе полимолочной кислоты для дальнейшей оптимизации использования изложенного протокола лечения отсроченных НЯ в клинической практике.
Заключение
Количество проводимых косметологических процедур в эстетической медицине постоянно и неуклонно увеличивается. Разрабатываются новые препараты и методики, что приводит к разнообразным осложнениям и требует изыскания путей их предупреждения или устранения.
Основываясь на полученных в ходе нашего исследования фактических данных, полагаем, что предлагаемый протокол лечения может стать одним из вариантов выбора, когда речь заходит о лечении отсроченных осложнений после применения ИТН на основе полимолочной кислоты, с учетом высокого профиля их безопасности и продемонстрированной эффективности. Тем не менее вопрос предполагаемой оценки годовой частоты рецидивов, регресса и безопасности использования данного подхода остается открытым и требует дальнейшего изучения.
1Aesthetic Fillers Market Size & Share Analysis — Growth Trends & Forecasts (2024–2029). Mordor Intelligence industry reports, 2024. (Electronic resource.) URL: https://www.mordorintelligence.com/industry-reports/aesthetic-filler-market (access date: 20.03.2024).
Информация с rmj.ru







