Введение
В последние годы интенсивно развивается такое направление в медицине, как метабология. Однако в классических медицинских образовательных курсах ей пока уделяется недостаточно внимания. В связи с этим мы открываем цикл обзорных статей, посвященных метабологии, которая тесно связана с эндокринологией. Так как общепринятых определений рассматриваемых областей в настоящее время нет, вначале мы хотели бы дать наши определения терминов, основанные на изучении научных публикаций.
Метаболические заболевания — болезни или синдромы, при которых ведущим проявлением является нарушение обмена веществ, в том числе и преобразование энергетических субстратов в энергию в клетке, а также влияющие на течение внутриклеточных биохимических процессов энергообмена. К числу так называемых «метаболических болезней» можно отнести сахарный диабет (СД), ожирение. Кроме того, это могут быть нарушения обмена веществ, возникающие у терапевтических больных (например, вызванные диареей) или после хирургических вмешательств (например, бариатрических).
Метаболическая медицина — это профилактика, диагностика и лечение заболеваний, основанное на биохимических представлениях, а также генетической и молекулярной биологии, метаболических процессах в норме и при патологии.
Метаболическая терапия — это комплексный подход к лечению и профилактике заболеваний, основанный на коррекции метаболических процессов в организме. Он включает в себя диетические рекомендации, изменение образа жизни, физические упражнения и, при необходимости, медикаментозное вмешательство.
Предмет «Метаболическая медицина»
За последние годы метаболическая медицина превратилась в уникальную дисциплину, для освоения которой требуются как специальная общеклиническая подготовка, так и обширные биохимические знания.
Специалисты по нарушению обмена веществ (метабологи) лечат заболевания от самых распространенных до очень редких. Например, на консультацию к метабологу могут обратиться как пациенты с ожирением или метаболическим синдромом (МС), так и пациенты с митохондриальными заболеваниями или дефицитом массы тела неясной этиологии. Общим у таких пациентов является то, что каждый из них страдает болезнью, при которой нарушения в метаболизме служат основным этиологическим фактором заболевания, а лечение основывается на изменении питания и других терапевтических и хирургических методах воздействия на метаболизм.
Метаболическую медицину можно рассматривать как прикладную биохимию. Поэтому необходимо глубокое понимание биохимических метаболических путей. Это совершенно очевидно, когда речь идет о врожденном нарушении обмена веществ. Но также актуально и для лечения рядового пациента, страдающего СД 2 типа (СД2) или дислипидемией.
Метаболог должен обладать хорошими навыками в области физикального обследования и клинической диагностики пациентов с метаболическими нарушениями, по крайней мере на уровне врача общей практики. Кроме того, так как практически все гормоны, и прежде всего инсулин, обладают системным метаболическим эффектом, то необходима также основательная подготовка и в области эндокринологии.
Метаболог также должен иметь некоторый опыт и знания в области психологии и патопсихологии, поскольку лечение основывается в значительной мере на изменении образа жизни (в плане питания и физической активности, например).
Во всем мире программы обучения метаболической медицине различаются по своей глубине и сложности. Различия обусловлены высоким темпом развития этой области медицинских знаний, а также отличием в системах здравоохранения разных стран.
В России «метаболог» еще не включен в номенклатуру медицинских специальностей. В связи с этим врачи, специализирующиеся в области метаболической медицины, получают специализацию по нескольким медицинским направлениям (эндокринология, диетология, лечебная физкультура и др.). Вместе с тем «никому не объять необъятного». И потому в современной медицине постдипломное образование направлено на специализацию, а не на подготовку специалистов «широкого профиля», обладающих высокопрофессиональными навыками работы в разных медицинских направлениях.
Исходя из вышесказанного, целесообразно рассматривать метаболога в качестве организатора работы команды различных медицинских специалистов, оказывающих лечебную помощь больному в направлениях, которые задает метаболог.
Возникает вопрос: специалист какого направления в медицине в наилучшей степени подойдет для работы в качестве метаболога?
Очевидно, что это эндокринолог, особенно диабетолог, который в силу своей специальности достаточно глубоко изучает биохимию и энергообмен, знания которых, в частности, лежат в основе диетотерапии СД.
В США метаболическая медицина, как правило, включает три основных направления: недостаточное питание, ожирение и МС. В европейских странах больше внимания уделяется длительному наблюдению за пациентами с врожденным нарушением обмена веществ, поскольку большинство этих пациентов нуждаются в наблюдении и лечении пожизненно.
Кроме того, современные высокотехнологичные методы диагностики (например, анализ мочи на органические кислоты) позволяют диагностировать легкие, ранее не диагностировавшиеся формы наследственных метаболических заболеваний.
Содержание статьи
- 1 Этапы развития метаболической медицины
- 2 Развитие методов лечения недостаточного питания
- 3 Группа нутритивной поддержки
- 4 Амбулаторная нутритивная поддержка
- 5 Ожирение и его лечение
- 6 Кто и как должен лечить ожирение?
- 7 Метаболический синдром и профилактика сердечно-сосудистых заболеваний
- 8 Новые направления в области метаболической медицины
- 9 Бариатрическая/метаболическая хирургия
- 10 Метабология и бариатрическая хирургия
- 11 Функционал врача-метаболога при ведении бариатрических пациентов
- 12 Заключение
Этапы развития метаболической медицины
Развитие метаболической медицины целесообразно рассматривать с учетом эволюции науки о питании, так как они тесно связаны.
Возникновение направления «метаболическая медицина» было связано с необходимостью организации стационарного лечения пациентов, страдающих от недостаточного питания (фактически голодания). В связи с этим была начата подготовка специалистов в области интенсивного диетического лечения, которое включало, например, полное парентеральное питание и было основано на биохимии питания.
Возникновение в мире эпидемии ожирения в последние десятилетия и связанного с ним МС как фактора риска СД и сердечно-сосудистых заболеваний расширили востребованность в метаболической медицине от нишевой практики до широкого применения при распространенных заболеваниях.
Что касается диагностики и лечения синдрома недостаточного питания, то вначале оно касалось только тяжелых пациентов стационаров, страдающих по той или иной причине от недостатка поступления питательных веществ. Особый интерес к этой проблеме возник после Второй мировой войны, когда медицинское обслуживание стало переходить на новый, более технологичный уровень, а курс стационарного лечения пациентов становился все более длительным и сложным.
Большинство врачей той эпохи были незнакомы с научными концепциями и подходами в области питания. Они были плохо подготовлены к лечению пациентов, страдающих от тяжелого недоедания. С другой стороны, было мало разработано для клинической практики вариантов лечения или апробировано методик для проведения нутритивной терапии у истощенных пациентов [1, 2].
Развитие методов лечения недостаточного питания
Кардинальные изменения произошли в конце 1960-х годов, когда шведские ученые разработали и применили в клинике методы внутривенной нутритивной поддерживающей терапии, которая была названа «гипералиментацией» [3, 4].
Гипералиментация — это питание, избыточное по калорийности и нутритивному составу по сравнению с нормальным, разработанное специально для истощенных пациентов.
После того как было установлено, что в этой терапии нуждаются практически все больницы, были разработаны схемы парентерального и энтерального питания госпитализированных истощенных больных [3–7]. С тех пор появилось много новых препаратов для парентерального питания. Вместе с тем принцип нутритивного лечения остается очень близким к методике, впервые описанной шведскими учеными более полувека назад.
Группа нутритивной поддержки
Первоначальная функция врача — специалиста по болезням нарушения обмена веществ заключалась в руководстве многопрофильной группой, так называемой группой нутритивной поддержки (ГНП). В состав ГНП входили врач, диетолог, фармацевт и медсестра для проведения инъекций [8].
Создание таких мультидисциплинарных команд поддерживалось администрацией большинства больниц, поскольку для безопасного проведения гипералиментации необходимо было обеспечить многостороннее обоснование рекомендованной терапии. Однако по мере оптимизации лечения больницы стали сокращать расходы, связанные с работой ГНП, или даже их ликвидировать.
В определенный период времени ГНП эволюционировала в комплексную услугу, объединяющую консультативную деятельность по выявлению дефицита питания у пациентов, терапевтическую помощь для тех, кто сталкивается с подобными проблемами, а также помощь в установке центральных венозных катетеров. ГНП осуществляла мониторинг всех пациентов с недостаточным питанием, выполняя такие рутинные задачи, как замена катетеров и контроль лабораторных показателей; давала рекомендации и регулярно вносила коррективы в диету в зависимости от состояния пациента.
В связи с сокращением или ликвидацией должностей специалистов, входивших в ГНП, врач, занимающийся коррекцией нарушенного обмена веществ, оказался перед выбором: либо взять на себя функции специалистов ГНП, либо прекратить предоставление услуг по нутритивной поддержке.
Часть врачей прекратили свое участие в организации нутритивной поддержки стационарных больных из-за прекращения функционирования ГНП. Другие взяли на себя задачу объединения функций врача, диетолога, фармацевта и эксперта по проведению инъекций, чтобы стать консультантами по вопросам коррекции нарушенного обмена веществ у пациента, находящегося в стационаре.
В результате в задачи врача — специалиста по нутритивной поддержке вошли диагностика состояний недостаточности питания, разработка курса терапии, установка центрального венозного катетера, заказ парентерального питания и контроль проводимой терапии.
Примерно в то же время, когда на первый план вышла задача сокращения расходов в больницах на нутритивную поддержку, были разработаны более совершенные, но при этом упрощенные и безопасные методы парентерального питания. Например, были предложены безопасные для здоровья пациента липидные эмульсии для внутривенного введения (ВЛЭ).
Следует заметить, что первые лекарственные формы внутривенной жировой эмульсии были признаны токсичными и изъяты с фармрынка [9]. Однако позднее было установлено, что жировая эмульсия безопасна для внутривенного введения, если она имитирует естественный процесс переноса жира кровью. В частности, были разработаны искусственные хиломикроны [10], размер липидных глобул и биологические свойства которых были идентичны естественным хиломикронам.
Синтезированные ВЛЭ оказались эффективным средством лечения истощенных пациентов, так как позволяли насыщать организм пациента калориями, которыми богаты жиры. Кроме того, использование ВЛЭ позволило в два раза снизить количество калорий, поступающих в виде глюкозы, избыток которой в крови повышает риск развития СД.
Современные препараты для парентерального питания содержат сбалансированный состав энергосубстратов (белков, жиров и углеводов), а также покрывают физиологическую потребность в микроэлементах. Подход к нутритивной поддержке с точки зрения сбалансированного состава входящих в нее элементов противоречит устаревшей концепции «гипералиментации». В связи с этим было предложено для нутритивного питания другое, более адекватное определение: «полное парентеральное питание» [11].
Амбулаторная нутритивная поддержка
В конце 1970-х появилась новая парадигма оказания медицинской помощи: обеспечить бóльшую независимость и самостоятельность пациента в лечении своего заболевания.
Этот подход предполагает, что пациент является активным потребителем услуг здравоохранения, а не пассивным получателем помощи. В 1980-е годы необходимость ограничения затрат на стационарную помощь и потребность в большем участии пациента в процессе лечения привели к применению схем нутритивной поддержки у истощенных пациентов и после выписки из стационара [12]. В результате организация нутритивной поддержки на дому стала еще одной задачей метаболической медицины. Методы ухода на дому становились все более стандартизированными и рутинными, что позволило перейти к амбулаторному лечению пациентов методами парентерального питания.
Благодаря знаниям, полученным в ходе регулярного наблюдения за людьми, страдающими от недостатка питательных веществ, стало очевидно, что кроме недостатка энергосубстратов существуют и другие нутритивные дефициты, например нехватка в организме витаминов и минералов.
Такого рода дефициты часто наблюдаются у пациентов с синдромом короткого кишечника или кишечно-кожными свищами.
Позже данные метаболического мониторинга пациентов после бариатрических вмешательств еще больше расширили практические знания относительно дефицита микроэлементов и витаминов.
Ожирение и его лечение
Медицинское направление, связанное с профилактикой и лечением ожирения, также появилось в 1960-е годы, примерно в то же время, что и нутритивная поддержка пациентов с недостатком питания.
Следует заметить, что лечением ожирения занимаются врачи разных специальностей, преимущественно эндокринологи и диетологи и в меньшей степени терапевты и кардиологи. Для лечения они используют неинвазивные методы и в основном в амбулаторных условиях. Но сегодня в Интернете можно найти специалиста «обеситолога» (от англ. obese — «полный»), то есть специализирующегося на лечении ожирения.
Кто и как должен лечить ожирение?
Проблемы недостатка или избытка массы тела объединяет то, что в обоих случаях необходимо устранить дисбаланс в энергообмене. При этом у пациентов как с ожирением, так и дефицитом питания состав тела нарушен, а лечение направлено на его восстановление.
По мере того как проблема ожирения стала достигать масштабов эпидемии, в медицинском сообществе возникло понимание необходимости его профилактики и активного лечения.
Представляется очевидным, что врачи, специализирующиеся в лечении истощенных больных в стационаре (диетологи, например), могли бы применить полученные знания о метаболизме и для профилактики и лечения ожирения.
Для синтеза знаний и практических навыков врачей, занимающихся вопросами недостаточного питания, и теми, кто лечит ожирение, в 1970-х годах доктором G.L. Blackburn [13] была создана специальная образовательная платформа. Его концепция лечения ожирения называлась «модифицированное протеин-сберегающее голодание» (МПСГ) [13, 14], она была основана на его опыте стационарного лечения пациентов с ожирением специальной диетой с резким ограничением ее калорийности (лечебное голодание).
Его работы по изучению энергетического и азотного баланса при недостаточном питании получили высокую оценку медицинского научного сообщества, и он стал широко известен как лидер в области нутритивной поддержки. Внедрение программы МПСГ в клиническую практику стало одним из важных направлений метаболической медицины.
Научная концепция МПСГ была взята метабологами для лечения ожирения у некоторых пациентов. Оно проводилось в два этапа: вначале в стационаре, а затем продолжалось в амбулаторных условиях. МПСГ развилось и усложнилось настолько, что некоторые врачи сменили свою прежнюю специальность на нутрициологию как основной вид клинической деятельности.
С этого момента метаболическая медицина стала развиваться как самостоятельная специальность [15].
Метаболический синдром и профилактика сердечно-сосудистых заболеваний
Еще одно важное историческое событие в развитии метаболической медицины произошло через 10 лет после внедрения в практику МПСГ.
В 1988 г. доктор G.M. Reaven прочел ежегодную лекцию по лечебному голоданию в Стэнфордском университете. В этой лекции он высказал мнение, что ожирение, снижение толерантности к глюкозе, гиперлипидемия и гипертония связаны общей нитью — инсулинорезистентностью (ИР) [16]. И это сочетание патологических состояний он назвал «синдромом Х», в дальнейшем оно получило и другие названия: «метаболический синдром», «кардиометаболический синдром», «синдром Ривена». На сегодня общепринятым считается название «метаболический синдром».
С клинической точки зрения, МС — это сочетание центрипетального ожирения (увеличение окружности талии), артериальной гипертензии, дислипидемии (повышение в крови уровня триглицеридов и снижение уровня липопротеинов высокой плотности), а также нарушения толерантности к глюкозе (в том числе СД) [17], так называемый «смертельный квартет», поскольку на его фоне существенно возрастает риск смерти от сердечно-сосудистых заболеваний.
В последнее время к характерным признакам МС относят ряд биомаркеров воспаления, таких как высокочувствительный С-реактивный белок [18]. Кроме того, установлено, что неалкогольная жировая болезнь печени часто развивается у людей с ИР и МС [19].
Распространенность МС в развитых странах составляет более 25% [20] и, кроме того, он наблюдается у 75% пациентов с СД2 и у 50% пациентов с ишемической болезнью сердца (ИБС) [21]. Было также показано, что МС предшествует как СД, так и сердечно-сосудистым заболеваниям. Поэтому его раннее выявление и лечение являются важным инструментом профилактики сердечно-сосудистых заболеваний и смертности от них.
В практической деятельности метаболога треть его пациентов составляют пациенты с МС. Вместе с тем лечением СД2 на фоне МС занимаются эндокринологи. С учетом вышесказанного совместная работа эндокринолога и метаболога могла бы заключаться в том, что при МС метаболог назначает лечение, предотвращающее развитие СД2, а в тех случаях, когда СД2 развился, он передает лечение эндокринологу. Аналогично кардиологи лечат ИБС, атеросклероз и гипертонию на фоне МС, а врачи-метабологи в этом случае сосредоточены на их профилактике у лиц с МС.
Новые направления в области метаболической медицины
Знания в области метаболической медицины настолько расширились, что появилась возможность подбирать специальное диетическое лечение в зависимости от заболевания или комплекса болезней у пациента. В частности, роль метаболога может оказаться одной из ведущих в лечении не только признанных болезней нарушенного обмена, но, например, в неврологии, нефрологии, урологии, ревматологии, офтальмологии, иммунологии, пульмонологии, гастроэнтерологии, гепатологии, дерматологии и др. В этой связи метаболическая медицина может оказаться частью так называемой интегративной (прецизионной) медицины.
Бариатрическая/метаболическая хирургия
Новое развитие метаболическая медицина получила с внедрением и развитием бариатрической хирургии. С начала 1950-х годов были предложены различные виды бариатрических операций. Сегодня они условно подразделяются на 2 категории:
Рестриктивные (направлены на уменьшение размеров желудка, следствием чего являются уменьшение объема потребляемой пищи и снижение аппетита). Наиболее частой из них является продольная резекция желудка (см. рисунок, А).
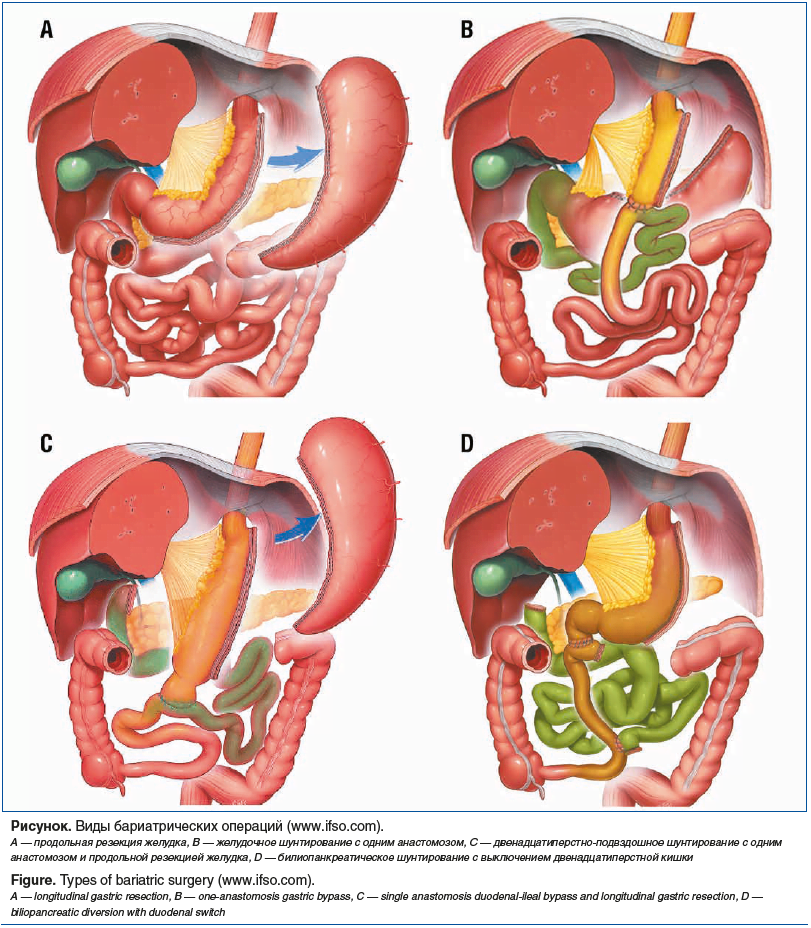
Комбинированные (шунтирующие) (сочетают в себе два компонента: рестриктивный — уменьшение объема желудка, создаваемое различными способами, и мальабсорбтивный — снижение всасывания питательных веществ за счет уменьшения длины тонкой кишки, по которой продвигается пищевой комок).
Мальабсорбтивные операции в традиционном их понимании (еюноилеошунтирование, еюноколоношунтирование) были оставлены по причине возможного развития неконтролируемой избыточной мальабсорбции.
Важно отметить, что в отношении снижения массы тела и одновременной коррекции сопутствующей патологии наибольшей эффективностью обладают шунтирующие операции.
Принцип операции шунтирования желудка был разработан E.E. Mason в 1966 г. [22]. Он заметил, что у пациентов, перенесших резекцию желудка с гастроэнтеростомией, происходило заметное снижение массы тела. Автор предложил выполнять горизонтальную резекцию проксимальной части желудка, при которой приблизительно 1/5 (проксимальная) часть в области дна желудка анастомозируется с петлей тощей кишки примерно в 60 см от связки Трейца. Затем в 1977 г. J.F. Alden [23] модифицировал эту операцию, предложив выключение большей части желудка из пассажа пищи без резекции желудка, но эта операция не нашла широкого клинического применения.
Модификацию желудочного шунтирования по Ру (Roux-en-Y) впервые предложил W.O. Griffen [24] в 1977 г. Долгое время эта операция считалась «золотым стандартом» в бариатрической хирургии. У большинства пациентов она обеспечивала потерю до 75% избыточной массы тела (ИзМТ) через 2 года после выполнения и до 60% к 5 годам наблюдения. Также была отмечена ремиссия СД2 у 50% пациентов в течение 5 лет послеоперационного наблюдения.
В настоящее время существует несколько модификаций желудочного шунтирования, которые были предложены в связи с недостаточным эффектом стандартного варианта операции. В 1991 г. J.K. Torres разработал методику дистального гастрошунтирования с формированием алиментарной петли длиной 200–250 см [25]. Эта операция приводила к хорошей, более стойкой потере ИзМТ, но давала большее число побочных эффектов, связанных с избыточной мальабсорбцией и диарейным синдромом. В 1991 г. М. Fobi модифицировал желудочное шунтирование по Ру, дополнив его нерегулируемым бандажированием малого желудка (операция Fobi-Pouch), для усиления рестриктивного компонента и уменьшения проявлений демпинг-синдрома [26]. Данная модификация приводила к уменьшению растяжения малого желудка, но провоцировала развитие кислотного рефлюкса, что в принципе не является характерным побочным эффектом гастрошунтирования.
В 1997 г. R. Rutledge предложил новую модификацию операции, суть которой состояла в создании обходного желудочного шунта с использованием только одного анастомоза (минигастрошунтирование по Rutledg) (см. рисунок, B) [27]. Эта операция включает в себя разделение желудка на две части — большой (отключенный) желудок и малый узкий желудочек, сформированный вдоль малой кривизны, длиной 25 см, с внутренним диаметром 1,0 см — и формирование анастомоза между дистальным концом малого желудка и петлей тощей кишки на расстоянии 150–250 см от связки Трейца. Сравнительно недавно эффективность этой операции была оценена в крупномасштабном многоцентровом рандомизированном исследовании (исследование YOMEGA, 2019) [28]. Было показано, что при большей технической простоте выполнения и значительно более коротком времени выполнения минигастрошунтирования по Rutledg в сравнении с желудочным шунтированием по Ру обе операции одинаково эффективны в плане снижения ИзМТ, нормализации уровня глюкозы и гликированного гемоглобина. Однако у пациентов, перенесших минигастрошунтирование Rutledg, была выявлена более высокая частота дефицитов питательных веществ. По этой причине многие хирурги в настоящее время выступают за использование более короткой билиопанкреатической петли (150 см) при выполнении обеих модификаций желудочного шунтирования [29].
Несмотря на широкое использование и растущую популярность гастрошунтирования, следует отметить возможность специфических осложнений и побочных эффектов, таких как демпинг-синдром, язвы или стеноз гастроэнтероанастомоза, несостоятельность шва большого и малого желудков, развитие внутренних грыж, желчный рефлюкс. Также многие хирурги высказывают опасения относительно возможности развития злокачественных новообразований в большом желудке и невозможности его рутинного обследования при любом варианте гастрошунтирования.
Недостаточная эффективность желудочного шунтирования с точки зрения долгосрочного удержания сниженной массы тела и достижения длительной ремиссии СД2 все чаще заставляет хирургов прибегать к более эффективным, комбинированным бариатрическим операциям, таким как билиопанкреатическое шунтирование (см. рисунок, С, D).
Показатели потери ИзМТ (60%) и ремиссии СД2 (50%) к 5 годам наблюдения после желудочного шунтирования аналогичны во многих рандомизированных контролируемых исследованиях. Модификации билиопанкреатического шунтирования обеспечивают более существенную потерю ИзМТ (95–75%), значительно более высокую частоту длительной ремиссии СД2 и меньший риск его рецидива. При этом гастрошунтирование обеспечивает оптимальный гликемический и метаболический контроль у 50–60% пациентов с меньшим количеством побочных эффектов нарушения всасывания питательных веществ и микроэлементов, меньшую частоту развития диарейного синдрома, что в свою очередь позволяет многим пациентам оценивать качество жизни выше, чем после билиопанкреатического шунтирования. Этот факт позволяет предположить, что на сегодняшний день желудочное шунтирование имеет более благоприятное соотношение риска и пользы, чем билиопанкреатическое шунтирование, тогда как последнее может быть более эффективным у пациентов со сверхожирением и длительным анамнезом СД2.
Метаболическая хирургия определяется как «оперативное вмешательство на нормальном органе или системе органов для достижения биологического результата с целью потенциального улучшения здоровья» [30]. В отличие от бариатрической хирургии, которая направлена на снижение массы тела, основным принципом метаболической хирургии является лечение заболеваний с многочисленными клиническими проявлениями, сопутствующими морбидному ожирению, в первую очередь СД2.
В настоящее время не существует однозначного мнения относительно того, какая операция предпочтительнее, как и не существует конкретного алгоритма выбора операции с учетом клинических особенностей каждого пациента. Некоторые авторы полагают, что билиопанкреатическое шунтирование должно стать «золотым стандартом» бариатрической хирургии, так как обеспечивает более выраженное и наиболее стабильное снижение массы тела, а также уменьшение коморбидности по сравнению с желудочным шунтированием, при этом метаболический эффект билиопанкреатического шунтирования является максимальным по сравнению со всеми другими бариатрическими операциями. В то же время на сегодняшний день билиопанкреатические вмешательства продолжают оставаться сравнительно редкими из-за технических сложностей выполнения и в связи с более высокой опасностью развития послеоперационных осложнений, в частности избыточной мальабсорбции и диарейного синдрома.
Метабология и бариатрическая хирургия
Появление бариатрической хирургии и признание ее роли в значительном изменении метаболизма при ожирении (как в положительном, так и в отрицательном направлении) способствовало повышению востребованности во врачах-метабологах. Прежде всего потому, что оперированные пациенты сталкиваются с целым рядом нарушений в обмене микроэлементов, которые с увеличением длительности послеоперационного периода могут становиться все более выраженными.
Диагностика, профилактика и лечение недостаточности витаминов и микроэлементов, как правило, не входят в компетенцию бариатрического хирурга. Большинство терапевтов были также плохо подготовлены к точной диагностике и лечению этих состояний. Но врач-метаболог, обладающий опытом в лечении хронического недоедания, идеально подходит для решения этой клинической задачи.
Функционал врача-метаболога при ведении бариатрических пациентов
В дополнение к мониторингу, профилактике и управлению дефицитом микроэлементов, врач-метаболог призван помочь бариатрическим больным, при необходимости, корректировать сахароснижающую терапию СД2, а также схемы лечения гипотензивными и гиполипидемическими препаратами.
Врач-метаболог обычно берет на себя и лечение пациентов с синдромом ночного апноэ, в частности контроль за эффективностью CPAP-терапии (CPAP — Constant Positive Airway Pressure — режим искусственной вентиляции легких постоянным положительным давлением) по мере снижения массы тела.
При возникновении осложнений после бариатрической хирургии врач-метаболог должен использовать свои навыки в области нутритивной терапии, чтобы помочь бариатрическим пациентам, которые не могут самостоятельно соблюдать необходимый рацион питания. Особую тревогу вызывает подгруппа пациенток, которые беременеют в течение года после бариатрической операции и все еще быстро теряют в весе, несмотря на беременность.
Навыки врача-метаболога при медицинском снижении массы тела также полезны тем бариатрическим пациентам, которые испытывают трудности с достижением целевой массы тела. Около 20–40% пациентов после бариатрической хирургии отмечают рецидив набора массы тела, особенно после рестриктивных операций.
Заключение
Таким образом, в последние годы метабология приобретает все большее значение в медицине, особенно в контексте лечения метаболических заболеваний, таких как СД и ожирение. Однако значимость метабологии не всегда отражается в медицинских образовательных программах. В то же время глубокое понимание биохимических процессов и метаболических патологий является одним из определяющих факторов в достижении успеха в лечении. Развитие метаболической медицины и подходов к нутритивной поддержке представляет собой важный этап в современной медицине, обеспечивая эффективное лечение и повышение качества жизни пациентов с нарушениями обмена веществ.
Сведения об авторах:
Древаль Александр Васильевич — д.м.н., профессор, заведующий кафедрой эндокринологии и цифровой медицины ФУВ ФГБНУ «Национальный НИИ общественного здоровья имени Н.А. Семашко»; 105064, Россия, г. Москва, ул. Воронцово Поле, д. 12, стр. 1; ORCID iD 0000-0002-3135-9003
Нечаева Ольга Анатольевна — к.м.н., доцент кафедры эндокринологии и цифровой медицины ФУВ ФГБНУ «Национальный НИИ общественного здоровья имени Н.А. Семашко»; 105064, Россия, г. Москва, ул. Воронцово Поле, д. 12, стр. 1.
Древаль Олег Александрович — к.м.н., научный сотрудник отделения терапевтической эндокринологии отдела общей эндокринологии ГБУЗ МО МОНИКИ им. М.Ф. Владимирского; 129110, Россия, г. Москва, ул. Щепкина, д. 61/2; ORCID iD 0000-0002-8944-9837
Бритвин Тимур Альбертович — д.м.н., ведущий научный сотрудник отдела хирургии ГБУЗ МО МОНИКИ им. М.Ф. Владимирского; 129110, Россия, г. Москва, ул. Щепкина, д. 61/2; ORCID iD 0000-0001-6160-1342
Габриелян Артур Рудольфович — профессор кафедры общественного здоровья и здравоохранения ФУВ ФГБНУ «Национальный НИИ общественного здоровья имени Н.А. Семашко»; 105064, Россия, г. Москва, ул. Воронцово Поле, д. 12, стр. 1.
Контактная информация: Древаль Александр Васильевич, e-mail: endocrinolog-cab@yandex.ru
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 11.07.2024.
Поступила после рецензирования 05.08.2024.
Принята в печать 28.08.2024.
About the authors:
Alexander V. Dreval — Dr. Sc. (Med.), Professor, Head of the Department of Endocrinology and Digital Medicine, N.A. Semashko National Research Institute of Public Health; 12, build. 1, Vorontsovo Pole, Moscow, 105064, Russian Federation; ORCID iD 0000-0002-3135-9003
Olga A. Nechaeva — C. Sc. (Med.), Associate Professor of the Department of Endocrinology and Digital Medicine, N.A. Semashko National Research Institute of Public Health; 12, build. 1, Vorontsovo Pole, Moscow, 105064, Russian Federation.
Oleg A. Dreval — C. Sc. (Med.), Researcher at the Department of Therapeutic Endocrinology of the Department of General Endocrinology. M.F. Vladimirskiy Moscow Regional Research and Clinical Institute; 61/2, Shchepkin str., Moscow, 129110, Russian Federation; ORCID iD 0000-0002-8944-9837
Timur A. Britvin — Dr. Sc. (Med.), Leading Researcher at the Department of Surgery, M.F. Vladimirskiy Moscow Regional Research and Clinical Institute; 61/2, Shchepkin str., Moscow, 129110, Russian Federation; ORCID iD 0000-0001-6160-1342
Artur R. Gabrielyan — Professor of the Department of Public Health and Healthcare, N.A. Semashko National Research Institute of Public Health; 12, build. 1, Vorontsovo Pole, Moscow, 105064, Russian Federation.
Contact information: Alexander V. Dreval, e-mail: endocrinolog-cab@yandex.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 11.07.2024.
Revised 05.08.2024.
Accepted 28.08.2024.
Информация с rmj.ru






