Введение
Носовые кровотечения (НК) — кровотечения, возникающие при нарушении целостности сосудов, расположенных в полости носа, околоносовых пазухах, носоглотке, а также кровотечение из сосудов полости черепа при нарушении целостности верхней стенки полости носа. НК представляют собой широко распространенную проблему и отмечаются у 60% населения отдельных стран [1]. Несмотря на то, что у большинства пациентов НК кратковременны и незначительны, порядка 6% пациентов с НК нуждаются в специализированной медицинской помощи [1].
Рецидивирующие НК у детей чаще имеют спонтанный характер, не связанный непосредственно с механической травмой. НК отмечаются более чем у половины детей в возрасте до 10 лет, причем у 9% из них имеют место рецидивирующие НК [2]. В 86–90% случаев у детей источник НК располагается в передненижнем отделе носовой перегородки — в зоне Литтла — Киссельбаха [2]. Доказано, что в развитии спонтанных рецидивирующих НК важную роль играют нарушения местного сосудистого гемостаза слизистой оболочки полости носа, которые являются следствием дефекта сосудистой стенки и нарушения вегетативной регуляции сосудистого тонуса [3, 4]. Также предполагается, что колонизация полости носа Staphyloccocus aureus с последующим развитием хронического воспаления может вносить значительный вклад в патогенез НК у детей [3].
При лечении рецидивирующих НК рекомендуется «ступенчатый подход»: на первом этапе воздействуют на кровоточащий участок с целью купирования кровотечения, а на втором — предупреждают рецидив заболевания, воздействуя на его патогенез [5]. Рекомендации по неотложной помощи достаточно хорошо отработаны. Назальная компрессия, коагуляция области кровотечения и/или тампонада полости носа, хотя зачастую и являются достаточно агрессивными способами [6], широко применяются в оказании экстренной помощи как у взрослых, так и у детей1. Основными подходами к медикаментозному лечению НК являются использование смягчающих средств, таких как вазелин или антибиотические мази, применение сосудосуживающих препаратов, увлажнение слизистой оболочки [1].
В то же время, учитывая имеющиеся ограничения для применяемых на настоящий момент методов лечения НК, а также более сложный патогенез, не ограничивающийся механическим повреждением слизистой оболочки носа, отмечается необходимость разработки новых подходов к патогенетически обоснованному лечению рецидивирующих НК у детей [6]. В связи с этим особый интерес представляют препараты на основе гиалуроновой кислоты, обладающие противовоспалительным, антибактериальным [7] и заживляющим [8] действием. Ранее нами была продемонстрирована высокая эффективность использования Олифрина после эндоскопической эндоназальной хирургии у детей и взрослых [9]. Также отмечены положительные результаты применения препаратов на основе гиалуроновой кислоты в лечении атрофического ринита, сопровождающегося НК [10, 11]. Имеются отдельные указания на использование гиалуроновой кислоты в комбинации с другими действующими веществами для лечения НК, однако подтверждающие данные крайне ограничены [12, 13].
Цель исследования: оценка клинической эффективности комбинированного спрея для интраназального применения спрея Олифрин, содержащего, наряду с гиалуроновой кислотой, витамин Е и эфирное масло лимона, в комплексном лечении рецидивирующих НК у детей.
Материал и методы
Исследование выполнено в соответствии с этическими стандартами, установленными в Хельсинкской декларации (1964) и ее последующих поправках. Протокол исследования одобрен локальным этическим комитетом ФГБУ «СПб НИИ ЛОР» Минздрава России. Перед проведением обследования было получено письменное информированное согласие на участие в исследовании от законных представителей пациентов.
В ходе настоящего сравнительного проспективного рандомизированного исследования обследованы 60 пациентов детского возраста обоих полов в возрасте от 3 до 17 лет с диагнозом «рецидивирующие носовые кровотечения» (код по МКБ-10 R04.0). В соответствии с применяемыми схемами лечения обследуемые распределены на две группы по 30 человек: опытную, где при лечении пациентов применяли стандартную терапию, в составе которой дополнительно интраназально использован комбинированный спрей Олифрин (ООО «Гротекс», Россия), содержащий гиалуроновую кислоту, α-токоферол, эфирное масло лимона, для местного применения дозированный, согласно инструкции по применению препарата; контрольную, в лечении пациентов которой использовали только стандартную терапию. Статистически значимых различий в половом (р=0,628) и возрастном (р=0,804) составе групп выявлено не было.
С целью предотвращения влияния сторонних факторов на результаты исследования использованы следующие критерии исключения: наличие гиперчувствительности к компонентам применяемых препаратов; наличие НК, связанных с механической и операционной травмой, сосудистыми опухолями, гранулемами, язвами; злокачественными новообразованиями, нарушением коагуляционных свойств крови; наличие соматических, психических и инфекционных заболеваний; существенные отклонения от нормы в лабораторных показателях; участие в каком-либо другом клиническом исследовании в настоящий момент или месяцем ранее; невозможность/неспособность пациента (родителей ребенка) выполнять процедуры исследования.
В стадии кровотечения пациенты получали стандартную терапию согласно приказу Минздрава России от 20.12.2012 № 1209н «Об утверждении стандарта первичной медико-санитарной помощи при носовом кровотечении»1. В период отсутствия кровотечения стандартная терапия включала интраназальную ирригационную терапию стерильным изотоническим 0,9% раствором NaCl, по показаниям: деконгестанты согласно возрасту короткими курсами, препараты кальция, комплекс аскорбиновой кислоты и рутозида курсами согласно возрасту, а также препараты, нормализующие церебральную гемодинамику и функцию вегетативной нервной системы (фитопрепарат для улучшения мозгового и периферического кровообращения, винпоцетин).
Состояние пациентов оценивали в двух контрольных точках с целью последующей оценки динамики.
1-й визит (до начала лечения): консультация ЛОР-специалиста, ЛОР-обследование, включение в исследование, подписание информированного согласия, заполнение регистрационной карты на пациента, рандомизация, назначение препаратов; получение материала со слизистой оболочки верхних дыхательных путей для цитологического исследования (риноцитограммы), выполнение видеориноскопии, получение материала со слизистой оболочки носа для выполнения микробиологического посева, микробиологическое (культуральное) исследование мазков из носа на аэробные и факультативные анаэробные микроорганизмы.
2-й визит (30-й день от начала лечения): проведение повторного физикального, инструментального и лабораторного обследования пациентов в полном объеме.
Для оценки эффективности применения различных схем лечения пациентов с рецидивирующими НК регистрировали максимальное количество эпизодов НК в месяц, а также максимальную длительность эпизодов НК (мин) самим пациентом. На основании полученных данных проводили расчет безразмерного коэффициента K по следующей формуле:
![]()
где maxдо — максимальное количество эпизодов НК в месяц или максимальная длительность НК до лечения; maxпосле — максимальное количество эпизодов НК в месяц или максимальная длительность НК в месяц после курса лечения.
Результаты трактовали следующим образом: хороший, если сумма коэффициентов была более 1,1 (максимальная длительность и максимальное количество НК уменьшались более чем в 2 раза); удовлетворительный, если 0,6
Выраженность жалоб на слабость, недомогание, головную боль, нарушение носового дыхания, выделения из носа, постназальные выделения, нарушение обоняния, сухость в горле, кашель, снижение качества жизни, сухость в носу, образование корок в носу самим пациентом (или законными представителями ребенка) оценивали по модифицированной 10-балльной визуально-аналоговой шкале (ВАШ) от 0 (очень хорошо, отсутствие жалоб) до 10 (очень плохо).
Оценку клинического состояния пациентов, включающего степень затруднения носового дыхания, выраженность ринореи, гнойный характер носового секрета, гиперемию слизистой оболочки носа, выраженность отека слизистой оболочки носа, сужение носовых ходов, наличие корок в полости носа, а также выраженность атрофических изменений слизистой оболочки проводил ЛОР-специалист по балльной системе от 0 (отсутствие нарушения) до 3 баллов (максимальная выраженность).
Оценку эндоскопической картины полости носа и носоглотки пациентов до и после лечения выполняли видеоэндоскопом 2,4 мм с дополнительным режимом NBI (narrow band imaging — узкоспектральная эндоскопия) (Olympus, Германия) по балльной системе — от 0 (отсутствие) до 2 баллов (выраженное наличие) — по шкале Lund — Kennedy [15]. В ходе исследования оценивали наличие полипов, отека слизистой оболочки, отделяемого в носовых ходах и рубцов, а также образование корок. Отдельно фиксировали данные с каждой стороны, в последующем данные суммировались.
Цитологическое исследование мазков с поверхности слизистой оболочки верхних дыхательных путей (риноцитограмма) выполняли методом окрашивания нативных препаратов мазков слизистой оболочки полости носа по Романовскому — Гимзе. Стерильной ватной палочкой осуществляли забор отделяемого со слизистой оболочки полости носа (с двух сторон), наносили на предметное стекло и высушивали при комнатной температуре. Затем мазок фиксировали и окрашивали по Романовскому — Гимзе. Под микроскопом оценивали общее количество лейкоцитов по 4-балльной шкале, где 1 — 1–5 в поле зрения (п/з); 2 — 6–20 в п/з; 3 — 21–40 в п/з; 4 — более 41 в п/з. Анализ относительного количества отдельных видов лейкоцитов проводили посредством подсчета процентного соотношения лимфоцитов (референтное значение — 1–5), нейтрофилов (референтное значение — 65–70), эозинофилов (референтное значение — 0–5), макрофагов/моноцитов (референтное значение — 0–10). Присутствие в мазках эпителия и слизи оценивали по шкале от 0 (нет) до 2 (выраженное).
Микробиологическое исследование мазков из носа заключалось в посеве исследуемого материала на питательные среды с целью выявления и идентификации чистой культуры возбудителя и его чувствительности к расширенному спектру антибиотиков. Материал из носа забирали стерильным ватным тампоном в пластиковые одноразовые стерильные пробирки и сразу доставляли в лабораторию. Проводили качественную (да/нет) и полуколичественную (0 — нет, 1 — скудно; 2 — умеренно, от 103–105; 3 — более 106) оценку присутствия в мазках S. aureus, Streptococcus pneumoniae и Streptococcus viridans.
Статистический анализ полученных данных проводили с использованием программного пакета Statistica 10.0 (Statsoft, США). Характер распределения данных оценивали с применением критерия Шапиро — Уилка. В связи с отсутствием гауссова распределения данные представлены в виде медианы и соответствующих границ межквартильного интервала (IQR). Достоверность изменения анализируемых показателей в ходе лечения (до и после) оценивали с использованием непараметрического критерия знаков. Сравнительный анализ между группами на каждом из этапов (до и после лечения) проведен с использованием непараметрического U-критерия Манна — Уитни. Различия считали статистически значимыми при p<0,05.
Результаты исследования
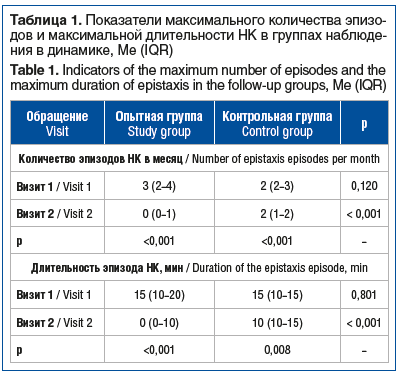
Полученные данные свидетельствуют о том, что оба подхода к лечению приводят к достоверному снижению количества эпизодов и максимальной длительности НК по сравнению с исходными показателями. В то же время применение комбинированного интраназального спрея сопровождалось выраженным снижением количества эпизодов вплоть до полного их отсутствия у большинства пациентов, тогда как на фоне стандартной терапии отмечалось лишь относительное снижение. Как следствие, максимальное количество эпизодов НК после окончания лечения у пациентов, применявших комбинированный спрей, было достоверно ниже такового в группе стандартного лечения. Аналогичный характер изменений отмечался для показателя максимальной длительности НК. Установлено, что в опытной группе имели место случаи практически полного прекращения НК (с 15 до 0 мин), тогда как при использовании стандартного подхода к лечению длительность кровотечения только снижалась на 33% (с 15 до 10 мин). Как следствие, максимальная длительность НК в опытной группе была статистически значимо ниже таковой в контрольной (табл. 1).
На основе характера изменений максимального количества эпизодов НК и длительности кровотечений рассчитаны условные коэффициенты эффективности. Установлено, что Kкол-во в опытной группе превышал таковой в контрольной группе более чем в 3 раза (1 (0,7–1,0) против 0,3 (0,0–0,5); p<0,001). Еще более выраженные различия отмечались у Kдлит, величина которого в опытной группе выраженно превышала таковую в контрольной группе (1 (0,3–1,0) против 0 (0,0–0,3); p<0,001). Наконец, суммарный коэффициент в группе пациентов, применявших Олифрин, превышал величину 1,1, что указывает на хороший результат лечения со снижением максимального количества эпизодов НК и их длительности более чем в 2 раза. При этом значения данного показателя в опытной группе более чем в 6 раз превышали таковые в контрольной группе (2 (0,9–2,0) против 0,3 (0,0–0,5); p<0,001).
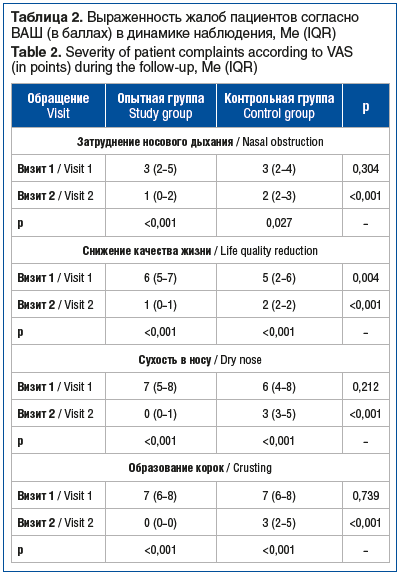
Наряду со снижением длительности и количества эпизодов НК лечение в обеих группах приводило к значительному снижению выраженности жалоб пациентов (табл. 2). В частности, в обеих группах отмечалось статистически значимое снижение выраженности жалоб на затруднение носового дыхания, выделения из носа, постназальные выделения, снижение качества жизни, сухость в носу и образование корок. При этом стоит отметить отсутствие исходно значимых различий в выраженности подавляющего большинства жалоб между группами наблюдения, что указывает на идентичное состояние пациентов в группах и позволяет провести сравнительный анализ.
В то же время в опытной группе отмечалось более выраженное уменьшение жалоб. В частности, пациенты характеризовались 3-кратным снижением выраженности жалоб на затруднение носового дыхания по сравнению с обследуемыми в контрольной группе, у которых отмечалось снижение на 33%. Как следствие, к моменту окончания наблюдения выраженность жалоб на затруднение носового дыхания у пациентов в опытной группе была вдвое ниже таковой в контрольной группе. Несмотря на то, что жалобы на снижение качества жизни у пациентов в группе применения комбинированного спрея до начала лечения достоверно превышали соответствующий показатель в группе стандартного лечения, после проведенного лечения отмечалось 6-кратное снижение выраженности жалоб. В то же время в группе пациентов, получавших стандартную терапию, снижение выраженности жалоб на снижение качества жизни являлось 2,5-кратным. В связи с этим выраженность данной группы жалоб у пациентов, применявших Олифрин, была в 2 раза меньше по сравнению с группой стандартного лечения. Максимальные различия между группами отмечались в случае жалоб на сухость в носу и образование корок. На фоне стандартного лечения отмечалось более чем 2-кратное снижение выраженности данных групп жалоб. При этом в группе пациентов, применявших спрей, выраженность жалоб на сухость в носу и образование корок снижалась вплоть до их полного отсутствия.
Стоит отметить, что у обследованных обеих групп практически отсутствовали (0–1 баллов) жалобы на слабость и недомогание, головную боль, ухудшение обоняния, сухость в горле, кашель и постназальные выделения, в связи с чем не было выявлено достоверного влияния различных схем лечения на данные группы жалоб, равно как и различий между применяемыми терапевтическими подходами (данные не представлены).
Оценка суммарной выраженности жалоб продемонстрировала, что в обеих группах отмечалось достоверное снижение данного показателя. В то же время в опытной группе снижение суммарной выраженности жалоб являлось более чем 7-кратным (28 (26–31) баллов против 4 (3–6) баллов; p<0,001), тогда как на фоне стандартного лечения данное снижение являлось 2-кратным (26 (23–29) баллов против 13 (11–16) баллов; p<0,001). Как следствие, после проведенного лечения суммарная выраженность жалоб у пациентов опытной группы была более чем в 3 раза ниже по сравнению с соответствующими показателями в контрольной группе (p<0,001).
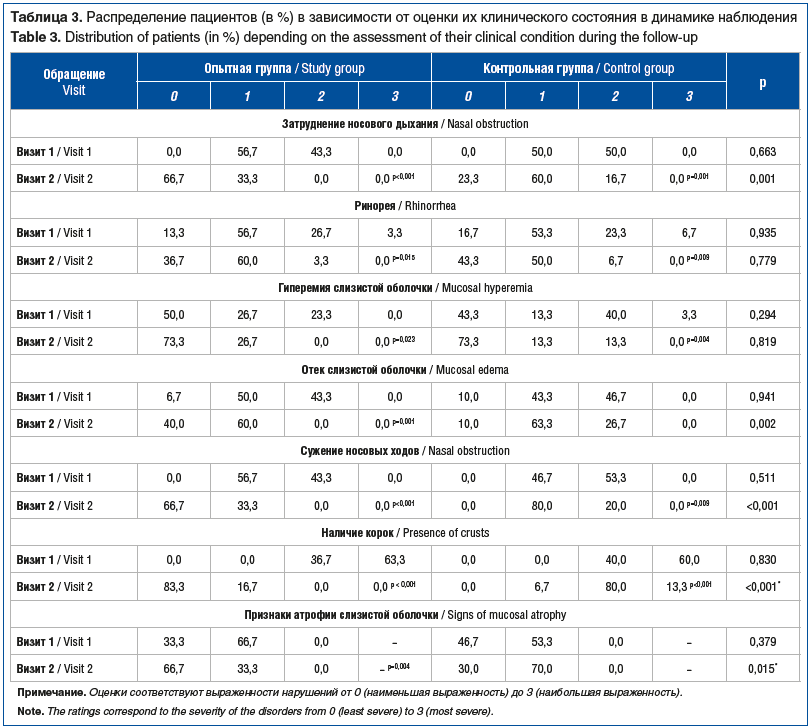
Оценка клинического состояния пациентов также продемонстрировала эффективность обеих схем лечения: в обеих группах отмечалось достоверное снижение затруднений носового дыхания, ринореи, гиперемии слизистой оболочки, сужения носовых ходов, а также образования корок (табл. 3).
В то же время отмечались существенные различия в изменении отдельных показателей клинического состояния пациентов на фоне различных подходов к лечению. В частности, после проведения лечения с использованием интраназального спрея у большинства (66,7%) пациентов отмечалось свободное носовое дыхание, тогда как в группе стандартного лечения у большей части (60%) обследуемых регистрировалось умеренное затруднение носового дыхания. Как следствие, затруднение носового дыхания в группе пациентов, применявших Олифрин, было достоверно менее выражено по сравнению с группой стандартного лечения. Аналогично по окончании лечения у большинства пациентов в опытной группе отмечались свободные носовые ходы, тогда как среди пациентов, проходивших лечение в соответствии со стандартной схемой, у подавляющего большинства (80%) регистрировалось умеренное сужение носовых ходов. Еще более выраженные различия имели место при наличии корок. Так, на фоне применения исследуемого спрея у подавляющего большинства (83,3%) пациентов корки отсутствовали, тогда как после стандартного лечения у пациентов регистрировались умеренные (80%) и даже выраженные (13,3%) корки. Как следствие, сужение носовых ходов и наличие корок по окончании лечения было достоверно менее выраженным у пациентов, применявших Олифрин. Стоит отметить, что в обеих группах до начала лечения в большинстве случаев изменения слизистой оболочки полости носа носили субатрофический характер (66,7 и 53,3% соответственно). Выраженность признаков субатрофии слизистой оболочки после 30 дней применения спрея Олифрин снизилась на 50%, в то время как в контрольной группе данные признаки усилились на 31% (табл. 3). Кроме того, в опытной группе отмечалось достоверное снижение выраженности отека слизистой оболочки носа, тогда как в группе стандартного лечения значимых изменений данных показателей выявлено не было. Не установлено значимой динамики характера носового секрета на фоне различных схем применения, равно как и различий между ними (данные не представлены).
При анализе суммарной выраженности признаков синоназальной патологии установлено, что применение обеих схем лечения приводило к ее достоверному снижению. В то же время в опытной группе снижение суммарной выраженности признаков являлось более чем 3-кратным (11 (9–12) против 3 (2–4); p<0,001), тогда как в группе лечения с применением стандартной терапии снижение составило лишь 27% (11 (9–11) против 8 (7–9); p<0,001). Более того, сравнительный анализ продемонстрировал, что суммарная выраженность признаков синоназальной патологии на фоне применения комбинированного спрея была статистически значимо ниже таковой в группе стандартного лечения более чем в 2 раза (p<0,001), что указывает на бóльшую эффективность спрея Олифрин в отношении улучшения клинического состояния пациентов по сравнению со стандартным подходом к терапии.
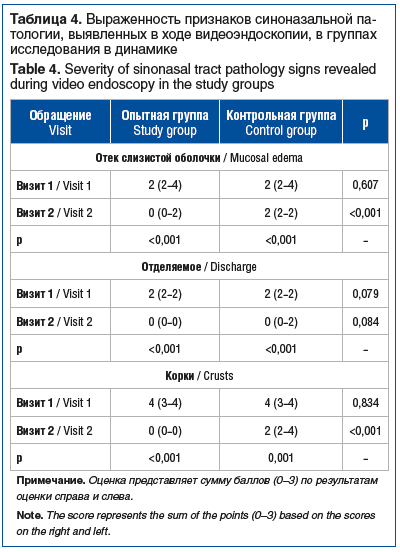
Результаты видеоэндоскопического исследования также подтвердили эффективность обеих схем лечения (табл. 4). В обеих группах наблюдалось статистически значимое снижение выраженности отека слизистой оболочки носа, образования отделяемого и корок по окончании лечения. В то же время в отношении ряда показателей выявлены межгрупповые различия. Так, применение интраназального спрея приводило к выраженному снижению отека слизистой оболочки вплоть до его отсутствия. Несмотря на статистически значимое снижение по сравнению с исходными показателями, в группе стандартного лечения отек слизистой оболочки сохранялся. Также в опытной группе наблюдалось практически полное отсутствие корок, тогда как на фоне стандартного лечения отмечалось 2-кратное снижение выраженности образования корок, тем не менее не приводящее к их полному отсутствию. В целом выраженность отека слизистой оболочки носа и образования корок в группе применения спрея была достоверно меньшей по сравнению с группой стандартного лечения. У пациентов обеих групп отсутствовали полипы и рубцы на слизистой оболочке носа.
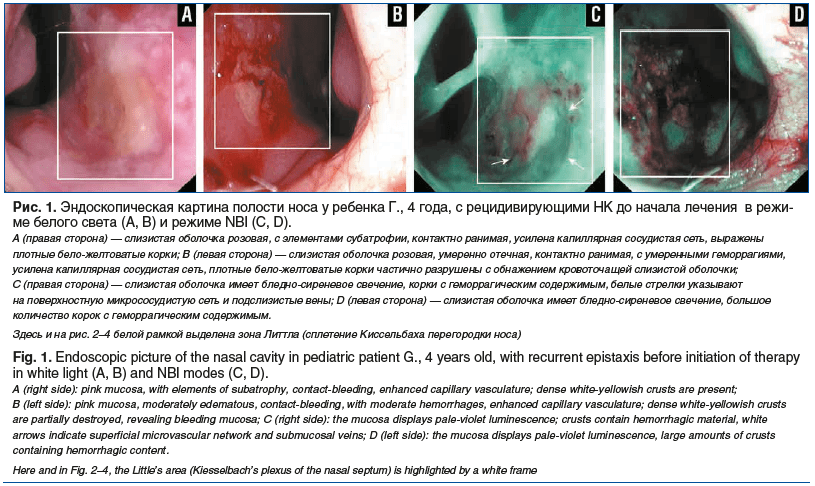
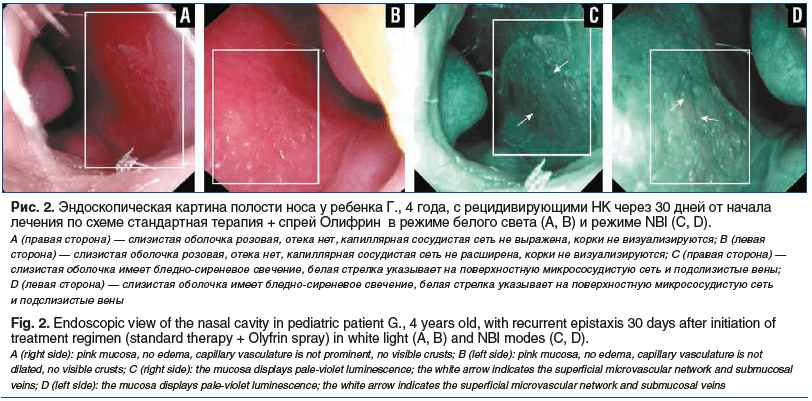
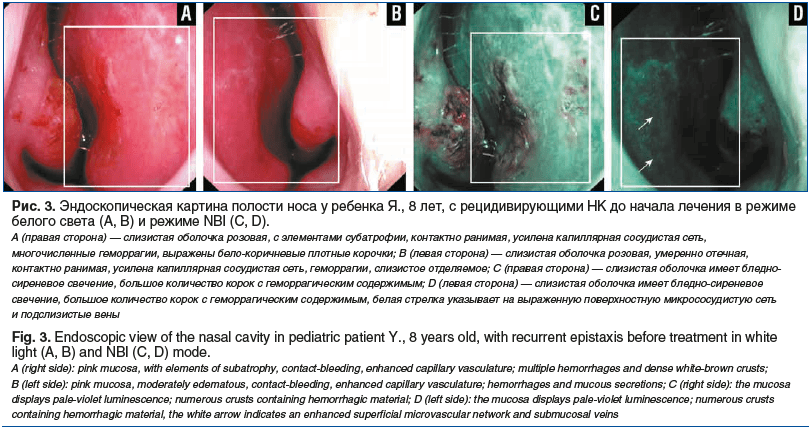
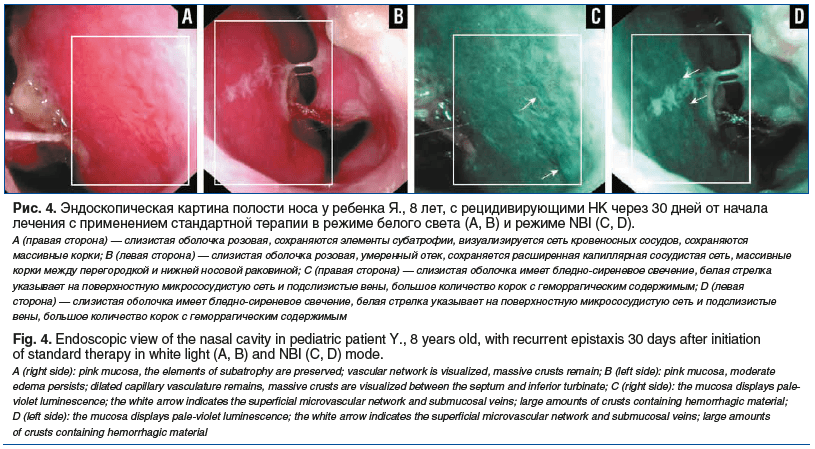
При оценке суммарной выраженности патологических находок при видеоэндоскопическом исследовании установлено ее достоверное снижение в обеих группах. Так, на фоне стандартной терапии отмечалось достоверное снижение данного показателя в 1,6 раза (8 (8–10) против 5 (4–6); p<0,001), тогда как в опытной группе снижение являлось 8-кратным (8 (7–9) против 1 (0–2); p<0,001). Как следствие, применение комбинированного спрея приводило к достоверно меньшей суммарной выраженности патологических находок в ходе видеоэндоскопического исследования при сравнении со стандартной терапией (p<0,001) (рис. 1–4).
Цитологическое исследование мазков с поверхности слизистой оболочки носа продемонстрировало, что применение спрея Олифрин приводит к некоторому снижению количества эпителия в мазках по сравнению с исходными показателями, однако данное изменение лишь приближалось к уровню статистической значимости (p<0,1). В то же время по окончании лечения количество эпителия в мазках пациентов в опытной группе было достоверно ниже такового в контрольной группе. Значимых различий и изменений в количестве слизи при риноцитологическом исследовании выявлено не было (данные не представлены).
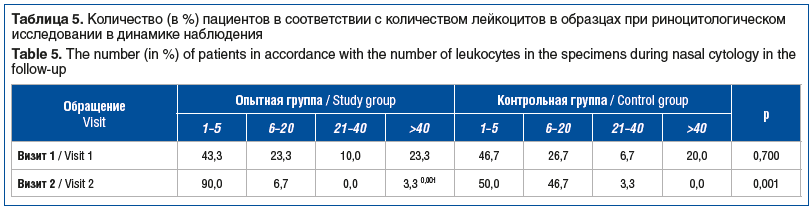
Анализ количества лейкоцитов в мазке с поверхности слизистой оболочки носа (табл. 5) показал, что после лечения с применением спрея Олифрин отмечалось статистически значимое снижение количества лейкоцитов вплоть до достижения референтных показателей (1–5 в п/з) в подавляющем большинстве (90%) случаев. При этом лечение с использованием стандартной терапии также приводило к снижению количества лейкоцитов в мазке, однако референтные значения после лечения наблюдались лишь в 50% случаев, тогда как у остальных пациентов в данной группе регистрировали умеренное увеличение количества лейкоцитов в мазке (6–20 в п/з). Таким образом, применение спрея Олифрин приводило к достоверно более выраженному снижению количества лейкоцитов в мазке с поверхности слизистой оболочки носа по сравнению со стандартной терапией (см. табл. 5).
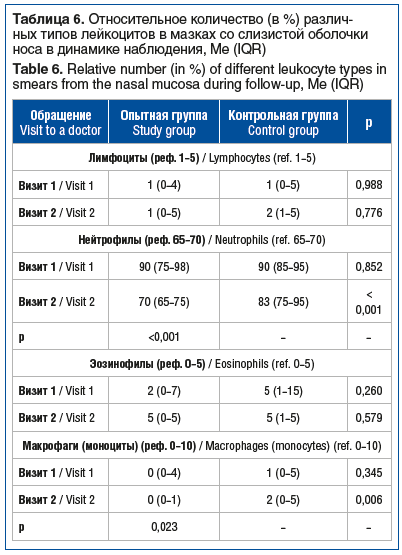
В связи с выявленными изменениями в количестве лейкоцитов проведено дальнейшее исследование изменений относительного количества отдельных типов лейкоцитов у пациентов на фоне лечения (табл. 6). Установлено, что значимых межгрупповых различий или изменений количества лимфоцитов и эозинофилов на фоне лечения не выявлено. В то же время применение спрея Олифрин приводило к достоверному снижению количества нейтрофилов в мазке на 22% по сравнению с исходными показателями. Применение стандартной терапии сопровождалось 8% снижением относительного количества нейтрофилов, не являющимся при этом статистически значимым. Как следствие, по окончании лечения относительное количество нейтрофилов в мазке пациентов в опытной группе было достоверно ниже такового в контрольной группе на 16%. Аналогичные различия отмечались в показателях относительного количества макрофагов (см. табл. 6).
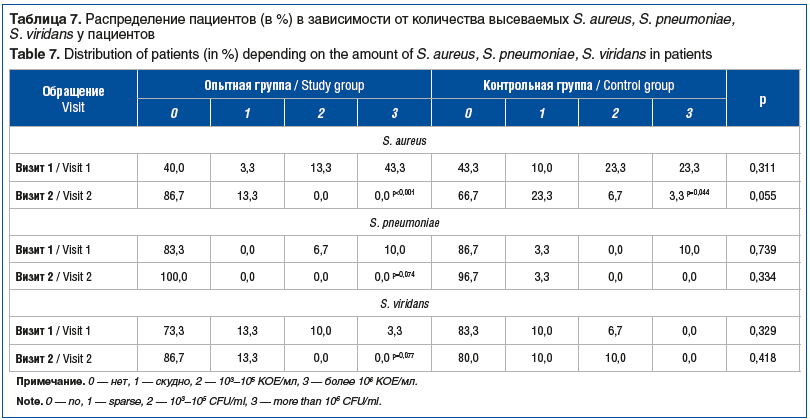
Результаты микробиологического исследования образцов мазков со слизистой оболочки носа свидетельствовали о том, что применение спрея сопровождалось снижением относительного количества случаев персистенции S. aureus у пациентов по сравнению с исходными значениями (60% против 13,3%; p=0,001), тогда как, несмотря на некоторую тенденцию к снижению, лечение с использованием стандартной терапии не приводило к достоверным изменениям (56,7% против 33,3%; p=0,146). Дополнительное применение спрея сопровождалось тенденцией к снижению числа случаев персистенции S. pneumoniae (16,7% против 0%; p=0,074). Значимого влияния стандартной терапии на количество случаев персистенции S. pneumoniae не отмечено, хотя и имелась некоторая тенденция к снижению (13,3% против 3,3%; p=0,248). Ни одна из схем лечения не оказывала значимого влияния на количество случаев персистенции S. viridans (данные не представлены).
Количественный анализ бактериальной обсемененности (табл. 7) продемонстрировал достоверное снижение количества колоний S. aureus. В то же время отсутствие S. aureus констатировали в 86,7 и 66,7% наблюдений в опытной и контрольной группах соответственно. Как следствие, количество S. aureus, высеянных с поверхности слизистой оболочки носа пациентов, в опытной группе было ниже такового в контрольной группе. Причем данные различия находились на границе статистической значимости (p=0,055). В случае S. pneumoniae и S. viridans установлено, что применение комбинированного спрея приводило к некоторому снижению количества высеваемых микроорганизмов, однако изменения лишь приближались к уровню статистической значимости. В свою очередь, лечение с применением стандартного подхода не оказывало сколько-нибудь значимого влияния на количество S. pneumoniae и S. viridans, однако и достоверных различий между группами выявлено не было. Данные наблюдения свидетельствуют в пользу некоторого антибиотического действия спрея Олифрин (см. табл. 7).
Таким образом, результаты проведенного исследования свидетельствуют об эффективности применения комбинированного спрея Олифрин в дополнение к стандартной терапии в лечении пациентов с НК в уменьшении количества эпизодов НК, а у ряда пациентов, полном сокращении до 0, а также их длительности. Полученные данные согласуются с результатами других исследований, продемонстрировавших эффективность топического применения препаратов на основе гиалуроновой кислоты для снижения НК. В частности, применение геля на основе гиалуроновой кислоты в комбинации с антибиотиками окситетрациклином и полимиксином В предотвращало развитие НК у 71,6% детей с рецидивирующими НК [13]. Результаты обследования пациентов с хроническим риносинуситом с назальным полипозом также продемонстрировали, что применение спрея с гиалуроновой кислотой снижает частоту НК вплоть до их полного отсутствия [16]. Применение спрея на основе гиалуроновой кислоты также снижало кровоточивость слизистой оболочки носа после проведения плановых хирургических вмешательств в полости носа, параназальных синусах и носоглотке [17]. Аналогично комбинированный спрей, содержащий гиалуроновую кислоту и ксилитол, существенно снижал частоту НК у пациентов, перенесших радиоволновую вазотомию [18].
Эффективность спрея Олифрин обусловлена в первую очередь наличием в его составе гиалуроновой кислоты. В частности, снижение выраженности и частоты НК под влиянием топического воздействия гиалуроновой кислоты обусловлено ролью гиалуроната в поддержании целостности кровеносных сосудов, в том числе за счет регуляции гликокаликса сосудистого эндотелия [19]. Гиалуроновая кислота также способствует ремоделированию межклеточного матрикса и созреванию коллагена, что приводит к ускорению заживления ран [20]. Ранее отмечалось, что комбинация гиалуроновой кислоты, α-токоферола, нитрата серебра и D-пантенола способствует остановке НК вследствие повышения свертываемости крови, причем действие гиалуроната может быть опосредовано ингибированием плазмина [21]. Помимо этого, гиалуроновая кислота способствует восстановлению слизистой оболочки носа после травматизации посредством стимуляции процессов реэпителизации [22].
В одном из проведенных ранее исследований высказывается предположение, что возможным механизмом влияния гиалуроновой кислоты в сочетании с транексамовой кислотой при НК наряду с заживлением ран является торможение продукции активных форм кислорода и продукции провоспалительных цитокинов [12]. Данное предположение согласуется с результатами метаанализа, продемонстрировавшего эффективность гиалуроновой кислоты в лечении воспалительных заболеваний полости носа [23].
Эффективность гиалуроновой кислоты может быть также обусловлена ее ингибирующим влиянием на формирование бактериальных биопленок при патологиях верхних дыхательных путей [24]. При этом в большей степени применение гиалуроновой кислоты снижало адгезивную способность и биопленкообразование на эпителии верхних дыхательных путей для S. aureus по сравнению с Haemophilus influenzae и Moraxella catarrhalis [25].
Наряду с гиалуроновой кислотой спрей содержит и другие активные компоненты, такие как α-токоферол и эфирное масло лимона, которые могут отчасти опосредовать наблюдаемые эффекты. Ранее проведенные исследования продемонстрировали, что топическое воздействие α-токоферола приводило к увлажнению слизистой оболочки носа и снижению образования корок у пациентов с атрофическим ринитом [26], что также может вносить определенный вклад в снижение частоты НК. Помимо этого, воздействие α-токоферола сопровождается интенсификацией процессов заживления слизистой оболочки носа [27].
Другим активным компонентом спрея Олифрин является эфирное масло лимона. Несмотря на отсутствие данных о применении эфирного масла лимона для лечения НК, терапевтический эффект может достигаться за счет противовоспалительного эффекта в слизистой оболочке носа [28]. Эфирное масло лимона также обладает тормозным влиянием на рост и образование биопленок патогенными микроорганизмами [29]. Стоит также отметить имеющиеся указания на эффективность применения цитрусовых, в частности Citrus aurantifolia, в остановке НК [30].
Таким образом, результаты проведенного исследования указывают на эффективность применения комбинированного интраназального спрея Олифрин для снижения частоты и длительности НК у детей, о чем свидетельствуют характер динамики жалоб, улучшение качества жизни, а также результаты клинического обследования. При этом данные эффекты могут быть обусловлены снижением выраженности воспалительной реакции и колонизации слизистой оболочки носа патогенными и условно-патогенными микроорганизмами под влиянием активных компонентов препарата. Учитывая роль хронического воспаления и персистенции патогенных микроорганизмов в патогенезе НК, справедливо предположить, что спрей Олифрин может рассматриваться в качестве патогенетической терапии НК.
Сведения об авторах:
Алексеенко Светлана — д.м.н., доцент, ведущий научный сотрудник научно-исследовательского отдела патологии верхних дыхательных путей ФГБУ «СПб НИИ ЛОР» Минздрава России; 190013, Россия, г. Санкт-Петербург, ул. Бронницкая, д. 9; профессор кафедры оториноларингологии ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; заведующая оториноларингологическим отделением СПб ГБУЗ «ДГМКЦ ВМТ им. К.А. Раухфуса»; 191036, Россия, г. Санкт-Петербург, Лиговский пр-т, д. 8; ORCID iD 0000-0002-3377-8711
Янов Юрий Константинович — академик РАН, д.м.н., профессор кафедры оториноларингологии ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; Военно-меди-
цинская академия; 194044, Россия, г. Санкт-Петербург, ул. Академика Лебедева, д. 6, лит. Ж; ORCID iD 0000-0001-9195-128X
Дворянчиков Владимир Владимирович — д.м.н., профессор, заслуженный врач России, директор ФГБУ «СПб НИИ ЛОР» Минздрава России, 190013, Россия, г. Санкт-Петербург, ул. Бронницкая, д. 9; ORCID iD 0000-0002-0925-7596
Рязанцев Сергей Валентинович — д.м.н., профессор, заместитель директора по научно-координационной работе ФГБУ «СПб НИИ ЛОР» Минздрава России; 190013, Россия, г. Санкт-Петербург, ул. Бронницкая, д. 9; ORCID iD 0000-0001-1710-3092
Кривопалов Александр Александрович — д.м.н., руководитель научно-исследовательского отдела патологии верхних дыхательных путей ФГБУ «СПб НИИ ЛОР» Минздрава России; 190013, Россия, г. Санкт-Петербург, ул. Бронницкая, д. 9; доцент кафедры оториноларингологии ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; ORCID iD 0000-0002-6047-4924
Контактная информация: Алексеенко Светлана, e-mail: svolga-lor@mail.ru
Источник финансирования: исследование проведено при поддержке ООО «Гротекс».
Конфликт интересов отсутствует.
Статья поступила 01.08.2025.
Поступила после рецензирования 18.08.2025.
Принята в печать 29.08.2025.
About the authors:
Svetlana Alekseenko — Dr. Sc. (Med.), Associate Professor, Leading Researcher at the Research Department of Upper Respiratory Tract Pathology, St. Petersburg Research Institute of Ear, Throat, Nose and Speech; 9, Bronnitskaya str., St. Petersburg, 190013, Russian Federation; Professor of the Department of Otorhinolaryngology, North West State Medical University named after I.I. Mechnikov; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; Head of the Department of Otorhinolaryngology, St. Petersburg
K.A. Raukhfus Children’s City Multidisciplinary Clinical Center of High Medical Technologies; 8, Ligovsky Lane, St. Petersburg, 191036, Russian Federation; ORCID iD 0000-0002-3377-8711
Yuri K. Yanov — Academician of the Russian Federationn Academy of Sciences, Dr. Sc. (Med.), Professor of the Department of Otorhinolaryngology, North West State Medical University named after I.I. Mechnikov; 41, Kirochnaya str.,
St. Petersburg, 191015, Russian Federation; Military Medical Academy; 6 lit. Zh, Akademika Lebedeva str., St. Petersburg, 194044, Russian Federation; ORCID iD 0000-0001-9195-128X
Vladimir V. Dvoryanchikov — Dr. Sc. (Med.), Professor, Distinguished Physician of the Russian Federationn Federation, Director of the St. Petersburg Research Institute of Ear, Throat, Nose and Speech; 9, Bronnitskaya str., St. Petersburg, 190013, Russian Federation; ORCID iD 0000-0002-0925-7596
Sergey V. Ryazantsev — Dr. Sc. (Med.), Professor, Deputy Director for Scientific and Coordination Work of the St. Petersburg Research Institute of Ear, Throat, Nose and Speech; 9, Bronnitskaya str., St. Petersburg, 190013, Russian Federation; ORCID iD 0000-0001-1710-3092
Alexander A. Krivopalov — Dr. Sc. (Med.), Head of the Research Department of Upper Respiratory Tract Pathology of the St. Petersburg Research Institute of Ear, Throat, Nose and Speech; 9, Bronnitskaya str., St. Petersburg, 190013, Russian Federation; Associate Professor of the Department of Otorhinolaryngology, North West State Medical University named after I.I. Mechnikov; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; ORCID iD 0000-0002-6047-4924
Contact information: Svetlana Alekseenko, e-mail: svolga-lor@mail.ru
Funding Source: the study was conducted with the support of Grotex LLC.
There is no conflict of interest.
Received 01.08.2025.
Revised 18.08.2025.
Accepted 29.08.2025.
1Об утверждении стандарта первичной медико-санитарной помощи при носовом кровотечении: приказ Министерства здравоохранения Российской Федерации от 20 декабря 2012 г. № 1209н. Министерство здравоохранения Российской Федерации. (Электронный ресурс.) URL: https://clck.ru/3NUDwr (дата обращения: 04.08.2025).
Обсуждение
Заключение
Информация с rmj.ru






