Введение
Остеоартрит (ОА) плечевого сустава (ОАпс) — это комплексное заболевание всех его структур, приводящее к боли, уменьшению диапазона движений и прогрессирующей потере функции [1, 2]. Согласно ряду эпидемиологических исследований, распространенность ОАпс достигает 20–25% у пациентов старше 55 лет [3]. Примечательно, что именно ОАпс трудно поддается лечению, а тотальное эндопротезирование сопряжено со многими сложностями. Имеются скромные результаты в отношении восстановления функции в связи с уникальной анатомией сустава, выраженным болевым синдромом в послеоперационном периоде и дорогостоящей реабилитацией, а также неполноценным качеством жизни из-за существенных ограничений бытовой активности [3–5]. Современное консервативное лечение предлагает применение анальгетиков и инъекции кортикостероидов. Однако достаточного количества работ, убедительно доказывающих их эффективность, в доступной литературе не представлено, притом что само их использование сопряжено со значительным количеством побочных эффектов со стороны желудочно-кишечного тракта, почек и сердца [3–5].
В этом отношении гиалуроновая кислота (ГК) рассматривается как альтернативный метод лечения ОА, не требующий хирургического вмешательства. ГК обладает как обез-боливающим, так и хондропротективными свойствами. Применение ГК в виде инъекций у пациентов с ОАпс обосновано рядом клинических исследований [1, 2, 5].
Представляем клиническое наблюдение, демонстрирующее эффективность применения вязкоэластичного имплантата для внутрисуставных инъекций на основе ГК у пациентки с посттравматическим омартрозом.
Содержание статьи
Клиническое наблюдение
Пациентка Л., 1951 г. р., обратилась в клинико-диагностическое отделение НИИТОН ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России (далее НИИТОН) с жалобами на постоянные ограничения движений в правом плечевом суставе, боль пульсирующего характера в области правой лопатки и невозможность отведения руки с лопаткой кзади.
Из анамнеза заболевания известно, что в феврале 2024 г. после бытовой травмы (падение на льду на правую руку) появилась резкая боль в правом плече стреляющего характера, резкая потеря движений. Пациентка была консультирована ортопедом НИИТОН (выполнена обзорная рентгенография правого плечевого сустава), выставлен диагноз: «Оскольчатый перелом эпиметафиза плечевой кости с отрывом большого бугорка и поперечным переломом шейки плечевой кости со смещением фрагментов по ширине на толщину кости». Прооперирована в НИИТОН методом наложения аппарата внешней фиксации (АВФ) с последующим достижением сращения и удалением АВФ (рис. 1).
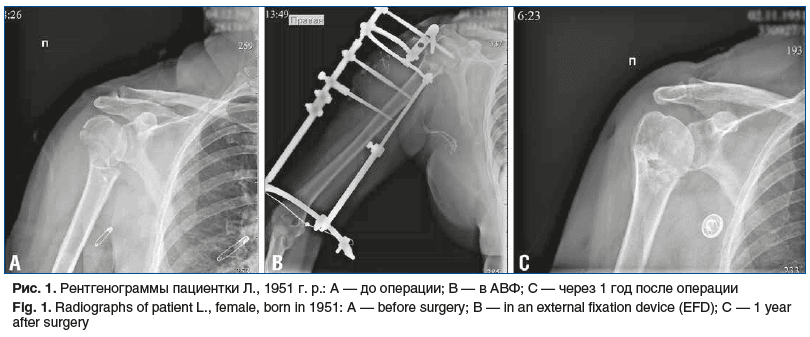
До января 2025 г. пациентка неоднократно получала курсы консервативного лечения, включая санаторно-курортное, ударно-волновую терапию, блокаду надлопаточного нерва ввиду болевых ощущений при движениях, PRP-терапию и хондропротекторы параартикулярно, индивидуальную гимнастику для разработки движений верхней конечности, кинезиотейпинг. Совокупность проведенных мероприятий позволила практически полностью избавиться от боли, но не вернула полноценный объем движений в правом плечевом суставе.
Физикальная диагностика. Клинический осмотр ортопеда в НИИТОН в январе 2025 г: контуры правого плечевого сустава не изменены. Отмечается атрофия надостной и под-остной мышц справа, что визуально сформировало псевдокрыловидную лопатку. При пальпации боль отсутствует. Объем движений в правом плечевом суставе снижен как по сравнению с контралатеральной конечностью, так и по сравнению с нормальными показателями (см. таблицу).

По данным дообследований (контрольная рентгенограмма плечевого сустава в двух проекциях, УЗИ мягких тканей правого плечевого сустава) выявлены: неравномерное истончение гиалинового хряща до 1,1 мм с наличием дефектов 2-й степени по OUTERBRIDGE с поверхностным разволокнением хряща; неравномерное сужение суставной щели; единичные краевые остеофиты суставной впадины, внутрисуставная жидкость не визуализируется. Отмечаются признаки субдельтовидного бурсита.
Клинико-инструментальный диагноз: посттравматический омартроз 2-й стадии по Н.С. Косинской с функцио-нальной недостаточностью 1-го класса, повреждением хрящевой ткани, сопутствующим формированием вторичной миофасциальной дисфункции.
Лечение. В связи с угрозой прогрессирования омартроза, вторичного комплексного регионального болевого синдрома I типа, а также снижением функциональной мобильности плечевого сустава и качества жизни, наличием болевых ощущений проведено следующее лечение: введение двукратно (с перерывом в 10 дней) высококогезивного 3% геля гиалуроновой кислоты Флексотрон® МАГНУМ молекулярной массой 2,2 МДа и разработка движений на аппарате «Артромот S3» курсом 14 сеансов.
Исход. При контрольном осмотре в марте 2025 г. пациентка не предъявляла жалоб, продемонстрировала увеличение объема движений в правом плечевом суставе (рис. 2), который оценивался как достаточный: отведение без лопатки достигло 80°/ отведение с лопаткой ~90°; сгибание без лопатки 20°/ с лопаткой 150°; разгибание ~20°; ротационные движения не изменились вследствие сохраняющихся симптомов посттравматической остаточной нейропатии надлопаточного нерва.
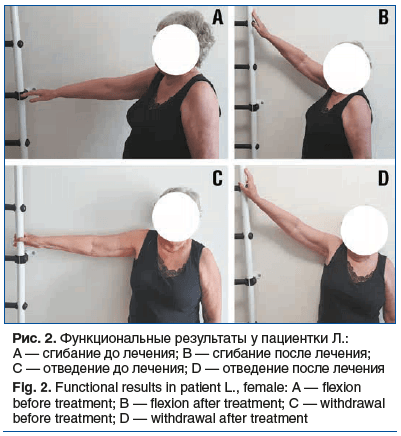
В настоящее время (апрель 2025 г.) пациентка удовлетворена достигнутым объемом движений, регулярно выполняет гимнастику, посещает бассейн, однако от активных лечебных мероприятий, в том числе с использованием внутрисуставных поддерживающих инъекций, отказывается. На наш взгляд, это связано с рядом обстоятельств: пожилым возрастом, значимым травматическим опытом, хорошим качеством жизни, обеспечивающим ежедневную трудовую активность и, главное, отсутствием значимого болевого синдрома.
Обсуждение
В настоящее время накопилось достаточное количество публикаций, свидетельствующих о пользе интраартикулярной инъекции ГК при ОА, в том числе ОАпс [6–8]. Предварительные данные о применении ГК при ОАпс многообещаю-щие, но пока не окончательные. Точный клеточный механизм работы ГК еще до конца не изучен, преимущественно его связывают с обезболиванием и хондропротективным действием, объясняющими его клинические эффекты.
Представленное клиническое наблюдение продемонстрировало несомненную пользу применения внутрисуставной инъекции 3% ГК у пациентки при посттравматическом омартрозе на фоне перелома проксимального отдела плеча. В связи с выраженными повреждениями самого сустава, повреждением хрящевой ткани и параартикулярных образований, в том числе плечевого сплетения и сосудистого пучка, развитие ОА было неизбежно. Основная задача лечения при этом — снизить темпы прогрессии омартроза и функциональную недостаточность, в том числе посредством внутрисуставных инъекций ГК.
Поскольку концентрация нативной ГК при ОА снижается примерно до 50% от физиологического показателя [9], внутрисуставная инъекция ГК оказывает мгновенный эффект. Она действует как смазка при медленных движениях с низкой скоростью скольжения суставных концов, повышая вязкость синовиальной жидкости, а также обеспечивает амортизацию при быстрых движениях с высокой скоростью скольжения, выступая в качестве упругого твердого тела [5]. Кроме того, ГК поддерживает реологические свойства суставной жидкости, обеспечивает антиоксидантный эффект, снижает продукцию матриксных металлопротеиназ и провоспалительных цитокинов, способствует регенерации хряща [5, 10].
Гиалуроновая кислота также связывается с рецептором гиалуронанопосредованной подвижности (RHAMM), который, как считается, способствует хондропротекции за счет снижения активности нативных лейкоцитов в плане выброса агрессивных цитокинов, способствующих аутоповреждению хрящевой ткани. Апоптоз хондроцитов дополнительно снижается за счет связывания ГК с CD44, что приводит к уменьшению экспрессии дезинтегрина и металлопротеиназы с тромбоспондиновыми мотивами (ADAMTS). В настоящее время подчеркивается, что развитие ОА связано с повышением экспрессии ADAMTS 4 и 5, выступающих как протеолитические ферменты, которые разрушают протеогликаны гиалинового хряща [10]. Показано, что биологический механизм, с помощью которого ГК влияет на уровень аггрекана в хряще, заключается в связывании с CD44 и молекулой межклеточной адгезии (ICAM) 1 [10].
Некоторые авторы указывают, что внутрисуставные инъекции ГК, по-видимому, превосходят по эффективности типичные нехирургические методы лечения, которые в настоящее время рассматриваются в качестве стандарта терапии первой линии при ОАпс, такие как физиотерапия или инъекции кортикостероидов [5].
В нашем клиническом наблюдении был использован имплантат вязкоэластичный на основе 3% ГК Флексотрон® МАГНУМ. Основная его черта — высокая когезивность, обусловленная высокой концентрацией гиалуроната натрия (3%) (молекулярная масса 2,2 МДа), что обеспечивает надежную защиту разрушенных участков хряща. Когезия характеризует прочность тела и его способность противостоять внешнему воздействию за счет взаимного притяжения одинаковых молекул. Таким образом, чем выше когезия, тем лучше способность геля сохранять свою форму в тканях при воздействии механических и физических факторов. Флексотрон® МАГНУМ позволяет при двукратном и даже однократном применении обеспечить устойчивый длительный эффект в таком динамически сложном и активном суставе, как плечевой. Кроме того, благодаря молекулярной массе 2,2 МДа он хорошо купирует боль, снижает уровень брадикинина и PGf2α, ингибирует ЦОГ-2. Использование ГК в виде когезивного геля способствует перемещению вновь синтезированного протеогликана из матрикса, связанного с клетками, в более удаленный матрикс в данной модели, что позволяет предположить, что 3% ГК (типа Флексотрон® МАГНУМ) может оказывать терапевтическое воздействие при ОА, укрепляя межтерриториальный матрикс хряща [5, 7, 10].
Заключение
Лечение пациентов с ОА плечевого сустава до настоящего времени сопряжено с большими трудностями ввиду сложности анатомии, ограниченных возможностей восстановления полноценного объема движений, купирования болевого синдрома. Представленное клиническое наблюдение убедительно продемонстрировало возможности использования высококогезивного 3% геля гиалуроната натрия в реабилитации больных с посттравматическим ОАпс. Структурная особенность — высокая когезивность и молекулярная масса 2,2 МДа — позволила достичь хорошего объема движений у пациентки, полностью купировать болевой синдром и расширить физическую активность, значительно повысить качество жизни.
СВЕДЕНИЯ ОБ АВТОРЕ:
Сертакова Анастасия Владимировна — к.м.н., врач-травматолог-ортопед клинико-диагностического и реабилитационного отделения НИИТОН ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава России; 410012, Россия, г. Саратов, ул. Большая Казачья, д. 112; ORCID iD 0000-0002-4375-0405
Контактная информация: Сертакова Анастасия Владимировна, e-mail: anastasiya-sertakova@yandex.ru
Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 08.04.2025.
Поступила после рецензирования 18.04.2025.
Принята в печать 30.04.2025.
ABOUT THE AUTHOR:
Anastasia V. Sertakova — C. Sc. (Med.), orthopedic traumatologist of the Clinical Diagnostic and Rehabilitation Department of the Scientific Research Institute of Traumatology, Orthopedics and Neurosurgery, V.I. Razumovskiy Saratov State Medical University, 112, Bolshaya Kazachya str., Saratov, 410012, Russian Federation; ORCID iD 0000-0002-4375-0405
Contact information: Anastasia V. Sertakova, e-mail: anastasiya-sertakova@yandex.ru
Financial Disclosure: the author has no a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 08.04.2025.
Revised 18.04.2025.
Accepted 30.04.2025.
Информация с rmj.ru






