Введение
Вирус простого герпеса (ВПГ) является широко распространенной инфекцией. По некоторым оценкам, 491,5 млн человек инфицированы ВПГ 2-го типа, что составляет 13,2% населения мира в возрасте 15–49 лет, 3752 млн человек инфицированы ВПГ 1-го типа, что соответствует общемировой распространенности в 66,6% среди людей в возрасте от 0 до 49 лет [1].
До 10 млн человек во всем мире страдают от герпетического кератита (ГК), а заболеваемость им составляет примерно 30 случаев на 100 тыс. человек в год [2].
Поражение глаз проявляется как первичная или пост-первичная форма и может охватывать все ткани глаза с развитием блефарита, конъюнктивита, эпителиального и стромального кератитов, ирита, ретинита [3]. Причем доминирующей формой поражения глаз является ГК [4].
Герпетический кератит характеризуется рецидивирующим течением, с многократными эпизодами поражения роговицы, приводящими к снижению остроты зрения, и является лидирующей причиной развития роговичной слепоты инфекционной этиологии [5]. Так, в ретроспективном эпидемиологическом исследовании 30-летнего периода наблюдения пациентов с рецидивирующим ГК у 11 из 20 пациентов с неблагоприятными исходами заболевания было отмечено снижение остроты зрения ниже 0,1 [6].
Лечение данной хронической, часто рецидивирующей патологии до сих пор остается сложной задачей практической офтальмологии. Существует множество причин неэффективности терапии. В частности, современные противогерпетические препараты не способны элиминировать ВПГ из организма человека, а только снижают его активность [7, 8].
Самым распространенным этиотропным препаратом для лечения герпетической инфекции является ацикловир [9]. Этот «золотой стандарт» этиотропной противогерпетической терапии с успехом применяется и в настоящее время. Однако как к ацикловиру, так и к другим аналогам нуклеозидов возможно развитие резистентности вируса [10], а также возникновение токсических реакций со стороны переднего отдела глаза. И хотя терапевтическую эффективность аналогов нуклеозидов трудно переоценить, комбинированная противогерпетическая терапия с использованием дополнительных иммунотропных препаратов давно доказала свою эффективность. Опыт применения при ГК в качестве противовирусного лечения глазных капель интерферон (ИФН) α-2b человеческий рекомбинантный в комплексе с препаратами группы ацикловира по некоторым критериям (сроки резорбции инфильтрации роговицы и длительность лечения) показал более высокие результаты, чем лечение только препаратами группы ацикловира [11]. В клинических исследованиях ИФН α-2b человеческий рекомбинантный оказывал выраженный терапевтический эффект в лечении всех клинических форм герпетических поражений глаз: при кератитах (эпителиальном, картообразном, стромальном), герпетической язве роговицы, кератоувеитах, увеитах. Так, при сравнительном исследовании 30 больных с ГК полная эпителизация и резорбция инфильтрации стромы завершились раньше в группе, получавшей препарат, по сравнению с группой контроля [11].
Очищенный экстракт побегов растения Solanum tuberosum относится к иммунотропным противовирусным средствам, имеет растительное происхождение, является отечественной разработкой. Основное действующее вещество препарата — гексозный гликозид, состоящий из глюкозы, рамнозы, арабинозы, маннозы, ксилозы, галактозы, уроновых кислот. В эксперименте in vitro под руководством проф. А.А. Кущ в лаборатории клеточной инженерии ГН НИИ вирусологии им. Д.И. Ивановского РАМН была доказана противовирусная активность Solanum tuberosum побегов суммы полисахаридов в отношении ВПГ 1-го и 2-го типа [12]. Проведенное исследование позволяет предложить интегративную схему механизма противовирусного действия гексозного гликозида. Препарат оказывает вирусостатическое действие, подавляет репликацию и полимеразные реакции вирусов, блокируя синтез вирусной ДНК в пораженных клетках слизистой оболочки глаза.
Все перечисленные выше качества Solanum tuberosum побегов суммы полисахаридов позволили спрогнозировать эффективность его применения в лечении ГК.
Цель исследования: сравнение эффективности лечения эпителиального ГК с применением глазной мази ацикловир или комбинированной терапии, включающей в себя глазную мазь ацикловир и глазные капли Solanum tuberosum побегов суммы полисахаридов.
Содержание статьи
Материал и методы
В проспективное одноцентровое исследование были включены 40 пациентов (25 мужчин и 15 женщин) в возрасте от 18 до 65 лет с постпервичным поверхностным ГК, подтвержденным методом полимеразной цепной реакции (ПЦР).
Критерии невключения: глубокие стромальные и эндотелиальные формы ГК, явления увеита, тяжелая некомпенсированная соматическая патология, беременность и лактация, невозможность или отказ пациента дать согласие на лечение и госпитализацию. За время исследования никто из пациентов не был исключен из исследования.
Пациенты были разделены путем рандомизации на 2 группы: 1-я группа (20 пациентов, 20 глаз) получала лечение в виде глазной мази ацикловир 3%, 2-я группа (20 пациентов, 20 глаз) — глазной мази ацикловир 3% совместно с глазными каплями 0,04 мг/мл Solanum tuberosum побегов суммы полисахаридов.
Пациенты обеих групп получали глазную мазь ацикловир 3% каждые 4 ч 5 р/сут. Мазь закладывали в виде полоски длиной 1 см в нижний конъюнктивальный мешок до заживления. Лечение продолжали еще в течение 3 сут после заживления. Во 2-й группе пациенты дополнительно получали инстилляции глазных капель Solanum tuberosum побегов суммы полисахаридов 0,04 мг/мл (Панавир®, ООО «Национальная Исследовательская Компания») по 2 капли 4 р/сут с интервалом 2 ч. С учетом нахождения пациентов в процессе лечения в стационаре наблюдение проводилось ежедневно весь период активного лечения, через 2 нед. и через 1 мес. после выздоровления пациентов осматривали амбулаторно. Помимо противовирусной терапии, пациенты обеих групп получали слезозаместительную и кератопротективную терапию.
Пациенты поступали в стационар с подтвержденным диагнозом ГК по данным жалоб, анамнеза, типичной клинической картины, результатов ПЦР-исследования соскоба с конъюнктивы. Сроки развития заболевания колебались от 2 до 7 дней. С момента появления первых жалоб до поступления в стационар пациенты терапию не получали. Лечение начиналось в день поступления в стационар.
При биомикроскопии оценивали состояние век, конъюнктивы, роговицы. При осмотре роговицы проводили оценку площади эпителиального дефекта посредством флюоресцеиновой пробы с помощь полосок офтальмологических диагностических. После окрашивания роговицы проводили фоторегистрацию с помощью фотощелевой лампы (SL-1800, Nidek, Япония). Далее изображение обрабатывали сервисом, работающим на основе искусственного интеллекта (ИИ), с получением маски сегментации дефекта. Вычисляли площадь эрозированной поверхности роговицы с получением численного значения площади поражения в процентах от общей площади.
Автоматический анализ гиперемии глаза проводили с помощью анализатора глазной поверхности (Ocular Surface Analyzer DA-1, ChongQing SunKingdom, Китай). Получали фото поверхности глаза, после чего снимок сравнивали со шкалой покраснения глаза: 0 — покраснения нет, 1 — покраснение легкой степени, 2 — покраснение умеренной степени, 3 — покраснение сильной степени, 4 — покраснение тяжелой степени.
Анализировали наличие при разных условиях освещения или отсутствие роговичного синдрома (светобоязнь, слезотечение, блефароспазм).
В ходе биомикроскопии субъективно проводили оценку наличия или отсутствия инфильтрации роговицы.
Визометрию проводили с помощью проектора знаков и набора пробных линз до и после лечения.
Статистический анализ проводили с использованием программы StatTech v. 4.7.1 (разработчик ООО «Статтех», Россия). Количественные показатели оценивали на предмет соответствия нормальному распределению с помощью критерия Шапиро — Уилка. Количественные показатели, выборочное распределение которых соответствовало нормальному, описывали с помощью средних арифметических величин (M) и стандартных отклонений (SD). В качестве меры репрезентативности для средних значений указывали границы 95% доверительного интервала (95% ДИ). В случае отсутствия нормального распределения количественные данные описывали с помощью медианы (Me) и нижнего и верхнего квартилей [Q1; Q3]. Сравнение групп по количественному показателю, распределение которого в каждой из групп соответствовало нормальному, при условии равенства дисперсий выполнялось с помощью t-критерия Стьюдента. Сравнение групп по количественному показателю, распределение которого отличалось от нормального, выполняли с помощью U-критерия Манна — Уитни. Различия считали статистически значимыми при p<0,05.
Результаты исследования
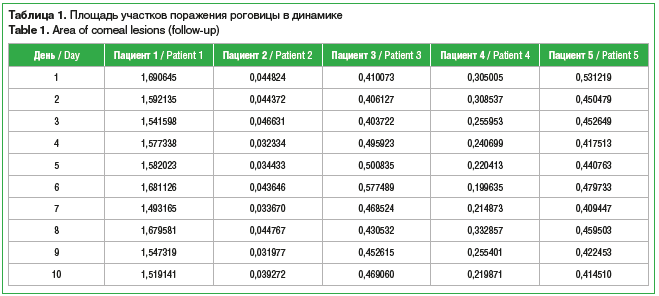
Для определения сроков эпителизации роговицы применяли сервис оценки эффективности лечения ГК на основе ИИ. В таблице 1 представлен фрагмент анализа площади зон поражения роговицы при древовидном кератите в динамике для нескольких пациентов, проведенный данным сервисом.
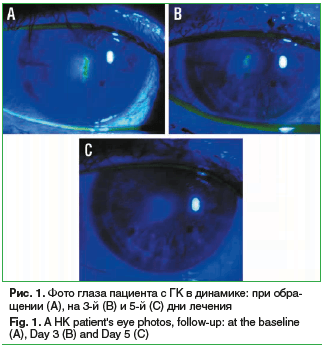
На рисунке 1 приведены фото глаза, демонстрирующие эпителизацию роговицы в динамике.
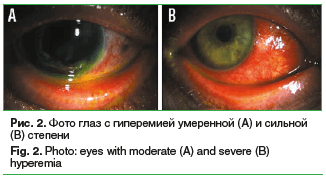
Выраженность гиперемии при поступлении варьировала от умеренной до сильной степени (рис. 2).
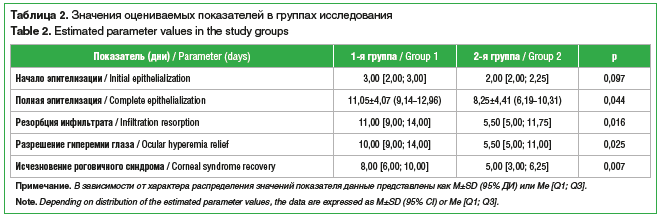
Был выполнен анализ всех оцениваемых показателей в группах наблюдения (табл. 2). При сопоставлении сроков начала эпителизации в зависимости от исследуемой группы не удалось выявить статистически значимых различий (p=0,097). Установлены статистически значимые межгрупповые различия по срокам полной эпителизации, резорбции инфильтрата, разрешения гиперемии глаза, исчезновения роговичного синдрома (p=0,044, p=0,016, p=0,025, p=0,007 соответственно).
Был проведен анализ динамики остроты зрения в обеих группах (табл. 3). При сравнении показателя остроты зрения до лечения нам не удалось установить статистически значимых межгрупповых различий (p=0,703), тогда как после лечения показатели в группах статистически значимо различались (p=0,038).

В обеих группах острота зрения после лечения статистически значимо отличалась от дооперационных значений (p<0,001 в обоих случаях).
Средние сроки пребывания в стационаре составили 10–14 дней. В процессе лечения ни в одной группе не было отмечено нежелательных явлений. В результате динамического наблюдения в установленные сроки через 14 дней и через 1 мес. после выписки рецидивов заболевания не наблюдалось в обеих группах.
Обсуждение
Эпителиальный ГК должен разрешиться в течение 2 нед., максимум 3 нед. при использовании местных противовирусных препаратов. Также известно, что эпителиальный ГК проходит самостоятельно в течение 2 нед. [13, 14]. Целью лечения является уменьшение боли и сокращение продолжительности заболевания [15].
К причинам затяжного течения ГК относят низкую приверженность пациентов лечению, метагерпетический кератит, являющийся разновидностью нейротрофического кератита, для которого характерно отсутствие активной вирусной инфекции и который проявляется наличием дендритной или географической язвы. Нераспознанное воспаление подлежащей стромы может служить фактором наличия стойкого изъязвления роговицы. Другой причиной является резистентность к противовирусной терапии, особенно у пациентов с ослабленным иммунитетом, в том числе у пациентов с атопией [15].
Существуют исследования, демонстрирующие превосходство комбинированной противовирусной терапии над монотерапией мазью ацикловира. Так, полная эпителизация роговицы на 5-й и 10-й день была зарегистрирована у значимо (р<0,001) большего количества пациентов в группе комбинированной терапии, получавшей ацикловир совместно с Solanum tuberosum побегов суммы полисахаридов, — 24 и 88% соответственно, в то время как в группе сравнения — 0 и 28,8% соответственно [16]. В данной работе критериями оценки эффективности терапии были: признаки полной эпителизации через 5, 10, 15 дней терапии, результаты колориметрии конъюнктивы, выраженность роговичного синдрома, чувствительность роговицы и острота зрения. В проведенном нами исследовании критериями являлись: начало эпителизации, полная эпителизация, при этом эпителизация оценивалась ежедневно, а сроки этих показателей определялись с помощью сервиса, работающего на основе ИИ; резорбция инфильтрата; разрешение гиперемии глаза; исчезновение роговичного синдрома; острота зрения. Настоящее исследование и работа [16] были разного дизайна, но продемонстрировали одинаково показательные положительные результаты комбинированной терапии ГК.
Анализ полученных нами результатов показал, что сроки начала эпителизации в обеих группах совпадали, но сроки полной эпителизации статистически значимо (p=0,044) были короче во 2-й группе, что предположительно связано с синергизмом в отношении противовирусного действия ацикловира и Solanum tuberosum побегов суммы полисахаридов.
Были получены статистически значимые (p=0,016) различия сроков резорбции инфильтрации — через 11 и 5,5 сут для 1-й и 2-й группы соответственно, на основании чего можно сделать вывод о противовоспалительном действии Solanum tuberosum побегов суммы полисахаридов.
Сокращение сроков разрешения гиперемии глаза и исчезновения роговичного синдрома (p=0,007) в группе комбинированной терапии по сравнению с классической терапией (см. табл. 2), вероятно, связано с более быстрыми сроками эпителизации эрозированного дефекта роговицы и резорбции инфильтрации во 2-й группе по сравнению с 1-й.
Повышение остроты зрения в период клинического выздоровления является одним из показателей эффективности лечения ГК. Более существенное повышение остроты зрения во 2-й группе по сравнению с 1-й группой (см. табл. 3) позволяет сделать вывод о положительном влиянии комбинированной терапии на зрительные функции в исходе ГК.
В целом исследование показало, что совместное применение ацикловира, глазной мази, и Solanum tuberosum побегов суммы полисахаридов, глазных капель (Панавир®), имело более высокую терапевтическую эффективность, что проиллюстрировано более быстрым разрешением гиперемии глаза, сокращением сроков эпителизации роговицы, ранним купированием воспалительных явлений (инфильтрации роговицы), что помогло добиться более высоких зрительных функций в исходе заболевания.
Заключение
Резюмируя вышесказанное, можно сделать вывод о более высокой клинической эффективности комбинированной терапии эпителиального ГК с использованием глазной мази ацикловир совместно с глазными каплями Solanum tuberosum побегов суммы полисахаридов в сравнении с изолированным применением глазной мази ацикловир. Вывод сделан в том числе на основе данных о сроках эпителизации, полученных с помощью сервиса, работающего на основе ИИ.
Полученные результаты позволяют рекомендовать к применению в составе комплексной терапии ГК глазные капли 0,04 мг/мл Solanum tuberosum побегов сумма полисахаридов с целью сокращения сроков лечения и получения в исходе заболевания более высоких показателей остроты зрения.
СВЕДЕНИЯ ОБ АВТОРАХ:
Яни Елена Владимировна — к.м.н., и. о. начальника отдела инфекционных и аллергических заболеваний глаз ФГБУ «НМИЦ ГБ им. Гельмгольца» Минздрава России; 105062, Россия, г. Москва, ул. Садовая-Черногрязская, д. 14/19; ORCID iD 0000-0003-1527-9414
Ступакова Мария Михайловна — аспирант отдела инфекционных и аллергических заболеваний глаз ФГБУ «НМИЦ ГБ им. Гельмгольца» Минздрава России; 105062, Россия, г. Москва, ул. Садовая-Черногрязская, д. 14/19; ORCID iD 0000-0003-4943-5286
Контактная информация: Ступакова Мария Михайловна, e-mail: bliznec.masha@mail.ru
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 11.03.2025.
Поступила после рецензирования 03.04.2025.
Принята в печать 28.04.2025.
ABOUT THE AUTHORS:
Elena V. Yani — C. Sc. (Med.), Acting Head of the Department of Infectious and Allergic Eye Diseases, Helmholtz National Medical Research Center; 14/19, Sadovaya-Chernogryazskaya str., Moscow, 105062, Russian Federation; ORCID iD 0000-0003-1527-9414
Maria M. Stupakova — Postgraduate Student of the Department of Infectious and Allergic Eye Diseases, Helmholtz National Medical Research Center; 14/19, Sadovaya-Chernogryazskaya str., Moscow, 105062, Russian Federation; ORCID iD 0000-0003-4943-5286
Contact information: Maria M. Stupakova, e-mail: bliznec.masha@mail.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 11.03.2025.
Revised 03.04.2025.
Accepted 28.04.2025.
материал rmj.ru
