Введение
Расчет оптической силы интраокулярной линзы (ИОЛ) на предоперационном этапе при хирургии хрусталика играет одну из определяющих ролей в достижении «рефракционного успеха» после операции [1–3]. Существующие на сегодняшний день современное хирургическое оборудование и высокоточные методы диагностики позволяют добиться хороших функциональных результатов в 70–80% случаев [4–6]. Однако возрастающие требования и ожидания пациентов определяют необходимость оптимизации и совершенствования методов и алгоритмов предоперационного расчета оптической силы ИОЛ, особенно при имплантации мультифокальных и торических линз [1, 7]. Таким образом, максимально точное и надежное прогнозирование послеоперационного результата является актуальной задачей современной катарактальной хирургии [8].
Известно, что при расчете ИОЛ, кроме оптической силы роговицы, учитываются глубина передней камеры, центральная толщина роговицы, толщина хрусталика и расстояние «от белого до белого» [1, 3, 9]. Точность определения указанных параметров связана с принципом работы биометра (ультразвуковой или оптический), в то время как значение оптической силы роговицы зависит не только от используемого прибора, но и от принципов измерения радиуса кривизны ее поверхности, способов расчета кератометрии, предпочтений и поправок хирурга [9, 10]. Таким образом, точное определение биометрических параметров глаза является своеобразным фундаментом для последующего расчета ИОЛ и, соответственно, достижения запланированной цели при интраокулярной коррекции аномалий рефракции и афакии.
Традиционно оптическая сила роговицы определяется с использованием инструментов (ручные кератометры, автоматические кератометры, оптическая когерентная томография, кератотопография с использованием колец Пласидо), способных измерять радиус кривизны ее передней поверхности [10, 12–14]. После преобразования этого радиуса в оптическую силу с помощью кератометрического индекса полученное значение можно использовать во всех формулах расчета ИОЛ для большинства пациентов [15].
Появившиеся в последние десятилетия новые диагностические технологии, такие как Scheimpflug-камера, имеют дополнительную возможность — измерение радиуса кривизны задней поверхности роговицы [16–18], что теоретически может привести к повышению точности расчета ИОЛ, поскольку появляется возможность конкретного определения общей оптической силы роговицы (Total Cornea Power, TCP), а не примерное представление о ней за счет кератометрического индекса.
В реальной клинической практике значение TCP не предназначено для расчета ИОЛ с помощью стандартных формул. Существующие исследования, посвященные изучению точности TCP в расчете ИОЛ, немногочисленны, а результаты некоторых из них противоречивы.
Таким образом, целью настоящей работы явилась оценка точности расчета мультифокальной интраокулярной линзы (мИОЛ) по данным общей оптической силы, определенной при помощи трассировки лучей (Total Cornea Refractive Power, TCRP), в 10 зонах роговицы по 10 формулам.
Содержание статьи
Материал и методы
В исследование вошли 117 пациентов с катарактой, которым на базе СПб филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России» была выполнена факоэмульсификация катаракты (ФЭК) с имплантацией мИОЛ. Все пациенты были информированы о ходе и целях исследования, подписали добровольное информированное согласие на хирургическое вмешательство. Исследование было одобрено локальным этическим комитетом ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» Минздрава России (протокол № 9 от 12.10.2022).
На предоперационном этапе были выполнены стандартное офтальмологическое обследование, оптическая биометрия (OA-2000 Tomey corp., ver. 3B), кератотомография (Pentacam HR, Oculus ver 1.21r65), а также расчет мИОЛ по данным OA-2000 и индивидуальным поправкам хирурга.
Всем пациентам ФЭК была выполнена одним хирургом с использованием фемтосекундного лазера (LenSx, Alcon inc.) и имплантации в капсульный мешок трифокальной ИОЛ Acrysof IQ PanOptix. Фемтолазерное сопровождение включало капсулорексис диаметром 5,5 мм и факофрагментацию.
Главным критерием включения в исследование явилось достижение целевой эмметропической рефракции, которая не требовала сферической коррекции на дальнем, среднем и близком расстояниях через 3 и 6 мес. после операции.
К критериям исключения из исследования были отнесены операционные осложнения, офтальмологические вмешательства в анамнезе, миопия и гиперметропия высокой степени, общий роговичный астигматизм более 0,75 дптр и другие патологии органа зрения.
Через 6 мес. для пациентов, которые соответствовали критериям включения и исключения, проводили ретроспективный расчет сферического эквивалента мИОЛ по 10 формулам (SRK/T, Holladay 1, Holladay 2, Haigis, Hoffer Q, Barrett 2 Universal, Olsen, Kane, EVO ver. 2.0, Hill RBF ver. 3.0). Биометрические данные (переднезадняя ось (ПЗО), глубина передней камеры, толщина хрусталика, расстояние «от белого до белого») использовали с OA-2000, кератометрические — с Pentacam-HR. Данные кератометрии применяли с зон от 0,5 до 5 мм (исследование зон до 5,0 мм связано со средними диаметрами зрачка и капсулорексиса) и шагом 0,5 мм по карте Total Cornea Refractive Power с центрацией по апексу и зрачку. Таким образом, при расчете ИОЛ для каждого пациента было использовано 2 показателя кератометрии по 10 зонам и 10 формулам, что в итоге составило 200 вариантов расчета для каждого пациента.
Для каждой комбинации формула/зона были рассчитаны: средняя ошибка послеоперационной прогнозируемой рефракции (mean error, ME), отличие ME от нуля (в связи с ненормальностью распределения — критерий Уилкоксона, различия статистически значимы при p<0,05) и значение медианы с учетом знака. Следующим этапом выполняли оптимизацию констант линзы путем вычисления средней арифметической ошибки с учетом знака и корректировки данных на величину, равную данной ошибке, в каждой группе. После оптимизации констант рассчитывали среднюю (mean absolute error, MAE) и срединную (median absolute error, MedAE) абсолютные ошибки расчета SE мИОЛ, а также стандартное отклонение (standard deviation, SD). Статистический анализ полученных данных выполняли при помощи программ Statistica 10 и Microsoft Office Excel.
Результаты исследования
В исследование включили 98 пациентов (98 глаз), которые соответствовали критериям включения: 37 мужчин и 61 женщина, средний возраст 67,2±8,1 года. Предоперационные биометрические и кератометрические данные представлены в таблице.
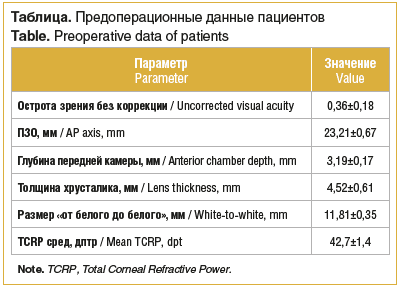
Сферический эквивалент имплантированной мИОЛ в среднем составил 23,37±4,15 дптр.
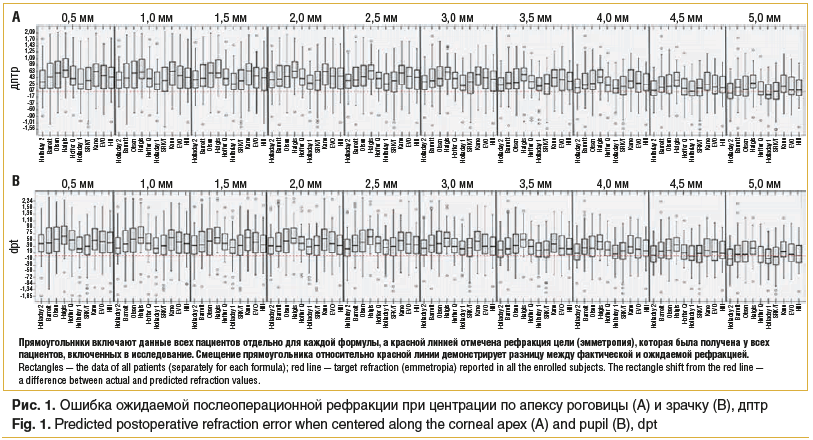
На рисунке 1 диаграмма отражает ошибку ожидаемой рефракции для каждой формулы по 10 зонам при центрации по апексу и зрачку. До зоны 3,5 мм все формулы дают ошибку в сторону гиперметропии (прямоугольник смещен выше красной линии), а с зоны 4,0 мм ошибка прогнозируемой рефракции начинает смещаться в сторону эмметропии с лучшими показателями в зоне 5,0 мм.
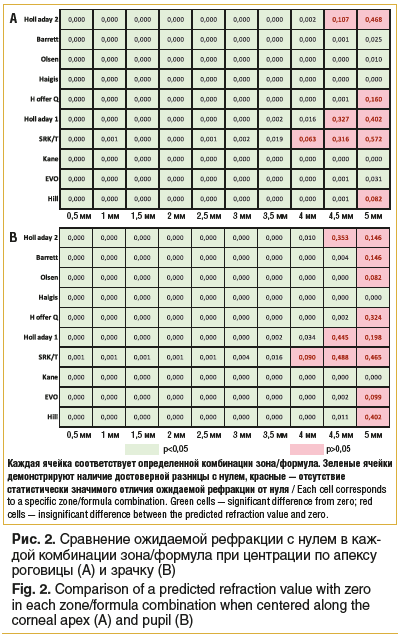
Значения критерия Уилкоксона (рис. 2) более 0,05, т. е. отсутствие статистически значимых различий (что говорит об отсутствии разницы между ожидаемой и фактической рефракцией), определены для большинства формул в зоне 5,0 мм при центрации по зрачку, кроме формул Haigis и Kane.
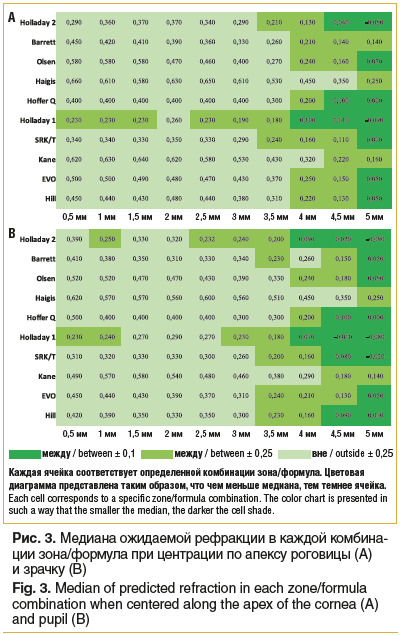
Значения медианы ожидаемой рефракции (рис. 3) не отличались в зависимости от центрации. Показатели в пределах ±0,1 большинство формул демонстрирует в периферических зонах, формулы Holladay 1, Holladay 2, Hoffer Q, SRK/T — в зонах 4,5–5,0 мм, формулы Barret, Olsen, EVO, Hill — в зоне 5,0 мм. Минимальные значения для формул Haigis и Kane оказались в пределах ±0,25 в зоне 5,0 мм.
Следующие статистические показатели (MAE, MedAE, SD) были рассчитаны после оптимизации констант.
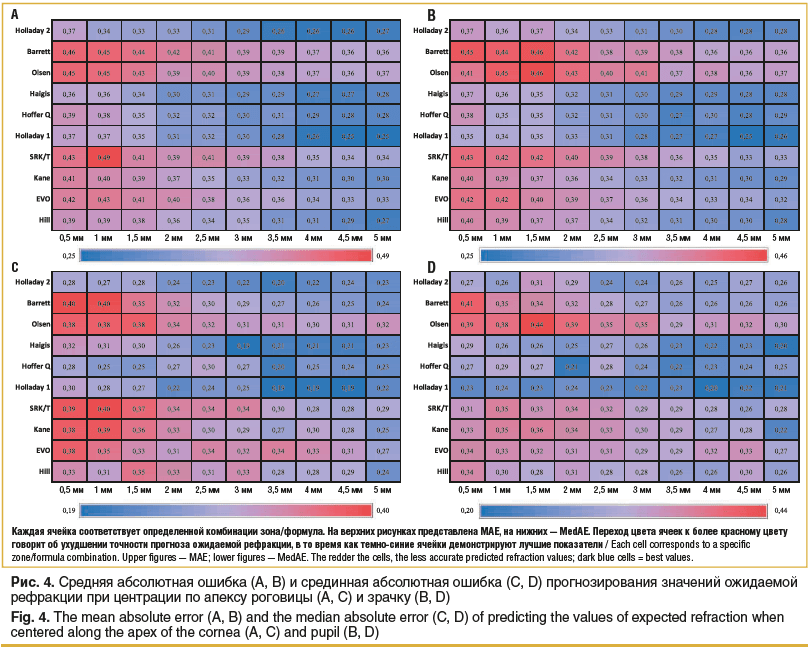
Для оценки точности прогноза ожидаемой рефракции были рассчитаны MAE и MedAE для каждой комбинации зона/формула с центрацией по зрачку и апексу. Распределение значений продемонстрировано на рисунке 4 в виде цветовой диаграммы, где низкие показатели обозначены синим цветом. На всех рисунках общей тенденцией является уменьшение значений MAE и MedAE ближе к периферии роговицы. Максимальные показатели MAE демонстрируют формулы Barrett, Olsen, SRK/T, EVO. Эти же формулы, а также формула Kane показали высокие значения MedAE. Низкие показатели MAE определены для формул Holladay 2, Haigis, Hoffer Q, Holladay 1 (с минимальными значениями в зонах 4,0–5,0 мм).
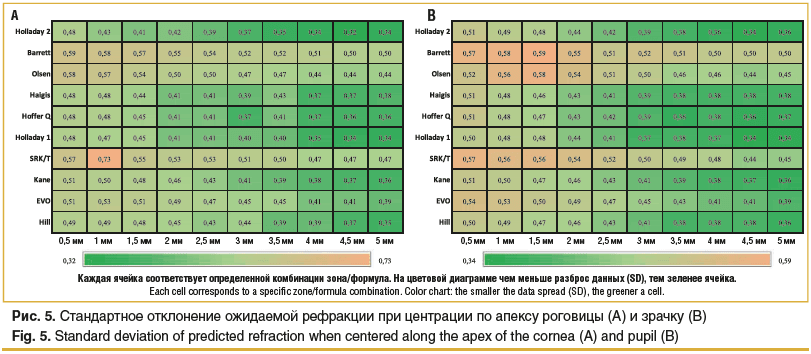
Стандартное отклонение — это показатель, который демонстрирует разброс данных, т. е. как распределены значения относительно среднего уровня в выборке. Все формулы имеют тенденцию к уменьшению дисперсии с увеличением размера зоны, с наилучшими показателями в зонах 4,0–5,0 мм для формул Holladay 2, Haigis, Hoffer Q и Holladay 1 (рис. 5). Формулы Kane, EVO и Hill также продемонстрировали низкие значения в зонах 4,0–5,0 мм, однако в других зонах определены высокие значения SD (более 0,45). Наибольшая дисперсия определена в формулах Barrett, Olsen и SKR/T при любом наборе данных, что подразумевает высокую нестабильность в этих вычислениях.
Обсуждение
Вращающаяся Scheimpflug-камера сканирует более 130 000 точек как с передней, так и с задней поверхности роговицы, формируя ее трехмерное изображение [16–18]. Полученные данные анализируются с помощью встроенного программного обеспечения, что на выходе дает большое количество информации с переднего сегмента глаза: толщина роговицы, показатели глубины передней камеры, толщины хрусталика, диаметр зрачка, а также около 40 значений различных вариантов кератометрии [16–18], что, с одной стороны, является преимуществом данной технологии, но с другой — ставит перед врачом проблему выбора оптимальных параметров.
Настоящее исследование посвящено изучению TCRP с помощью Scheimpflug-камеры. Это значение рассчитывается с применением метода трассировки лучей, а не формулы Gaussian [19, 20], которая зависит от законов параксиальной оптики. Для определения TCRP используются закон Снеллиуса, показатели преломления воздуха, роговицы и водянистой влаги, а также радиус кривизны двух поверхностей роговицы [10, 15, 20–22]. Полученные данные отображаются на дисплее для измерительных диаметров от 1,0 до 8,0 мм по кольцу или зоне с центрацией по зрачку и апексу роговицы [20].
При сравнении значений TCRP с показателями стандартной кератометрии (SimK) ряд исследований показал достоверную разницу между SimK и TCRP, а именно меньшие значения TCRP [11, 15, 20–22]. Полученные результаты могут быть объяснены разными значениями отношения радиуса кривизны передней поверхности к задней [15]. При SimK это соотношение зависит от радиуса кривизны только передней поверхности, так как задняя не измеряется, а моделируется при помощи стандартного кератометрического индекса, в то время как при TCRP реальное измерение радиуса кривизны задней поверхности приводит к увеличению ее «отрицательного» вклада и, соответственно, к уменьшению значения общей оптической силы роговицы.
В настоящем исследовании был осуществлен системный подход к расчету оптической силы мИОЛ при хирургии катаракты, где в каждом конкретном случае выполняли расчет сферического эквивалента линзы с использованием одинаковых биометрических параметров, кроме значения кератометрии, которое вводили в формулы по зонам TCRP с Pentacam-HR с использованием метода картирования. Дальнейший статистический анализ позволил определить общую тенденцию для всех формул — чем ближе зона к периферии роговицы, тем меньше значения MAE, MedAE, SD и меньше сдвиг ожидаемой послеоперационной рефракции от нуля независимо от центрации.
Если проанализировать формулы в частности, то в первую очередь можно выделить формулу Holladay 1, которая показала лучшие результаты во всех зонах, особенно в 4,0–5,0 мм. Формулы Holladay 2, Haigis, Hoffer Q продемонстрировали меньшие по сравнению с другими значения MAE, MedAE и SD с минимальными показателями в зонах 3,0–5,0 мм. Следующей по точности идет группа современных формул Kane, EVO и Hill в зонах 4,0–5,0 мм. Остальные формулы (Barrett, Olsen и SKR/T) продемонстрировали высокие значения показателей, характеризующих их точность, во всех зонах, однако также с тенденцией уменьшения их значений к 5-миллиметровой зоне.
Радиус кривизны задней поверхности роговицы не является постоянным значением, следовательно, его игнорирование и стандартизация могут привести к ошибкам измерения и влиять на точность попадания в рефракцию цели. Возможность анализа информации с задней поверхности роговицы долгое время была недоступной, и появившиеся за последние десятилетия новые диагностические технологии, обладающие данной функцией, вывели предоперационную диагностику на новый уровень. Несмотря на это, существующие исследования по сравнению SimK и TCRP в точности расчета оптической силы ИОЛ показывают противоречивые результаты. В некоторых работах [10, 12] было показано, что учет задней поверхности роговицы, в том числе с использованием Scheimpflug-камеры, не дает более точные послеоперационные результаты по сравнению со стандартной кератометрией, а G. Savini et al. [20] продемонстрировали, что при определенном наборе данных использование TCRP может быть более точным, в то время как авторы других исследований считают нецелесообразным использование значений TCRP в расчете ИОЛ в связи с высокими показателями MAE и MedAE [15].
В настоящем исследовании не сравнивались значения SimK и TCRP, а была предпринята попытка определения оптимальных зон TCRP, использование которых при расчете оптической силы мИОЛ может привести к более точному попаданию в рефракцию цели. Привязка к 10 зонам роговицы и использование 10 формул разных поколений с анализом большого количества значений на 1 пациента определяют особенность данной работы. В немногочисленных работах по изучению данного вопроса имеются как совпадения, так и различия результатов по сравнению с настоящим исследованием.
G. Savini et al. [20] сравнили значения различных видов кератометрии, в том числе TCRP, и использовали их для расчета ИОЛ. Показатели TCRP применялись в зонах 2,0 и 3,0 мм в формулах Hoffer Q, Holladay 1 и SKR/T. Как наиболее точную авторы определили формулу SKR/T, которая продемонстрировала меньшие значения MAE (0,34 и 0,35 для зон 2,0 и 3,0 мм соответственно) и MedAE (0,22 и 0,19 для зон 2,0 и 3,0 мм соответственно) и большее количество пациентов с ожидаемой рефракцией в диапазоне ±0,25 дптр. В настоящем исследовании формула SKR/T показала сопоставимые данные MAE в указанных зонах, но более высокие значения MedAE (0,34 для обеих зон). Для формул Hoffer Q и Holladay 1 результаты сопоставимы.
В другом исследовании показатели TCRP (нет привязки к зоне), а также SimK использовались в формулах Haigis, Hoffer Q, Holladay 1 и SKR/T. Для сравнения формул была вычислена MedAE, которая составила 0,34, 0,31, 0,29, 0,3 для указанных формул соответственно. Полученные результаты схожи с данными настоящего исследования, если для формул Haigis, Hoffer Q, Holladay 1 их сравнивать с центральными зонами, а для SKR/T — с периферическими [15].
E. Saad et al. [21] сравнили точность различных вариантов кератометрии, используя 3 формулы в зависимости от ПЗО глаза: Hoffer Q (ПЗО менее 22 мм), Holladay 1 (ПЗО от 22 до 26 мм) и SKR/T (от 26 мм). Значения TCRP использовались в зонах 2,0, 3,0, 4,0 и 5,0 мм. Минимальные MAE и MedAE, а также большее количество пациентов с ожидаемой рефракцией в диапазоне ±0,5 дптр были выявлены при применении TCRP в зоне 4,0 мм, что коррелирует с результатами настоящего исследования. Худшие показатели были определены в зоне 5,0 мм, в то время как по нашим данным в этой зоне все формулы продемонстрировали лучшие результаты.
В указанных работах имплантированная ИОЛ была монофокальной, использовали всего 3–4 формулы, а значения TCRP применяли в небольшом измерительном диапазоне, что может объяснять различие некоторых результатов по сравнению с настоящей работой.
Ограничениями данного исследования являются небольшая выборка пациентов, оценка результатов только по одной модели ИОЛ, ограничение зоны кератометрии до 5 мм.
Заключение
Наиболее точный предоперационный расчет сферического эквивалента мИОЛ с применением значений TCRP возможен при использовании формулы Holladay 1 в зонах 4,0–5,0 мм. Формулы Holladay 2, Haigis, Hoffer Q более эффективны в зонах 3,0–5,0 мм. Для формул Kane, EVO и Hill оптимальные значения TCRP находятся в зонах 4,0–5,0 мм. Формулы Barrett, Olsen и SKR/T нецелесообразно использовать с данными TCRP в связи с высокими значениями MAE, MedAE и SD.
Сведения об авторах:
Петросян Юрий Микаелович — врач-офтальмолог СПб филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России»; 192283, Россия, г. Санкт-Петербург, ул. Ярослава Гашека, д. 21а; аспирант кафедры офтальмологии ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; ORCID iD 0000-0003-4081-0078
Бойко Эрнест Витальевич — д.м.н., профессор, заслуженный врач РФ, директор СПб филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России»; 192283, Россия, г. Санкт-Петербург, ул. Ярослава Гашека, д. 21а; заведующий кафедрой офтальмологии ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; профессор кафедры оториноларингологии и офтальмологии
СПбГУ; 199034, Россия, г. Санкт-Петербург, Университетская наб., д. 7–9; ORCID iD 0000-0002-7413-7478
Шухаев Сергей Викторович — к.м.н., врач-офтальмолог СПб филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России»; 192283, Россия, г. Санкт-Петербург, ул. Ярослава Гашека, д. 21а; ORCID iD 0000-0001-7047-615X
Литвин Ирина Богдановна — к.м.н., доцент, заведующая научно-образовательным отделом СПб филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России»; 192283, Россия, г. Санкт-Петербург, ул. Ярослава Гашека, д. 21а; доцент кафедры офтальмологии ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России; 191015, Россия, г. Санкт-Петербург, ул. Кирочная, д. 41; ORCID iD 0000-0002-1549-3341
Контактная информация: Петросян Юрий Микаелович, e-mail: petrosyan.yurij@yandex.ru
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 18.03.2024.
Поступила после рецензирования 10.04.2024.
Принята в печать 06.05.2024.
About the authors:
Yurii M. Petrosyan — Ophthalmologist, St. Petersburg Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 21a, Yaroslav Gashek str., St. Petersburg, 192283, Russian Federation; postgraduate student of the Department of Ophthalmology, North West State Medical University named after I.I. Mechnikov; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; ORCID iD 0000-0003-4081-0078
Ernest V. Boiko — Dr. Sc. (Med.) Professor, Honored Physician of the Russian Federation, Director, St. Petersburg Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 21a, Yaroslav Gashek str., St. Petersburg, 192283, Russian Federation; Head of the Department of Ophthalmology, North West State Medical University named after I.I. Mechnikov; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; Professor of the Department of Otorhinolaryngology and Ophthalmology, St. Petersburg State University; 7–9, Universitetskaya emb., St. Petersburg, 199034, Russian Federation; ORCID iD 0000-0002-7413-7478
Sergei V. Shukhaev — C. Sc. (Med.), Ophthalmologist, St. Petersburg Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 21a, Yaroslav Gashek str., St. Petersburg, 192283, Russian Federation; ORCID iD 0000-0001-7047-615X
Irina B. Litvin — C. Sc. (Med.), Assistant Professor, Head of the Scientific and Educational Department, St. Petersburg Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 21a, Yaroslav Gashek str., St. Petersburg, 192283, Russian Federation; Assistant Professor of the Department of Ophthalmology, North West State Medical University named after I.I. Mechnikov; 41, Kirochnaya str., St. Petersburg, 191015, Russian Federation; ORCID iD 0000-0002-1549-3341
Contact information: Yurii M. Petrosyan, e-mail: petrosyan.yurij@yandex.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 18.03.2024.
Revised 10.04.2024.
Accepted 06.05.2024.
материал rmj.ru
