Введение
Несмотря на значительные достижения в области создания новых моделей интраокулярных линз (ИОЛ) и разработки формул последнего поколения для расчета их оптической силы, коррекция остаточных аметропий после факоэмульсификации катаракты или ленсэктомии и имплантации ИОЛ остается значимой проблемой в офтальмохирургии [1–3]. Частота остаточных аметропий невелика, однако их наличие осложняет зрительную и социальную адаптацию пациентов [4]. Из наиболее значимых параметров остаточных аметропий выделяют ошибку прогнозирования (prognostic error) и среднюю абсолютную погрешность (mean absolute error), при этом показано, что вид используемых формул для расчета оптической силы ИОЛ, характеристики имплантируемой линзы, возраст, пол пациентов и латеральность в одинаковой степени влияют на вероятность ошибки в послеоперационном периоде [5]. Вместе с тем в литературе доступно ограниченное количество работ, в которых проводят сравнительный анализ нескольких методов коррекции остаточных аметропий на псевдофакичных глазах.
Цель исследования — выполнить сравнительный анализ эффективности проведения лазерного кератомилеза in situ и имплантации добавочных ИОЛ для коррекции остаточных аметропий на артифакичных глазах.
Материал и методы
В исследование включены 74 пациента (98 глаз) с факоэмульсификацией катаракты (n=53) или удалением прозрачного хрусталика с рефракционной целью (n=45) и имплантацией ИОЛ в 2012–2017 гг. Критерием включения пациентов в исследование явилось наличие остаточных рефракционных погрешностей после имплантации ИОЛ в сроки 6 мес. и более, что привело к необходимости дополнительных хирургических вмешательств. Женщины составили 47,3% (n=35), мужчины — 52,7% (n=39). Возрастной диапазон варьировал от 19 до 86 (51,7±11,2) лет.
Всем пациентам проводили как стандартное (авторефрактометрия, тонометрия, визометрия, компьютерная периметрия, биомикроскопия, офтальмоскопия в условиях максимального мидриаза), так и специальное (кератотопография, эхография, ультразвуковая пахиметрия, оптическая когерентная биометрия с определением аксиальной длины глаза, глубины передней камеры и кривизны роговицы, по показаниям — оптическая когерентная томография) офтальмологическое обследование.
Вид используемой докоррекции определил выделение групп пациентов. Группу I составили 50 пациентов, которым проводили LASIK (72 глаза) по стандартной методике. В 6 (8,3%) случаях использовали сопровождение на фемтосекундном лазере FS200 WaveLight (Alcon, США). Средняя оптическая сила имплантированных до начала исследования ИОЛ составила 21,7±3,4 (от 13 до 30) дптр. Целевая рефракция варьировала в диапазоне от -0,25 до 0,25 дптр у большинства пациентов (97,5%), в 2 случаях она составила -1,5 и -2,5 дптр. Средний период наблюдения составил 7,1±1,2 (от 6 до 12) мес.
В группу II вошли 24 пациента (26 глаз), которым проводили имплантацию добавочных ИОЛ Rayner Sulcoflex (n=19; 73,1%) и Add-onTorica-sPB A4FW (n=7; 26,9%) согласно методикам, описанным нами ранее [6, 7]. Целевая рефракция также варьировала в диапазоне от -0,25 до 0,25 дптр. Средний период наблюдения составил 6,6±1,0 (от 6 до 10) мес.
Из сопутствующей офтальмологической патологии в группе I в предоперационном периоде отмечали: сочетание «сухой» формы возрастной макулярной дегенерации (ВМД), миопии высокой степени и стафиломы (n=2; 2,8%), ВМД (n=12; 16,7%), глаукому I стадии (n=1; 1,4%), амблиопию различного генеза (n=21; 29,2%) и дистрофию Фукса (n=2; 2,8%). В группе II определяли ВМД (n=3; 11,5%), глаукому I стадии (n=2; 7,7%), стационарный кератоконус (n=3; 11,5%), амблиопию (n=2; 7,7%) и состояние после
LASIK при миопии высокой степени (n=2; 7,7%).
У всех пациентов монолатерально исследовали основные биометрические и рефракционные функциональные параметры в послеоперационном периоде. Помимо этого, определяли индексы безопасности и эффективности. Индекс эффективности соответствовал соотношению средней некорригированной (НКОЗд) и максимально корригированной (МКОЗд) остроты зрения вдаль в послеоперационном периоде, а индекс безопасности — средней МКОЗд в после- и дооперационном периоде.
Основные характеристики пациентов приведены в таблице 1.
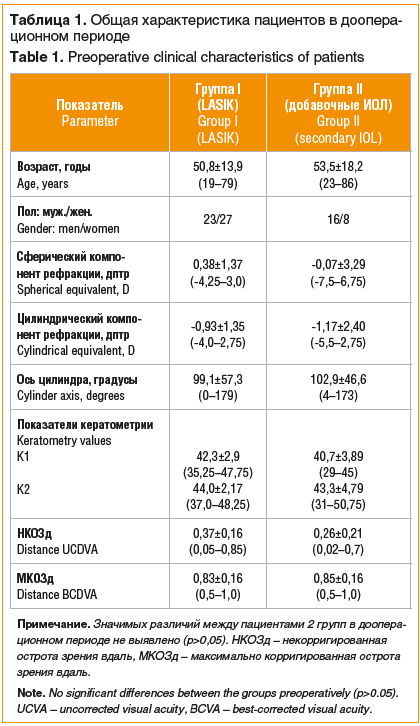
Статистическую обработку результатов исследования проводили с применением компьютерных программ Microsoft Excel 2010 (Miscrosoft corp., США) и Statistica 10.1 (StatSoft, США). Рассчитывали среднее арифметическое значение (M), стандартное отклонение от него (SD), минимальные и максимальные значения. При оценке достоверности результатов применяли t-критерий Стьюдента. Для сравнения частоты встречаемости признака применяли точный критерий Фишера. Доверительный интервал составил 95%.
Результаты и обсуждение
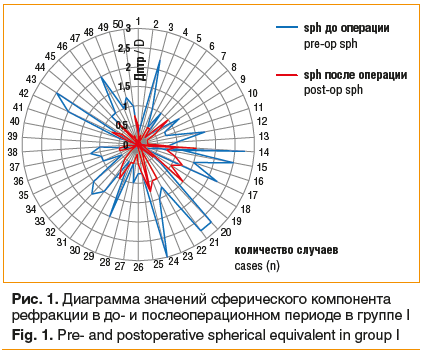
В группе I значимых изменений сферического компонента рефракции в послеоперационном периоде не выявлено (0,38±1,37 дптр и 0,33±0,55 дптр соответственно), при этом максимальное значение составило ±1,5 дптр (рис. 1).
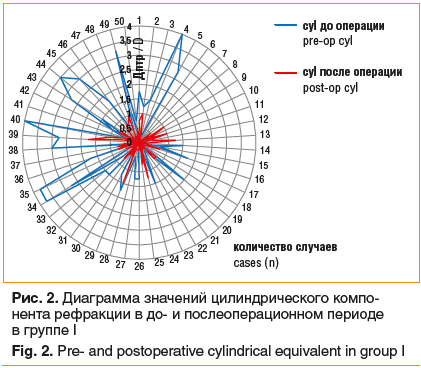
Отмечено статистически значимое (p<0,05) снижение цилиндрического компонента рефракции с -0,93±1,35 до -0,12±0,73 (рис. 2), в 3 случаях значения показателя превысили ±1,5 дптр. В максимальном периоде наблюдения отмечено статистически значимое (p<0,05) увеличение НКОЗд с 0,37±0,16 до 0,76±0,19, МКОЗд оставалась на дооперационном уровне. При анализе данных кератометрии в послеоперационном периоде (К1=42,2±2,14 и К2=43,5±6,12) значимых различий по сравнению с дооперационными показателями не выявлено (p>0,05).
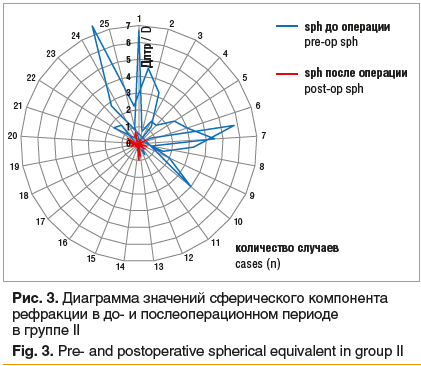
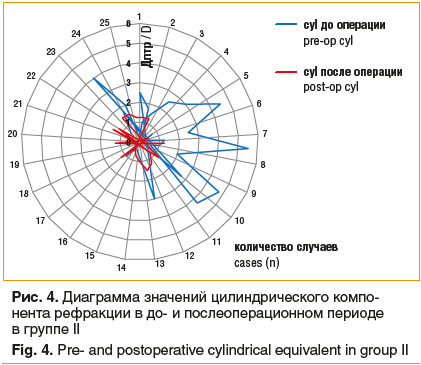
В группе II в послеоперационном периоде показано статистически значимое (p<0,05) увеличение НКОЗд с 0,26±0,21 дптр до 0,84±0,16 дптр, а также незначимое (p>0,05) увеличение МКОЗд с 0,85±0,16 дптр до 0,89±0,15 дптр. Отмечено уменьшение сферического компонента рефракции с -0,07±3,3 до 0,02±0,48 дптр, цилиндрического компонента рефракции — с -1,17±2,4 до -0,55±,91 дптр, однако различия в до- и послеоперационном периоде не были статистически значимыми (p>0,05). Для сферического компонента рефракции максимальное значение составило -1 дптр, для цилиндрического — -1,5 дптр (рис. 3, 4). Отсутствие значимых различий выявлено и при сравнении показателей кератометрии в группах I и II (40,7±3,89 и 40,6±4,05 для К1 и 43,3±4,79 и 43,1±4,96 для К2 соответственно). В 4 случаях отмечена ротация имплантированной добавочной ИОЛ, что потребовало дополнительного хирургического вмешательства.
При анализе индекса безопасности его значение в группе I составило 1,03, а в группе II — 1,06, при этом различия не были статистически значимыми (p>0,05). Аналогичные различия получены и для индекса эффективности (0,92 в группе I и 0,99 в группе II соответственно; p>0,05), что может быть связано с бóльшим разбросом дооперационных значений НКОЗд и МКОЗд в группе II.
Дополнительно пациентов обеих групп разделили в зависимости от типа аметропии на подгруппы: А — пациенты с гиперметропией и гиперметропией в сочетании с астигматизмом, В — с миопией и миопией в сочетании с астигматизмом.
В группе IА (49 глаз) отмечено увеличение НКОЗд с 0,38±0,16 дптр до 0,75±0,18 дптр (p<0,05), изменения МКОЗд не достигли уровня статистической значимости. Показано статистически значимое снижение сферического компонента рефракции с 1,22±0,41 дптр до 0,45±0,08 дптр (p<0,05), цилиндрического компонента рефракции — с -0,98±0,2 дптр до -0,09±0,17 дптр (p<0,05). Показатели кератометрии К1 и К2 изменялись незначимо (41,4±2,18 против 41,8±2,25 и 43,4±2,08 против 43,3±1,9 соответственно; p>0,05).
Для пациентов группы IВ показан рост НКОЗд с 0,30±0,15 дптр до 0,78±0,21 дптр (p<0,05), МКОЗд — с 0,84±0,11 дптр до 0,87±0,12 дптр (p>0,05). Отмечено значимое изменение сферического компонента рефракции с -0,96±0,7 дптр до 0,05±0,65 дптр, т. е. целевой эмметропии (p<0,05), и статистически незначимое — цилиндрического компонента рефракции с -0,8±0,53 дптрдо -0,39±0,42 дптр (p>0,05). В послеоперационном периоде показано статистически незначимое снижение показателей кератометрии К1 и К2 — с 44,2±1,6 до 43,2±1,7 и с 45,3±1,4 до 44,2±1,5 соответственно (p<0,05).
В группе IIА (13 глаз) отмечен рост НКОЗд с 0,34±0,22 дптр в дооперационном периоде до 0,87±0,13 дптр в послеоперационном (p<0,05), значения МКОЗд оставались аналогичными таковым до операции. Отмечено статистически значимое (p<0,05) снижение сферического компонента рефракции с 2,42±1,74 дптр до -0,14±0,5 дптр, а также изменение цилиндрического компонента рефракции с -0,17±2,42 дптр до -0,15±0,91 дптр (p>0,05).
Группа IIВ (12 глаз) при исходно более низких показателях НКОЗд (0,16±0,15 дптр) характеризовалась значимым ростом показателя до 0,80±0,18 дптр (p<0,05), а также статистически незначимым увеличением МКОЗд с 0,81±0,15 дптр до 0,91±0,13 дптр в послеоперационном периоде (p>0,05). Отмечено снижение сферического компонента рефракции с -2,95±2,27 дптр до 0,16±0,42 дптр (p<0,05) и цилиндрического компонента рефракции с -2,61±1,55 дптр до -0,59±0,96 дптр в максимальном периоде наблюдения (p<0,05).
При проведении сравнительного анализа между группами IА и IIА, IВ и IIВ отмечено преимущество метода имплантации добавочных ИОЛ для коррекции остаточной гиперметропии средней и высокой степени, а также миопии высокой степени. У пациентов с остаточной миопией слабой и средней степени, а также гиперметропией слабой степени возможна эффективная коррекция с применением LASIK.
Выбор метода докоррекции остаточных аметропий после имплантации ИОЛ остается актуальной проблемой офтальмологии. Широкое внедрение в клиническую практику новых технологий коррекции, разработка новых режимов рефракционной хирургии и типов добавочных ИОЛ позволяют проводить коррекцию в зависимости от конкретных анатомических и функциональных характеристик пациента.
Нам не удалось найти в литературе аналогичных исследований, посвященных сравнительному анализу результатов проведения LASIK и имплантации добавочных ИОЛ у сопоставимых групп пациентов. Проведено большое количество исследований, посвященных основным методам коррекции аметропий на псевдофакичных глазах, включая рефракционные вмешательства, замену ИОЛ и имплантацию добавочной ИОЛ [8–12]. Вместе с тем в большинстве работ представлен анализ собственных данных об эффективности применения одного из указанных методов докоррекции. В единичных работах приведены данные о результатах сравнительного анализа двух и более способов коррекции остаточных аметропий. Так, в работе Н.Е. El Awady et al. представлен анализ результатов докоррекции у 23 пациентов методами имплантации добавочных сулькусных ИОЛ и замены ИОЛ. Согласно мнению авторов имплантация добавочной ИОЛ является безопасной, эффективной и технически несложной альтернативой замены ИОЛ у пациентов с остаточной миопией или гиперметропией после имплантации первой ИОЛ [13].
В России сравнительный анализ впервые проведен в работе М.М. Бикбова и соавт. (2012). Авторы изучали изменения аберраций оптической системы артифакичного глаза после имплантации добавочной ИОЛ Sulcoflex и LASIK, при этом в обеих группах отмечено уменьшение аберраций низшего порядка без увеличения суммарных аберраций высшего порядка [14]. Схожие данные представлены в работе Ю.В. Тахтаева и Е.Г. Богачука. Авторы проводили оценку индуцированных аметропий и контрастной чувствительности после выполнения LASIK, имплантации добавочных ИОЛ и замены ИОЛ на артифакичных глазах. Наименьшие значения контрастной чувствительности получены в группе с имплантацией добавочных ИОЛ [15]. В нашей работе оценку данных показателей не проводили.
В работе M.I. Khan и М. Muhtaseb представлены данные об имплантации добавочной ИОЛ Sulcoflex 4 пациентам, при этом у одного из них в анамнезе отмечены двухсторонний LASIK и рефракционная ленсэктомия с имплантацией аккомодирующей ИОЛ, а у троих — экстракция катаракты с имплантацией монофокальной ИОЛ. Во всех описанных случаях отмечена положительная рефракционная динамика [16].
Заключение
Проведенный сравнительный анализ подтвердил эффективность выполнения LASIK и имплантации добавочных ИОЛ как эффективных методов коррекции остаточной аметропии на псевдофакичных глазах. Во всех группах отмечено значимое увеличение НКОЗд. Выполнение LASIK ассоциировано со значимым снижением цилиндрического компонента рефракции. Индексы эффективности и безопасности были сопоставимы в обеих группах. Для коррекции остаточной высокой миопии и гиперметропии показана имплантация добавочных ИОЛ, а для коррекции миопии слабой и средней степени, а также гиперметропии слабой степени — LASIK. Полученные данные позволяют рекомендовать применение обоих методов докоррекции на артифакичных глазах в клинической практике.
Сведения об авторах:
1Гурмизов Евгений Петрович — к.м.н., главный врач, ORCID iD 0000-0002-3438-3404;
2Першин Кирилл Борисович — д.м.н., профессор, медицинский директор, ORCID iD 0000-0003-3445-8899;
2Пашинова Надежда Федоровна — д.м.н., главный врач, ORCID iD 0000-0001-5973-0102;
2Цыганков Александр Юрьевич — к.м.н., научный референт медицинского директора, ORCID iD 0000-0001-9475-3545.
1 ООО «ДЦ «Зрение». 191023, Россия, г. Санкт-Петербург, Апраксин пер., д. 6.
2ООО «СовМедТех». 109147, Россия, г. Москва, ул. Марксистская, д. 3, стр. 1.
Контактная информация: Цыганков Александр Юрьевич, e-mail: alextsygankov1986@yandex.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 05.11.2019.
About the authors:
1Evgeniy P. Gurmizov — MD, PhD, Head Doctor, ORCID iD 0000-0002-3438-3404;
2Kirill B. Pershin — MD, PhD, Professor, Medical Director, ORCID iD 0000-0003-3445-8899;
2Nadezhda F. Pashinova — MD, PhD, Head Doctor, ORCID iD 0000-0001-5973-0102;
2Aleksandr Yu. Tsygankov — MD, PhD, Scientific Advisor of Medical Director, ORCID iD 0000-0001-9475-3545.
1LLC “Diagnostic Center “Vision”. 6, Apraksin lane, St. Petersburg, 191023, Russian Federation.
2LLC “SovMedTech”. 3/1, Marksistskaya str., Moscow, 109147, Russian Federation.
Contact information: Aleksandr Yu. Tsygankov, e-mail: alextsygankov1986@yandex.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 05.11.2019.
.
материал rmj.ru
