Материал и методы: обследовано в СПб НИИ ЛОР 233 ребенка в возрасте от 3 до 16 лет с острым лимфопролиферативным синдромом, 157 детей в возрасте от 3 до 16 лет с хроническим лимфопролиферативным синдромом, 100 детей в возрасте от 1 до 7 лет с высокой степенью тугоухости. Помимо общего осмотра осуществлялось гематологическое обследование, включая верификацию диагноза герпесвирусной инфекции.
Результаты исследования: установлено, что острая форма лимфопролиферативного синдрома в 33,5% случаев была вызвана бета-гемолитическим стрептококком.
У 30,9% обследованных детей выявлены в сыворотке крови гетерофильные антитела, ассоциированные с инфекционным мононуклеозом. У 16% детей диагностирован острый лимфопролиферативный синдром смешанной этиологии: инфекционный мононуклеоз и стрептококковая инфекция. Хронический лимфопролиферативный синдром выявлен у 157 детей из числа обратившихся для решения вопроса о необходимости проведения хирургического лечения. Установлено, что в большинстве случаев (более 74%) этиологическим фактором развития лимфоидной пролиферации является вирус Эпштейна — Барр (ВЭБ). Цитомегаловирусная инфекция в большинстве случаев обнаруживалась в сочетании с другими патогенами — в 34,39% случаев с ВЭБ, в 14,65% — с ВЭБ и бета-гемолитическим стрептококком.
Заключение: для верификации диагноза целесообразным в настоящее время является внедрение современных методов лабораторной диагностики в практику, что позволит повысить уровень оказания помощи пациенту в связи с постановкой этиологического диагноза. Уточнение этиологии лимфаденопатии инфекционного генеза — необходимое
условие проведения адекватной этиотропной терапии. Появление сведений о новых этиологических агентах лимфопролиферативного синдрома у детей и современных лабораторно-диагностических технологиях вселяет определенные надежды на разработку действенных мероприятий по профилактике и лечению данных заболеваний и уменьшению бремени экономической нагрузки на государство.
Ключевые слова: цитомегаловирус, вирус Эпштейна — Барр, дети, лимфопролиферативный синдром, высокая степень тугоухости.
Для цитирования: М.В.Дроздова, Ю.С.Преображенская, Е.В.Тырнова, С.Н.Ларионова Особенности этиологической диагностики лимфопролиферативного синдрома у детей // РМЖ. 2018. №102. С. 63-67
M.V.Drozdova, Yu.S. Preobrazhenskaya, E.V.Tyrnova, S.N.Larionova
Saint Petersburg Research Institute of Ear, Throat, Nose and Speech
Aim: to analyse the features of etiological diagnosis of lymphoproliferative syndrome in children-candidates for surgical treatment.
Patients and Methods: 233 children aged from 3 to 16 years with acute lymphoproliferative syndrome, 157 children aged from 3 to 16 years with chronic lymphoproliferative syndrome, 100 children aged from 1 to 7 years with a high degree of hearing loss were examined in Saint Petersburg Research Institute of Ear, Throat, Nose and Speech. In addition to a general examination, hematological examination was carried out, including verification of the diagnosis of herpes infection.
Results: it was established that the acute form of lymphoproliferative syndrome in 33.5% of cases was caused by beta-hemolytic streptococcus. In 30.9% of the examined children, heterophilic antibodies associated with infectious mononucleosis were detected in the serum. In 16% of children, the acute lymphoproliferative syndrome of mixed etiology was diagnosed: infectious mononucleosis and streptococcal infection. Chronic lymphoproliferative syndrome was detected in 157 children from among those who applied to decide on the need for surgical treatment. It was established that in most cases (more than 74%) the Epstein-Barr virus (EBV) is the etiological factor in the development of lymphoid proliferation. Cytomegalovirus infection in most cases was detected in combination with other pathogens — in 34.39% of cases with EBV, and in 14.65% — with EBV and beta-hemolytic streptococcus.
Conclusion: for verification of the diagnosis, it is now advisable to introduce modern methods of laboratory diagnostics, which will increase the level of patient care in connection with the etiological diagnosis. Clarification of the etiology of lymphadenopathy of infectious origin is a necessary condition for adequate etiotropic therapy. The emergence of information about new etiological agents of lymphoproliferative syndrome in children and modern laboratory and diagnostic technologies gives some hope for the development of effective measures to prevent and treat these diseases and reduce the burden of economic load on the state.
Key words: cytomegalovirus, Epstein-Barr virus, children, lymphoproliferative syndrome, high degree of hearing loss.
For citation: Drozdova M.V., Preobrazhenskaya Yu.S., Tyrnova E.V., Larionova S.N. Features of etiological diagnosis
of lymphoproliferative syndrome in children // RMJ. 2018. № 10(II). P. 63–67.
Особенности этиологической диагностики лимфопролиферативного синдрома у детей
Содержание статьи
Введение
Вирусные заболевания человека в наше время претерпевают значительные изменения и характеризуются многообразием клинических проявлений. Среди них герпесвирусные инфекции занимают одно из ведущих мест, т. к. обладают тенденцией к затяжному, нередко тяжелому течению, что сопровождается явным снижением качества жизни и социальной дезадаптацией пациентов [1–3].
Путей передачи герпесвирусов множество [4]. После первичного инфицирования происходит переход герпесвируса в латентное состояние с возможными эпизодами реактивации [5]. По данным литературы, реактивация вирусов из латентной формы происходит на фоне стрессов, эндокринных нарушений, у больных с первичным и вторичным иммунодефицитом, а также у пациентов, проходящих иммуносупрессивную терапию.
Существуют различные клинические формы проявления герпетических инфекций. Длительная персистенция вируса в организме человека может иметь латентную форму, при которой нарушается полный репродуктивный цикл вируса и он находится в клетках хозяина в виде субвирусных структур. Герпесвирусная инфекция может реактивироваться, а при неблагоприятном исходе перейти в генерализованную форму. Все формы тесно связаны между собой и могут переходить одна в другую. В любом случае герпесвирусы, будучи инкорпорированными в хромосомы клетки, длительное время не только сохраняются, но и передаются дочерним клеткам и остаются в инфицированном организме пожизненно [6].
В настоящее время известно 8 видов герпесвирусов человека. Наибольший интерес представляют вирус Эпштейна — Барр (ВЭБ) и цитомегаловирус (ЦМВ).
ВЭБ — это ДНК-содержащий вирус, относящийся к подсемейству Gamma Herpesviridae рода Gymphocryptovirus, является вирусом герпеса человека 4-го типа. ДНК ВЭБ кодирует около 80 белков, способных поддерживать жизненный цикл вируса на всех его стадиях от литической до латентной [7]. Тропность ВЭБ к эпителиальным и лимфоидным образованиям носоглотки обусловливает возникновение острого и хронического лимфопролиферативного синдрома [8].
По современным данным, клиническая форма заболевания, обусловленного ВЭБ, отличается при первичном инфицировании и при реактивации. Первичное инфицирование характеризуется литической репликацией вирусной ДНК, вирусным воспроизводством и лизисом инфицированной клетки. При первичной инфекции наиболее распространенной формой является инфекционный мононуклеоз [9]. Данный процесс следует рассматривать не как самостоятельное заболевание, а как синдром, поскольку подобная клиника характерна для ВЭБ, ЦМВ, вируса герпеса 6-го типа и др.
ЦМВ-инфекция — вирусное заболевание преимущественно детей раннего возраста, характеризующееся многообразием клинической симптоматики и специфической морфологической картиной с присутствием цитомегалических клеток на фоне лимфогистиоцитарных инфильтратов. Возбудитель принадлежит к семейству Herpesviridae (вирус герпеса человека 5-го типа), подсемейству бета, роду Cytomegalovirus. ЦМВ — условно-патогенный возбудитель, как и другие вирусы этого семейства, он способен вызывать персистентную и латентную инфекцию и реактивироваться в условиях ослабления иммунитета организма, вызывая резкое угнетение клеточного иммунитета. ЦМВ распространен повсеместно и может персистировать в организме человека пожизненно [9, 10].
ЦМВ-инфекция представляет собой классическую оппортунистическую инфекцию, проявления которой зависят от характера и степени дефектов иммунитета. Проникнув в кровь, ЦМВ репродуцируется в лейкоцитах и в клетках моноцитарно-макрофагальной системы или персистирует в лимфоидных органах [11]. На фоне снижения реактивности организма цитопролиферативная активность ЦМВ может вызвать местную гиперплазию лимфоидной ткани, что приводит к поражению глоточной и небных миндалин.
Детям с хроническим лимфопролиферативным синдромом при решении вопроса о проведении хирургического лечения в области лимфоэпителиального глоточного кольца (аденотомия, тонзиллотомия, тонзиллэктомия) целесообразно провести комплексное клинико-лабораторное обследование [12]. Выделение этих возбудителей с помощью традиционного бактериологического исследования невозможно [13]. Необходимо проведение развернутого лабораторного обследования путем обнаружения вирусного генома ВЭБ и ЦМВ (метод полимеразной цепной реакции, ПЦР) и определения профиля вирусоспецифических антител в сыворотке крови (иммуноферментный анализ). Это позволит установить стадию инфекционного процесса при хроническом лимфопролиферативном синдроме герпесвирусной этиологии и определить тактику лечения [12].
Уточнение этиологической роли ВЭБ и ЦМВ в развитии лимфопролиферативного синдрома при патологии лимфоэпителиального глоточного кольца у детей требует проведения адекватной клинико-лабораторной диагностики.
Цель исследования: анализ особенностей этиологической диагностики лимфопролиферативного синдрома у детей — кандидатов для проведения оперативного лечения.
Материал и методы
Отбор пациентов для проведения исследования осуществлялся по критериям, характерным для острого и хронического лимфопролиферативного синдрома.
Критерии острого лимфопролиферативного синдрома:
гипертрофия небных миндалин II–III степени с остаточными явлениями фаринготонзиллита;
аденоидит с нарушением функции носового дыхания;
длительность заболевания 2–6 дней, но не более месяца;
шейная лимфаденопатия;
возникновение клинических симптомов, связанных с перенесенной ангиной или острой респираторной вирусной инфекцией.
Критерии хронического лимфопролиферативного синдрома:
гипертрофия глоточной и небных миндалин II–III степени;
выраженная назальная обструкция;
длительность заболевания не менее 3–6 мес.;
наличие шейной лимфаденопатии с увеличением лимфатических узлов шейной группы при объективном осмотре;
указания на обострения воспалительного процесса в области лимфоглоточного кольца и повторные бактериальные инфекции — по данным анамнеза.
Клинико-лабораторное экспресс-обследование применено:
в поликлинической практике СПб НИИ ЛОР при диагностике острого лимфопролиферативного синдрома у 233 детей в возрасте от 3 до 16 лет;
у 157 детей в возрасте от 3 до 16 лет с хроническим лимфопролиферативным синдромом, обратившихся для решения вопроса о необходимости проведения хирургической санации в области лимфоглоточного кольца (аденотомии, тонзиллотомии, тонзиллэктомии);
у 100 детей в возрасте от года до 7 лет с высокой степенью тугоухости, кандидатов для проведения операции «кохлеарная имплантация» для мониторинга острого и хронического лимфопролиферативного синдрома.
Методы диагностики:
сбор жалоб и данных анамнеза (интоксикационный синдром: фебрильная или субфебрильная температура тела, озноб, головная боль, общая слабость; признаки кардиального и артралгического синдромов: боли в сердце и крупных суставах; гепатолиенальный синдром; боли в горле и затруднение носового дыхания);
ЛОР-осмотр (степень гипертрофии глоточной и небных миндалин, фаринготонзиллит, аденоидит с нарушением функции носового дыхания). Визуальная и пальпаторная оценка лимфатических узлов (величина, болезненность, спаянность с окружающими тканями);
гематологическое обследование (клинический анализ крови, скрининг с определением гетерофильных антител, ассоциированных с инфекционным мононуклеозом, маркеров активности воспалительного процесса (С-реактивный белок, ревматоидный фактор);
верификация диагноза герпесвирусной инфекции:
обнаружение вирусного генома (ДНК) ВЭБ и ЦМВ в лимфоцитах крови и в соскобах со слизистой оболочки ротоглотки методом ПЦР;
определение профиля вирусоспецифических антител в сыворотке крови иммуноферментным методом: специфические антитела к антигенам ЦМВ классов IgM и IgG и антитела к различным антигенам ВЭБ — к комплексу ранних, вирусному капсидному, ядерному антигенам. Данное исследование позволяет не только установить отсутствие или наличие инфицирования ВЭБ, ЦМВ, но и определить стадию инфекционного процесса (первичная инфекция, ранняя паст-инфекция, поздняя паст-инфекция, реактивация).
Возможная интерпретация результатов серологических исследований в отношении ВЭБ-инфекции широко описана в современной литературе и представлена в таблице 1.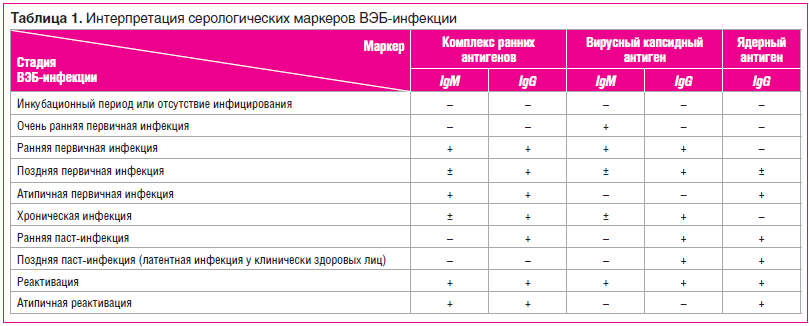
Следует подчеркнуть, что обнаружение вирусного генома (ДНК) ВЭБ, ЦМВ в крови указывает на активность инфекционного процесса и является противопоказанием к проведению хирургического лечения хронического лимфопролиферативного синдрома у детей.
При подозрении и с целью диагностики острого лимфопролиферативного синдрома в условиях амбулаторно-поликлинического приема пациента ЛОР-врачом проводился ряд скрининговых тестов (гемагглютинационный и латексные экспресс-тесты), которые позволили в 64% случаев дифференцировать этиологию острого состояния менее чем за 60 мин.
Результаты исследования
По результатам обследования установлено, что острая форма лимфопролиферативного синдрома в 33,5% случаев была вызвана бета-гемолитическим стрептококком. У данной категории детей в крови определялось повышение титра антистрептолизина-О (от 200 до 800 МЕ/мл), подтверждающее роль Streptococcus pyogenes как этиологического фактора в патогенезе острого лимфопролиферативного синдрома. Также выявлено повышение в сыворотке крови концентрации острофазового реактанта С-реактивного белка: у 65% детей в 1,5–2 раза, у 35% — в 4–8 раз, повышение концентрации ревматоидного фактора в 4,3% случаев (в т. ч. у 4-летнего мальчика в 5 раз).
У 30,9% обследованных детей выявлены в сыворотке крови гетерофильные антитела, ассоциированные с инфекционным мононуклеозом, что в сочетании с клиническими признаками лимфопролиферативного, инфекционно-воспалительного, интоксикационного, астеновегетативного, артралгического, кардиального синдромов позволило диагностировать инфекционный мононуклеоз. В наших наблюдениях гетерофильные антитела обнаруживались начиная с 3-го дня болезни и сохранялись по 30-й день.
У 16% детей диагностирован острый лимфопролиферативный синдром смешанной этиологии — инфекционный мононуклеоз и стрептококковая инфекция.
Установлено, что в ЛОР-учреждения обращаются больные с легкой и средней степенью тяжести, а также стертой клинической картиной инфекционного мононуклеоза, это требует особого внимания со стороны ЛОР-врачей. Кроме того, при выявлении развернутой клинической картины инфекционного мононуклеоза необходимо учитывать особенности патогенетической терапии. Своевременное уточнение этиологии острого лимфопролиферативного синдрома позволяет выбрать оптимальную тактику лечения больных.
Хронический лимфопролиферативный синдром выявлен у 157 детей из числа обратившихся в СПб НИИ ЛОР для решения вопроса о необходимости проведения хирургического лечения. На момент осмотра ЛОР-хирургом клинических данных за острую патологию выявлено не было. При объективном осмотре выявлена лимфоидная пролиферация, проявляющаяся гипертрофией глоточной, небных миндалин, а также увеличением шейных и подчелюстных лимфатических узлов. На основании результатов лабораторного обследования установлено, что в большинстве случаев (более 74%) этиологическим фактором развития лимфоидной пролиферации был ВЭБ, антитела к которому выявлены методами иммуноферментного анализа и ПЦР.
ЦМВ в большинстве случаев обнаруживался в сочетании с другими патогенами: в 34,39% случаев с ВЭБ, в 14,65% с ВЭБ и бета-гемолитическим стрептококком.
В 30% случаев у детей с признаками хронического лимфопролиферативного синдрома, основываясь на данных лабораторного обследования, установлены маркеры различных стадий активного инфекционного процесса (стадия первичной инфекции, реактивация, ранняя паст-инфекция). В остальных случаях по результатам иммуноферментного анализа и ПЦР выявлен латентный характер течения герпес-вирусных инфекций (поздняя паст-инфекция).
По результатам комплексного тестирования 100 детей с высокой степенью тугоухости, кандидатов для проведения операции кохлеарной имплантации на базе детского хирургического отделения СПб НИИ ЛОР, на антитела к ВЭБ и ЦМВ в крови методом иммуноферментного анализа, а также определения вирусного генома в биологических жидкостях (ВЭБ-инфекции и ЦМВ-инфекции с выявлением вирусной ДНК в соскобах с задней стенки глотки и в лимфоцитах крови) установлено наличие различных комбинаций маркеров герпесвирусных инфекций (ВЭБ, ЦМВ). Данных за активный инфекционный процесс не выявлено.
В послеоперационном периоде у 20% детей данной группы наблюдалось развитие лимфопролиферативного синдрома с повышением температуры тела до 38 °C, аденоидитом, ринофарингитом.
При обследовании в клиническом анализе крови выявлены характерные для инфекционного процесса изменения (лимфоцитоз свыше 15% по сравнению с возрастной нормой, атипичные мононуклеары). У 10% заболевших детей изменение общего состояния сопровождалось особенностями заживления со стороны послеоперационной области (формирование гематомы в области ниши кохлеарного имплантата). Клиническая картина и данные лабораторного обследования свидетельствуют в пользу активного инфекционного процесса, а также позволяют предположить реактивацию герпесвирусной инфекции, выявленной ранее. Активность герпесвирусных инфекций, сопровождающаяся нарушениями в системе гемостаза, требует подбора адекватной терапии для предотвращения развития осложнений в послеоперационном периоде, а при отсутствии этиотропной противовирусной и иммуномодулирующей терапии является противопоказанием к оперативному лечению.
Заключение
В настоящее время в практике детского ЛОР-врача особое место занимают обращения с патологией лимфоэпителиального глоточного кольца, а также с шейным и подчелюстным лимфаденитом. В подавляющем большинстве таких обращений регистрируются случаи мононуклеозоподобного синдрома. Далее перед врачами стоят непростые задачи дифференциальной диагностики, выявления этиологических факторов и подбора соответствующей терапии.
Этиологическая диагностика в последние годы претерпела значительные изменения. Комбинация специфических методов лабораторного скрининга с выявлением дискретных антигенов — маркеров остроты и тяжести воспалительного процесса инфекционного мононуклеоза и стрептококковой инфекции при остром лимфопролиферативном синдроме — позволяет в амбулаторно-поликлинических условиях верифицировать диагноз в 64% случаев.
В случаях хронического лимфопролиферативного синдрома после оценки клинических признаков рекомендуем лабораторную диагностику: детекцию в крови ДНК ВЭБ, ЦМВ (метод ПЦР) и определение профиля вирусоспецифических антител к вирусному капсидному антигену, комплексу ранних и ядерному антигенам ВЭБ и специфические антитела к антигенам ЦМВ классов IgM и IgG (иммуноферментный метод).
Клинико-лабораторное экспресс-обследование позволяет провести диагностику мононуклеозного синдрома и установить факт текущего контакта с ВЭБ у 30% обследованных детей с острым лимфопролиферативным синдромом. Этиологическим фактором острого лимфопролиферативного синдрома в 34% случаев является острая стрептококковая инфекция. Острый лимфопролиферативный синдром у 16% детей обусловлен комбинацией инфекционного мононуклеоза, вызванного ВЭБ и стрептококковой инфекцией.
Серологические и молекулярно-генетические маркеры инфицирования ВЭБ выявлены при хроническом лимфопролиферативном синдроме у 75% детей. Хронический лимфопролиферативный синдром у 30% детей, направленных для решения вопроса о хирургическом лечении, обусловлен активной фазой ВЭБ-инфекции (поздняя первичная инфекция или реактивация), являющейся противопоказанием к оперативному лечению.
Развитие лимфопролиферативного синдрома выявлено у детей, кандидатов для проведения операции кохлеарной имплантации, в 20% случаев, в 10% из которых общее состояние сопровождалось особенностями заживления со стороны послеоперационной области (формирование гематомы в области ниши кохлеарного имплантата). Это свидетельствует о необходимости обследования детей на наличие инфекционных патогенов.
Многообразие клинической картины значительно усложняет процесс выявления герпесвирусных инфекций у разных групп пациентов. Для верификации диагноза целесообразным в настоящее время является внедрение современных методов лабораторной диагностики, что позволит повысить уровень оказания помощи пациенту при постановке этиологического диагноза.
Уточнение этиологии лимфаденопатии инфекционного генеза является необходимым условием проведения адекватной этиотропной терапии.
Появление сведений о новых этиологических агентах лимфопролиферативного синдрома у детей и современных лабораторно-диагностических технологиях вселяет определенные надежды на разработку действенных мероприятий по профилактике и лечению данных заболеваний и уменьшение бремени экономической нагрузки на государство.
Литература
1. Викулов Г.Х. Клинико-иммунологическая характеристика герпесвирусных инфекций в отдаленном после облучения периоде у лиц, подвергавшихся воздействию радиационного фактора: дис. … канд. мед. наук. М. 2009. 200 с. [Vikulov G.H. Kliniko-immunologicheskaja harakteristika gerpesvirusnyh infekcij v otdalennom posle obluchenija periode u lic, podvergavshihsja vozdejstviju radiacionnogo faktora: dis.… kand. med. nauk. M. 2009. 200 s. (in Russian)].
2. Исаков В.А., Архипова Е.И., Исаков Д.В. Герпесвирусные инфекции человека: руководство для врачей. СПб.: Спецлит. 2013. 670 с. [Isakov V.A., Arhipova E.I., Isakov D.V. Gerpesvirusnye infekcii cheloveka: rukovodstvo dlja vrachej. SPb.: Speclit. 2013. 670 s. (in Russian)].
3. Schiffer J.T., Abu-Raddad L., Mark K.E. et al. Frequent Release of Low Amounts of Herpes Simplex Virus From Neurons: Results of a Mathematical Model // Sci. Transl. Med. 2009. Vol. l(7). P.178–184.
4. Тамразова О.Б., Стадникова А.С., Рудикова Е.В., Кузнецова Т.А. Современные особенности течения герпетической инфекции у детей // Клиническая дерматология и венерология. 2015. №14(4). C.59–68 [Tamrazova O.B., Stadnikova A.S., Rudikova E.V., Kuznecova T.A. Sovremennie osobennosti techenija gerpeticheskoj infekcii u detej // Klinicheskaja dermatologija i venerologija. 2015. №14(4). S.59–68 (in Russian)].
5. Сиразитдинова В.Ф., Дмитриев Г.А., Маннанов А.М. Герпесвирусная инфекция у детей // Клиническая дерматология и венерология. 2012. №10(6). C.10–15 [Sirazitdinova V.F., Dmitriev G.A., Mannanov A.M. Gerpesvirusnaja infekcija u detej // Klinicheskaja dermatologija i venerologija. 2012. №10(6). S.10–15 (in Russian)].
6. Касихина Е.И., Глазко И.И., Чекмарев А.С. Герпетическая инфекция: механизмы латентности и реактивации. Возможности управления // Клиническая дерматология и венерология. 2014. №12(1). C.75–80 [Kasihina E.I., Glazko I.I., Chekmarev A.S. Gerpeticheskaja infekcija: mehanizmi latentnosti i reaktivacii. Vozmozhnosti upravlenaja // Klinicheskaja dermatologija i venerologija. 2014. №12(1). S.75–80 (in Russian)].
7. Cohen J.I. Epstein-Barr virus infection // N. Engl. J. Med. 2000. Vol. 343. P.481–492.
8. Преображенская Ю.С., Дроздова М.В. Тырнова Е.В. Экссудативный средний отит у детей с хроническим лимфопролиферативным синдромом // Рос. оторинолар. 2011. №4 (53). С.62–68 [Preobrazhenskaja Y.S., Drozdova M.V. Ekssudativnij srednij otit u detej s hronicheskim limfoproliferativnim sindromom // Rossijskaja otorinolar. 2011. №4(53). S.62–68 (in Russian)].
9. Львов Н.Д. Герпесвирусы человека — системная, интегративная, лимфопролиферативная иммуноонкопатология // Дерматология. РМЖ. 2012. №22. С.3–12 [L’vov N.D. Gerpesvirusy cheloveka — sistemnaja, integrativnaja, limfoproliferativnaja immunoonkopatologija // Dermatologija. RMZh. 2012. №22. S. 3–12 (in Russian)].
10. Хунафина Д.Х., Галиева А.Т., Агадуллина Э.Я. Цитомегаловирусная инфекция // Мед. вестник Башкортостана. 2011. №(6)5. С.128–130 [Hunafina D.H., Galieva A.T., Agadullina E.Ja. Citomegalovirusnaja infekcija // Med. vestnik Bashkortostana. 2011. №(6)5. S.128–130 (in Russian)].
11. Викулов Х.Г. Иммунологические аспекты герпес-вирусных инфекций // Клиническая дерматология и венерология. 2015. №14(5). С.104–116 [Viculov H.G. Immunologicheskie aspect gerpes-virusnih infekcij // Klinicheskaja dermatologija i venerologija. 2015. №14(5). S.104–116 (in Russian)].
12. Преображенская Ю.С., Дроздова М.В. Особенности лечения пациентов с патологией лимфоэпителиального глоточного кольца, осложненной развитием экссудативного среднего отита // Российская оторинолар. 2014. №3(70). С.89–96 [Preobrazhenskaja Y.S., Drozdova M.V. Osobennosti lechenia pacientov s patologiej limfoepitelial’nogo glotochnogo kol’ca, oslognennoy razvitiem ekssudativnogo srednego otita // Rossijskaja otorinolar. 2014. №3(70). S.89–96 (in Russian)].
13. Srinivasan A., Gu Z., Smith T. et al. Prospective detection of respiratory pathogens in symptomatic children with cancer // Pediatr. Infect. Dis. J. 2013. Vol. 32(3). P.99–104.
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
материал rmj.ru
