Введение
За последние 20 лет благодаря появлению оптического когерентного томографа и трех поколений антиангиогенных препаратов стали лучше понимать патогенез возрастной макулярной дегенерации (ВМД), были достигнуты успехи в диагностике и лечении данного заболевания. Многочисленные исследования, прошедшие в разных странах, продолжительностью от 1 года до 15 лет (MARINA, ANCHOR, PIER, HARBOR, ABC, CATT, IVAN, GEFAL, LUCAS, ALTAIR, SAVE-AMD, EXCITE, TREX-AMD, CANTREAT, VIEW 1, VIEW 2, TREND, HAWK, HARRIER и др.) продемонстрировали высокую эффективность и высокий профиль безопасности антиангиогенной терапии [1–12]. Благодаря внедрению анти-VEGF-препаратов в клиническую практику при лечении макулярной неоваскуляризации (МНВ) прогноз заболевания резко изменился. Вероятность улучшения остроты зрения в течение первых двух лет лечения от почти нулевой (т. е. «достоверной» слепоты) [1] приблизилась к 30% [9–12]. Настало время для анализа негативных результатов, их прогнозирования и перехода к профилактике неблагоприятных исходов.
В настоящее время стало очевидно, что ответ на лечение анти-VEGF-препаратами при активной МНВ зависит от сложившейся комбинации системных и местных факторов, а также от продолжительности заболевания и регулярности введения препарата [9–15]. К системным факторам относят артериальное давление (АД), атеросклероз, ожирение и/или гипотиреоз, наличие сахарного диабета, перенесенные инфаркты и инсульты в анамнезе [13, 14]. Под местными факторами понимают характеристику и локализацию очага неоваскуляризации (тип МНВ), активность заболевания, архитектонику и плотность сосудов в поверхностном и глубоком ретинальном сплетении макулы и состояние хориоидальных сосудов под ней, наличие интраретинального и преретинального фиброза (по данным оптической когерентной томографии (ОКТ)) [15–18]. Раскрыта и обоснована причинно-следственная связь эффективности лечения практически с каждым из перечисленных показателей. Аналогично ретроспективный post hoc анализ выявил основные ОКТ-характеристики МНВ, ассоциированные с неэффективностью антиангиогенного лечения. Так, с низким функциональным результатом исследование PIER [15] связало размер МНВ >4 DA, а исследования MONT BLANC [16], VIEW1/VIEW2 [17] в качестве маркеров неблагоприятного ответа указали интраретинальные кисты (в сочетании с субретинальной жидкостью (subretinal fluid, SRF) или отслойкой ретинального пигментного эпителия (pigment epithelial detachments, PED). В исследовании CATT худший функциональный результат ассоциировали с повышением пигментного эпителия сетчатки (retinal pigment epithelium, RPE), географической атрофией и тонкой фовеа [18], указав на них как на маркеры неблагоприятного ответа на интравитреальные инъекции (ИВИ). При этом не было найдено публикаций, раскрывающих взаимосвязь эффективности антиангиогенного лечения с такими важными факторами, как среднее перфузионное глазное давление (СПГД) и внутриглазное давление (ВГД). Между тем последние являются своеобразным «мостиком» между системными и местными факторами, более того, именно ишемия на уровне СПГД признана одним из ключевых патогенных механизмов ВМД и индуктором неоваскуляризации [19–21].
Цель исследования: проанализировать исходные показатели СПГД и ВГД у больных МНВ во взаимосвязи с ответом на антиангиогенную терапию.
Содержание статьи
Материал и методы
Все пациенты подписывали информированное добровольное согласие на участие в исследовании. Протокол исследования был одобрен этическим комитетом ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА. Исследование проводилось в соответствии с принципами Хельсинкской декларации.
Нами был выполнен post hoc анализ; в исследование включили 84 пациента (29 мужчин, 55 женщин; 92 глаза) с впервые выявленным диагнозом МНВ и признаками активности заболевания. Возраст пациентов варьировал от 52 до 97 лет (средний возраст 73,4±8,5 года). У 18 (19,5%) человек процесс был двусторонним. Из 92 глаз с МНВ в 55,5% глаз был собственный хрусталик, в 44,5% случаев была артифакия.
Больных с активной МНВ лечили ИВИ афлиберцепта в соответствии с инструкцией к препарату и национальными рекомендациями: 40 мг/мл в фиксированном режиме. В обязательном порядке три загрузочных ИВИ выполнялись сертифицированным хирургом в условиях операционной. Контроль лечения проводили спустя 4 нед. после каждой инъекции. В отсутствие функционального улучшения и положительной динамики морфоструктурных показателей после трех загрузочных ИВИ лечение афлиберцептом прекращали и переходили на другой препарат. Ежемесячные инъекции продолжали до достижения сухости макулы. Инъекции афлиберцепта повторяли на глазах с признаками персистирующей активности (свежее кровоизлияние, SRF, интраретинальная жидкость (intraretinal fluid, IRF) или жидкость суб-RPE). Глаза, показавшие полную регрессию или резорбцию экссудата при последовательном обследовании до или после завершения трех ИВИ, классифицировали как «хорошо реагирующие» (синоним: респонденты); глаза с рецидивом, персистированием экссудации или прогрессирующим ухудшением после трех ИВИ классифицировали как «плохо реагирующие» (синоним: нереспонденты).
При проведении исследования особое внимание уделяли поиску возможных системных и локальных факторов риска плохого ответа на интравитреальное лечение ангиостатиками. В качестве таковых рассматривали и анализировали анамнестические данные. В частности, учитывали перенесенные инфаркты миокарда, инсульты, тромбоэмболии, атеросклероз, гипертоническую болезнь, заболевания желудочно-кишечного тракта, мочевыделительной системы, легочные заболевания, гиперхолестеринемию, сахарный диабет, гипотиреоз, тиреотоксикоз, диффузно-токсический зоб, тиреоидит и другие аутоиммунные и наследственные заболевания. В исходную базу данных вносили данные систолического артериального давления (САД) и диастолического артериального давления (ДАД), пульсовое давление, СПГД рассчитывали по двум известным формулам [22] и вносили в базу оба варианта:
СПГД1 = ДАД + ⅓(САД — ДАД).
СПГД2 = ⅔(САД — ВГД)
Кроме того, для каждого глаза рассчитывали так называемый коэффициент перфузии (КП), представляющий собой отношение СГПД к ВГД. КП показывает, во сколько раз давление в сосудах глаза превышает ВГД.
Критерии включения: пациенты старше 55 лет; все экссудативные формы ВМД (1, 2, 3-й типы МНВ); верификация МНВ методами ОКТ/ОКТ-А, флюоресцентной ангиографии глаза (ФАГ); отсутствие предшествующего лечения (лазеротерапия, фотодинамическая терапия, интравитреальная и антиоксидантная терапия, биологические активные добавки, витамины, ретробульбарные инъекции пептидов); острота зрения должна была не превышать 20/30 и быть не ниже 20/320 (ETDRS).
Критерии невключения: наличие МНВ иного генеза, отличного от ВМД (осложненная миопия высокой степени); наличие сопутствующей макулопатии, приводящей к потере зрения (центральная серозная хориопатия, диабетический отек макулы); лазерное или хирургическое вмешательство на глазу с МНВ по поводу витреоретинальной патологии или катаракты за 6 мес. до настоящего исследования; серозная отслойка ретинального пигментного эпителия без других признаков МНВ; хирургическое лечение катаракты за 6 мес. до настоящего исследования; наличие в анамнезе коронарного шунтирования, операций на опорно-двигательном аппарате, требующих приема антикоагулянтов; трансплантации органа, перорального приема химиотерапевтических агентов или иммунодепрессантов, а также моноклональных антител или иммуноглобулинов; наличие противопоказаний к введению ангиостатиков; наличие любой патологии сетчатки или зрительного нерва со снижением зрения; любое снижение прозрачности оптических сред, способное повлиять на функциональный результат.
Диагностику проводили по МКБ-10 (Н35.3). Выполняли полное офтальмологическое обследование: определяли максимально корригированную остроту зрения по таблице Снеллена, измеряли ВГД бесконтактным методом, выполняли биомикроскопию переднего и заднего сегментов глаза, офтальмоскопию, ОКТ сетчатки (DRI OCT Triton plus, Topcon Corporation, Япония, Swept Source; скорость сканирования 100 000 А-сканов/с, 1050 нм). По данным ОКТ верифицировали тип МНВ в соответствии с последней международной классификацией [23]. Выделяли тип 1 МНВ (сосуды под пигментным эпителием сетчатки), тип 2 (сосуды расположены субретинально) и тип 3 (сосуды расположены интраретинально). Активность заболевания верифицировали по данным ОКТ (центральной толщине сетчатки (central retinal thickness, CRT), суб- и интраретинальной жидкости (SRF, IRF) и PED), свежим кровоизлияниям при офтальмоскопии и протечке красителя на ФАГ. Фоторегистрацию глазного дна, ангиографию с красителями и аутофлюоресценцией выполняли на каждом визите пациента, определяли морфометрические параметры: CRT, SRF, IRF и PED. В анализ вошел 281 показатель каждого из пациентов на входе и выходе из исследования.
Глаза со свежими кровоизлияниями офтальмоскопически, с ОКТ-признаками жидкости в виде SRF, IRF или суб-RPE и ФАГ-признаками протечки красителя классифицировали как имеющие активную МНВ. Их лечили ангиостатиками [23, 24]. Все 84 пациента (92 глаза, 100%) завершили исследование, их данные включены в оценку результатов.
Продолжительность исследования составила 12 мес.
Результаты анализировали с помощью пакета прикладных статистических программ SPSS Statistics v. 26 IBM Corporation. Для показателей, измеренных по интервальной (количественной) шкале и имеющих нормальное распределение, рассчитывали среднее значение, среднеквадратичное отклонение и ошибку среднего. При сравнении групп по количественным показателям использовался критерий Стьюдента (t-критерий), коэффициенты корреляции рассчитывали по методу Пирсона. При сравнении групп по номинальным показателям применялся критерий χ2 или критерий Фишера (при малых частотах).
Результаты исследования
Идеальными респондентами на ИВИ используемым препаратом были 19 (21,7%) глаз из 92. Остальные 73 глаза сформировали группу нереспондентов. Проанализированы среднегрупповые показатели СПГД и ВГД респондентов и нереспондентов. Выявлены статистически значимые межгрупповые различия, в связи с чем для более глубокого понимания характера этой связи мы прибегли к ранжированию терапевтического ответа на лечение, распределяя нереспондентов на 5 следующих подгрупп [25]:
-
подгруппа 0 — ухудшение с прогрессированием (увеличение SRF/IRF, высоты и площади PED, свежие кровоизлияния);
-
подгруппа 1 — тахифилаксия (изначально хороший ответ со временем снижается);
-
подгруппа 2 — истинные нереспонденты (не изменяются SRF, IRF, остается экссудат под RPE);
-
подгруппа 3 — зависимые от анти-VEGF (регрессия экссудата сразу после ИВИ, рецидив активности по SRF/IRF, экссудат суб- RPE или PED при интервале между ИВИ более 4 нед.);
-
подгруппа 4 — частичные нереспонденты (≤15% регрессии SRF и/или IRF; слабое снижение активности на фоне лечения);
-
подгруппа 5 — идеальные респонденты.
Самые высокие среднегрупповые показатели СПГД1 и СПГД2 оказались у пациентов с ухудшением морфометрических показателей (подгруппа 0); для сравнения: СПГД2 составило 96,2±2,1 мм рт. ст. (подгруппа 0) против 91,6±1,6 мм рт. ст. (подгруппа 5; p=0,125). Заметим, что статистическая значимость различий не достигнута исключительно из-за малочисленности подгруппы 0, поэтому связь расценена как сильная тенденция (р=0,125) (табл. 1). Ближе всего к показателям истинных респондентов приблизились показатели подгруппы 3, высокозависимой от ИВИ ангиостатика. Так как в этой подгруппе было 26 глаз, межгрупповые различия с респондентами статистически значимы (р=0,0059).
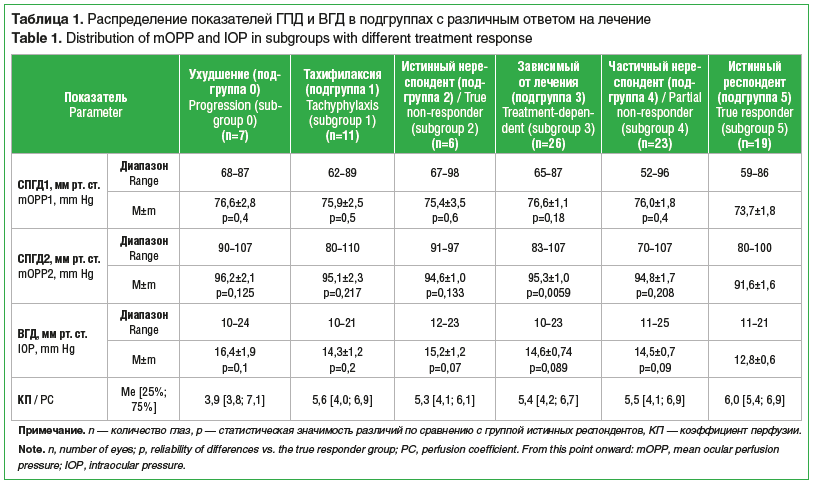
В подгруппе истинных респондентов (подгруппа 5), напротив, среднегрупповые показатели СПГД1 и СПГД2 оказались самыми низкими.
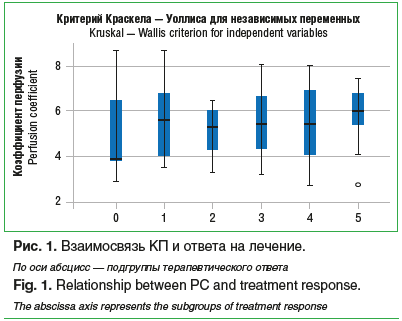
В подгруппе с прогрессированием оказался самый низкий КП — 3,9 (рис. 1). При этом КП четырех других типов нереспондентов (подгруппы 1–4) были сопоставимы между собой и ненамного ниже показателей глаз идеальных респондентов. Следует подчеркнуть, что самый высокий КП оказался у идеальных респондентов — 6,0.
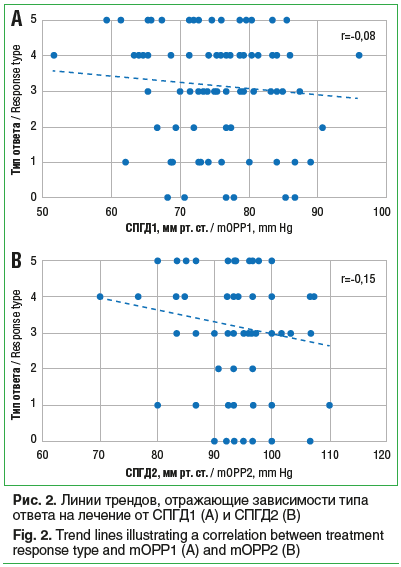
Угол наклона линии тренда, представленной на рис. 2А, подтвердил слабую отрицательную (r=-0,08) и статистически незначимую связь между СПГД1 и ответом глаза на лечение. С другой стороны, перфузионное давление СПГД2, рассчитанное по второй указанной формуле (см. выше), продемонстрировало более значимую отрицательную связь (r=-0,15; рис. 2В).
Вполне ожидаемой оказалась высокодостоверная отрицательная корреляционная связь между ВГД и СПГД1/СПГД2: коэффициент линейной связи Ро=-0,325 (p<0,01; табл. 2).

Далее мы проанализировали среднегрупповые показатели ВГД в выделенных клинических подгруппах. В отличие от глаз с полным (подгруппа 2) и частичным (подгруппа 4) отсутствием ответа, а также от высокозависящих от ИВИ ангиостатика глаз (подгруппа 3), где крайние значения ВГД выходили за границы физиологического офтальмотонуса (21 мм рт. ст.) (см. табл. 1), самые низкие среднегрупповые показатели ВГД (12,8±0,6 мм рт. ст.) и самый высокий КП оказались у идеальных респондентов (подгруппа 5), при этом разброс значений их офтальмотонуса находился в диапазоне физиологических значений — 11–21 мм рт. ст.
Корреляционный анализ связи количественных показателей ВГД с ответом на лечение подтвердил слабую устойчивую отрицательную статистически значимую линейную корреляцию (r=-0,216, р=0,038). Ее демонстрирует линия тренда, представленная на рисунке 3.
Корреляц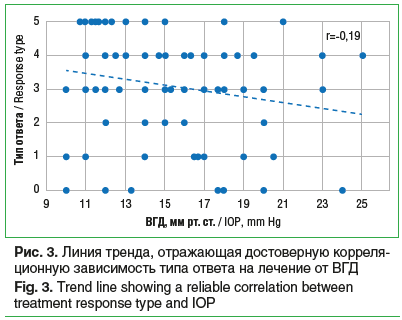 ионный анализ вскрыл некоторые корреляционные связи морфометрических ОКТ-показателей сетчатки с показателями СПГД и ВГД (табл. 3).
ионный анализ вскрыл некоторые корреляционные связи морфометрических ОКТ-показателей сетчатки с показателями СПГД и ВГД (табл. 3).
Показатели СПГД1 изначально не коррелировали с типом МНВ и маркерами активности МНВ (SRF, IRF), с толщиной сетчатки в центре (CRT); связь с высотой отслойки пигментного эпителия (PED) была слабой, но статистически значимой. При этом CПГД1 положительно коррелировало с динамикой на фоне антиангиогенного лечения SRF, IRF (p<0,05) и экссудата под RPE, отрицательно коррелировало с высотой PED (p<0,05) и толщиной сетчатки в центре (CRT, p<0,01) (см. табл. 3).
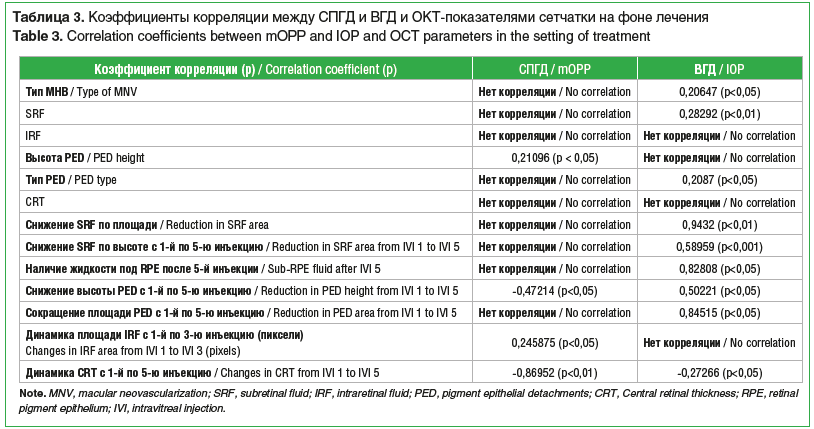
Заметим, что ВГД прямо коррелировало с исходными показателями SRF (p<0,01) и типом PED (p<0,05).
С исходными показателями ВГД прямо и положительно коррелировала также динамика ОКТ маркеров активности заболевания на фоне лечения анти-VEGF-препаратом (снижение SRF по площади и высоте, снижение количества экссудата под RPE, сокращение площади PED (в пикселях) (см. табл. 3). При этом корреляционная связь ВГД и CRT была отрицательной: чем выше ВГД, тем хуже динамика CRT. Выявленные корреляции говорили о приоритетной роли офтальмотонуса в ответных реакциях глаза на антиангиогенную терапию. Исходя из этого, можно отметить, что офтальмогипертензия автоматически входила в категорию самостоятельного и независимого фактора риска плохого ответа на лечение. В связи с этим мы рассчитали 95% доверительный интервал (95% ДИ) в выделенных клинических подгруппах, он представлен на рисунке 4.
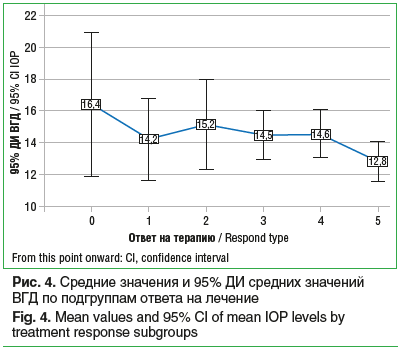
Мы также провели ROC-анализ с оценкой чувствительности и специфичности ВГД в качестве маркера неблагоприятного ответа на лечение и оценили его связь с лечением (рис. 5).
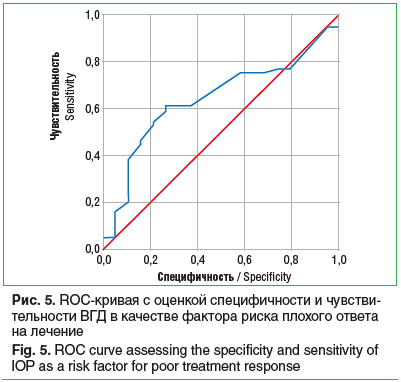
Площадь области под кривой составила 0,645, что свидетельствует о значимом умеренном влиянии ВГД на исход. В качестве маркера было выбрано ВГД 12,6 мм рт. ст. — точка баланса, в которой чувствительность и специфичность плохого ответа примерно совпадали. При этом значении ВГД чувствительность плохого ответа составила 0,603, а специфичность — 0,737. В группе нереспондентов с ВГД <12,6 мм рт. ст. было 40% наблюдений, а в группе респондентов — 74%. Таким образом, если исходное ВГД превышает 12,5 мм рт. ст., то шансы плохого ответа на лечение увеличиваются примерно в 4 раза (табл. 4). Границы 95% ДИ не пересекаются, что свидетельствует о высокой статистической значимости полученных результатов: р=0,00784.

Обсуждение
Несмотря на то, что технология ИВИ предполагает адресную доставку ангиостатика в стекловидное тело с последующим всасыванием (?) сетчаткой, приоритетная роль хориоидеи в этом процессе очевидна. Сосудистой оболочке принадлежит доминирующая роль в кровоснабжении сетчатки. Благодаря фенестрации хориокапилляры обеспечивают высокую белковую проницаемость, создавая высокое онкотическое давление, способствующее движению тока жидкости вместе с фармпрепаратом из сетчатки в очаги МНВ и глубже [25–30]. Процессу способствует и биохимическое сродство анти-VEGF-препарата с природными рецепторами, экспрессирующимися на эндотелии новообразованных сосудов МНВ. Неслучайно технология ИВИ с введением ангиостатиков получила название таргетной терапии. В этом смысле хориоидея, ее морфометрические ОКТ-показатели и такая важная характеристика, как СПГД, представляют особый интерес, поскольку предполагается, что именно аномалии хориоидального кровотока (ишемия) способствуют развитию МНВ [19–21].
Что такое перфузионное глазное давление по своей сути? СПГД — это разница между артериальным и венозным давлением в сосудах глаза. Именно этот показатель отражает условия, в которых происходит тканевой обмен. Косвенно СПГД отражает гемодинамику хориоидеи. Более высокое СПГД способствует циркулярному стрессовому повреждению стенки хориоидальных сосудов, приводя их к постоянной дилатации и последующей гиперперфузии [27]. При этом растет чистый градиент давления от сосудов к тканям и увеличивается экссудация жидкости из хориоидальных сосудов (закон Старлинга), повышается риск разрыва сосудистой стенки и появления кровоизлияний (закон Лапласа) [27, 32]. Повышенное СПГД прямо коррелирует с системной артериальной гипертензией, в тандеме с которой становится главным этиологическим механизмом структурных изменений хориоидеи. Повышенные показатели СПГД, как правило, сочетаются с увеличением толщины хориоидеи, причем не только на глазах с полипоидальной хориоидальной васкулопатией (ПХВ), но и на парных глазах без ПХВ. Морфологически это проявляется расширением лакун и заполнением их кровью, т. е. венозным застоем, вторичным по отношению к атеросклеротическим изменениям стенок хориоидальных сосудов. Клинически это проявляется серозными отслойками RPE (PED) и полипоидными поражениями [31]. В наших исследованиях показатели СПГД изначально прямо коррелировали с высотой PED (p<0,05). Исходя из этого, мы полагали, что можно постулировать, что более высокое СПГД ассоциируется с повышенным риском прогрессирования МНВ без учета фактора лечения ИВИ. Полагаем, именно поэтому причинно-следственная связь не нашла подтверждения в линии тренда.
Однако более высокие уровни СПГД в сочетании с низким КП в нашем исследовании ассоциировались с плохим ответом на лечение: хуже нивелировались PED (p<0,05) и IRF (p<0,05), нормализовалась толщина сетчатки (CRT, p<0,01). Более того, на фоне повышенных по сравнению с другими клиническими подгруппами 1–4 среднегрупповых показателей СПГД ухудшалось клиническое течение заболевания в подгруппе 0. Справедливости ради следует заметить, что, с учетом выдвинутого нами постулата, это могло произойти и без лечения. Скорее всего, высокие уровни СПГД следует рассматривать в целом как фактор риска прогрессирования МНВ.
Идеальные респонденты, напротив, имели наименьшие уровни СПГД и ВГД, показатели которого укладывались в «физиологический коридор» (10–21 мм рт. ст.), при этом их КП был наиболее высоким.
Известно, что повышенное СПГД наблюдается и при глаукоме. Повышение СПГД, как правило, ассоциируется с нарушением ауторегуляции хориоидального кровотока. Глубину этих нарушений, по-видимому, и отражает комплексно триада показателей: СПГД, ВГД и КП.
В сосудистой оболочке глаза человека представлены разные типы ауторегуляции. Например, кровоток изменяется при снижении перфузионного давления либо при повышении ВГД [32–34]. Перфузионное давление снижается в ответ на повышение ВГД, что, собственно, и подтвердила выявленная в наших исследованиях обратная корреляционная связь.
Благодаря нашему ретроспективному исследованию были выявлены некоторые закономерности. В частности, было установлено, что ухудшение клинического течения МНВ на фоне ИВИ ассоциировалось с самыми высокими показателями СПГД в сочетании с низким КП. При этом ВГД выступило в качестве модифицируемого самостоятельного и независимого фактора риска плохого ответа на антиангиогенное лечение. Биомаркером, ассоциированным с идеальным ответом на лечение, стал показатель 12,6 мм рт. ст., а диапазон рекомендуемых оптимальных значений совпал с физиологическими значениями офтальмотонуса (11–21 мм рт. ст.) Исходно повышенный офтальмотонус с выходом персонифицированных значений ВГД за этот диапазон коррелирует с плохим исходом лечения. Вполне вероятно, что этот модифицируемый фактор может стать неплохим инструментом для снижения риска плохого ответа на лечение.
Заметим, что ранее показатели ВГД рассматривались в контексте офтальмогипертензии, развивающейся после ИВИ. Установлено, что ИВИ антиангиогенных препаратов сопровождаются острыми эпизодами повышения ВГД или хронической офтальмогипертензией. По данным литературы, случаи клинически значимого повышения ВГД (определяемые исследователями как увеличение на ≥6 мм рт. ст. по сравнению с исходным уровнем), приводящего к ВГД ≥21 мм рт. ст., составляют 2,6% против 1,5% в парном нелеченом глазу [35, 36]. J. Kim et al. [37] показали, что сразу после ИВИ ВГД повышается в среднем до 44 мм рт. ст. и затем в течение 15 мин снижается до уровня 30 мм рт. ст. и ниже. Согласно исследованию, проведенному M. Gismondi et al. [38], 88,9% глаз имели ВГД более 30 мм рт. ст. непосредственно после ИВИ ранибизумаба. У большинства пациентов ВГД приблизилось к нормальному уровню через 30–60 мин после ИВИ [35–38]. Острое повышение ВГД признано наиболее распространенным осложнением ИВИ анти-VEGF-препаратов. Можно предположить, что небольшой стандартный рекомендуемый объем вводимого фармпрепарата не может привести к столь значительным перепадам офтальмотонуса без важных причин. Нарушение ауторегуляции хориоидального кровотока — одна из таких причин. И в этом аспекте эпизоды офтальмогипертензии могут служить косвенным подтверждением нарушений ауторегуляции хориоидального кровотока.
Наряду с этим есть публикации, демонстрирующие снижение исходного ВГД на фоне многократных ИВИ антиангиогенных препаратов. Так, E.A. Atchison et al. [39] на основе данных 23 776 пациентов (американский регистр IRIS, Intelligent Research in Sight Registry) показали, что практически у всех пациентов с ВМД, получавших не менее 12, 18 и 25 инъекций одного из трех препаратов (бевацизумаб, афлиберцепт или ранибизумаб), наблюдали снижение ВГД по сравнению с исходным уровнем в среднем на 0,9 мм рт. ст. в леченых глазах по сравнению со средним снижением на 0,2 мм рт. ст. в парных нелеченых глазах (р<0,01). Клинически значимое повышение ВГД в отдаленном периоде наблюдения наблюдали реже — в <3% глаз, получавших инъекции, по сравнению с 1,5% в парных глазах без лечения [39–42]. Об эпизодах офтальмогипертензии написано в российских клинических рекомендациях [24].
Таким образом, если изменения показателей ВГД на фоне антиангиогенного лечения изучались и результаты исследований представлены в литературе, то взаимосвязь между исходными показателями ВГД и/или перфузионного давления и ответом на лечение глаза с активной МНВ практически осталась без внимания офтальмологического сообщества.
Изначально было неясно, что сильнее влияет на эффективность — СПГД или ВГД? И что предпочтительнее сделать для улучшения лечебного процесса? Нормализовать показатели АД гипотензивными препаратами? Или подкорректировать ВГД местными инстилляциями гипотензивных препаратов? Представленные нами данные подтвердили приоритетную роль значений офтальмотонуса в лечебном процессе ИВИ-технологии антиангиогенной терапии. Наряду с этим КП, отражающий, во сколько раз давление в сосудах глаза превышает истинное ВГД, показал, что все важно в комплексе, включая соотношение СПГД и ВГД. Самые низкие показатели КП ассоциировались с ухудшением клинического течения заболевания и морфоструктурных показателей сетчатки. Поэтому этот аспект причинно-следственных связей еще предстоит изучать.
Выявление модифицируемых факторов риска неблагоприятного ответа на лечение имеет чрезвычайно большое значение в практической офтальмологии, поскольку дает возможность повысить шансы пациента на лучший исход терапии.
Наше исследование имеет ряд ограничений. Одно из них связано с малочисленностью некоторых подгрупп с неблагоприятным ответом на лечение, что не позволяет достичь статистической значимости различий. Кроме того, мы не изучали вопрос гипотензивной терапии на этапе предоперационной подготовки к ИВИ во взаимосвязи с ответом на лечение. Этот аспект еще подлежит отдельному изучению. В-третьих, мы не модифицировали офтальмотонус на глазах с ВГД, превышающим рекомендуемые показатели. Этот вопрос также необходимо отдельно изучать.
Заключение
Выявлен модифицируемый фактор риска плохого ответа на лечение анти-VEGF-препаратом больных МНВ. Установлены диапазоны оптимальных значений ВГД, ассоциированные с хорошим ответом, что является ценной информацией, имеющей большое практическое значение для офтальмологов. Рассчитан обладающий высокой чувствительностью и специфичностью биомаркер (ВГД 12,6 мм рт. ст.) — точка баланса, в которой чувствительность и специфичность плохого ответа примерно совпадают.
Сведения об авторах:
Лихванцева Вера Геннадьевна — старший научный сотрудник группы офтальмологии лаборатории № 12 мультидисциплинарных клинических исследований отдела № 2 клинической и радиационной медицины ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России; 123182, Россия, г. Москва, ул. Живописная, д. 46; д.м.н., профессор кафедры офтальмологии Академии постдипломного образования ФГБУ ФНКЦ ФМБА России; 125371, Россия, г. Москва, Волоколамское ш., д. 91; ORCID iD 0000-0002-3175-9592.
Капкова Cветлана Георгиевна — к.м.н., доцент, заведующая офтальмологическим отделением ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России; 123182, Россия, г. Москва, ул. Живописная, д. 46; доцент кафедры офтальмологии Академии постдипломного образования ФГБУ ФНКЦ ФМБА России; 125371, Россия, г. Москва, Волоколамское ш., д. 91; ORCID iD 0000-0002-0934-725Х.
Третьяк Евгения Борисовна — к.м.н., врач-офтальмолог офтальмологического отделения ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России; 123182, Россия, г. Москва, ул. Живописная, д. 46; ORCID iD 0000-0002-5304-1434.
Рычкова Светлана Игоревна — д.м.н., врач‑офтальмолог, ведущий научный сотрудник лаборатории «Зрительные системы» ИППИ РАН; 127051, Россия, Б. Каретный пер., д. 19; доцент кафедры глазных болезней МБУ ИНО ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России; 123098, г. Москва, ул. Живописная д. 46, стр. 8; ORCID iD 0000-0001-6764-8950.
Геворкян Армине Сейрановна — соискатель кафедры офтальмологии Академии последипломного образования ФГБУ ФНКЦ ФМБА России; 125371, Россия, г. Москва, Волоколамское ш., д. 91; ORCID iD 0000-0003-0773-1933.
Борисенко Татьяна Евгеньевна — консультант по доказательной медицине ФГБНУ «НИИГБ им. М.М. Краснова»; 119021, Россия, г. Москва, ул. Россолимо, д. 11, корп. А, корп. Б.
Контактная информация: Лихванцева Вера Геннадьевна, e-mail: likhvantseva-4@yandex.ru.
Источник финансирования: исследование проходило в рамках НИР (шифр «Профтруд-2», № 10.020.21.800).
Конфликт интересов отсутствует.
Статья поступила 07.09.2023.
Поступила после рецензирования 02.10.2023.
Принята в печать 25.10.2023.
About the authors:
Vera G. Likhvantseva — Dr. Sc. (Med.)., senior researcher of the Group of Ophthalmology of the Laboratory No. 12 of Multidisciplinary Clinical Trials of the Division No. 2 of the Clinical and Radiation Medicine, A.I. Burnazyan Federal Medical Biophysical Center of the Federal Medical Biological Agency of Russia; 46, Zhivopisnaya str., Moscow, 123182, Russian Federation; professor of the Department of Ophthalmology, Academy of Postgraduate Education of the Federal Scientific and Clinical Center of the Federal Medical Biological Agency of Russian Federation; 91, Volokolamskoe road, Moscow, 125310, Russian Federation; ORCID iD 0000-0002-3175-9592.
Svetlana G. Kapkova — C. Sc. (Med.), Associate Professor, Head of the Ophthalmological Department, A.I. Burnazyan Federal Medical Biophysical Center of the Federal Medical Biological Agency of Russia; 46, Zhivopisnaya str., Moscow, 123182, Russian Federation; associate professor of the Department of Ophthalmology, Academy of Postgraduate Education of the Federal Scientific and Clinical Center of the Federal Medical Biological Agency of Russian Federation; 91, Volokolamskoe road, Moscow, 125310, Russian Federation; ORCID iD 0000-0002-0934-725Х.
Evgeniya B. Tretyak — C. Sc. (Med.), ophthalmologist of the Ophthalmological Department, A.I. Burnazyan Federal Medical Biophysical Center of the Federal Medical Biological Agency of Russia; 46, Zhivopisnaya str., Moscow, 123182, Russian Federation; ORCID iD 0000-0002-5304-1434.
Svetlana I. Rychkova — Dr. Sc. (Med.), ophthalmologist, leading researcher of the Laboratory «Visual Systems», Institute for Information Transmission Problems of the RAS (Kharkevich Institute); 19, Bol’shoy Karetnyy lane, Moscow, 127051, Russian Federation; associate professor of the Department of Eye Diseases, Medical Biologial University of Innovations and Continuous Education of the A.I. Burnazyan Federal Medical Biophysical Center of the Federal Medical Biological Agency of Russia; 46, build. 8, Zhivopisnaya str., Moscow, 123098, Russian Federation; ORCID iD 0000-0001-6764-8950.
Armine S. Gevorkyan — applicant of the Federal Scientific and Clinical Center of the Federal Medical Biological Agency of Russian Federation; 91, Volokolamskoe road, Moscow, 125310, Russian Federation; ORCID iD 0000-0003-0773-1933.
Tatyana E. Borisenko — consultant for evidence-based medicine, M.M. Krasnov Research Institute of Eye Diseases; 11A, B, Rossolimo str., Moscow, 119021, Russian Federation.
Contact information: Vera G. Likhvantseva, e-mail: likhvantseva-4@yandex.ru.
Financial Disclosure: the study was conducted within the framework of the research work (cipher: «Proftrud-2», No. 10.020.21.800).
There is no conflict of interest.
Received 07.09.2023.
Revised 02.10.2023.
Accepted 25.10.2023.
материал rmj.ru
