Введение
Уровень выживаемости крайне недоношенных детей в последние годы значительно повысился благодаря улучшению методов неонатальной интенсивной терапии. При этом исходы психомоторного развития (ПМР) у данной группы детей остаются недостаточно изученными [1]. Около 50% детей, рожденных крайне недоношенными, имеют пограничные и грубые задержки этапов ПМР к 2 годам жизни [2].
К факторам риска неблагоприятного исхода ПМР относят гестационный возраст (ГВ), тяжелый респираторный дистресс-синдром (РДС), некротизирующий энтероколит, бронхолегочную дисплазию (БЛД), гемодинамически значимый функционирующий артериальный проток (ГЗФАП) и постнатальную задержку роста в первые месяцы жизни [3–6].
Недостаточная прибавка массы тела у детей после преждевременных родов ассоциирована с задержкой ПМР в последующие годы наблюдения [7–9]. При этом динамика роста окружности головы (ОГ) в большей степени соотносится с когнитивными исходами, поскольку размер головы связан с размером головного мозга и созреванием коры больших полушарий к возрасту 3 лет [10, 11]. Однако лишь единичные исследования показывают важность оценки динамики роста ОГ именно в 1-й месяц жизни как в особенный период развития незрелого головного мозга [11, 12]. В ряде работ проводились замеры ОГ при рождении и каждую неделю в течение 1-го месяца жизни. В лонгитюдных исследованиях по траекториям роста ОГ выделялись подгруппы детей, демонстрирующие различные модели развития [11, 14, 15], что побудило нас к подобному анализу.
Цель исследования: изучить взаимосвязь траектории роста ОГ в 1-й месяц жизни у детей, рожденных крайне недоношенными, с исходами ПМР к возрасту 3 лет.
Содержание статьи
Материал и методы
Было проведено ретроспективное когортное исследование, в которое было включено 140 детей.
Критерии включения: масса тела ребенка при рождении менее 1000 г; ребенок рожден на территории Ярославской области в период с 2012 по 2018 г. и находился под наблюдением специалистов амбулаторного отделения для детей раннего возраста ГБУЗ ЯО «Областной перинатальной центр».
Критерии невключения: «маловесный» для гестационного возрата плод, малый размер плода для гестационного возраста, наличие генетических синдромов и тяжелых поражений ЦНС (внутрижелудочковое кровоизлияние 3–4-й степени, перивентрикулярная лейкомаляция, гидроцефалия).
Антропометрические показатели оценивались по шкалам INTERGROWTH-21 на ГВ при рождении и на постконцептуальный возраст (ПКВ) на момент выписки из стационара.
Данные замеров ОГ при рождении использовались как базовые показатели, а через 1 мес. формировались подгруппы детей с учетом процентного увеличения ОГ за этот промежуток времени.
Дети, имеющие прибавку ОГ менее 4% к значению при рождении, составили группу замедленного роста; от 4 до 10% — группу догоняющего роста; более 10% — группу быстрого догоняющего роста ОГ.
Для выявления причин, влияющих на формирование динамики роста ОГ в 1-й месяц жизни, использовался многофакторный анализ, который включал в себя оценку перинатальных и неонатальных факторов риска, а также заболевания в неонатальном периоде.
Психомоторное развитие детей оценивали на момент посещения ребенком врача-педиатра в возрасте 3 лет с использованием шкалы «КАТ-КЛАМС». Шкала позволяет оценить формирование навыков по трем основным линиям: «КЛАМС» (язык/речь), «КАТ» (решение задач) и «Моторика» [13]. Результаты анализировали по каждой линии отдельно. Исходы ПМР были определены как норма, диссоциация развития (различия показателей шкалы «КАТ-КЛАМС» и моторики) и задержка.
Сбор данных и их систематизация проводились в таблицах Microsoft Office Excel (2007). Статистическая обработка данных выполнялась в программах Statistica 10 и Medcalc. Используя критерий Шапиро — Уилка, было установлено, что количественные показатели не соответствуют нормальному распределению, поэтому в дальнейшем применялись непараметрические статистические методы. Для описания распределения использовались медианы и интерквартильные размахи. Для сравнения выборок применялся многофакторный дисперсионный анализ ANOVA и метод множественной логистической регрессии. Статистически значимыми считали различия при p<0,05.
Результаты исследования
На основании траекторий прибавки ОГ в 1-й месяц жизни выявлены три различные модели роста: замедленный рост (n=37; 26,4%), догоняющий рост (n=69; 49,3%) и быстрый догоняющий рост (n=34; 24,3%).
В группе замедленного роста ОГ максимальный прирост показателя составил 3,9% от измерения при рождении; в группе догоняющего роста — от 4 до 10%, в группе быстрого догоняющего роста — более 10%.
Оценка ПМР крайне недоношенных детей в возрасте 3 лет показала, что нормальное ПМР наблюдалось у 55 (39,3%) обследованных, диссоциация развития — у 27 (19,3%), задержка — у 58 (41,4%).
Нами выявлены существенные различия в показателях ПМР обследованных детей в зависимости от темпов прибавки ОГ за 1-й месяц жизни (табл. 1).
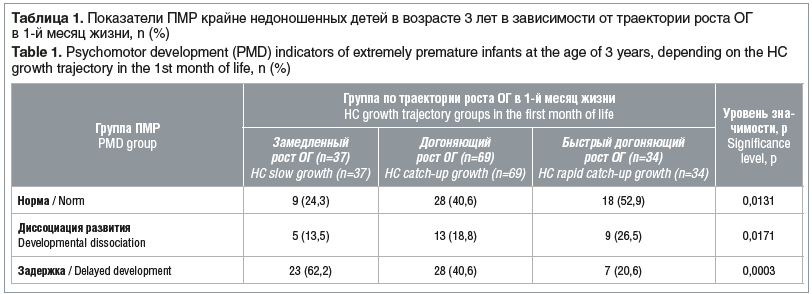
Согласно представленным данным процент детей с нормальным ПМР в группе быстрого догоняющего роста ОГ был наивысшим и составил 52,9%; в группе замедленного роста ОГ — наименьшим и равнялся 24,3% (p=0,0131). У детей с догоняющей траекторией роста ОГ в 1-й месяц после рождения нормальное ПМР в возрасте 3 лет зарегистрировано в 40,6% случаев.
Задержка ПМР статистически значимо чаще определялась в группах детей с догоняющим и замедленным ростом ОГ (p=0,0003). При этом диссоциация развития более характерна для детей с быстрым догоняющим ростом ОГ (см. табл. 1).
Нами проведен сравнительный анализ факторов риска у крайне недоношенных детей с разными траекториям роста ОГ в 1-й месяц после рождения, получены значимые различия по таким показателям, как ГВ, масса тела при рождении, ОГ при рождении, длительность нахождения на искусственной вентиляции легких (ИВЛ), наличие БЛД, ГЗФАП, постнатальная задержка роста плода (дефицит массы тела на ПКВ при выписке из стационара), способ вскармливания (табл. 2).
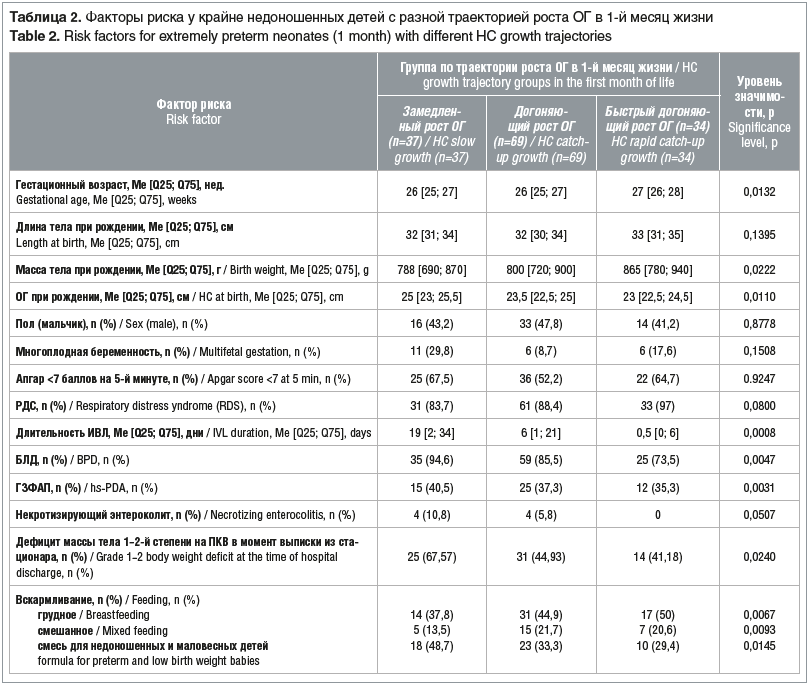
Результаты однофакторного логистического регрессионного анализа с последующим использованием пошагового отбора выявили значительную степень зависимости траектории роста ОГ в 1-й месяц жизни у обследованных детей от таких показателей, как ГВ при рождении, масса тела при рождении, ОГ при рождении и наличие ГЗФАП (табл. 3).
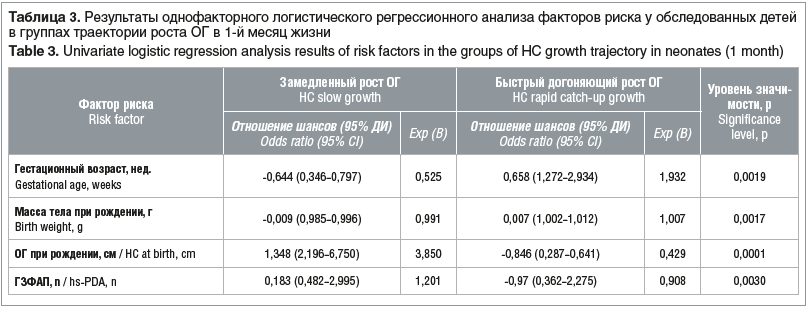
Исходя из значений регрессионных коэффициентов, быстрый догоняющий рост ОГ напрямую связан с ГВ и массой тела при рождении. При увеличении ГВ на 1 нед. шанс догоняющего роста ОГ увеличивается в 1,9 раза. Увеличение массы тела при рождении на 1 г увеличивает шанс быстрого догоняющего роста в 1,007 раза. При этом была выявлена обратная взаимосвязь между быстрым догоняющим ростом ОГ и ГЗФАП.
Кроме этого, нами проанализирована взаимосвязь траектории роста ОГ в 1-й месяц жизни и показателей физического развития (ФР) детей на момент выписки из стационара (табл. 4).
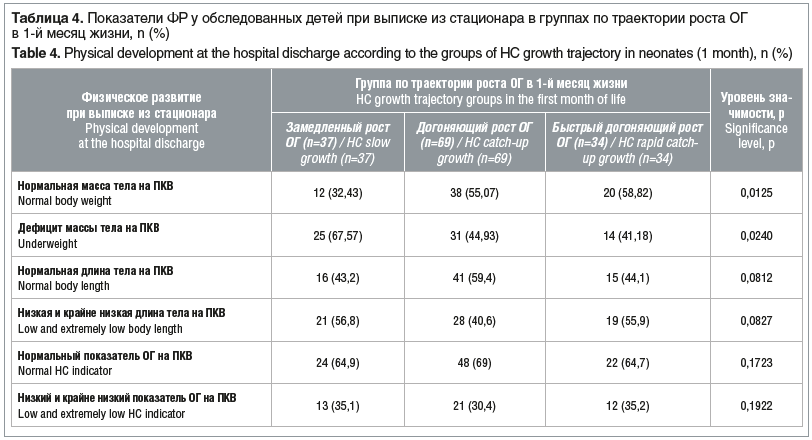
Как видно из представленных данных, дети с догоняющим и быстрым догоняющим ростом ОГ в 1-й месяц после рождения чаще имеют нормальную массу тела на ПКВ при выписке из стационара. В то же время дети с замедленным ростом ОГ в последующем чаще выписываются с дефицитом массы 1-й и 2-й степени на ПКВ, что указывает на постнатальную задержку роста (см. табл. 4).
Статистически значимых различий в группах по траекториям роста ОГ в 1-й месяц жизни и показателям длины тела и ОГ на момент выписки не было установлено.
Обсуждение
По данным литературы, недостаточный прирост ОГ у недоношенных детей в первые 2 года жизни ассоциируется с задержкой ПМР в возрасте 1,5 и 2 лет [4, 5, 7, 11]. При этом, как правило, используются популяционные нормативы ОГ при рождении, а изменения показателя Z-score оцениваются относительно здорового «эталонного» плода. Для недоношенных детей, получающих лечение в ОРИТ, прирост ОГ с использованием Z-score не может отражать реальную динамику у каждого конкретного ребенка. Для группы крайне недоношенных детей важен анализ фактической прибавки ОГ за 1-й месяц жизни, когда наблюдаются резкие изменения роста и велико влияние осложнений и вмешательств, предпринятых по поводу незрелости органов и систем.
Изучение траектории роста ОГ в 1-й месяц жизни у детей, рожденных крайне недоношенными, и анализ причин, влияющих на траекторию роста ОГ, являются весьма актуальными, так как позволяют выделить группы риска по отставанию в ПМР в раннем возрасте.
В нашей работе были сформированы подгруппы недоношенных детей путем выявления однородных кластеров при разнородных данных, которые имели схожие измерения размеров головы в 1-й месяц жизни [15]. Моделирование, основанное на группах, определяет не только подгруппы по росту ОГ в 1-й месяц жизни, но и прогнозирует соответствующий уровень ПМР в катамнезе.
В исследование не были включены дети «маловесные» и «маленькие» для ГВ, так как у них другие траектории роста, другие процессы нейросозревания и исходы ПМР по сравнению с недоношенными без указаний на недостаточные показатели массы и роста [16, 17].
С учетом траектории прибавки ОГ в 1-й месяц жизни нами выявлены три различные модели роста ОГ крайне недоношенных детей: замедленный рост, догоняющий рост и быстрый догоняющий рост. На основании траекторий роста ОГ были выделены подгруппы, которые значительно отличаются по исходам ПМР в первые 3 года жизни.
Так, в группе детей с быстрым догоняющим ростом ОГ больше половины (52,9%) имеют нормальное ПМР, а в группе с замедленным ростом ОГ — только четверть (24,3%). Дети из группы замедленного роста ОГ имеют самый высокий процент отставания в ПМР по сравнению с двумя другими группами: 62,2% против 40,6% и 20,6% соответственно.
Таким образом, динамика роста ОГ в 1-й месяц жизни ассоциирована с последующими исходами когнитивного развития.
В свою очередь, доказано влияние на рост ОГ таких показателей, как ГВ, масса тела при рождении, ОГ при рождении, длительность нахождения на ИВЛ, наличие БЛД, ГЗФАП, постнатальная задержка роста плода (дефицит массы тела на ПКВ при выписке из стационара), способ вскармливания.
Одними из наиболее значимых факторов являются ГВ и масса тела при рождении. Крайне недоношенные дети, рожденные на 27–28-й неделе гестации, чаще имеют быстрый догоняющий рост ОГ, чем дети, рожденные в более ранние сроки. Масса тела при рождении имеет прямое влияние на возможную траекторию роста ОГ. Дети с массой тела при рождении от 780 до 940 г чаще имеют быстрый догоняющий рост ОГ. Для детей с меньшей массой тела при рождении характерен замедленный рост ОГ в 1-й месяц жизни.
ОГ при рождении предопределяет потенциал роста ОГ в дальнейшем: чем меньше ОГ при рождении, тем чаще отмечается ее быстрый догоняющий рост. ОГ при рождении 25 см и более увеличивает шансы замедленного роста ОГ в 3,8 раза.
По нашим данным, замедленный рост ОГ в 1-й месяц жизни чаще встречается у детей с ГЗФАП и сформировавшейся БЛД в будущем. Известно, что ГЗФАП нарушает гемодинамику и может изменять легочную механику.
Длительность ИВЛ связана с возникновением БЛД и ее тяжестью [18]. Кроме того, субоптимальная церебральная оксигенация вследствие ГЗФАП и формирующейся БЛД в критический период жизни могут негативно влиять на рост мозга и исходы развития нервной системы [19].
Оптимальное вскармливание, особенно достаточное поступление общего числа килокалорий и достаточное количество белка, предопределяет рост ОГ и влияет на ПМР недоношенных детей в раннем возрасте [12, 20]. По результатам исследования, в группе быстрого догоняющего роста ОГ половина детей (50,0%) получала грудное молоко вместе с частичным парентеральным питанием, при этом в группе замедленного роста ОГ 48,7% детей находились на искусственном вскармливании с частичным парентеральным питанием. Следовательно, необходимы крупные мультицентровые исследования для рандомизированного клинического изучения влияния различных вариантов лечебного питания на рост ОГ у крайне недоношенных детей в течение 1-го месяца жизни и когнитивные исходы.
Известно, что ПМР не является постоянным показателем на протяжении всего периода взросления ребенка, что крайне недоношенные дети могут догонять по своему развитию сверстников в разные периоды жизни. В нашей работе почти четверть детей в группе замедленного роста ОГ имеют нормальное ПМР. Это свидетельствует о том, что замедленный рост ОГ в 1-й месяц жизни не всегда связан с плохими исходами. Изменение структурных взаимосвязей головного мозга может лежать в основе траекторий роста ОГ в раннем возрасте и предопределять исходы ПМР к 3 годам жизни [21, 22].
Психомоторное развитие является длительным и динамическим процессом, на который влияют различные факторы, которые могут по-разному распределяться во времени. После выписки из стационара социально-экономический статус родителей и методы ухода будут играть важную роль в развитии нервной системы недоношенного ребенка [23]. Окружающая среда, физические упражнения, умственная стимуляция и социальные взаимодействия могут улучшить прогноз ПМР недоношенных детей [24].
Таким образом, имея возможность выделения групп высокого риска еще в возрасте 1 мес. жизни, можно улучшить прогноз долгосрочных перспектив ПМР детей, обучая матерей и планируя мероприятия по раннему вмешательству и дальнейшей реабилитации. Оценка ПМР в первые 2–3 года жизни позволяет спрогнозировать когнитивные функции недоношенных детей в дошкольном возрасте [23–25].
Заключение
Крайне недоношенные дети с замедленным ростом ОГ в 1-й месяц жизни имеют неблагоприятный прогноз по ПМР в первые 3 года жизни. Важно оценивать не только динамику прибавки массы тела, но и более детально отмечать рост ОГ, начиная с этапа отделения реанимации и интенсивной терапии новорожденных.
В зарубежных исследованиях доказана важность измерения ОГ каждую неделю на 1-м месяце жизни. Это позволяет определить траекторию роста ОГ и повлиять на модифицируемые факторы, например на получаемое ребенком питание. Дети, получавшие грудное молоко через зонд, в дальнейшем чаще имеют быстрый догоняющий рост ОГ и более высокие показатели ПМР к 3 годам жизни по сравнению с получавшими смесь для недоношенных и маловесных детей.
Распределение крайне недоношенных детей на группы по траекториям роста ОГ в 1-й месяц жизни можно использовать в качестве маркера для более поздних нарушений ПМР. Что еще более важно, данный подход может быть применен для выделения группы высокого риска с целью раннего вмешательства в развитие нервной системы и смягчения неблагоприятных долгосрочных последствий.
Сведения об авторах:
Щербакова Валентина Петровна — аспирант кафедры педиатрии ИНПО ФГБОУ ВО ЯГМУ Минздрава России; 150000, Россия, г. Ярославль, ул. Революционная, д. 5; врач-педиатр амбулаторного отделения для детей раннего возраста ГБУЗ ЯО «Областной перинатальный центр»; 150042, Россия, г. Ярославль, Тутаевское ш., д. 31в; ORCID iD 0000-0002-6921-5689.
Мозжухина Лидия Ивановна — д.м.н., профессор, заведующая кафедрой педиатрии ИНПО ФГБОУ ВО ЯГМУ Мин-здрава России; 150000, Россия, г. Ярославль, ул. Революционная, д. 5; ORCID iD 0000-0003-2153-8662.
Строева Лариса Емельяновна — к.м.н., доцент кафедры педиатрии ИНПО ФГБОУ ВО ЯГМУ Минздрава России; 150000, Россия, г. Ярославль, ул. Революционная, д. 5; ORCID iD 0000-0002-0921-8212.
Калгина Светлана Евгеньевна — ассистент кафедры педиатрии ИНПО ФГБОУ ВО ЯГМУ Минздрава России; 150000, Россия, г. Ярославль, ул. Революционная, д. 5; врач-анестезиолог-реаниматолог ГБУЗ ЯО «Областной перинатальный центр»; 150042, Россия, г. Ярославль, Тутаевское ш., д. 31в; ORCID iD 0000-0003-4242-5835.
Кисельникова Ольга Викторовна — к.м.н., доцент кафед-ры педиатрии ИНПО ФГБОУ ВО ЯГМУ Минздрава России; 150000, Россия, г. Ярославль, ул. Революционная, д. 5; ORCID iD 0000-0002-1722-8285.
Контактная информация: Щербакова Валентина Петровна, e-mail: thanatolog@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 15.02.2023.
Поступила после рецензирования 13.03.2023.
Принята в печать 03.04.2023.
About the authors:
Valentina P. Shcherbakova — post-graduate student of the Department of Pediatrics, Yaroslavl State Medical University; 5, Revolutsionnaya str., Yaroslavl, 150000, Russian Federation; pediatrician of the Outpatient Department for Infants, Regional Perinatal Center; 31V, Tutaevskoe Lane, Yaroslavl, 150042, Russian Federation; ORCID iD 0000-0002-6921-5689.
Lidiya I. Mozzhukhina — Dr. Sc. (Med.), Professor, Head of the Department of Pediatrics, Yaroslavl State Medical University; 5, Revolutsionnaya str., Yaroslavl, 150000, Russian Federation; ORCID iD 0000-0003-2153-8662.
Larisa E. Stroeva — C. Sc. (Med.), Associate Professor of the Department of Pediatrics, Yaroslavl State Medical University; 5, Revolutsionnaya str., Yaroslavl, 150000, Russian Federation; ORCID iD 0000-0002-0921-8212.
Svetlana E. Kalgina — Assistant Professor of the Department of Pediatrics, Yaroslavl State Medical University; 5, Revolutsionnaya str., Yaroslavl, 150000, Russian Federation; anesthesiologist-resuscitator, Regional Perinatal Center; 31V, Tutaevskoe Lane, Yaroslavl, 150042, Russian Federation; ORCID iD 0000-0003-4242-5835.
Olga V. Kiselnikova — C. Sc. (Med.), Associate Professor of the Department of Pediatrics, Yaroslavl State Medical University; 5, Revolutsionnaya str., Yaroslavl, 150000, Russian Federation; ORCID iD 0000-0002-1722-8285.
Contact information: Valentina P. Shcherbakova, e-mail: thanatolog@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 15.02.2023.
Revised 13.03.2023.
Accepted 03.04.2023.
Информация с rmj.ru






