Итоприд как ключевой элемент
лечения функциональной (неязвенной) диспепсии у
взрослых
И.Г. Никитин, А.М. Алиева
Кафедра госпитальной терапии №2 им. акад. Г.И.
Сторожакова
Лечебного факультета ФГАОУ ВО “Российский
национальный исследовательский медицинский
университет им. Н.И. Пирогова” Минздрава России,
Москва
В статье приводятся сведения о клинических
проявлениях, эпидемиологии и патогенетических
механизмах формирования функциональной (неязвенной)
диспепсии у взрослых. Также представлены данные
проведенного исследования по клинической
эффективности, безопасности и переносимости
гастропрокинетика Итоприд-СЗ у взрослых пациентов
с диагностированной функциональной диспепсией.
Ключевые слова: функциональная (неязвенная)
диспепсия, синдром абдоминальной боли,
постпрандиальная диспепсия, Итоприд-СЗ
Функциональная (неязвенная) диспепсия (ФД)
– комплекс жалоб, включающих в себя боль и
ощущение жжения в подложечной области, ощущение
переполнения в эпигастрии после еды и раннее
насыщение, которые отмечаются у пациента в
последние 3 мес (при общей продолжительности не
менее 6 мес) и которые не могут быть объяснены
органическими причинами. Диагноз ФД обсуждается в
тех случаях, когда у больного отсутствуют
органические заболевания (язвенная болезнь желудка
и двенадцатиперстной кишки, опухоли, хронический
панкреатит, хронические заболевания желчевыводящих
путей и др.), позволяющие отнести имеющиеся жалобы
к так называемой группе “органической диспепсии”,
или “вторичной диспепсии”. В последней версии
рекомендаций международного консенсуса Римские
критерии IV (Rome IV), опубликованной в 2016 г.,
ФД рассматривается как один из составляющих
элементов так называемой группы функциональных
гастроинтестинальных расстройств. В свою очередь,
функциональные гастроинтестинальные расстройства в
Римских критериях IV определяются как расстройства
взаимодействия желудочно-кишечный
тракт–центральная нервная система [1].
Функциональные гастроинтестинальные расстройства
включают в себя 4 группы функциональных нарушений:
- группа 1 – ФД (подгруппа 1a –
постпрандиальный дистресс-синдром; подгруппа 1b
– эпигастральный болевой синдром); - группа 2 – расстройства отрыгивания
(подгруппа 2a – чрезмерная супрагастральная
отрыжка; подгруппа 2b – чрезмерная желудочная
отрыжка); - группа 3 – тошнотные и рвотные расстройства
(подгруппа 3a – синдром хронической тошноты и
рвоты; подгруппа 3b – цикличный рвотный синдром;
подгруппа 3с – синдром чрезмерной канабиоидной
рвоты); - группа 4 – руминационный синдром.
Справедливости ради следует подчеркнуть, что
для единообразия терминологического восприятия в
последних Римских критериях IV вместо термина
“органическая диспепсия” всё же рекомендовано
использовать термин “вторичная диспепсия” [1].
По данным современных эпидемиологических
исследований, те или иные диспепсические жалобы
отмечаются у 26–41% населения. В Российской
Федерации, по результатам проведенных
исследований, распространенность ФД может
достигать 30–40%, причем указанное заболевание
встречается достоверно чаще в молодом возрасте
(17–35 лет), а женщины страдают этим расстройством
практически в 2 раза чаще мужчин. При этом
необходимо отметить, что приведенные показатели
распространенности диспепсических жалоб в
популяции относятся к так называемой
“неисследованной диспепсии”, истинная же
распространенность ФД, вероятно, составляет 2–7%
среди пациентов, приходящих на прием к врачу общей
практики [2].
В зависимости от клинической картины различают 3
варианта ФД:
1) язвенноподобный (превалируют боли, напоминающие
по локализации и выраженности боли при язвенной
болезни желудка или двенадцатиперстной кишки);
2) дискинетический (превалируют ощущение тяжести
после еды, вздутие живота, тошнота);
3) неспецифический или недифференцированный (нет
четкого превалирующего компонента, а симптомы
имеют смешанный характер).
Большое значение в реализации патофизиологических
механизмов развития ФД придается таким факторам,
как:
- гиперсекреция соляной кислоты;
- алиментарные погрешности;
- психогенные факторы;
- нарушение моторики желудочно-кишечного
тракта (пищеводно-желудочный рефлюкс, замедление
эвакуации из желудка, нарушение
антродуоденальной координации); - снижение порога чувствительности стенки
желудка к растяжению; - инфекция Helicobacter pylori.
Определенная роль в развитии ФД отводится
генетическим факторам. К настоящему времени
установлено, что полиморфизм гена GNβ3 (guanine
nucleotide binding protein beta 3 –
гуанин-нуклеотидсвязывающий белок бета-3), а
именно аллель rs5443 (C825T) тесно связан с
развитием ФД, а его гомозиготная мутация с
генотипом СС практически в 2 раза чаще встречается
в обсуждаемой группе пациентов, чем гетерозиготный
генотип СТ или гомозиготный вариант без
соответствующей нуклеотидной замены. Было также
отмечено, что при наличии генотипа CC гена GNβ3 в
значительной степени нарушается чувствительность
рецепторов к нейротрансмиттерам, стимулирующим
двигательную функцию желудка, например
5-НТ4-рецепторов, широкой подгруппы семейства
рецепторов к серотонину. При этом надо напомнить,
что именно нарушение двигательной функции верхних
отделов желудочно-кишечного тракта является
ключевым фактором, определяющим как клинические
проявления ФД, так и патогенетические звенья ее
развития [1, 3–6]. Следует отметить, что реальная
клиническая проблема ФД, ее медико-социальное
значение заключаются прежде всего в низком или
значительно сниженном качестве жизни пациентов
[4–6]. В связи с этим важно добиваться воздействия
на различные звенья патогенеза развития ФД, а
таких возможностей на самом деле совсем немного в
современном фармакологическом арсенале
гастроэнтерологов и терапевтов.
Исходя из изложенного, мы считаем актуальным
представить результаты собственного исследования,
в котором оценивались переносимость, клиническая
эффективность и побочные эффекты отечественного
препарата Итоприд-СЗ у взрослых пациентов с ФД.
Клиническое исследование проводилось на базе ФГАУ
“Национальный медицинский исследовательский центр
“Лечебно-реабилитационный центр” Минздрава России.
Исследование было одобрено локальным комитетом по
этике, проведено в строгом соответствии с
протоколом исследования.
Цель исследования – оценка клинической
эффективности и переносимости препарата Итоприд-СЗ
у пациентов с диагностически верифицированной ФД.
Характеристика и вид исследования: простое
сравнительное исследование в репрезентативных
группах с использованием группы сравнения.
Исследуемый лекарственный препарат:
Итоприд-СЗ – коммерческий вариант итоприда
гидрохлорида (итоприда), являющегося
гастропрокинетиком с двойным механизмом действия –
антагонизмом к дофаминовым D2-рецепторам и
ингибированием ацетилхолинэстеразы. Таким образом,
в результате действия итоприда увеличивается
концентрация ацетилхолина, что приводит к усилению
моторики желудка, повышению тонуса нижнего
пищеводного сфинктера, ускорению процесса
опорожнения желудка и улучшению гастродуоденальной
координации. Итоприд также оказывает четко
выраженный противорвотный эффект за счет
взаимодействия с дофаминовыми D2-рецепторами,
расположенными в хеморецепторной триггерной зоне
продолговатого мозга.
Материал и методы
Обследовано 60 пациентов с диагностированной ФД
(25 мужчин, 35 женщин) в возрасте от 18 до 39 лет
(средний возраст 25,6 ± 13,7 года). Учитывая
диагностические критерии ФД, пациенты были
обследованы по протоколу, позволяющему прежде
всего исключить органическую диспепсию.
Обследование включало в себя клинический анализ
крови, биохимический анализ крови (аспартатаминотрансфераза
(АСТ), аланинаминотрансфераза (АЛТ), γ-глутамилтранспептидаза
(ГГТП), щелочная фосфатаза (ЩФ), билирубин и
фракции, глюкоза, мочевина, креатинин, холестерин
(ХС) общий, ХС липопротеидов высокой плотности, ХС
липопротеидов низкой плотности), ультразвуковое
исследование органов брюшной полости,
эзофагогастродуоденоскопию, дополненную
исследованием на наличие Helicobacter pylori,
электрогастрографию (ЭГГ), гастродуоденальную
манометрию, исследование кала на скрытую кровь,
общий анализ мочи, стандартную 12-канальную
электрокардиографию (ЭКГ), заполнение Европейского
опросника по оценке качества жизни (European
Quality of Life 5 Dimensions 3 Level Version,
EQ-5D-3L). Были намечены контрольные визиты,
предусматривающиеся протоколом исследования в
каждой временной точке, а именно:
- визит 0 (в течение 14 дней до начала
исследования) – подписание пациентом
информированного согласия на все перечисленные
выше исследования, сопоставление
анамнестических, клинических и инструментальных
данных обследований, данных физикального осмотра
с критериями включения и исключения,
установленных протоколом исследования; - визит 1 (1-й день) – заполнение опросника
EQ-5D-3L, клиническая оценка данных физикального
осмотра, клинический и биохимический анализы
крови, ЭКГ, общий анализ мочи, ЭГГ. Назначение
исследуемого препарата по утвержденной
протоколом исследования схеме – 50 мг 3 раза в
день за 30 мин до еды у пациентов в основной
группе; - визит 2 (14-й день) – заполнение опросника
EQ-5D-3L, клиническая оценка данных физикального
осмотра, клинический и биохимический анализы
крови, ЭКГ, общий анализ мочи, ЭГГ. Оценка
приверженности лечению, предписанному протоколом
исследования, с использованием дневника приема
препарата; - визит 3 (21-й день) – заполнение опросника
EQ-5D-3L, клиническая оценка данных физикального
осмотра, клинический и биохимический анализы
крови, ЭКГ, ЭГГ, оценка приверженности лечению,
предписанному протоколом исследования, с
использованием дневника приема препарата.
Формирование базы данных, оценка полученных
результатов осуществлялись c использованием
стандартной программы Statistica 2.0. В качестве
основного статистического метода применялась
оценка параметрических значений в репрезентативных
группах с использованием средних значений и
квадратического отклонения, статистически
значимыми считались результаты при значении р
Результаты исследования и их
обсуждение
Дизайн исследования предполагал формирование 2
клинических групп: 1-я группа – 30 пациентов,
получавших в качестве лекарственного препарата
Итоприд-СЗ в дозе 50 мг 3 раза в день на фоне
соблюдения стандартных диетических рекомендаций;
2-я группа – 30 пациентов, соблюдавших
исключительно диетические рекомендации и не
получавших никаких иных лекарственных средств.
Половозрастная характеристика пациентов обеих
групп представлена в табл. 1.

Из табл. 1 следует, что сравниваемые группы
были репрезентативны и не отличались друг от друга
по возрасту. При этом в 1-й группе преобладали
женщины, в то время как во 2-й группе
распределение пациентов по полу было одинаковым.
Проведенный комплекс лабораторных и
инструментальных исследований, а также
анамнестические данные позволили подтвердить
диагноз ФД. Клинические варианты ФД у пациентов
обеих групп представлены в табл. 2.
Как следует из данных, представленных в табл. 2,
частота встречаемости клинических вариантов ФД
была одинаковой – постпрандиальная диспепсия (ППД)
имела место у 14 пациентов 1-й группы и у 14
пациентов 2-й группы (p > 0,005), синдром
эпигастральной боли (СЭБ) – у 16 и 16 пациентов
соответственно. А вот распределение клинических
вариантов ФД по полу достоверно различалось. Так,
у женщин в обеих группах частота выявления ППД
была достоверно выше в сравнении с СЭБ:
соответственно, у 12 из 20 и у 8 из 20 (p
Достоверных различий по результатам клинического и
биохимического анализов крови, инструментальных
методов обследования (ультразвуковое исследование
органов брюшной полости), ЭКГ на старте включения
пациентов в исследование выявлено не было. При
этом следует остановиться на результатах ЭГГ у
обследованных. В норме частота сокращения желудка
составляет 2,8–3,3 волны в 1 мин, значение этого
показателя 3,6 волны в 1 мин – как тахигастрия.
В табл. 3 представлены данные ЭГГ пациентов обеих
групп.

В целом нормальные показатели сократимости
желудка были выявлены только у 5 пациентов 1-й
группы (1 мужчина, 4 женщины) и у 3 пациентов 2-й
группы (2 мужчины, 1 женщина). У мужчин обеих
групп наиболее часто встречалась брадигастрия (у 7
из 10 мужчин 1-й группы и у 9 из 15 мужчин 2-й
группы), в то время как у женщин преобладала
тахигастрия (у 13 из 20 женщин 1-й группы и у 11
из 15 женщин 2-й группы), таким образом,
выявленные различия по полу и результатам ЭГГ были
достоверными в обеих группах: для мужчин наиболее
характерным являлся брадигастрический вариант ЭГГ,
часто сочетающийся с клиническим вариантом ФД СЭБ,
в то время как для женщин – тахигастрия,
ассоциирующаяся с клиническим вариантом ФД ППД.
Анализируя клиническую эффективность Итоприда-СЗ у
пациентов, мы сознательно не вводили режим
плацебо, а в качестве базисной терапии в обеих
группах были выбраны исключительно диетические
мероприятия. Это было сделано с той целью, чтобы,
с одной стороны, исключить необходимость анализа
межлекарственных взаимодействий, а с другой –
получить наиболее объективную картину клинической
эффективности исследуемого препарата.
Интересными оказались результаты тестирования
пациентов с использованием опросника EQ-5D-3L. Все
пациенты отмечали боль и дискомфорт той или иной
степени выраженности (от 1 до 2 баллов), а тревога
и депрессия регистрировались у 21 пациента (70%)
(3 мужчины (10%), 18 женщин (60%); p
При анализе приема препарата за весь период
клинического исследования было установлено
следующее. Не было выявлено ни одного серьезного
нежелательного явления, ни один пациент 1-й группы
не прекратил прием препарата и не пропустил ни
одной дозы рекомендованного приема. Среди
зарегистрированных побочных явлений у 4 пациентов
отмечались кратковременное сердцебиение и
покраснение лица. Все эти побочные явления
упомянуты в официальной инструкции к
лекарственному препарату, они носили
кратковременный характер и не повлияли на
продолжение приема исследуемого средства –
Итоприда-СЗ. Динамика клинических и
инструментальных показателей пациентов обеих групп
приведена в табл. 4.
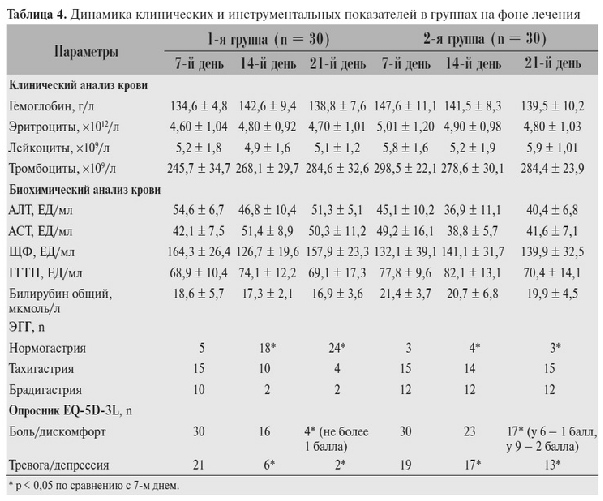
Представленные в табл. 4 данные позволили
сделать следующие важные выводы. Во-первых,
препарат Итоприд-СЗ обладает хорошей
переносимостью и выраженной клинической
эффективностью. Были установлены статистически
значимые различия по частоте и выраженности ярких
симптомов ФД, таких боль и дискомфорт, а также
тревоги и депрессии между основной группой и
группой сравнения. Во-вторых, как минимум на
протяжении всего периода наблюдения не было
выявлено признаков гемотоксичности и
гепатотоксичности.
Функциональная диспепсия – клиническое состояние,
значительно снижающее качество жизни пациентов.
Исходя из более или менее изученных к сегодняшнему
дню патогенетических механизмов развития ФД, мы
четко должны представлять себе, что ведение таких
пациентов требует глубоких профессиональных
навыков не только гастроэнтерологов и терапевтов,
но и психиатров, физиотерапевтов, курортологов,
реабилитологов и врачей иных специальностей. Это
сложные пациенты, как правило ищущие у себя
“серьезное” заболевание и уходящие разочарованными
после того, как доктор сообщает им: “Это у вас всё
от головы”. Тем не менее пациент часто тревожен,
активно ищет помощи, меняет врачей. В таких
случаях важно иметь под рукой надежный,
нетоксичный, хорошо переносимый лекарственный
препарат, воздействующий хотя бы на одну из
патогенетических составляющих ФД. Именно таким
препаратом выбора (а зачастую единственным
препаратом) в лечении ФД, по нашим данным,
является Итоприд-СЗ, продемонстрировавший свою
безопасность и клиническую эффективность в
представленном клиническом исследовании.
Список литературы /
References
- Stanghelini V. Functional dyspepsia and
irritable bowel syndrome: beyond Rome IV.
Digestive Diseases (Basel, Switzerland).
2017;35(Suppl 1):14-17. DOI: 10.1159/000485408 - Скворцов В.В., Потапова М.В., Скворцов К.Ю.,
Федорова О.Ф. Современные проблемы диагностики и
лечения функциональной (неязвенной) диспепсии.
Экспериментальная и клиническая
гастроэнтерология. 2016;2(126):56-63. [Skvortsov
VV, Potapova MV, Skvortsov KYu, Fedorova OF.
Modern problems of diagnosis and treatment of
functional (non-ulcer) dyspepsia. Experimental
and Clinical Gastroenterology.
2016;2(126):56-63. (In Russ.).] DOI:
10.31146/1682-8658-ecg-2-56-63 - Fei D, Yaping L, Haitao S, Shugoing G, Jun S,
Lei D, Jingyun Y. Association of genetic
variants in GNβ3 with functional dyspepsia: a
meta-analysis. Digestive Diseases and Sciences.
2014;59(8):1823-1830. DOI:
10.1007/s10620-014-3057-y - Oh JH, Kwon JG. Functional dyspepsia. Korean
Journal of Gastroenterology. 2019;73(2):77-83.
DOI: 10.4166/kjg.2019.73.2.77 - Miwa H, Nagahara A, Asakawa A, Arai M, T
Oshima, Kasugai K, Kamada K, Suzuki H, Tanaka F,
Tominaga K, Futagami S, Hoji M, Mihara H,
Higuchi K, Kusano M, Arisawa T, Kato M, Joh T,
Mochida S, Enomoto N, Shimosegawa T, Koike K.
Evidence-based clinical practice guidelines for
functional dyspepsia. Journal Gastroenterology.
2022;57(2):47-61. DOI:
10.1007/s00535-021-01843-7 - Black CJ, Paine PA, Agrawal A, Aziz I,
Eugenicos ME, Houghton LA, Hungin P, Overshott R,
Hasant DV, Rudd Sh, Winning RC, Corsetti M, Ford
AC. British Society of Gastroenterology
guidelines on the management of functional
dyspepsia. Gut. 2022;71:1697-1723. DOI:
10.1136/gutjnl-2022-327737
Статья опубликована на сайте
http://www.gastroscan.ru
материал MedLinks.ru






