Эффективность, безопасность и комплаенс — три слагаемых успеха в снижении уровня холестерина
Содержание статьи
Введение
Сердечно-сосудистые заболевания (ССЗ) являются причиной более 4,3 млн смертей ежегодно в Европе, что составляет 54% всех случаев смерти среди женщин и 43% — среди мужчин. В 2016 г., по данным ВОЗ, от ССЗ умерли 17,9 млн человек, что составило 31% всех случаев смерти в мире. Из них 85% смертей произошло в результате инфаркта миокарда и инсульта — нозологий, четко ассоциированных с атеросклеротической болезнью. В России от ССЗ ежегодно умирают около 1 млн 300 тыс. человек, что составляет более чем 55% от числа всех смертей [1–4].
Основными формами ССЗ во всем мире и в России являются артериальная гипертония, ишемическая болезнь сердца (ИБС) и цереброваскулярные заболевания. Один из ведущих факторов патогенеза этих ССЗ — дислипидемия, которая вносит существенный вклад в общую и сердечно-сосудистую смертность. Стратегию лечения и профилактики дислипидемии составляют изменение образа жизни и назначение липидоснижающей терапии. К основным липидоснижающим препаратам относятся:
ингибиторы 3-гидрокси-3-метилглутарил-КоА-редуктазы (статины: розувастатин, аторвастатин, симвастатин и др.);
производные фиброевой кислоты (фибраты: активаторы липопротеинлипазы);
селективные ингибиторы абсорбции холестерина (ХС) (средства, угнетающие всасывание ХС в кишечнике, например эзетимиб);
препараты никотиновой кислоты (ингибиторы триглицеридлипазы);
секвестранты желчных кислот (ионообменные смолы);
омега 3-полиненасыщенные жирные кислоты;
ингибиторы пропротеин конвертазы субтилизин/кексин типа 9 (PCSK9) [5–8].
Бесспорно, самыми изученными и потому широко назначаемыми гиполипидемическими препаратами являются статины, которые тормозят прогрессирование ССЗ и достаточно результативны в их предотвращении. Они понижают плазменные уровни липопротеидов низкой плотности (ЛПНП) за счет подавления активности ГМГ-КоА-редуктазы — ключевого фермента в синтезе ХС. Подавление внутриклеточного синтеза ХС уменьшает его содержание в клетке. При истощении депо ХС в печени плотность липопротеиновых рецепторов в гепатоцитах увеличивается, что активирует рецептор-зависимый эндоцитоз холестеринсодержащих липопротеидов из плазмы крови, а также снижение синтеза липопротеидов очень низкой плотности. Конечным результатом этого становится уменьшение в плазме крови количества атерогенных липопротеидов [6–8].
Гиполипидемическая эффективность монотерапии статинами
Статины — одна из наиболее эффективных групп гиполипидемических средств. Тем не менее исследования показывают, что только 20–64% пациентов, принимающих статины, достигают целевых значений уровня ХС ЛПНП (табл. 1) — ключевого предиктора высокого риска развития ССЗ [9–16]. В то же время исследования показывают, что чем ниже достигнутый уровень ХС, тем выше клиническая и экономическая польза от лечения, по крайней мере для определенных групп пациентов с ССЗ [17–19].
![Таблица 1. Целевые уровни ХС ЛПНП для больных в зависимости от категории риска ССЗ [5, 20, 21] Таблица 1. Целевые уровни ХС ЛПНП для больных в зависимости от категории риска ССЗ [5, 20, 21]](https://medblog.su/wp-content/uploads/2019/09/effektivnost-bezopasnost-i-komplaens-tri-slagaemyh-uspeha-v-snizhenii-urovnya-holesterina-maksimov-m-l-obrezan-a-g-burashnikova-i-s-shikaleva-a-a.png)
По результатам российского многоцентрового эпидемиологического исследования по изучению распространенности факторов риска ССЗ в 13 регионах РФ — «ЭССЕ-РФ» [22], статины принимают только 9,7% больных ИБС от 25 до 64 лет (в группах высокого и очень высокого риска около 7% мужчин и 7,2% женщин регулярно принимают статины), из которых всего 9,2% (14,4% мужчин и 4,8% женщин) достигают целевых значений ХС ЛПНП [22, 23].
Также в исследовании T. Schleyer et al. [17] из 89 267 пациентов в возрасте >45 лет, принимавших статины, 33,7% не достигли рекомендованных целевых значений ХС ЛПНП, а в подгруппе высокого и очень высокого сердечно-сосудистого риска (подгруппа с вторичной профилактикой ССЗ, которые имели ССЗ до начала приема статинов или СД с признаками ИБС) не достигли целевых цифр ХС ЛПНП 58,1% пациентов.
В то же время рассчитано, что каждое снижение ЛПНП на 1,0 ммоль/л (38,67 мг/дл) снижает ежегодную частоту основных сосудистых событий, таких как инфаркт миокарда, реваскуляризация и ишемический инсульт, более чем на 20%. Теоретически рассчитанная потенциальная общая экономия затрат при гипотетическом достижении целевых значений ХС ЛПНП у каждого пациента составляет около 37 300 долл. США [17].
В исследовании P.H. Jones et al. [12] у пациентов повышенного риска ССЗ с ИБС или с ИБС в анамнезе при монотерапии статином >90 дней целевых уровней ХС ЛПНП <70 мг/дл достигали 20–26% пациентов, а уровня ХС ЛПНП <100 мг/дл — 67–77% [12].
Опубликованные результаты метаанализа VOYAGER (An indiVidual patient data metaanalysis Of statin therapY in At risk Groups: Effects of Rosuvastatin, atorvastatin and simvastatin) [24, 25], основанного на данных 32 258 пациентов, демонстрируют наилучшее достижение целевых значений ХС ЛПНП (<70 мг/дл или его снижения на 50%) на розувастатине 10–40 мг (43,8–79,0%) в сравнении с равной или удвоенной дозировкой аторвастатина (16,1–65,2%) или симвастатина (0–39,7%). При анализе выделенной когорты пациентов с СД (8859 (27,5%)) розувастатин оказался наиболее эффективным из трех назначаемых статинов как для снижения уровня ХС ЛПНП, так и для достижения целевого уровня <70 мг/дл для ХС ЛПНП. Он также был более эффективным, чем аторвастатин, в повышении уровня ХС ЛПВП в популяции больных СД (рис. 1) [24, 25]. При этом важно отметить, что конечные точки исходов сердечно-сосудистой патологии при достижении целевого уровня ЛПНП корректировались более существенно.
![Рис. 1. Отклонение от базового уровня ХС ЛПНП (А), ХС ЛПВП (Б) и триглицеридов (В) в зависимости от дозы розувастатина, аторвастатина и симвастатина у пациентов в исследовании VOYAGER [25] Рис. 1. Отклонение от базового уровня ХС ЛПНП (А), ХС ЛПВП (Б) и триглицеридов (В) в зависимости от дозы розувастатина, аторвастатина и симвастатина у пациентов в исследовании VOYAGER [25]](https://medblog.su/wp-content/uploads/2019/09/1569669338_104_effektivnost-bezopasnost-i-komplaens-tri-slagaemyh-uspeha-v-snizhenii-urovnya-holesterina-maksimov-m-l-obrezan-a-g-burashnikova-i-s-shikaleva-a-a.png)
Парные сравнения результатов в метаанализе VOYAGER показали статистически значимые преимущества розувастатина 10 мг перед аторвастатином 10–20 мг и симвастатином 10–20 мг; розувастатина 20 мг перед аторвастатином 20–40 мг и симвастатином 20–80 мг; розувастатина 40 мг перед аторвастатином 40–80 мг и симвастатином 40–80 мг [23–25].
В исследовании В.П. Михина и соавт. [26] проведена сравнительная оценка гиполипидемической и плейотропной эффективности розувастатина и аторвастатина у 114 больных артериальной гипертонией с высокой и очень высокой степенью риска ССЗ при длительном амбулаторном применении. За 1 год до включения в исследование больным в амбулаторных условиях был назначен аторвастатин 20 мг/сут, который они получали в течение года, однако целевой уровень общего ХС и ХС ЛПНП не был достигнут. Замена аторвастатина на розувастатин в комплексной терапии больных высокого и очень высокого сердечно-сосудистого риска сопровождалась дальнейшим снижением атерогенных липидов крови: общего ХС на 24%, ХС ЛПНП на 53% — и сочеталась с уменьшением параметров жесткости сосудистой стенки. Концентрация С-реактивного белка (СРБ) к 6 мес. терапии розувастатином снизилась на 26%, к 12 мес. — на 35% [26].
Из вышесказанного очевидно, что статины, и в особенности розувастатин, являются лекарственными средствами первого выбора при гиперлипидемии, обеспечивая клинически значимое снижение атерогенных липопротеидов, улучшая состояние и прогноз пациентов с ССЗ, и, что далеко не второстепенно, снижая потенциально высокие расходы на здравоохранение.
Эффективность комбинированной гиполипидемической терапии
Однако, учитывая неудовлетворительное количество пациентов, которые достигают целевых значений ХС ЛПНП, становится актуальным вопрос о комбинированной терапии. Больным с высоким риском ССЗ целесообразно назначение статинов в сочетании с другими гиполипидемическими препаратами, например с секвестрантами желчной кислоты, никотиновой кислотой или ингибитором абсорбции ХС для эффективного снижения уровня ХС ЛПНП [20, 27, 28].
Учитывая перечень и органотропность побочных эффектов той или иной группы антиатеросклеротических препаратов (табл. 2), вопрос комбинированной фармакотерапии приходится признать не таким уж и простым.
![Таблица 2. Нежелательные лекарственные реакции гиполипидемических препаратов [5–8, 29] Таблица 2. Нежелательные лекарственные реакции гиполипидемических препаратов [5–8, 29]](https://medblog.su/wp-content/uploads/2019/09/1569669338_896_effektivnost-bezopasnost-i-komplaens-tri-slagaemyh-uspeha-v-snizhenii-urovnya-holesterina-maksimov-m-l-obrezan-a-g-burashnikova-i-s-shikaleva-a-a.png)
Одной из наиболее безопасных и достаточно эффективных комбинаций считается сочетание статинов с эзетимибом. Эзетимиб является представителем относительно нового класса гиполипидемических средств, которые селективно ингибируют абсорбцию ХС и некоторых растительных стеролов в кишечнике. Механизм действия эзетимиба отличается от механизма действия других классов гиполипидемических средств (например, ингибиторов ГМГ-КоА-редуктазы (статинов), секвестрантов желчных кислот, фибратов и растительных станолов). Молекулярной мишенью эзетимиба является транспортный белок Niemann-Pick C1-Like1 (NPC1L1), ответственный за всасывание в кишечнике ХС и фитостеролов. Эзетимиб, применяемый одновременно со статинами, снижает концентрацию общего ХС, ХС ЛПНП, АпоВ, ХС не-ЛПВП и триглицеридов (ТГ), а также повышает концентрацию ХС ЛПВП в плазме крови у пациентов с гиперхолестеринемией в большей степени, чем эзетимиб или статин, применяемые в монотерапии. Эзетимиб ингибирует всасывание [14С] —
ХС и не оказывает влияния на всасывание ТГ, жирных кислот, желчных кислот, прогестерона, этинилэстрадиола или жирорастворимых витаминов А и D [5–8, 29, 30], что делает его липидоснижающие эффекты физиологичными.
В фокусе исследования C.M. Ballantyne et al. [31] были эффективность и безопасность терапии розувастатином в дозе 40 мг отдельно или в комбинации с эзетимибом в дозе 10 мг у 469 больных с гиперхолестеринемией и ИБС в анамнезе или клиническими проявлениями атеросклероза с высоким риском развития ИБС. В результате через 6 нед. лечения 94,0% больных на комбинированной терапии розувастатином в дозе 40 мг и эзетимибом в дозе 10 мг достигли целевого уровня ХС ЛПНП (<100 мг/дл) по сравнению с монотерапией розувастатином в дозе 40 мг (79,1%) (p<0,001). Через 6 нед. больше больных в группе очень высокого риска достигли целевого уровня ХС ЛПНП <70 мг/дл на комбинированной терапии (79,6%) по сравнению с монотерапией (35,0%; p<0,001). Также после 6 нед. терапии среднее снижение уровня вчСРБ было значительно больше при комбинированной терапии розувастатином и эзетимибом (-46,4%), чем при монотерапии (-28,6%; p<0,001). Терапия хорошо переносилась в обеих группах. Миалгия оказалась наиболее распространенным нежелательным явлением, но большинство побочных явлений были легкой и умеренной степени тяжести. Наиболее частые нежелательные явления: повышение уровня АЛТ в группе комбинированной терапии (6 человек [2,5%]) и миалгия в группе монотерапии (5 пациентов [2,2%]). Процент больных, прекративших терапию вследствие каких-либо нежелательных явлений, был низким (в группе комбинированной терапии — 2,5%, в группе монотерапии — 1,3%) [31].
Схожие данные получены в исследованиях других авторов, где отмечалось дополнительное снижение уровня ХС ЛПНП на 13% при терапии эзетимибом в комбинации с максимальной дозой симвастатина (80 мг) и дополнительное снижение более чем на 7% при терапии эзетимибом в комбинации с максимальной дозой аторвастатина (80 мг) [32–34].
Важно подчеркнуть, что состояние больных с высоким риском ИБС улучшается при снижении уровня ХС ЛПНП до целевых значений, и чем больше снижение уровня ХС ЛПНП, тем лучше клинические исходы [35, 36].
В ходе другого открытого рандомизированного многоцентрового исследования [37] анализировали эффективность, безопасность и влияние на биомаркеры метаболизма ХС и липопротеидов при комбинированной терапии розувастатином (в дозе 10 или 20 мг) и эзетимибом (в дозе 10 мг) по сравнению с высокодозовой комбинированной терапией симвастатином (40 или 80 мг) и эзетимибом (10 мг) у 833 больных высокого риска (пациенты с ИБС или эквивалентным риском развития ИБС). Снижение уровня ХС ЛПНП розувастатином 10 мг и эзетимибом 10 мг (59,7%) было значительно сильнее (p=0,002), чем при терапии симвастатином 40 мг и эзетимибом 10 мг. Комбинация розувастатина в дозе 20 мг и эзетимиба в дозе 10 мг снизила уровень ХС ЛПНП на 63,5% относительно исходного уровня, а комбинация симвастатина в различных дозах и эзетимиба снизила уровень ХС ЛПНП на 55,2–57,4% (p<0,001). По сравнению с монотерапией статинами терапия с добавлением эзетимиба показывала дополнительное снижение ХС ЛПНП. Следует отметить, что значительно бóльшая доля больных достигала целевого уровня ХС ЛПНП <100 мг/дл и <70 мг/дл при применении комбинации эзетемиба 10 мг и розувастатина 20 мг (95,6%) и розувастатина 10 мг (77,0%), чем при применении комбинации эзетимиба 10 мг и симвастатина в дозах 40 и 80 мг (87,4–88,6% и 55,3– 67,7% соответственно) (p≤0,007) (рис. 2) [37].
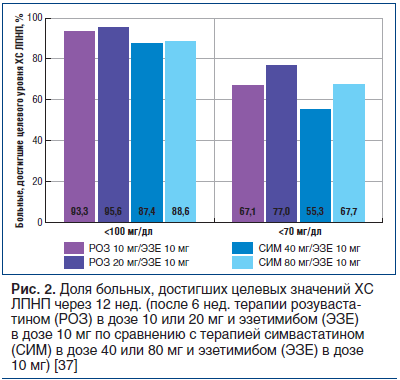
Доля больных, достигших целевого уровня ХС ЛПНП <100 мг/дл, была значительно больше при комбинированной терапии розувастатином в дозе 10 мг и эзетимибом в дозе 10 мг (93,3%) по сравнению с терапией симвастатином в дозе 40 мг и эзетимибом в дозе 10 мг. Монотерапия статинами сократила уровень биомаркеров синтеза ХС и желчных кислот, эзетимиб сократил уровень бета-ситостерола (маркера абсорбции стерола), а при помощи комбинированной терапии удалось достичь дополнительного сокращения массы и активности липопротеин-ассоциированной фосфолипазы А2, свободного ХС и 7-кетохолестерина. Профили безопасности комбинаций розувастатин+эзетимиб и симвастатин+эзетимиб были сопоставимыми [37].
Таким образом, применение розувастатина в дозе 10 или 20 мг в комбинации с эзетимибом помогло добиться значительного улучшения липидного профиля у пациентов в группе высокого риска по сравнению с применением комбинации симвастатина в дозе 40 или 80 мг и эзетимиба (p<0,001) [37]. Схожей гиполипидемической эффективности комбинации розувастатина и эзетимиба, по-видимому, следует ожидать и при сравнении с комбинацией аторвастатина и эзетимиба [30, 37]. Результаты вышеприведенных исследований демонстрируют, что комбинация розувастатина и эзетимиба более эффективна, чем комбинация других статинов и эзетимиба, и может оказаться верным вариантом дополнительного снижения уровня ХС ЛПНП у больных с гиперхолестеринемией, трудно поддающейся терапии, с высоким уровнем ХС ЛПНП и не способных достигнуть целевого уровня ХС ЛПНП на монотерапии.
Статины снижают уровень ланостерола, маркера синтеза ХС, а эзетимиб снижает уровень ситостерола, маркера абсорбции ХС. Наблюдения дополнительного снижения массы и активности липопротеин-ассоциированной фосфолипазы А2 и 7-кетохолестерина наряду с АпоB, ХС не-ЛПВП и ХС ЛПНП предполагают, что комбинированная терапия может обеспечить дополнительную эффективность и улучшить прогноз у больных, у которых высокий уровень атерогенных липопротеидов и биомаркеров метаболизма ХС не снижается на монотерапии статинами [30, 37].
В связи с вышесказанным можно считать своевременным, целесообразным и интересным появление на российском фармацевтическом рынке первой фиксированной комбинации розувастатина с эзетимибом — препарата Розулип® Плюс. По результатам ранее проведенных исследований и многолетнего применения комбинации розувастатина и эзетрола в реальной клинической практике можно заключить, что фиксированная комбинация розувастатина с эзетимибом эффективна у взрослых пациентов с гиперхолестеринемией с гипертриглицеридемией или без таковой, вне зависимости от расовой принадлежности, пола или возраста, в т. ч. у пациентов с СД и семейной гиперхолестеринемией. Представляется обоснованным и актуальным клиническое применение комбинации розувастатина с эзетимибом у всех пациентов, получающих статины (в монотерапии или в свободной комбинации с эзетимибом), но не достигающих целевых значений ХС ЛПНП.
Заключение
Важность использования эффективного статина в адекватной дозе для достижения целевых значений уровня ХС у пациентов с высоким риском ССЗ очевидна. Рандомизированными клиническими исследованиями и результатами клинической практики показано, что достижение целевых уровней ХС ЛПНП может привести к значительному снижению риска сердечно-сосудистых осложнений и экономии затрат на здравоохранение. Добавление эзетимиба к розувастатину приводит к более выраженному снижению уровня ХС ЛПНП и является более безопасным в отношении нежелательных лекарственных реакций по сравнению с увеличением дозы статинов в монотерапии. По сравнению с монотерапией розувастатином комбинация розувастатин+эзетимиб дает больший эффект в достижении целевого уровня ХС не ЛПВП благодаря синергичному действию обоих компонентов. Следует отметить, что фиксированная комбинация увеличивает комплаенс пациентов, что является залогом более успешного лечения. Фиксированную комбинацию розувастатина с эзетимибом — препарат Розулип® Плюс — можно считать препаратом выбора у пациентов с дислипидемией высокого и очень высокого сердечно-сосудистого риска как с клинической, так и с экономической точки зрения.
Список литературы Вы можете найти на сайте http://www.rmj.ru
Информация с rmj.ru