Введение
Анкилозирующий спондилит (АС) — хроническое воспалительное заболевание из группы спондилоартритов, характеризующееся обязательным поражением крестцово-подвздошных суставов и/или позвоночника с потенциальным исходом в анкилоз и частым вовлечением в патологический процесс энтезисов и периферических суставов [1].
К настоящему времени для лечения АС в Российской Федерации без учета биоаналогов зарегистрировано 8 генно-инженерных биологических препаратов (ГИБП) (адалимумаб (АДА), этанерцепт (ЭТ), инфликсимаб (ИНФ), голимумаб (ГОЛ), цертолизумаба пэгол (ЦП), нетакимаб (НЕТ), секукинумаб (СЕК), иксекизумаб (ИКС)) и 2 таргетных синтетических препарата (тофацитиниб (ТОФ), упадацитиниб (УПА)) из группы ингибиторов янус-киназ (иЯК). ТОФ назначается решением врачебной комиссии. В реальной клинической практике при выборе оптимальной стратегии лечения информация о выживаемости ГИБП является одним из ключевых факторов оценки сравнительной клинической эффективности и безопасности [2].
Выживаемость ГИБП определяется как время от начала биологической терапии до ее прекращения по каким-либо причинам, в том числе в результате перехода на другой ГИБП. Это интегральная характеристика, отражающая эффективность, переносимость и общую приемлемость препарата для пациента и врача [3]. Выживаемость терапии не может быть исследована в рандомизированных клинических исследованиях, так как в них она определяется дизайном исследования. Анализ причин отмены ГИБП и таргетных препаратов в перспективе может позволить использовать их более рационально, с учетом индивидуальных особенностей пациентов [4].
Цель исследования: оценить и сравнить выживаемость биологической терапии, найти предикторы отмены у пациентов с АС в условиях клинической практики.
Содержание статьи
Материал и методы
Нами проведено когортное исследование, основанное на ретроспективном анализе данных медицинской документации о 557 эпизодах лечения ГИБП, включающих результаты клинического, лабораторных и инструментальных методов обследования пациентов с подтвержденным диагнозом АС, установленным согласно диагностическим критериям (ASAS, 2009). Диагноз у 25 пациентов трактовался как аксиальный спондилоартрит (АксСпА). Обследованные пациенты длительное время находились на диспансерном учете в одних и тех же лечебных учреждениях и хотя бы однократно госпитализировались для оценки активности заболевания и коррекции терапии в ГБУЗ МО МОНИКИ им. М.Ф. Владимирского в период с 04.2018 по 08.2023, что обеспечило возможность включения их в исследование. Пациенты принимали ИНФ, ГОЛ, ЦП, НЕТ, СЕК, ИКС, ТОФ, БАР в дозах и путем введения согласно официальной инструкции к препаратам.
Критериями невключения являлись: наличие инфекционных, онкологических (в том числе лимфопролиферативных) и других ревматологических заболеваний, тяжелой дыхательной, печеночной, почечной недостаточности, проводимая анти-В-клеточная терапия.
Ретроспективно собраны данные на момент проведения анализа о диагнозе, возрасте, поле, времени, прошедшем от начала заболевания до верификации диагноза, времени, прошедшем от начала заболевания до начала лечения первым биологическим препаратом, наличии HLA-B27, особенностях течения заболевания, причинах прекращения приема биологических препаратов, лекарственный анамнез во время приема биологических препаратов, включая прием нестероидных противовоспалительных препаратов (НПВП), базисных противовоспалительных препаратов (БПВП) (таких как метотрексат, сульфасалазин и лефлуномид), данные о наличии вредных привычек (курение), сопутствующих заболеваний, осложнений основного заболевания, приеме ГИБП в анамнезе, наличии или отсутствии рентгенологических изменений крестцово-подвздошных суставов в соответствии с модифицированными Нью-Йоркскими критериями 2019 г., наличии или отсутствии внеаксиальных и внескелетных проявлений и другие характеристики.
Первичная конечная точка: прекращение приема ГИБП. Прекращение лечения определялось как прерывание лечения на период ≥2 мес.
Собраны данные о причине прекращения приема препарата по следующим предварительно определенным, взаимоисключающим категориям: первичная неэффективность, вторичная неэффективность, инфекции, аллергические реакции (местные и общие), иные медицинские причины, включая беременность, а также немедицинские причины, включая экономически обусловленные. Термин «первичная неэффективность» определялся как улучшение менее чем на 50% или как оценка более 2 баллов по шкале BASDAI через 3 мес. после начала лечения биологическим препаратом и каждые 6 мес. после этого. Термин «вторичная неэффективность» определялся как потеря первоначального ответа на биологический препарат в течение последующих 6 мес.
Проведен анализ выживаемости с оценкой рисков отмены ГИБП в сравнении с АДА. Проанализированы предикторы прекращения приема ГИБП, которые включали характеристики случаев приема ГИБП.
Статистический анализ проводили с применением пакета программ SPSS Statistics 26.0 (IBM Corp., США). Данные с неправильным распределением, обработанные с помощью непараметрических методов, представлены в виде медианы (Ме) с интерквартильным размахом [IQR]. Категориальные показатели представлены в виде абсолютных (n) и процентных (%) значений количества. Выживаемость ГИБП представлена с помощью кривых Каплана — Мейера, оценка значимости моделей проводилась с помощью лог-ранк критерия Мантеля — Кокса. С помощью метода регрессии Кокса в результате отбора предикторов методом исключения по Вальду выявлены факторы, оказавшие статистически значимое влияние на выживаемость ГИБП. Сравнение выживаемости ГИБП в зависимости от наличия или отсутствия данных факторов, оценка значимости моделей проводилась с помощью лог-ранк критерия Мантеля — Кокса. Оценка отношения рисков (ОР) прекращения лечения биологическими препаратами в сравнении с АДА проводилась с помощью метода регрессии Кокса. Различия считали статистически значимыми при р≤0,05.
Результаты исследования
Общая характеристика рассмотренных случаев приема ГИБП представлена в таблице 1.
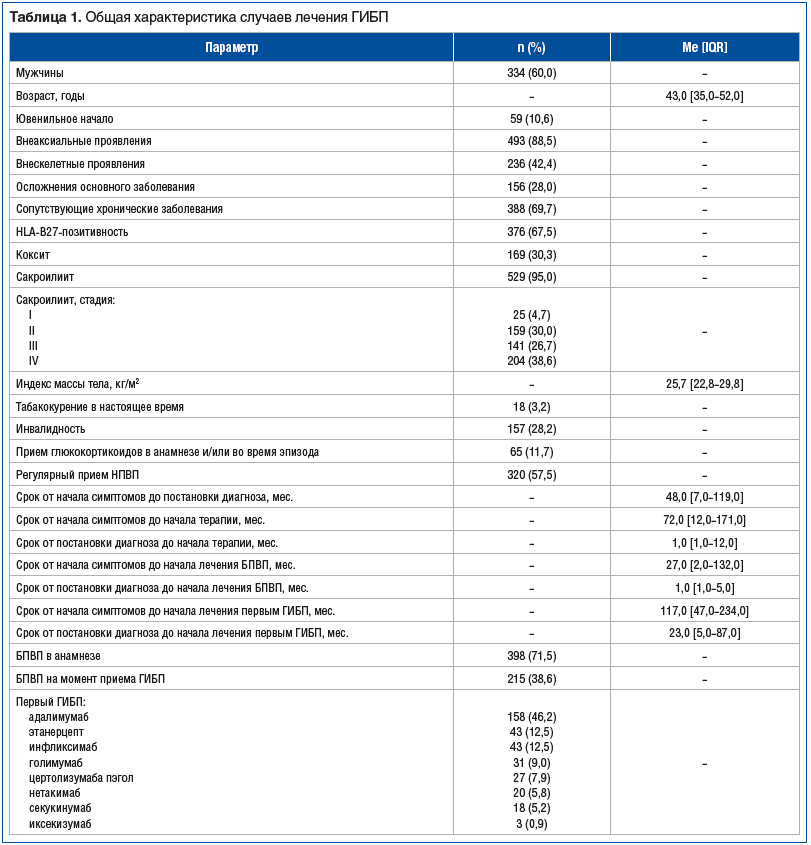
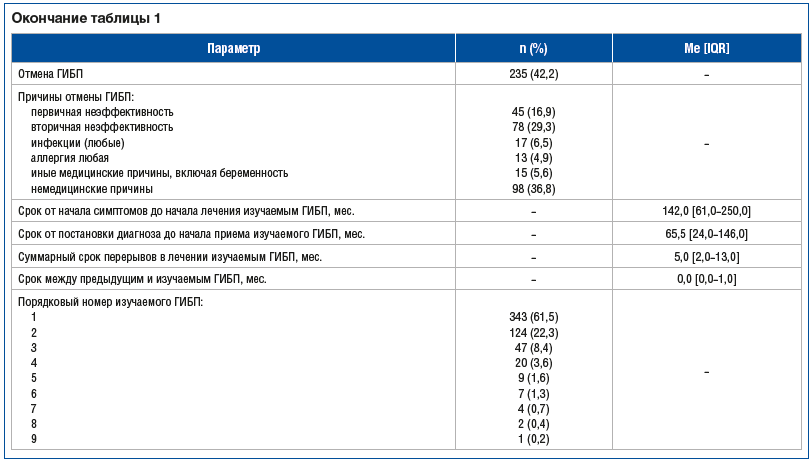
При анализе выживаемости ГИБП выявлено, что АДА имел большие медиану выживаемости — 54,77±15,58 (95% ДИ 24,24–85,30) мес. и средний срок отмены — 58,59±7,26 (95% ДИ 44,34–72,82) мес. в сравнении со всеми остальными ГИБП и иЯК. Медиана выживаемости ИНФ составила 20,27±2,43 (95% ДИ 43,93±7,64) мес. Выживаемость ГИБП представлена с помощью кривой Каплана — Мейера на рисунке 1.
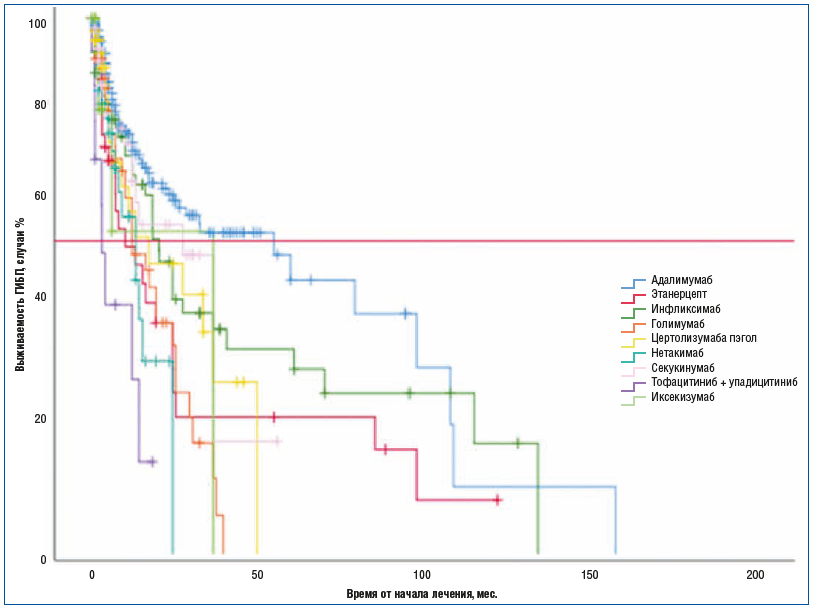
Модель оценена с помощью лог-ранк критерия Мантеля — Кокса, статистически значима (р<0,001). Горизонтальной красной линией обозначена медиана выживаемости ГИБП, соответствующая предполагаемому сроку отмены не менее чем в 50% случаев приема конкретного ГИБП.
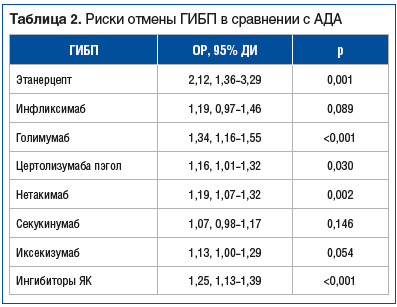
Риск отмены АДА оказался статистически значимо ниже, чем риск отмены ЭТ, ГОЛ, ЦП, НЕТ и иЯК. При этом риски отмены СЕК и ИНФ не были достоверно выше риска отмены АДА. ОР и статистическая значимость выявленных различий в выживаемости ГИБП приведены в таблице 2.
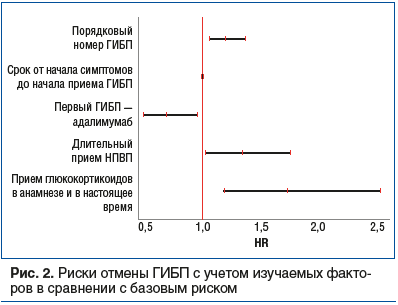
При оценке комплексного влияния факторов на риск отмены ГИБП у пациентов с АС с помощью метода регрессии Кокса в результате отбора предикторов методом исключения по Вальду выявлено, что с риском отмены ГИБП ассоциированы следующие факторы. Прием глюкокортикоидов на момент осмотра или в анамнезе в 1,73 раза (95% ДИ 1,18–2,53; р=0,005) увеличивал риск отмены ГИБП, а регулярный прием НПВП — в 1,34 раза (95% ДИ 1,02–1,76; р=0,037). Кроме того, риск отмены статистически значимо увеличивался при увеличении порядкового номера ГИБП на одно значение в 1,2 раза (95% ДИ 1,06–1,3; р=0,004). Зависимость риска отмены от порядкового номера ГИБП отражена на рисунке 2. Риск отмены уменьшался в 1,5 раза (95% ДИ 0,49–0,96; р=0,026), если первым назначался АДА. Влияние остальных проанализированных факторов не было статистически значимо (р>0,05).
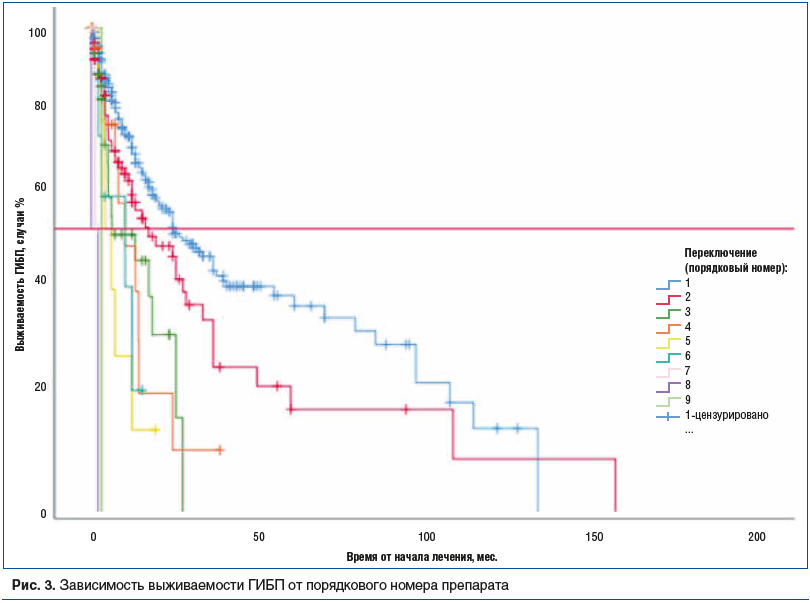
Зависимость выживаемости ГИБП от порядкового номера препарата представлена на рисунке 3.
Обсуждение
Особенностью нашего исследования является преобладание наиболее тяжелой группы пациентов с АС, требующих стационарного лечения, включающей в себя большое число так называемых «труднолечимых» пациентов, имеющих в анамнезе неэффективность ≥2 (11,6%) и ≥4 ГИБП (2,32%), что выше, чем в недавно опубликованной работе Ш.Ф. Эрдес и др. [5]. Выявлена четкая зависимость риска отмены от линии ГИБП, что согласуется с работами других авторов [6–10]. Также необходимо отметить высокую частоту отмены ГИБП (42,2%), в том числе по немедицинским (включая административные) причинам (36,8%). Наилучшие результаты в нашем исследовании показал АДА, что частично может быть обусловлено его наиболее частым назначением в 1-й линии терапии (75,8%). На этом фоне относительно неплохие результаты продемонстрировали ингибиторы интерлейкина 17: НЕТ назначался в 1-й линии в 52,5% случаев, СЕК — в 38,7%, ИКС — в 23,0%. Сопоставимые результаты показало исследование S. Alonso et al. [11], в отличие от данных T. Rusman et al. [12], в работе которых существенного влияния возраста на риск отмены ГИБП получено не было. Как и в работе X. Michelena et al. [13], рентгенологический статус не влиял на выживаемость ГИБП, что, вероятно, может быть связано с относительно поздней инициацией лечения: срок от постановки диагноза до инициации составил 23,0 (5,0–87,0) мес.
Среди выявленных нами предикторов отмены ГИБП у пациентов с АС прием глюкокортикоидов в анамнезе и на момент приема ГИБП, а также постоянный прием НПВП, по нашему мнению, в большей степени отражают высокую активность заболевания у данной группы пациентов.
Заключение
Выживаемость разных ГИБП в клинической практике неодинакова, наилучшие результаты в нашем исследовании показал АДА. Выявлены предикторы отмены ГИБТ у пациентов с АС. Данные результаты необходимо учитывать при выборе ГИБП в клинической практике.
Ретроспективный характер настоящего исследования, проведенного в одном центре, связан с некоторыми ограничениями, включая неполные данные и нестандартизованный объем обследования. Выбор ГИБП и иЯК зависел от клинических и экономических факторов, включая предпочтения пациента и врача. Другим ограничением была характеристика относительно небольшой и этнически однородной выборки пациентов, которые проживали в одном регионе и наблюдались в одних и тех же лечебных учреждениях, имели сравнительно одинаковый уровень жизни и доступности медицинской помощи. Однако наше исследование имеет сильные стороны — данные получены из реальной клинической практики, ретроспективно, за длительный промежуток времени, а также с поправкой на порядковый номер ГИБП.
Информация с rmj.ru
