Содержание статьи
Введение
Аккомодация — это адаптивная способность глаза человека, обеспечивающая четкое зрение при изменении линейного расстояния до визуальных целей [1]. К основным звеньям механизма аккомодации относятся хрусталик, связочный аппарат хрусталика и хориоидеа. Однако в обеспечение биомеханизма аккомодации в той или иной степени вовлечены практически все структуры глазного яблока [2]. Сужение зрачка при аккомодации позволяет увеличить глубину резкости изображения и, следовательно, уменьшить объем затрачиваемой аккомодации при рассматривании предметов, расположенных на близком расстоянии, или восполнить недостающий объем аккомодации, например, при ранних проявлениях пресбиопии [2]. Перенапряжение цилиарной мышцы может приводить к спазму аккомодации и, как следствие, к размытым изображениям.
Ведущую роль в возникновении и прогрессировании близорукости у детей играет расстройство аккомодации, возникающее в тот период, когда ребенок сталкивается с повышенными зрительными нагрузками [3]. Нормализация аккомодации у пациентов с миопией играет важную роль в стабилизации миопического процесса. Лечение перенапряжения аккомодации включает в себя комплекс профилактических и медикаментозных мероприятий: снижение зрительной нагрузки, увеличение времени на свежем воздухе, занятия физкультурой, спортом (бадминтон, теннис, плавание) и медикаментозное лечение [4]. Для медикаментозного лечения перенапряжения аккомодации используют α-адреномиметик — 2,5% фенилэфрин в виде глазных капель. На отечественном рынке в настоящее время появилось много лекарственных препаратов, содержащих 2,5% фенилэфрин, однако их клиническое применение приводит к различному по силе и длительности фармакологическому эффекту и нередко сопровождается развитием нежелательных явлений со стороны органа зрения, в частности местнораздражающим действием [5]. Это главным образом обусловлено составом вспомогательных компонентов, входящих в готовую лекарственную форму (ГЛФ).
Цель исследования: проведение сравнительного анализа клинической эффективности препаратов 2,5% фенилэфрина с гипромеллозой и без таковой для лечения перенапряжения аккомодации у пациентов-школьников с миопией и экспериментальное исследование фармакологического эффекта действующего вещества ГЛФ препаратов, содержащих 2,5% фенилэфрин с/без вспомогательных компонентов.
Материал и методы
Клиническое исследование проводилось на базе детского офтальмологического отделения ООО «Офтальмологическая Клиника Инновационных Технологий» (г. Ярославль). В исследовании приняли участие 122 школьника в возрасте от 11 до 17 лет с разной степенью перенапряжения аккомодации, наблюдавшиеся амбулаторно. Были сформированы 2 группы: 1-я получала по 1 капле на ночь в течение 30 дней Ирифрин® БК, содержащий 2,5% фенилэфрин с гипромеллозой (Ирифрин® БК — форма Ирифрина без консервантов), 2-я группа — препарат А (2,5% фенилэфрин без гипромеллозы) по той же схеме. В рамках исследования одной группе пациентов выписывали рецепт на препарат Ирифрин® БК (фенилэфрин 2,5%), а другой группе пациентов выдавали препарат А, при этом родители не знали, какую лекарственную форму они применяли. Аккомодативную функцию исследовали с помощью аккомодографа Speedy-i с расчетом аккомодографических коэффициентов: коэффициента аккомодационного ответа (КАО) и коэффициента аккомодативных микрофлюктуаций (КМФ) в динамике (до лечения и через 30 дней от начала терапии).
Экспериментальная часть работы выполнена на базе Сеченовского Университета на 40 половозрелых кроликах-самцах породы советская шиншилла, приобретенных в питомнике ФГБУН НЦБМТ ФМБА России. Работа выполнена в строгом соответствии с требованиями приказа Министерства здравоохранения Российской Федерации от 01.04.2016 № 199н «Об утверждении правил надлежащей лабораторной практики».
В исследование было включено 4 ГЛФ препаратов с 2,5% фенилэфрином, содержащих в качестве вспомогательного компонента гипромеллозу (Ирифрин® и Ирифрин® БК), гиалуроновую кислоту (препарат Б), и без вспомогательных веществ (препарат А). У животных оценивали динамику развития мидриатического эффекта (время начала, время достижения максимальной выраженности, продолжительность максимальной выраженности эффекта), глубину и длительность мидриатического эффекта, на 5-й минуте действия во влаге передней камеры глаза определяли концентрацию действующего вещества методом высокоэффективной газожидкостной хроматографии с тандемным масс-спектрометрическим детектированием [6] в собственной модификации. Работа одобрена локальным этическим комитетом ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
Статистическая обработка полученных результатов проведена с использованием программы Statistica 6.0, включала описательный анализ числовых характеристик признаков (рассчитывалось среднее значение (M) и стандартное отклонение), в клиническом исследовании оценивали значение R с использованием непараметрического критерия Спирмена и p-уровень критерия Уилкоксона. В эксперименте при сравнении количественных признаков проводили дисперсионный анализ для оценки нормальности распределения с последующим использованием ANOVA и применением функциональных возможностей критерия оценки множественных сравнений Ньюмена — Кейлса при 5% уровне значимости.
Результаты исследования
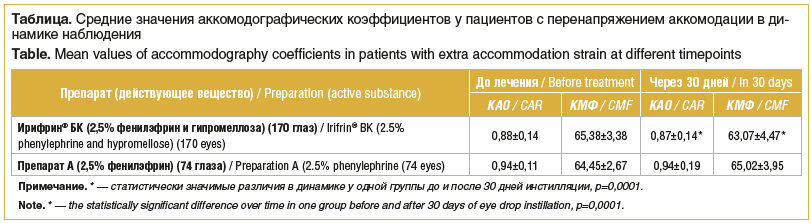
В клиническом исследовании средний возраст школьников 1-й группы (85 пациентов (170 глаз)) составил 14,54±2,69 года, средняя миопическая рефракция — (-3,63)±1,88 дптр, пациенты получали препарат Ирифрин® БК. Во 2-ю группу вошли 37 пациентов (74 глаза), средний возраст составил 11,62±2,67 года, средняя миопическая рефракция — (-2,50)±2,14 дптр, детям назначался препарат А. При анализе результатов лечебного эффекта препарата Ирифрин® БК на перенапряжение аккомодации через 30 дней терапии было выявлено статистически значимое снижение коэффициентов КМФ (характеризующего состояние аккомодации) и КАО. Группа, получавшая препарат А, не показала статистически значимых изменений аккомодографических коэффициентов (см. таблицу).
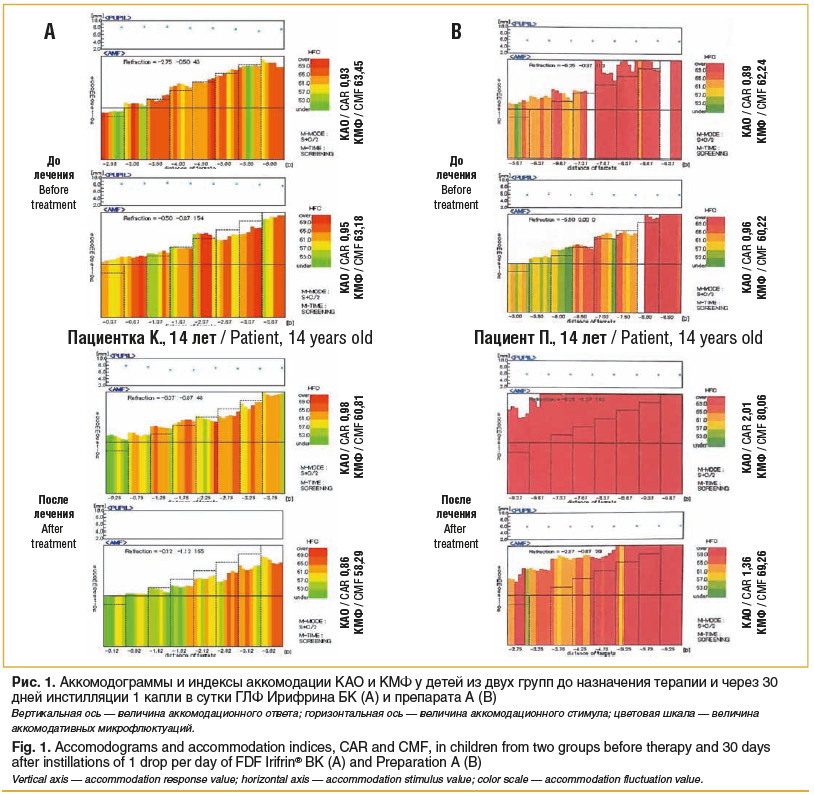
На рисунке 1 представлены изменения аккомодографических коэффициентов в динамике медикаментозного лечения двух пациентов из разных исследуемых групп, демонстрирующие эффективность лечения перенапряжения аккомодации препаратом Ирифрин® БК (рис. 1А) через 30 дней после его использования, тогда как использование препарата А не привело к снижению напряжения аккомодации (рис. 1В).
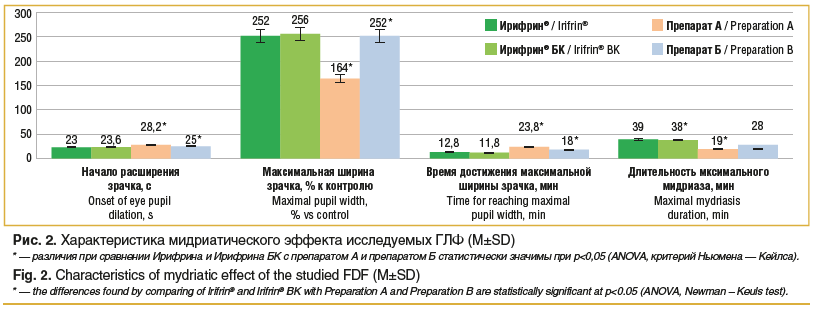
В экспериментальных исследованиях было показано, что Ирифрин® и Ирифрин® БК имеют оптимальное соотношение эффективность/безопасность в сравнении с препаратом Б. Глубина мидриатического эффекта после однократной инстилляции 1 капли 2,5% раствора фенилэфрина гидрохлорида, содержащего гипромеллозу в качестве вспомогательного вещества (Ирифрин® и Ирифрин® БК), была более выражена, чем после закапывания препарата А. Скорость достижения максимального мидриатического действия была быстрее, длительность — дольше на фоне применения 2,5% раствора фенилэфрина гидрохлорида, содержащего гипромеллозу, чем у препарата А без вспомогательного вещества, и у препарата Б с гиалуронатом натрия (рис. 2). Это обстоятельство позволяет предположить большую эффективность применения препаратов Ирифрин® и Ирифрин® БК по сравнению с препаратами А и Б.
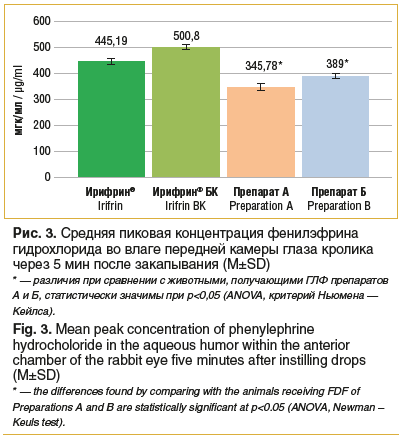
В ходе исследования также было изучено влияние ГЛФ (Ирифрин®, Ирифрин® БК, препараты А и Б) на уровень пиковой концентрации фенилэфрина во влаге передней камеры глаза кроликов (рис. 3). Через 5 мин после закапывания 1 капли исследуемых растворов ГЛФ установлены следующие средние концентрации действующего вещества фенилэфрина: после инстилляции Ирифрина — 445,19±12,13 мкг/мл, Ирифрина БК — 500,80±8,56 мкг/мл, препарата А — 345,78±13,95 мкг/мл, препарата Б — 389,00±8,75 мкг/мл.
Обсуждение
Для большей управляемости активным действующим веществом в современной офтальмологии в состав лекарственных форм для топического (местного) применения включаются природные биополимеры. Одним из таких повсеместно распространенных в природе биополимеров является гипромеллоза, или гидроксипропилметилцеллюлоза [7]. Уникальность этого полимера заключается в том, что в зависимости от выбранного при его производстве молекулярного веса можно получать вещество с заданными параметрами вязкости, эмульгирования, поверхностного натяжения, связи с активными веществами и внутренними средами организма, адгезии [8]. Применение гипромеллозы в глазных каплях эффективно и безопасно: описан хороший клинический эффект содержащих ее лекарственных форм нафазолина [9]; показано, что закапывание водного раствора гипромеллозы приводит к ускорению закрытия пункционного отверстия глазного яблока [10]. В данном исследовании при сравнении клинической эффективности ГЛФ Ирифрина БК и препарата А установлено, что ГЛФ Ирифрина БК с гипромеллозой более эффективна при медикаментозном лечении перенапряжения аккомодации у детей школьного возраста с миопией в течение 30 дней (однократная инстилляция 1 капли глазных капель на ночь) по сравнению с ГЛФ препарата А без гипромеллозы.
По результатам экспериментального исследования Ирифрин® и Ирифрин® БК, содержащие в качестве вспомогательного вещества гипромеллозу, обладают лучшими характеристиками мидриатического эффекта по сравнению с препаратами А и Б в данном исследовании, не содержащими в качестве вспомогательного вещества гипромеллозу: глубина мидриатического эффекта после однократной инстилляции 1 капли 2,5% раствора фенилэфрина гидрохлорида, содержащего гипромеллозу в качестве вспомогательного вещества, более выражена, чем после ГЛФ препарата А без вспомогательного вещества, а скорость достижения максимального мидриатического действия и его длительность — оптимальнее, чем у препаратов А и Б в данном исследовании. Это, на наш взгляд, демонстрирует более стабильные фармакологические свойства Ирифрина и Ирифрина БК в сравнении с отобранными воспроизведенными лекарственными препаратами (препарат А и препарат Б) и позволяет предположить более предсказуемое действие при клиническом применении.
При исследовании экспериментальной пиковой концентрации различных ГЛФ фенилэфрина в водянистой влаге передней камеры глаза через 5 мин после инстилляции 1 капли препаратов были получены статистически значимо более высокие концентрации у ГЛФ Ирифрин® и Ирифрин® БК, чем у препаратов А и Б, что также позволяет предполагать более полный и предсказуемый фармакологический эффект данных препаратов при клиническом применении по сравнению с отобранными воспроизведенными лекарственными препаратами. Полученные результаты позволяют предположить, что в основе оптимизации локальной биодоступности и фармакодинамики фенилэфрина гидрохлорида, являющегося действующим веществом ГЛФ Ирифрин® и Ирифрин® БК, лежит способность гипромеллозы облегчать прохождение фенилэфрина через тканевой барьер глаза и задерживать его элиминацию, повышая локальную экспозицию действующего вещества. Указанное предположение основано в том числе на известных данных о физико-химических свойствах и фармакодинамике гипромеллозы [11].
Заключение
Особое значение в терапии нарушения аккомодации, а также в профилактике прогрессирования истинной мио-пии у детей имеют быстрота всасывания ГЛФ препарата фенилэфрина, длительность его действия и, как результат, максимальный мидриатический эффект. Полученные результаты убедительно доказывают, что препараты Ирифрин® и Ирифрин® БК, содержащие 2,5% фенилэфрин и гипромеллозу, эффективны у детей с нарушением аккомодации при миопии. Содержание в ГЛФ, кроме 2,5% фенилэфрина, дополнительно гипромеллозы способствует улучшению фармакодинамики и фармакокинетики действующего вещества за счет ускорения его проникновения во влагу передней камеры глаза, повышения локальной биодоступности и пролонгирования времени экспозиции, что и обусловливает более выраженную клиническую эффективность ГЛФ Ирифрин® БК в лечении перенапряжения аккомодации на фоне миопии у детей по сравнению с препаратом А, которое выражается в статистически значимом улучшении индексов аккомодации в процессе лечения.
Сведения об авторах:
Махова Марина Валерьевна — ассистент кафедры офтальмологии ФГБОУ ВО ЯГМУ Минздрава России; 150000, Россия, г. Ярославль, ул. Революционная, д. 5.
Ших Евгения Валерьевна — д.м.н., профессор, заведующая кафедрой клинической фармакологии и пропедевтики внутренних болезней ИКМ им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-6589-7654.
Страхов Владимир Витальевич — д.м.н., профессор, заведующий кафедрой офтальмологии ФГБОУ ВО ЯГМУ Минздрава России; 150000, Россия, г. Ярославль, ул. Революционная, д. 5.
Блинов Дмитрий Сергеевич — д.м.н., доцент, заведующий отделом молекулярной и клинической фармакологии НИЯУ МИФИ; 115409, Россия, г. Москва, Каширское ш., д. 31; заведующий отделом научного проектирования и контролируемых клинических исследований ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России; 117198, Россия, г. Москва, ул. Саморы Машела, д. 1; ORCID iD 0000-0002-8385-4356.
Полуосьмак Галина Константиновна — аспирант кафедры клинической фармакологии и пропедевтики внутренних болезней ИКМ им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2.
Семелева Елена Владимировна — д.м.н., доцент, заведующая кафедрой общественного здоровья и здравоохранения ФГБОУ ВО МГУ им. Н.П. Огарева, 430000, Россия, г. Саранск, ул. Большевистская, д. 68; ORCID iD 0000-0001-6692-4968.
Блинова Екатерина Валериевна — д.м.н., профессор, профессор кафедры клинической фармакологии и пропедевтики внутренних болезней ИКМ им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ведущий научный сотрудник лаборатории бионанофотоники, профессор кафедры фундаментальной медицины НИЯУ МИФИ; 115409, Россия, г. Москва, Каширское ш., д. 31; ORCID iD 0000-0003-0050-0251.
Контактная информация: Блинова Екатерина Валериевна, e-mail: bev-sechenov@mail.ru.
Прозрачность финансовой деятельности: экспериментальная часть исследования проведена при поддержке компании SENTISS.
Конфликт интересов отсутствует.
Статья поступила 10.01.2023.
Поступила после рецензирования 20.01.2023.
Принята в печать 30.01.2023.
About the authors:
Marina V. Makhova — assistant of the Department of Ophthalmology, Yaroslavl State Medical University; 5, Revolutsionnaya str., Yaroslavl, 150000, Russian Federation.
Evgeniya V. Shikh — Dr. Sc. (Med.), Professor, Head of the Department of Clinical Pharmacology and Propedeutics of Internal Diseases, N.V. Sklifosovsky Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8 Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0001-6589-7654.
Vladimir V. Strakhov — Dr. Sc. (Med.), Professor, Head of the Department of Ophthalmology, Yaroslavl State Medical University; 5, Revolutsionnaya str., Yaroslavl, 150000, Russian Federation.
Dmitry S. Blinov — Dr. Sc. (Med.), associate professor, Head of the Department of Molecular and Clinical Pharmacology, National Research Nuclear University MEPhI; 31, Kashirskoe highway, Moscow 115409, Russian Federation; Head of the Department of Research Design and Controlled Clinical Trials, Dmitry Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology; 1, Samora Mashel str., Moscow, 117198, Russian Federation; ORCID iD 0000-0002-8385-4356.
Galina K. Poluosmak — postgraduate student of the Department of Clinical Pharmacology and Propedeutics of Internal Diseases, N.V. Sklifosovsky Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8 Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation.
Elena V. Semeleva — Dr. Sc. (Med.), associate professor, Head of the Department of Public Health and Healthcare Services, N.P. Ogarev National Research Mordovia State University, 68, Bolshevitskaya str., Saransk, 430000, Russian Federation; ORCID iD 0000-0001-6692-4968.
Ekaterina V. Blinova — Dr. Sc. (Med.), Professor, Professor of the Department of Clinical Pharmacology and Propedeutics of Internal Diseases, N.V. Sklifosovsky Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8 Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; leading researcher of the Bionanophotonics Laboratory, Professor of the Department of Fundamental Medicine, National Research Nuclear University MEPhI; 31, Kashirskoe highway, Moscow 115409, Russian Federation; ORCID iD 0000-0003-0050-0251.
Contact information: Ekaterina V. Blinova, e-mail: bev-sechenov@mail.ru.
Financial Disclosure: the experimental part of the study was supported by SENTISS.
There is no conflict of interests.
Received 10.01.2023.
Revised 20.01.2023.
Accepted 30.01.2023.
Информация с rmj.ru