Введение
Воспалительные заболевания верхних дыхательных путей (ВДП), такие как риносинусит, тонзиллофарингит и средний отит, остаются одной из наиболее распространенных причин обращения за медицинской помощью во всем мире. Доминирующей стратегией лечения бактериальных форм этих заболеваний является антибиотикотерапия. Однако глобальный рост антимикробной резистентности, вызванный бесконтрольным и часто неоправданным применением антибиотиков, привел к значительному снижению их клинической эффективности [1]. Штаммы Staphylococcus aureus, Streptococcus pneumoniae, Haemophilus influenzae и Pseudomonas aeruginosa, являющиеся ключевыми патогенами ВДП, демонстрируют все более высокие уровни устойчивости к антибактериальным препаратам первой и второй линии.
Хронический риносинусит (ХРС) остается одним из наиболее распространенных и клинически гетерогенных заболеваний в оториноларингологии, существенно снижающих качество жизни пациентов [1]. Несмотря на комплексный подход к лечению, включающий топические кортикостероиды, ирригационную терапию и эндоскопическую хирургию, значительное число случаев характеризуются персистирующим течением и рецидивированием [2].
Распространенность ХРС, по данным EPOS 2020, варьирует от 5,5 до 28% при оценке по симптомам, снижаясь до 3–6% при объективном подтверждении [1]. Российские данные также демонстрируют значительную долю этой патологии в структуре ЛОР-заболеваний: от 1,42% по официальной статистике до 14,6% по результатам эпидемиологических исследований [3]. Схожие показатели отмечаются и в глобальном масштабе, что подчеркивает особую значимость проблемы [4–6].
Хронический риносинусит определяется как воспалительное заболевание слизистой оболочки носа и околоносовых пазух (ОНП) продолжительностью свыше 12 нед. Диагноз устанавливается на основании наличия двух и более симптомов, к которым относятся назальная обструкция или ринорея, а также боль и/или ощущение давления в проекции ОНП, гипосмия/аносмия, эндоскопические признаки (отек, слизисто-гнойное отделяемое) и/или данные КТ-исследования [1, 2]. Выделяют две основные фенотипические формы: ХРС с назальными полипами (ХРС+НП) и без них (ХРС-НП) [2].
Дисбиоз и локальный иммунитет: ключевой патогенетический дуэт
Ключевым патогенетическим звеном ХРС является нарушение мукозального иммунитета и микробиоценоза слизистой оболочки ОНП. Первоначальным триггером хронического воспаления все чаще считается дисбиотическое нарушение микробиоты полости носа, ОНП и даже кишечника. Изменение кишечного микробиома способно опосредовать системное воспаление через эпигенетическую модификацию и нарушение функции иммунных клеток [7].
В норме синоназальный микробиоценоз характеризуется доминированием коринебактерий (тип Actinobacteria, ~36%) над стафилококками (тип Firmicutes, ~26%) [8, 9]. При ХРС наблюдается снижение α-разнообразия микробиома с уменьшением индекса Симпсона, что коррелирует с тяжестью воспаления [7, 9]. Отмечается чрезмерный рост численности условно-патогенных видов (например, Corynebacterium tuberculostearicum) на фоне уменьшения количества комменсалов (например, Lactobacillus sakei) [7].
Микробный пейзаж при ХРС представлен широким спектром возбудителей: среди грамположительных аэробов лидируют коагулазоотрицательные стафилококки (34,7%) и S. aureus (26,5%), среди грамотрицательных — H. influenzae (27,0%) и P. aeruginosa (21,6%) [10]. Возрастает роль анаэробной флоры (у 189 из 259 обследованных пациентов с ХРС), ассоциированной с более частыми рецидивами [11, 12].
Не менее значимо участие грибов (рода Alternaria) и вирусов. Последние, персистируя в слизистой оболочке, могут усиливать бактериальную адгезию, нарушать целостность эпителиального барьера и мукоцилиарный клиренс [13].
Особый интерес представляет фагом (сообщество вирусов), в частности бактериофаги, которые способны модулировать микробиом, влияя на экспрессию генов хозяина и горизонтальный перенос генов устойчивости [13, 14].
Доминирующую роль в поддержании хронического воспаления играют бактериальные биопленки, формируемые S. aureus, P. aeruginosa и другими патогенами [13]. Биопленки представляют собой структурированные конгломераты микроорганизмов, погруженные в экзополисахаридную матрицу, что обеспечивает им до 1000-кратного увеличения устойчивость к антибиотикам и защиту от факторов иммунной системы макроорганизма [4].
Биопленки выявляются в 80–100% биоптатов при ХРС и ассоциированы с тяжелым течением и рецидивированием [15, 16]. Показана связь между нарушением врожденного иммунитета (снижение экспрессии лактоферрина, дисфункция рецептора горького вкуса T2R38) и склонностью к биопленкообразованию [7].
Проблемы современной терапии ХРС и роль антибиотикорезистентности
Усугубляющей проблемой является глобальный рост антимикробной резистентности. Метициллин-резистентные штаммы S. aureus (MRSA) и мультирезистентные P. aeruginosa становятся частыми находками при рефрактерном ХРС, их присутствие существенно ухудшает результаты консервативного лечения [17]. В этой связи разработка и внедрение альтернативных или дополнительных к антибиотикам методов лечения является одной из приоритетных задач современной медицины. Одним из наиболее перспективных направлений представляется фаготерапия — использование бактериофагов для специфического подавления бактериальных патогенов.
Стандартные схемы антибактериальной терапии при ХРС зачастую оказываются неэффективными по нескольким причинам. Во-первых, проникновение антибиотиков в очаг хронического воспаления, и особенно внутрь биопленки, значительно ограничено [17]. Во-вторых, даже при достижении бактерицидных концентраций, антибиотики воздействуют преимущественно на планктонные формы бактерий, практически не затрагивая персистирующие и метаболически неактивные клетки внутри биопленки [18]. В-третьих, антибиотики нежелательно применять длительно в связи с развитием дисбиоза, риском супергрибковых инфекций и метаболомных нарушений, в особенности у иммунокомпрометированных пациентов [19–22].
В отличие от антибиотиков бактериофаги обладают селективным действием и могут применяться длительно не только для лечения, но и для профилактики заболеваний [23].
Исследования последних лет демонстрируют рост резистентности основных возбудителей ХРС. Современные микробиологические исследования выявляют ключевую роль полирезистентных бактериальных патогенов, таких как P. aeruginosa, S. aureus (включая MRSA), S. pneumoniae и H. influenzae, в патогенезе ХРС. Их способность к формированию биопленок не только обусловливает персистенцию воспаления и утяжеление течения заболевания, но и служит основной причиной неэффективности стандартной антибактериальной терапии. Наибольшую тревогу вызывают MRSA, β-лактамазы расширенного спектра действия и энтеробактерии, продуцирующие карбапенемазы [24, 25].
Помимо формирования классической резистентности, бактерии в биопленках проявляют фенотипическую толерантность, обусловленную гетерогенностью популяции, наличием «персистеров» — особых бактериальных клеток, находящихся в состоянии анабиоза со сниженной метаболической активностью [26]. Это делает хронические синуситы, ассоциированные с наличием биопленок, одной из наиболее сложных терапевтических проблем в оториноларингологии.
Бактериофаги: механизмы действия и преимущества
Бактериофаги (фаги) — это вирусы, избирательно инфицирующие бактериальные клетки. Их жизненный цикл может быть литическим (с разрушением клетки-хозяина и высвобождением новых вирионов) или лизогенным (с интеграцией в бактериальный геном) [27]. Для терапевтических целей используются исключительно литические фаги.
Основной механизм действия заключается в специфическом связывании с рецепторами на поверхности бактериальной клетки (например, с тейхоевыми кислотами у S. aureus или поринами у P. aeruginosa), инъекции фаговой ДНК, репликации внутри клетки и последующем ее лизисе с высвобождением зрелых фаговых частиц. Каждый цикл приводит к гибели одной бактериальной клетки и образованию множества (десятков или сотен) новых фагов, способных инфицировать соседние клетки [28].
Особую ценность представляет способность фагов разрушать биопленки. Фаги продуцируют ферменты — деполимеразы (эндолизины, экзолизины, гидролазы), которые специфически расщепляют компоненты экзополисахаридной матрицы (пептидогликан, альгинат и др.) [29]. Это позволяет им не только проникать в глубинные слои биопленки, но и нарушать ее структурную целостность, повышая чувствительность входящих в ее состав бактерий к антибиотикам и факторам врожденного и адаптивного иммунитета [14].
Преимущества бактериофагов:
высокая специфичность. Фаги действуют избирательно на целевые виды или даже штаммы бактерий, не нарушая нормоценоз слизистых оболочек [27, 30];
эффективность против антибиотикорезистентных штаммов. Резистентность бактерий к антибиотикам не влияет на эффективность фагов, так как механизмы проникновения и лизиса принципиально иные [30];
способность влиять на биопленки. В отличие от большинства антибиотиков, фаги активно проникают и лизируют бактерии внутри биопленочных структур [30];
самоамплификация в очаге инфекции. Фаги реплицируются только в присутствии целевого патогена, что позволяет создавать высокую локальную концентрацию именно в зоне воспаления [31];
медленное развитие фагорезистентности [32, 33];
возможности использования в синергизме с антибиотиками и другими противомикробными средствами [34];
опосредованная стимуляция врожденного и адаптивного иммунного ответа;
возможность использования для профилактики обострения заболевания и рецидива инфекции [32, 33]. Длительный срок применения;
благоприятный профиль безопасности. Фаги не взаимодействуют с клетками эукариот, сохраняя микробиом, и имеют минимальный риск развития системных побочных эффектов даже при превышении дозы [29, 33, 34].
Современные данные по применению фагов при ХРС
Первые пилотные исследования и клинические случаи демонстрируют обнадеживающие результаты применения фаговой терапии при рефрактерных инфекциях ВДП, в том числе и при ХРС [33].
Результаты исследования А.А. Кривопалова и соавт. [4] продемонстрировали высокую эффективность фаготерапии поливалентными бактериофагами по сравнению с антибиотикотерапией в лечении неосложненных обострений ХРС у взрослых пациентов. Подчеркнуто, что преимуществом фаготерапии является отсутствие влияния на рост антибиотикорезистентности патогенов, ассоциированных с обострением ХРС.
Так, M. Łusiak-Szelachowska et al. [35] отметили, что применение коктейля фагов против P. aeruginosa ex vivo снизило биомассу биопленки бактериальных изолятов, полученных из пазух пациентов с ХРС, в среднем на 70%. Кроме того, исследования на животных, проведенные на модели синусита у овец, продемонстрировали значительное снижение биомассы биопленки S. aureus и P. aeruginosa фаговыми коктейлями при сохранении безопасного длительного местного применения (до 20 дней).
Особый интерес представляет синергизм фагов и антибиотиков. Н.К. Абдраймова и соавт. [36] в обзоре литературы по проблеме фаготерапии и антибиотикорезистентности показали, что многочисленные экспериментальные данные подтверждают положительный эффект комбинации фагов и антибиотиков, заключающийся в существенно более выраженном подавлении бактерий по сравнению с монотерапией антибиотиком. При этом антагонизм между агентами наблюдается крайне редко. Сочетанная терапия эффективна против обеих форм инфекции — как планктонной, так и биопленочной, что особенно актуально для штаммов S. aureus, склонных к образованию биопленок.
Хронический риносинусит представляет собой идеальную модель для фаготерапии из-за частого образования бактериальных биопленок [31].
Исследование S.A. Fong et al. [30] продемонстрировало in vitro высокую литическую активность коктейля бактериофагов против биопленок, образованных клиническими изолятами P. aeruginosa от пациентов с ХРС.
Дополнительные исследования безопасности, такие как работа M.L. Ooi et al. [37], подтвердили хороший профиль переносимости локальной фаготерапии при ХРС. Проведенный 14-дневный курс интраназальной фаготерапии с применением коктейля бактериофагов в дозировке до 3×109 БОЕ продемонстрировал благоприятный профиль безопасности и хорошую переносимость, а также показал обнадеживающие предварительные результаты в отношении клинической эффективности.
Однако имеющаяся доказательная база ограничивается небольшими выборками, короткими сроками наблюдения и гетерогенными протоколами (различные фаговые коктейли, пути и режимы введения, неоднородные критерии отбора пациентов и оценки исходов), что не позволяет экстраполировать результаты на широкую клиническую практику и формировать четкие рекомендации. Остаются нерешенными принципиальные вопросы оптимального подбора фагов с учетом штамм-специфичности патогенов при заболеваниях ВДП, длительности и частоты курсов, сочетания с системными и местными антибиотиками, влияния на назальный и кишечный микробиом, риска формирования фагорезистентности, а также регуляторных и стандартизационных аспектов применения фагопрепаратов.
Цель исследования: исследовать эффективность бактериофагов в лечении ХРС-НП.
Материал и методы
В проспективное исследование, которое проходило в период с 2021 по 2025 г., вошли 66 пациентов с ХРС-НП в стадии обострения (группа 1), 39 женщин и 27 мужчин, средний возраст пациентов 42,81±1,36 года. Из них 25 пациентов, перенесших в анамнезе (от 1 года до 15 лет) эндоскопические вмешательства на пазухах носа, и 41 неоперированный пациент. Группу сравнения (группа 2) составили 30 пациентов с ХРС-НП в стадии обострения. Группа 2 была сопоставима с группой 1 по возрасту и полу — 17 женщин и 13 мужчин, средний возраст 42,17±2,01 года. По данным ВАШ течение синусита в обеих исследуемых группах оценено как среднетяжелое.
Все пациенты получали стандартную терапию согласно актуальным клиническим рекомендациям[1] (элиминационная терапия, топические интраназальные глюкокортикостероиды, топические антибактериальные препараты). Пациенты группы 1 в дополнение к стандартной терапии получали гель с бактериофагами (Отофаг). Его наносили после элиминационной терапии на слизистую носа по 2 мл 2 раза в день в течение 14 дней.
Все пациенты были осведомлены о предстоящем проведении исследований с применением бактериофагов, подписали информированное согласие на участие в исследовании. Исследование проведено в соответствии с принципами, изложенными в Хельсинкской декларации.
У всех участников исследования проводили риноцитограмму и идентификацию микроорганизмов, полученных из полости носа, с идентификацией чувствительности к антибиотикам и бактериофагам.
Микроскопическое исследование мазка со слизистой оболочки носа (риноцитограмма). Забор назального секрета проводили у всех включенных в исследование пациентов с использованием стерильного тампона. Полученный секрет наносили на предметное стекло и высушивали при комнатной температуре. Мазки фиксировали по Май-Грюнвальду и окрашивали по Романовскому — Гимзе. Цитологическое исследование проводили с применением светового микроскопа Zeiss PrimoStar (Германия) при 40- и 100-кратном увеличении (иммерсионный объектив). В препарате подсчитывали клетки с определением их типа (нейтрофилы, эозинофилы, базофилы, лимфоциты, моноциты, эпителиальные клетки). Изучали морфологию клеточных элементов. Оценивали наличие деструктивных изменений цитоплазмы, фагоцитоз.
Интерпретацию результатов проводили с учетом преобладания отдельных клеточных элементов. В качестве ориентировочных нормальных показателей риноцитограммы принимали: эозинофилы — 0–5% или единичные в поле зрения; нейтрофилы — единичные; лимфоциты — единичные; макрофаги — единичные; клетки эпителия — в умеренном количестве; слизь — в небольшом количестве. Повышение содержания эозинофилов более 5% расценивали как признак аллергического воспаления, преобладание нейтрофилов — как проявление воспалительного процесса [38].
Бактериологическое исследование. Для бактериологического исследования проводили забор мазка стерильным тампоном-зондом со слизистой оболочки носового хода. Материал доставляли в лабораторию с соблюдением всех требований транспортировки[2]. Посев проводили секторным методом на плотные питательные дифференциально-диагностические среды:
кровяной агар («Готовая питательная среда Колумбийский агар с бараньей кровью», «Биомедиа», Россия) — для выделения родов бактерий Streptococcus, Staphylococcus, Corynebacterium, Moraxella и др.;
желточно-солевой агар (Condalab, Испания) — для выделения и дифференциации стафилококков;
эндо (ФБУН ГНЦ ПМБ, Россия) — для выделения Enterobacteriaceae, грамотрицательных неферментирующих бактерий;
шоколадный агар (Condalab, Испания) — для выделения H. influenzae;
энтерококк-агар (Liofilchem, Италия) — для выделения бактерий рода Enterococcus.
Засеянные плотные питательные среды инкубировали в термостате при 37 °C в течение 24 ч1. Подсчет микроорганизмов и определение их концентрации (КОЕ/мл) проводили по расчетной таблице[3]
[39]. Клинически значимым считали титр ≥104 КОЕ/мл, положительным результатом лечения считали отсутствие роста или снижение титров патогенной и условно-патогенной флоры <104 КОЕ/мл.
Посевы оценивали, отмечали морфологию выросших колоний, форму роста микроорганизмов (в виде монокультуры или в смешанном виде). При обнаружении смешанной культуры на плотной питательной среде отмечали преимущественный рост какого-либо представителя. Производили рассевы отдельных колоний с целью получения чистых культур.
Видовую идентификацию бактерий проводили с помощью коммерческих наборов (Erba Lachema, EU) для биохимической идентификации: STAPHYtest, ENTEROtest, STREPTOtest, NEFERMtest на приборе ErbaScan. Для более точной идентификации представителей рода Staphylococcus использовали дополнительные тесты: на каталазную активность, коагулазную активность в отношении плазмы кролика, оксидазы, а также для представителей рода Enterobacter — тест на индол с использованием реактива Ковача, VP-тест (реакция Фогеса — Проскауэра), тест на оксидазную активность и тест сбраживания на трехсахарном агаре Олькеницкого.
Пробы были взяты у пациентов до начала терапии и не менее чем через 2 нед. после завершения лечения.
Также с целью субъективной оценки выраженности симптомов (боль в ОНП, гнойные выделения, головная боль, постназальный затек, снижение обоняние) пациентам проводили анкетирование по 10-миллиметровой визуальной аналоговой шкале (ВАШ) [40, 41].
Нежелательные явления оценивали в соответствии с Национальным стандартом РФ «Надлежащая клиническая практика»[4].
Статистическая обработка выполнена с использованием стандартных пакетов. Для определения характера распределения количественных показателей использовали критерий Колмогорова — Смирнова, для сравнения количественных показателей применяли t-критерий Стьюдента, для сравнения долей — критерий χ2. Различия считали статистически значимыми при p<0,05.
Результаты исследования
Микробиологические данные. До лечения в биологических образцах отделяемого из ОНП у большинства пациентов обеих групп преобладал S. aureus в клинически значимых титрах (≥104 КОЕ/мл). Также в клинически значимых титрах были выявлены патогены, вызывающие воспаление ВДП: Moraxella catarrhalis, P. aeruginosa, Escherichia coli и ряд других условно-патогенных микроорганизмов. После курса бактериофаготерапии в группе 1 у 52% прооперированных пациентов и у 38% неоперированных пациентов (в целом в 45% случаев) отмечена положительная динамика: увеличение количества комменсальной флоры (≥104 КОЕ/мл), снижение титров условно-патогенных бактерий (<104 КОЕ/мл) или их элиминация. В целом положительная динамика была отмечена у 30/66 (45%) пациентов в группе 1 против 6/30 (20%) в группе 2 (p=0,018).
Комбинированная терапия значимо чаще приводила к снижению выраженности воспаления, уменьшению количества нейтрофилов, лимфоцитов и десквамированного эпителия по данным риноцитограммы по сравнению со стандартной терапией: в группе 1 выявлено снижение воспаления у 32 (49%) пациентов, тогда как в группе 2 — только у 7 (23%) (p=0,016), что позволяет рассматривать фаготерапию как перспективный метод для уменьшения локального воспаления в полости носа.
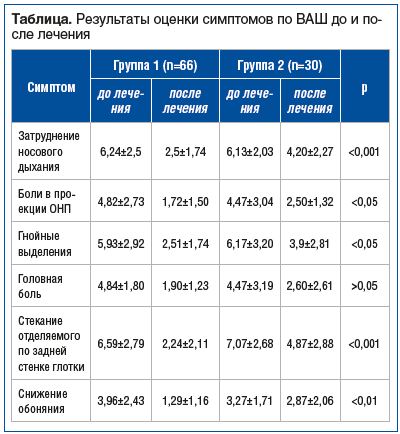
Клинические результаты по ВАШ. Среднее значение показателя ВАШ до лечения в группе 1 составило 5,40±2,55, в группе 2 — 5,26±2,70 (p=0,812), что соответствует среднетяжелому течению ХРС. После лечения средний балл по ВАШ в группе 1 составил 2,03±1,61, в группе 2 — 3,49±2,39 (p<0,01).
Как видно из таблицы, группа, получавшая Отофаг, продемонстрировала статистически значимо более выраженное улучшение, чем группа сравнения, по большинству оцениваемых субъективных симптомов. Наибольшая разница наблюдалась в динамике обоняния, постназального затека и затруднения носового дыхания. Балл по ВАШ относительно симптома «головная боль» достоверно снизился после лечения у всех обследованных пациентов, что указывает на положительную динамику этого симптома на фоне лечения, но статистических различий между группами 1 и 2 не получено. Это может быть обусловлено гетерогенностью причин, вызывающих головную боль.
Таким образом, результаты показывают, что добавление бактериофагов в стандартную терапию при ХРС-НП способствует улучшению микробиологической картины, снижает активность воспалительного процесса и уменьшает выраженность клинических симптомов.
Обсуждение
Хронический риносинусит без полипов представляет собой многофакторное, микробиологически и иммунологически сложное заболевание, в патогенезе которого ключевую роль играют дисбиоз синоназального микробиома, формирование устойчивых биопленок и антибиотикорезистентность основных бактериальных патогенов [14].
Результаты нашего исследования демонстрируют, что добавление комплексного препарата бактериофагов Отофаг к стандартной терапии ХРС-НП приводит к клинически и статистически значимому улучшению по целому ряду параметров: нормализация микробиоты, снижение воспалительной активности по данным риноцитограммы (уменьшение количества нейтрофилов, лимфоцитов и десквамированного эпителия) и уменьшение ведущих симптомов по ВАШ по сравнению со стандартной терапией. Нормализация микробиоты (элиминация или снижение титров S. aureus и других условно-патогенных бактерий <104 КОЕ/мл) достигнута у 45% пациентов основной группы против 20% в контроле, что согласуется с экспериментальными и клиническими работами, показавшими способность фаговых коктейлей эффективно лизировать клинические изоляты и разрушать биопленки P. aeruginosa и S. aureus у больных ХРС [33].
Показательно, что эффект фаготерапии оказался особенно выраженным у оперированных пациентов, перенесших эндоскопические вмешательства на ОНП. У этой подгруппы чаще формируются устойчивые биопленки и персистирующие формы инфекции, плохо поддающиеся системной и топической антибиотикотерапии, что ранее отмечалось в работах по микробным биопленкам при ХРС [41]. Наши данные о более высокой частоте нормализации микробиоты и снижении воспаления в подгруппе оперированных пациентов согласуются с концепцией «идеальной мишени» для фаготерапии, согласно которой предварительная хирургическая санация улучшает доступ препарата к биопленкам, а фаги, в свою очередь, обеспечивают дополнительную деконтаминацию и разрушение остаточных микробных сообществ [42]. Несмотря на полученные результаты, показывающие положительное влияние бактериофагов на состояние синоназального микробиома, полной элиминации патогенной флоры у пациентов группы 1 не наступило, что говорит о необходимости дальнейшего исследования особенностей топического влияния бактериофагов на состояние локального микробиома.
Отмеченное статистически значимое снижение выраженности симптомов (боль в области ОНП, гнойные выделения, постназальный затек, нарушение обоняния) в группе фаготерапии по сравнению с контролем коррелирует с лабораторными показателями и соответствует нашим данным пилотных клинических исследований локальной фаготерапии при ХРС, продемонстрировавших хорошую переносимость и клиническое улучшение при интраназальном применении фаговых коктейлей в течение 14–20 дней. Особенно важно, что достигнуто не только симптоматическое облегчение, но и объективное уменьшение воспалительной активности и коррекция микробного пейзажа, что потенциально должно приводить к снижению частоты обострений и потребности в повторных курсах антибиотиков [43].
Наши данные о более выраженной нормализации микробиоты и снижении воспаления при сочетанном использовании фагов и стандартной терапии хорошо вписываются в концепцию синергизма фагов и антимикробных препаратов, детально описанную в современных обзорах [44].
Клиническая значимость полученных результатов также связана с безопасностью фаготерапии. В наблюдаемой нами когорте не было зарегистрировано серьезных нежелательных реакций, требовавших отмены препарата; в 2 случаях отмечались лишь кратковременные местные явления (мимолетный дискомфорт, легкое жжение), не влияющие на приверженность лечению. Это согласуется с международным опытом применения фагов при ХРС и других хронических инфекциях ВДП, где фаготерапия демонстрирует благоприятный профиль безопасности даже при длительном и высокодозном местном применении [44, 45].
Несмотря на то, что полученные в ходе настоящей работы данные имеют предварительный характер ввиду особенностей дизайна исследования, проведенного с целью оценки перспективности использования бактериофагов в лечении пациентов с ХРС-НП (небольшой объем выборки, короткие сроки наблюдения, недифференцированный подход в зависимости от особенностей микробиома и т. д.), можно выделить направления для дальнейших исследований. В перспективе видится проведение рандомизированных двойных слепых плацебо-контролируемых исследований с длительным наблюдением, включающих объективные методы оценки состояния слизистой (эндоскопия, КТ), детальный микробиологический и метагеномный анализ синоназального микробиома и иммунологических показателей, изучение влияния фаготерапии на изменение факторов врожденного и адаптивного иммунитета, а также мониторинг возможного формирования фагорезистентности и ее клинического значения. Важным направлением является разработка стандартизированных, регистрируемых фаговых препаратов для оториноларингологии с четко определенным спектром действия, стабильностью и воспроизводимой концентрацией, а также интеграция фаготерапии в существующие клинические рекомендации по лечению ХРС в эпоху антибиотикорезистентности [45, 46].
Таким образом, наши результаты дополняют формирующуюся доказательную базу в пользу использования бактериофагов в комплексной терапии ХРС-НП и подтверждают, что фаготерапия обладает потенциалом в лечении пациентов с ХРС.
Заключение
Комплекс бактериофагов на гелевой основе может рассматриваться как эффективный компонент стандартной терапии ХРС-НП, мощный и перспективный инструмент в арсенале средств для лечения рефрактерного ХРС, особенно в случаях, ассоциированных с образованием биопленок и полирезистентными бактериальными патогенами. Уникальная способность фагов к специфическому лизису целевых бактерий и деструкции биопленочных матриц, сочетающаяся с благоприятным профилем безопасности, открывает новые возможности для преодоления ограничений антибиотикотерапии. Дальнейшие рандомизированные контролируемые исследования и работа по стандартизации препаратов являются необходимым условием для интеграции этого метода в рутинную клиническую практику оториноларингологии.
Статья опубликована при поддержке ООО НПЦ «МикроМир».
Конфликт интересов: Т.А. Кочеткова, Г.Т. Садикова, В.В. Юскевич, М.М. Гуркова являются сотрудниками ООО НПЦ «МикроМир».
Полный список литературы Вы можете найти на сайте http://www.rmj.ru
[1] Клинические рекомендации Минздрава России. Хронический синусит. 2025. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/view-cr/955_1 (дата обращения: 10.01.2026).
[2] Российские рекомендации по клинической микробиологии. Микробиологическое исследование биоматериалов из полости носа и околоносовых пазух. Документ 5/25 Год утверждения: 2025.
[3] Российские рекомендации. Определение чувствительности микроорганизмов к антимикробным препаратам. Версия 2024-02. Год утверждения (частота пересмотра): 2024 (пересмотр ежегодно). МАКМАХ, СГМУ: Смоленск; 2024.
[4] Национальный стандарт РФ ГОСТ Р 52379-2005 «Надлежащая клиническая практика». (Электронный ресурс.) URL: http://acto-russia.org/index.php?option=com_content&task=view&id=17#_Toc128806988 (дата обращения: 26.02.2026).
Информация с rmj.ru






