Введение
Внебольничная пневмония (ВП) является распространенным в педиатрической практике острым заболеванием инфекционной природы, характеризующимся преимущественным поражением паренхимы легких[1]. Поражения нижних дыхательных путей разнообразны и могут быть связаны с патогенами как вирусной, так и бактериальной природы. Особое место среди последних занимают атипичные микроорганизмы, в число которых входит Mycoplasma pneumoniae.
Установлено, что порядка 10% случаев ВП протекают осложненно. В число наиболее тяжелых осложнений ВП включают деструктивные, или некротизирующие, пневмонии (necrotizing pneumonia), при которых наблюдается некроз, гнойная деструкция с кавитацией легочной паренхимы [1].
Роль микоплазменной инфекции в развитии деструктивных пневмоний у детей в настоящее время остается до конца не ясной. Для неосложненных микоплазменных ВП характерно относительно доброкачественное течение с медленным развитием клинического процесса и склонностью к самостоятельному выздоровлению. Однако в последние годы все больше публикаций, особенно авторов из Восточной Азии, посвящено осложненному течению, в том числе деструкции легких, при ВП, вызванной M. pneumoniae [2, 3]. Таким образом, M. pneumoniae фигурирует в числе возможных этиологических факторов деструктивных пневмоний у детей, хотя и не входит в число основных патогенов, к которым относят Streptococcus pneumoniae, Staphylococcus aureus, Streptococcus pyogenes и Haemophilus influenzae [3–5]. Из-за отсутствия единых стандартов диагностики подтверждение микоплазменной инфекции является непростой задачей. Только при характерном анамнезе заболевания и клинической картине целесообразно исследование специфического IgM и определение ДНК M. pneumoniae в мазке со слизистой оболочки носо/ротоглотки при наличии сопутствующей эпидемиологической обстановки[2]. В то же время, учитывая распространенность микоплазменной инфекции, представляется важным исследование роли M. pneumoniae у детей при ВП, сопровождающихся деструкцией легочной ткани, что в России ранее не проводилось.
Цель исследования: установить роль M. pneumoniae при ВП, протекающих с деструкцией легочной ткани, у детей.
Содержание статьи
Материал и методы
Дизайн исследования — ретроспективное когортное наблюдательное исследование.
Нами была проанализирована медицинская документация детей, находившихся на стационарном лечении по поводу ВП в ГБУЗ «ДГКБ св. Владимира ДЗМ» в период с 01.01.2022 по 31.12.2024.
Критериями включения являлись: возраст 0–17 лет, диагноз ВП, положительный результат этиологической диагностики M. pneumoniae. Для подтверждения ассоциации с M. pneumoniae использовали полимеразную цепную реакцию (ПЦР) для выявления ДНК микроорганизма в мазке из ротоглотки, а также серологический метод с определением титра IgМ и IgG к M. pneumoniae.
Отдельно была выделена подгруппа детей с деструктивными осложнениями ВП, у которых, помимо стандартного, было проведено углубленное обследование: ПЦР с детекцией в режиме реального времени (ПЦР-РВ) ДНК M. pneumoniae в мазке из ротоглотки, жидкости бронхоальвеолярного лаважа (ЖБАЛ), плевральной жидкости. Кроме того, материал ЖБАЛ и/или содержимое плевральной полости исследовали в лаборатории молекулярной диагностики и эпидемиологии инфекций дыхательных путей ФБУН ЦНИИ Эпидемиологии Роспотребнадзора (г. Москва) с применением наборов реагентов для ПЦР-РВ производства АмплиСенс® (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора): Пневмо-квант-FL (для количественного определения ДНК S. pneumoniae и H. influenzae); S. pyogenes-скрин/монитор-FL (для количественного определения ДНК S. pyogenes); MRSA-скрин-титр-FL, Influenza virus A/B-FL (для выявления и количественного определения ДНК метициллин-чувствительного и метициллин-резистентного S. aureus, метициллин-резистентных коагулазонегативных Staphylococcus spp.), ОРВИ-скрин-FL; COVID-19-FL (для выявления и количественного определения РНК SARS-CoV-2); Enterovirus-FL (для выявления РНК энтеровирусов человека), а также лабораторной методики для выявления ДНК Acinetobacter baumannii, Klebsiella pneumoniae, Pseudomonas aeruginosa, Escherichia coli методом ПЦР-РВ.
Статистическая обработка результатов проведена в пакетах программ MS Office Excel 2019 и IBM SPSS Statistics (v.23). Нормальность распределения количественных переменных определена при помощи критерия Колмогорова — Смирнова. Данные описательной статистики представлены в виде средних и стандартных отклонений (M±SD) при нормальном распределении и в виде медианы и 1 и 3 квартилей (Ме, (Q1; Q3)) во всех остальных случаях. Качественные данные представлены в виде абсолютных значений и долей (в процентах от общего количества). Для сравнительного анализа использовали непараметрические критерии Манна — Уитни (при сравнении количественных показателей двух независимых групп) и Краскела — Уоллиса (при сравнении более двух групп), а также χ2 Пирсона или точный критерий Фишера (при сравнении качественных показателей). Различия считали статистически значимыми при р<0,05.
Результаты исследования
За трехлетний период (с 01.01.2022 по 31.12.2024) в ГБУЗ «ДГКБ св. Владимира ДЗМ» поступил 1271 ребенок с диагнозом «внебольничная пневмония». Из них у 308 (24,2%) человек (160 (51,9%) девочек и 148 (48,1%) мальчиков) определялись положительные маркеры M. pneumoniae. В таблице 1 представлены характеристики исследуемой когорты. В 78 (25,3%) случаях методом ПЦР-РВ в мазках из носо/ротоглотки был выявлен генетический материал возбудителя. У 271 (87,9%) ребенка серологическим методом были определены IgМ к M. pneumoniae, в 154 (50%) случаях были идентифицированы IgМ и IgG к M. pneumoniae.

У 65 (22,3%) пациентов (36 девочек и 29 мальчиков) ВП протекала с осложнениями: синпневмоническим плевритом, эмпиемой или ателектазированием.
У 14 человек (4,5% случаев во всей исследуемой когорте пациентов и 21,5% от всех случаев осложненных ВП) при инструментальном обследовании была диагностирована деструкция легочной ткани (деструктивная пневмония), в 12 случаях потребовались инвазивные вмешательства (санационная бронхоскопия, торакоскопия). По результатам ПЦР-РВ и определения уровня IgM во всех случаях деструктивных пневмоний инфицирование M. pneumoniae cчиталось подтвержденным. Также во всех случаях деструктивных пневмоний определялось сочетание M. pneumoniae со S. pneumoniae (n=4), S. pyogenes (n=3), Chlamydophila pneumoniae (n=4). В 3 случаях обнаружены вирусы: риновирус, метапневмовирус, бокавирус в сочетании с риносинцитиальным вирусом.
Результаты сравнительного анализа подгруппы детей с деструктивными пневмониями представлены в таблице 2. Для пациентов этой подгруппы характерны более тяжелое клиническое течение заболевания и выраженные изменения лабораторных показателей: у большинства пациентов (71%) отмечено диспноэ (р=0,013), продемонстрированы наибольшие показатели лейкоцитоза (р=0,011), уровня С-реактивного белка (СРБ) (р<0,0001), наименьшие показатели сатурации (р=0,037).
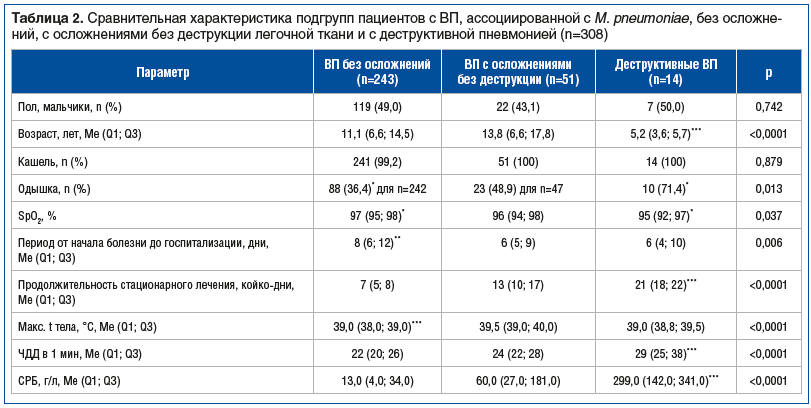
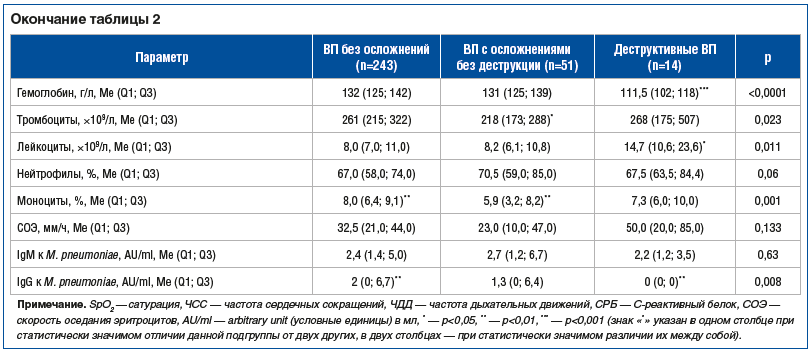
Все пациенты с деструктивными пневмониями получали антибактериальную терапию, однако препараты групп макролидов, тетрациклинов и фторхинолонов, обладающих доказанной эффективностью в отношении M. pneumoniae, были назначены только 3 больным из 14. В остальных случаях клинический эффект был достигнут при использовании стандартных схем антибактериальной терапии, назначаемых при деструктивных пневмониях. Летальных исходов в исследуемой когорте не было, у всех пациентов достигнуто клиническое выздоровление.
Обсуждение
Современные данные литературы подтверждают, что роль M. pneumoniae в качестве причины ВП в настоящее время увеличивается. Эта проблема наиболее актуальна в детской популяции старше 5 лет. Появляется все больше публикаций о тяжелом и осложненном течении ВП, вызванной M. pneumoniae [1, 6, 7].
Подтверждение микоплазменной пневмонии у детей является непростой задачей. Неспецифические клинические и рентгенологические проявления требуют лабораторного подтверждения. Метод ПЦР-РВ характеризуется высокой чувствительностью и специфичностью, однако период детекции ДНК M. pneumoniae после заражения может быть длительным, потенциально до 7 мес., а также возможно бессимптомное носительство M. pneumoniae. Поэтому положительный результат теста необходимо интерпретировать в совокупности с клиническими проявлениями [8, 9]. В то же время некоторые авторы называют ПЦР-РВ «золотым стандартом» диагностики микоплазменной инфекции. Дополнительной возможностью подтверждения инфицирования является оценка уровня специфических IgM, IgA, IgG. Их информативность ограничена в первые дни заболевания, так как IgM к M. pneumoniae определяются обычно не ранее 7 дней от начала заболевания, а у детей раннего возраста специфические антитела могут не выявляться из-за особенностей иммунного ответа [10]. Кроме того, существует риск ложноположительных результатов. Чувствительность серологического метода повышается при наличии парных образцов сыворотки, собранных с интервалом не менее 2 нед. для оценки сероконверсии или увеличения титра антител в 4 раза и более. Однако в клинической практике зачастую нет возможности контролировать уровень специфических антител после выписки пациента из стационара. В настоящей работе изучена M. pneumoniae у пациентов при ВП, осложненных деструкцией. При этом возбудитель, скорее всего, не является непосредственной причиной некроза участков легкого, но может быть фактором, провоцирующим реализацию другой бактериальной инфекции. Поэтому мы обсуждаем влияние M. pneumoniae на выраженность воспаления ткани легкого при деструктивной пневмонии.
Результаты нашего исследования продемонстрировали, что ВП, ассоциированные с M. pneumoniae, были зарегистрированы у 25% детей, находившихся на лечении в ГБУЗ «ДГКБ св. Владимира ДЗМ» с диагнозом «внебольничная пневмония». У 20% пациентов исследуемой когорты ВП протекала с различными осложнениями. Это превышает аналогичный показатель в исследовании X. Zhang et al. [11], согласно которому осложненные микоплазменные пневмонии были отмечены только у 12% детей с ВП. Вероятно, выявленные различия связаны с особенностями маршрутизации детей с осложненными пневмониями в г. Москве, согласно которой большинство из таких пациентов поступали в больницу, где набиралась исследуемая когорта.
Полученные результаты продемонстрировали, что деструктивная пневмония, ассоциированная с M. pneumoniae, встречается менее чем в 5% от всех выявленных случаев. Это соотносится с общемировыми данными, по которым некротизирующая пневмония развивается в 3–7% случаев от всех ВП с госпитализацией [7, 12].
Сравнительный анализ изучаемых подгрупп не выявил существенных отличий по полу и наличию кашля. Согласно полученным данным деструкция легочной ткани была характерна для детей младшего возраста, отличалась тяжелым течением с развитием у 75% детей диспноэ, высокой лихорадки, более низкими показателями SpO2. Диспноэ может рассматриваться как дифференциально диагностический критерий осложненного течения пневмонии. Статистически значимые различия выявлены между подгруппой детей с деструктивными изменениями и подгруппой неосложненной ВП (см. табл. 2). Также в подгруппе деструктивных пневмоний отмечены более высокие значения ряда лабораторных показателей: СРБ, количества лейкоцитов, процентного содержания нейтрофилов. Более низкие значения гемоглобина, более продолжительный срок госпитализации также характеризовали деструкцию легких. Выраженные как клинические, так и лабораторные изменения при деструктивной пневмонии объясняются воздействием патогенных микроорганизмов и гипервоспалительным ответом макроорганизма, скорее всего, при первой встрече с ними.
Согласно ряду исследований, различные респираторные патогены выявляются в 30–88% случаев микоплазменной ВП. При этом ко- и микст-инфекции характеризуются более тяжелым течением [13–16]. Утяжеление заболевания при сочетании M. pneumoniae с другими патогенами обусловлено несколькими механизмами. Локально повреждение тканей с выраженной воспалительной реакцией обеспечивает синергизм действия микробов, приводящий к нарушению мукоцилиарного клиренса. Аддитивное действие токсинов, которые продуцируют патогены, потенцирует воспалительный ответ. Иммунодисрегуляция проявляется гиперпродукцией провоспалительных цитокинов, в ряде случаев вплоть до «цитокинового шторма» с тяжелым повреждением легочной ткани и развитием некротизирующей пневмонии. На клеточном уровне дисфункция нейтрофилов и макрофагов ведет к нарушению элиминации бактерий, а также активации аутоиммунных процессов. Колонизация патогенами усиливается в результате дисбиоза микрофлоры бронхолегочного дерева, дисрегуляции рецепторов респираторных эпителиоцитов. Наконец, M. pneumoniae тропна к эндотелиальным клеткам и способна вызвать развитие эндотелиоза в очаге воспаления, приводящего к нарушению локального кровотока [17–19].
В нашем исследовании у детей с деструктивными пневмониями был отмечен более низкий титр IgM к M. pneumoniae (р>0,05) и отсутствие IgG, что может косвенно свидетельствовать о раннем первичном инфицировании. Скорее всего, первичное инфицирование M. pneumoniae способствовало выраженному локальному воспалительному процессу с дальнейшей реализацией инвазивной бактериальной инфекции с некрозом ткани легкого, вызванной грамположительной флорой. Однако следует помнить, что нельзя исключить и ложноположительный результат анализа из-за особенностей реагирования иммунной системы на другие патогены.
Следует также помнить об особенностях коллективного иммунитета в перипандемический период, когда во время пандемии COVID-19 циркуляция M. pneumoniae практически прекратилась, а в 2023–2024 гг. дети младшего возраста впервые столкнулись с возбудителем. Ответ на первичное инфицирование может быть иммунологически более ярким, приводя к выраженному воспалению. Коинфицирование в условиях напряженности иммунного ответа приводит к утяжелению течения заболевания [20].
Интересно, что в исследуемой когорте детей с деструктивными пневмониями антибактериальные препараты групп макролидов, тетрациклинов и фторхинолонов, обладающих доказанной эффективностью в отношении M. pneumoniae, получали только 3 пациента из 14. Однако клинический эффект был достигнут при использовании стандартных схем антибактериальной терапии, назначаемых при деструктивных пневмониях. Это, с одной стороны, вероятно, подтверждает только триггерную роль M. pneumoniae в развитии деструкции. С другой стороны, способность M. pneumoniae влиять на бронхиальную проводимость, в том числе из-за гиперпродукции густого секрета в результате индукции избыточной секреции муцинов MUC5AC и MUC5B, может удлинять течение заболевания [21]. Тяжесть течения заболевания на фоне ассоциации с M. pneumoniae также может усугубляться. Поэтому назначение антибактериальных препаратов, эффективных в отношении «атипичных» возбудителей, при лабораторном подтверждении такой ассоциации целесообразно.
Заключение
Маркеры M. pneumoniae были выявлены у 25% пациентов, находившихся на стационарном лечении по поводу ВП в исследуемый период. Установлено, что 20% случаев ВП, ассоциированной с M. pneumoniae, протекали с различными легочными осложнениями. Деструктивная пневмония была зарегистрирована в 4,5% случаев, при этом у всех пациентов выявлено сочетание M. pneumoniae с другими бактериями. Скорее всего, M. pneumoniae в случае развития деструкции при ВП играет роль триггера, который способствует активации более агрессивной патогенной флоры. Учитывая широкую распространенность микоплазменной инфекции в настоящее время, мы рекомендуем обследовать всех детей с осложненной пневмонией с целью подтверждения ассоциации с M. pneumoniae. При получении положительного результата целесообразно назначать антибактериальные препараты, эффективные в отношении «атипичных» возбудителей.
Полный список литературы Вы можете найти на сайте http://www.rmj.ru
[1] Клинические рекомендации Минздрава России. Пневмония (внебольничная). 2025. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/view-cr/714_2 (дата обращения: 20.12.2025).
[2] Клинические рекомендации Минздрава России. Бронхит. 2024. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/preview-cr/381_3 (дата обращения: 20.12.2025).
Информация с rmj.ru
