Содержание статьи
Введение
Врожденные пороки развития (аномалии, мальформации) женских половых органов — это стойкие внутриутробные отклонения от вариаций нормы величины, формы, пропорций, симметрии, топографии и органогенеза, повлекшие нарушение их функции [1, 2]. Женская репродуктивная система включает в себя матку, шейку матки, фаллопиевы трубы, яичники и влагалище. Считается, что фаллопиевы трубы, матка, шейка матки и верхние две трети влагалища берут свое начало из парамезонефрических (мюллеровых) протоков, тогда как нижняя часть влагалища образуется из урогенитального синуса [3, 4]. Врожденные пороки развития женских половых органов составляют 14% от всех врожденных аномалий развития [5] и 3–7% в структуре гинекологических заболеваний детей и подростков [1]. Аномалии развития женских половых органов занимают особое место в патогенезе бесплодия [6, 7]. Формы мальформаций женских половых органов могут варьировать в зависимости от тяжести течения. Выделяют легко протекающие и, как правило, бессимптомные аномалии, которые тем не менее способны вызывать грозные акушерские нарушения. В том числе существуют крайне серьезные пороки развития женских половых органов, такие как маточные и влагалищные агенезии, синдром Майера — Рокитанского — Кюстера — Хаузера (СМРКХ) и обструктивные маточно-влагалищные аномалии, к которым относятся гематокольпос, атрезия влагалища / шейки матки, поперечная и продольная влагалищные перегородки и рудиментарный рог матки [8–10].
Цель настоящего обзора: поиск актуальных классификаций и современных методов диагностики врожденных пороков развития половых органов у девочек для дальнейшего выбора персонализированной тактики лечения.
Поиск литературы для данного обзора проводили в базах данных PubMed и eLibrary. В процессе поиска была использована следующая комбинация ключевых слов: malformations AND congenital AND female AND genital. По результатам поиска найдено 485 работ — систематических обзоров, обзоров литературы и клинических исследований. Они были проанализированы по названию и абстракту, затем часть из них была изучена в полном тексте. В качественный анализ включены 48 статей.
Классификация врожденных пороков развития женских половых органов
В настоящее время наиболее современными классификациями аномалий женских половых органов являются классификация ESHRE 2013 г. [11] и обновленная классификация ASRM 2021 г. (MAC2021) [12].
Классификация ESHRE 2013 г. [11]
Аномалии женских половых органов в данной классификации делятся на 2 группы: 1) аномалии матки и 2) аномалии шейки матки и влагалища.
Аномалии развития матки, в свою очередь, разделяют на классы и подклассы.
Существует 6 больших классов аномалий развития матки:
-
U0 — нормальная матка;
-
U1 — аномальное строение матки, которое разделяют на следующие основные подклассы: Т-образная матка, инфантильная матка и др.;
-
U2 — матка с внутриматочной перегородкой. В данном классе выделяют 2 подкласса: частичная и полная внутриматочные перегородки;
-
U3 — удвоение матки. В данном классе выделяют 3 подкласса: частичное, полное удвоение матки и удвоенная матка, разделенная перегородкой;
-
U4 — однорогая матка, которая делится на 2 подкласса: однорогая матка с рудиментарной полостью или без таковой. Первый подкласс включает полость либо сообщающуюся с маткой, либо не сообщающуюся с ней. Соответственно второй подкласс может включать в себя рог без полости, либо рог может вовсе отсутствовать;
-
U5 — аплазия матки. Данный класс также разделяют на 2 подкласса — с рудиментарной полостью или без нее. Первый подкласс включает в себя уни-/билатеральный рог, а второй класс — уни-/билатеральный рог или непосредственно аплазию;
-
U6 — неклассифицируемые аномалии.
Аномалии шейки матки и влагалища разделяют на сосуществующие классы.
К мальформациям шейки матки относятся:
-
C0 — нормальная шейка матки;
-
С1 — шейка матки с перегородкой;
-
С2 — удвоение шейки матки;
-
С3 — аплазия одной из шеек;
-
С4 — аплазия шейки матки.
В свою очередь, аномалии влагалища включают следующие классы:
-
V0 — нормальное влагалище;
-
V1 — продольная перегородка влагалища без обструкции;
-
V2 — продольная перегородка влагалища с обструкцией;
-
V3 — поперечная перегородка влагалища и/или неперфорированная девственная плева;
-
V4 — аплазия влагалища.
В обновленной классификации ASRM 2021 г. (MAC2021) [12] выделяют 5 больших групп аномалий женских половых органов, к которым относятся: 1) аномалии матки; 2) аномалии влагалища; 3) комплексные аномалии; 4) агенезия мюллеровых протоков; 5) агенезия шейки матки.
Полная адаптированная классификация ASRM 2021 г. (MAC2021) представлена на рисунках 1 и 2.

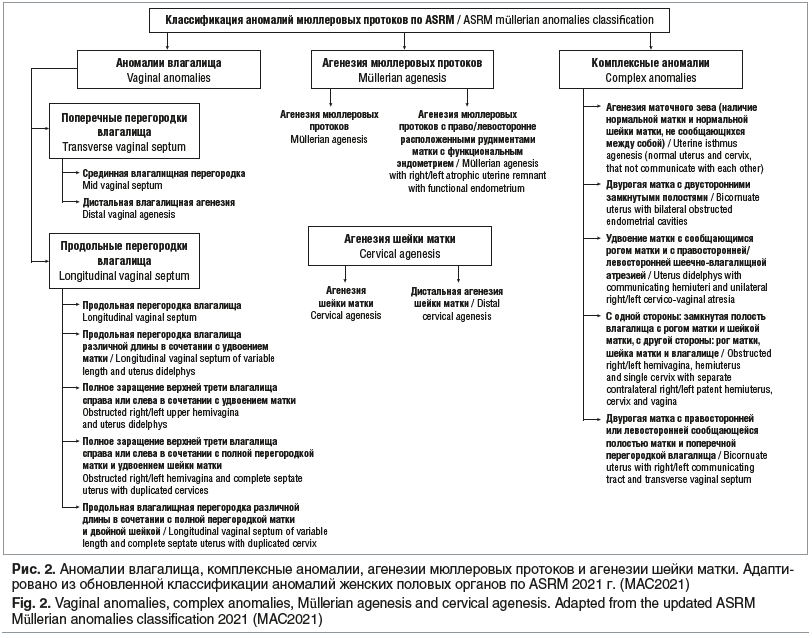
Несмотря на актуальность представленной выше обновленной классификации ASRM 2021 г. (MAC2021), A. Ludwin et al. [13] отмечают в ней следующие недостатки: данная классификация не поддерживается проспективными исследованиями и высококачественными систематическими обзорами, опубликованными за последние 30 лет; в списке литературы были упущены важные и надежные исследования, которые являются основой для создания качественной классификации наиболее распространенных врожденных аномалий матки [14–17]; одно из рандомизированных контролируемых исследований в области аномалий мюллеровых протоков также отсутствует в списке литературы [18].
Кроме представленных выше классификаций, существуют патологии, имеющие авторские названия:
Синдром Майера — Рокитанского — Кюстера — Хаузера — аплазия влагалища и матки, в том числе в сочетании с функционирующими рудиментами матки [1]. Данный синдром встречается у одной из 4500–5000 женщин [19]. Описано 2 типа СМРКХ: тип I включает только аплазию матки и влагалища с нормальным развитием яичников и других систем, а тип II, или MURCS-ассоциация (Mullerian duct aplasia, Renal dysplasia and Cervical Somite anomalies), включает аплазию матки и влагалища и сопутствующие дефекты, такие как пороки развития почек, скелета (чаще в шейно-грудном отделе), дефекты слуха и редкие сердечные аномалии [3, 20]. При агенезии мюллеровых протоков происходят следующие изменения: влагалище заметно укорочено и может выглядеть как ямочка под уретрой, могут присутствовать одиночный рудимент матки по средней линии или рога матки (с полостью или без полости). Яичники, учитывая их независимое эмбриологическое происхождение, обычно сохраняют нормальную структуру и функцию, хотя могут быть расположены атипично. Дифференциальную диагностику первичной аменореи необходимо проводить с такими патологиями, как: врожденные аномалии развития половых органов; 46 ХY — нарушения полового развития, включая синдром нечувствительности к андрогенам; неперфорированная девственная плева [21].
Синдром Херлина — Вернера — Вундерлиха, или OHVIRA (Obstructive Hemivagina и Ipsilateral Renal Anomaly), представляет собой ассоциативный порок развития мочеполовой системы: удвоение матки и одностороннюю аплазию нижних двух третей удвоенного влагалища и почки [22]. Распространенность данной патологии до сих пор неизвестна, по некоторым оценкам, она составляет 1 случай на 4000–50 000 женщин [23, 24]. Настоящий порок разделяют на 2 типа в зависимости от полного или неполного заращения влагалища. Синдром Херлина — Вернера — Вундерлиха с полной непроходимостью верхней трети влагалища обычно диагностируется в период полового созревания с такими симптомами, как циклическая тазовая боль и дисменорея из-за задержки менструальной крови. Напротив, у пациенток с неполной влагалищной непроходимостью регулярные менструации и медленное распространение гематокольпоса приводят к поздней диагностике [22, 25]. При данном варианте патологии пиометрокольпос может возникать из-за вторичного инфицирования скопившейся жидкости. Инфекция при неполном заращении верхней трети влагалища часто обостряется во время беременности, вероятно, из-за повышенной активности желез [26, 27].
Матка Роберта — это сочетание полной перегородки матки c наличием двух асимметричных полостей с ипсилатеральной агенезией почки [28].
Этиология и патогенез врожденных пороков развития женских половых органов
Врожденные пороки развития женских половых органов относятся к спорадическим заболеваниям, возникающим при сбое на каком-либо этапе эмбриогенеза, и их этиология до сих пор не установлена. Момент, в который происходит сбой, определяет тип порока развития, и чем раньше во время беременности он возникает, тем он серьезнее [1, 9]. Предполагается роль молекулярно-генетических, тератогенных, наследственных и других факторов в развитии данных аномалий [1]. Некоторые исследования отражают связь пороков развития женских половых органов с генными мутациями, и наиболее известными из них являются HOXA13 (ладонно-подошвенный генитальный синдром) [29] и HOXA10, экспрессируемые в эмбриональных парамезонефральных протоках [30]. На сегодняшний день выявлена причинно-следственная связь с врожденными пороками развития для еще нескольких генов — HNF1B, WNT4, WNT7A, однако подтверждения такой связи для большинства предполагаемых генов все еще нет [31]. Аномалии развития женских половых органов, вызванные влиянием таких лекарственных средств, как диэтилстилбестрол и талидомид, также описаны в литературе [9].
Выделяют 3 фазы развития мюллеровых протоков, нарушение любой из которых приводит к развитию врожденных аномалий женских половых органов: 1) органогенез — этап образования обоих парамезонефральных протоков; 2) слияние обоих мюллеровых протоков, что приводит к образованию матки и верхней части влагалища; 3) резорбция перегородки, включающая в себя лизис горизонтально сросшихся мюллеровых протоков, что приводит к образованию полости матки. Аномалии органогенеза заключаются в дефектах развития мюллеровых протоков и приводят к агенезии и гипоплазии (например, отсутствие матки или однорогая матка) [32].
Клинические проявления врожденных пороков развития женских половых органов
Аномалии развития матки и влагалища, которые вызывают нарушение оттока менструальной крови и клинически проявляются циклическими болями в дни менструации, образованием гематокольпоса, гематометры, гематосальпинкса и клиникой острого живота, являются наиболее частыми причинами обращений в стационар девочек-подростков [5, 33]. Клинические проявления пороков развития женских половых органов зависят от возраста манифестации патологии. Так, у младенцев данные аномалии приводят в большей степени к появлению общего беспокойства, выбухания тканей промежности в области вагинального кольца, реже вызывают клиническую картину острого живота, задержку мочеиспускания и кишечную непроходимость. В то же время атрезия девственной плевы или аплазия нижней трети влагалища у девочек-подростков при значительном гематокольпосе может проявляться болями в области промежности, затрудненным актом дефекации и мочеиспускания [1, 34, 35]. Пациентки, имеющие свищевые ходы между удвоенными влагалищами или матками, а также пациентки с наличием полной перегородки матки могут жаловаться на кровянистые или гнойные выделения из половых путей [36, 37]. В то же время клинические проявления в случае полного удвоения матки и влагалища или при наличии внутриматочной перегородки могут отсутствовать или же выражаться дисменореей умеренной степени выраженности [38]. Мальформации, имеющие авторские названия, такие как СМРКХ, синдром Херлина — Вернера — Вундерлиха, матка Роберта, проявляются следующим образом: первый из вышеперечисленных синдромов является наиболее частой причиной первичной аменореи у девочек-подростков и вызывает циклические тазовые боли, а также клинику острого живота, в то время как два других обычно проявляются схваткообразной болью в нижних отделах живота, которая может усиливаться с каждой последующей менструацией [1, 35]. Необходимо проводить дифференциальную диагностику врожденных пороков развития женских половых органов, вызывающих нарушения оттока менструальной крови, с неперфорированной девственной плевой. Неперфорированная девственная плева — это патология, которая может проявляться в неонатальном периоде в виде гидрокольпоса или же мукокольпоса, вызванных материнскими эстрогенами [10, 27, 39, 40]. У большинства пациенток с неперфорированной девственной плевой наблюдаются первичная аменорея, циклические тазовые боли или задержка мочи, вторичные по отношению к гематокольпосу или гематометрокольпосу [27, 41–43]. В период полового созревания у пациенток с гематокольпосом обычно наблюдается выпячивание во влагалище тонкой ткани с темным/голубоватым оттенком [10].
Диагностика врожденных пороков развития женских половых органов
Большинство врожденных пороков развития женских половых органов без нарушения оттока менструальной крови не имеют каких-либо характерных клинических проявлений и могут быть случайной находкой [1]. Значительная часть аномалий может быть найдена во время лечения бесплодия и поисков его причины. Точная диагностика и классификация мальформаций женских половых органов необходимы для консультирования пациенток относительно их лечения, потенциального репродуктивного прогноза и возможных рисков, а также для планирования любых вмешательств с целью улучшения результатов лечения бесплодия [44].
Оценка внешних и внутренних контуров дна матки является ключевым звеном, позволяющим корректно поставить диагноз и классифицировать те или иные аномалии матки [45–48]. В прошлом «золотым стандартом» диагностики врожденных пороков развития женских половых органов была комбинированная операция, включающая в себя одномоментную лапароскопию и гистероскопию, несмотря на то, что эти способы являются инвазивными. Методы визуализации, такие как ультразвуковое исследование (УЗИ) органов малого таза, гистеросальпингография (ГСГ), соногистерография и магнитно-резонансная томография (МРТ), являются менее инвазивными методами скрининга и поиска различных аномалий матки [45]. Несмотря на то, что стандартное 2D-трансвагинальное УЗИ (2-TVS) и ГСГ считаются эффективными и достоверными методами скрининга, 3D-TVS и МРТ точнее диагностируют врожденные мальформации женских половых органов, поскольку с их помощью возможно оценить внешние и внутренние контуры матки [44, 46].
2D-трансвагинальное УЗИ (2D-TVS) — это наименее инвазивный, легкодоступный, безопасный и наиболее экономически выгодный метод оценки морфологической структуры матки и исключения ее аномалий [47]. 2D-TVS, как правило, используется в качестве скринингового метода в учреждениях первичного звена здравоохранения [48].
Гистеросальпингография — это метод, обычно используемый для оценки проходимости маточных труб в рамках лечения бесплодия и поиска его причин, который также является хорошим скрининговым тестом на наличие врожденных аномалий половых органов [49]. Данный метод позволяет визуализировать полость матки только в том случае, если она сообщается с шейкой, следовательно, случаи несообщающихся рудиментарных рогов матки могут быть упущены из виду. Кроме того, ГСГ не позволяет оценить внешние контуры дна матки, поэтому ее невозможно применять для дифференциальной диагностики перегородчатой и двурогой матки [44, 47].
В то же время 3D-TVS является основным методом дифференциальной диагностики между двурогой, перегородчатой и седловидной матками, так как позволяет оценить внешний контур (серозную поверхность матки) и внутренний контур (полость матки) дна матки [50, 51].
При двурогой матке глубина вдавливания дна >1 см [12], при этом влагалище и шейка матки имеют нормальное строение.
В случае перегородчатой матки при УЗИ будут визуализироваться 2 близко расположенные полости матки и нормальный контур дна матки (в отличие от двурогой матки, при которой определяется вдавливание дна матки). Длина перегородки, измеренная от линии, проходящей через интерстиций дна матки, до вершины перегородки, составляет более 1 см, при этом угол вдавливания <90° [12]. Перегородка, разделяющая полость матки, обычно тонкая и может быть различной длины, продолжаясь до шейки матки или влагалища (продольная перегородка влагалища) [48]. Систематический обзор и метаанализ [52], сравнивающий эффективность применения 2D-TVS, 2D-соногистерографии и 3D-TVS для диагностики перегородчатой матки, показал следующие результаты: суммарная чувствительность и специфичность составили 83 и 99% для 2D-TVS, 94 и 100% для 2D-соногистерографии и 98 и 100% для 3D-TVS соответственно. Учитывая эти результаты и инвазивность двухмерной соногистерографии, можно сделать вывод, что 3D-TVS — лучший метод диагностики перегородчатой матки, но поскольку это оборудование доступно не во всех центрах, оптимальным вариантом диагностики перегородчатой матки может быть двухмерная соногистерография [52]. Для дифференциальной диагностики перегородчатой и двурогой матки было предложено измерять угол расхождения рогов матки: угол менее 75° характерен для перегородчатой матки, а угол более 105° — для двурогой [21].
Касаясь вопроса диагностики седловидной матки, важно обратить внимание на то, что такая матка имеет слабое вдавливание дна с расширением полости матки. УЗ-картина седловидной матки имеет следующие критерии: вдавливание дна матки менее или равно 1 см и угол вдавливания >90° [12].
Диагностика удвоения матки основывается на УЗ-картине, на которой визуализируются два далеко друг от друга расположенных маточных рога с глубоким вдавлением дна матки, одновременно с этим при влагалищном исследовании будут определяться две шейки матки. У 15–20% пациенток с удвоением матки встречаются полное заращение верхней трети влагалища и ипсилатеральная агенезия почки; в 65% случаев аномалии развиваются справа [53]. Во всех вышеперечисленных случаях 3D-TVS помогает подтвердить тот или иной диагноз. Данные, продемонстрированные в работе А.С. Аракелян и соавт. [48], подтверждают диагностические преимущества 3D-TVS перед 2D-TVS и отражают необходимость более широкого применения 3D-TVS на этапе предоперационной подготовки для выбора оптимальной хирургической тактики.
Магнитно-резонансная томография — это чувствительный способ идентификации всех аномалий матки, который обеспечивает получение многоплоскостной характеристики мягких тканей и, одновременно, позволяет оценивать различные показатели шире, чем другие методы визуализации, включая УЗИ [38]. Также данный способ оказывается крайне полезным в диагностике сочетанных аномалий шейки матки и влагалища. Кроме того, МРТ позволяет точно определить аберрантное расположение гонад или анатомию почек и является неинвазивным методом по сравнению с лапароскопией и гистероскопией.
В качестве дополнительных методов исследования при аномалиях женских половых органов рекомендуют проводить УЗИ органов брюшной полости или МРТ c целью выявления возможных аномалий развития почек (из-за возможной связи с почечными аномалиями ввиду тесного эмбриогенеза) [44]. Так, в исследовании P.K. Heinonen [54] из 378 пациенток с аномалиями развития женских половых органов у 18,8% были выявлены аномалии развития почек, причем наиболее частым пороком была односторонняя агенезия почки (12,2%), реже выявлялись подковообразная почка, удвоение собирательной системы почки, тазовая почка и др.
Заключение
Врожденные пороки развития (аномалии, мальформации) — это внутриутробные отклонения от показателей нормы величины, формы, пропорций, симметрии, топографии и органогенеза, приводящие к нарушению функции соответствующего органа. Распространенность данной патологии составляет 3–7% среди гинекологических заболеваний детей и подростков и занимает особое место у пациенток с бесплодием. Как систематизация, так и диагностика данных аномалий крайне сложны, и на сегодняшний день не существует единой общепринятой классификации врожденных патологий развития половых органов у девочек.
Дальнейший поиск новых методов диагностики и выявление современных «золотых стандартов» диагностики, а также составление единой классификации необходимы для верной постановки диагноза и определения дальнейшей персонализированной тактики лечения врожденных пороков развития половых органов у девочек.
Сведения об авторах:
Адамян Лейла Владимировна — д.м.н., профессор, академик РАН, главный специалист по гинекологии Минздрава России, заведующая кафедрой репродуктивной медицины и хирургии ФПДО ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; заместитель директора по научной работе, руководитель отделения оперативной гинекологии ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России; 117997, Россия, г. Москва, ул. Академика Опарина, д. 4; ORCID iD 0000-0002-3253-4512.
Сибирская Елена Викторовна — д.м.н., профессор кафедры репродуктивной медицины и хирургии ФДПО ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; профессор кафедры акушерства и гинекологии имени академика Г.М. Савельевой ПФ РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; главный внештатный специалист гинеколог детского и юношеского возраста Министерства здравоохранения МО, заведующая хирургическим гинекологическим отделением РДКБ — филиала ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 119571, Россия, г. Москва, Ленинский пр-т, д. 117, к. 1; ORCID iD 0000-0002-4540-6341.
Пивазян Лаура Горовна — ординатор 2-го года ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России; 117997, Россия, г. Москва, ул. Академика Опарина, д. 4; ORCID iD 0000-0002-6844-3321.
Давыдова Юлия Денисовна — студентка 6-го курса ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-9840-3710.
Тарлакян Вероника Артуровна — студентка 4-го курса ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0009-0003-5302-3097.
Контактная информация: Пивазян Лаура Горовна, e-mail: laurapivazyan98@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов: отсутствует.
Статья поступила 18.08.2023.
Поступила после рецензирования 12.09.2023.
Принята в печать 05.10.2023.
About the authors:
Leyla V. Adamyan — Dr. Sc. (Med.), Professor, Academician of the Russian Academy of Sciences, Chief Obstetrician-gynecologist of the Ministry of Health of the Russian Federation, Head of the Department of Reproductive Medicine and Surgery, A.I. Yevdokimov Moscow State University of Medicine and Dentistry; 4, Dolgorukovskaya str., Moscow, 127006, Russian Federation; Deputy Director for Research, Head of the Department of Operative Gynecology, Kulakov National Medical Research Center for Obstetrics, Gynecology and Perinatology; 4, Academician Oparin str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-3253-4512.
Elena V. Sibirskaya — Dr. Sc. (Med.), Professor of the Department of Reproductive Medicine and Surgery, A.I. Yevdokimov Moscow State University of Medicine and Dentistry; 4, Dolgorukovskaya str., Moscow, 127006, Russian Federation; Professor
of the Department of Obstetrics and Gynecology named after Academician G.M. Savelyeva, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; Chief Consultant Obstetrician-gynecologist of Children and Young Adults of the Ministry of Health of the Moscow Region, Head of the Department of Surgical Gynecology, Republican Children’s Clinical Hospital, the Branch of Pirogov Russian National Research Medical University; 117, bldg. 1, Leninskii Ave, Moscow, 119571, Russian Federation; ORCID iD 0000-0002-4540-6341.
Laura G. Pivazyan — resident physician of the 2nd year, Kulakov National Medical Research Center for Obstetrics, Gynecology and Perinatology; 4, Academician Oparin str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-6844-3321.
Yulia D. Davydova — 6th year student, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, bldg. 2, Trubetskaya str., Moscow, 119991, Russian Federation, ORCID iD 0000-0001-9840-3710.
Veronika A. Tarlakyan — 4th year student, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, bldg. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0009-0003-5302-3097.
Contact information: Laura G. Pivazyan, e-mail: laurapivazyan98@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 18.08.2023.
Revised 12.09.2023.
Accepted 05.10.2023.
Информация с rmj.ru