Введение
Розацеа – это хроническое воспалительное поражение кожи сложного генеза, которое преимущественно проявляется в центральной области лица, развитие которого в основном обусловлено ангиопатиями и иммунными отклонениями [1]. Клинические проявления розацеа вариабельны, определяют подтип заболевания и проявляются от транзиторной эритемы до развития папуло-пустулезных высыпаний, фим и поражения глаз [2].
Ввиду преимущественной локализации розацеа на коже лица, у пациентов часто наблюдаются сопутствующие выраженные психоэмоциональные отклонения, включая снижение уверенности в себе и трудности в общении. Пациенты часто страдают от значительных психологических расстройств и проблем с самооценкой, находятся в состоянии постоянного стресса и социальной дезадаптации, что негативно сказывается на качестве их жизни [3].
Розацеа характеризуется хроническим течением, при котором периоды улучшения состояния чередуются с обострениями, сопровождается постепенным нарастанием симптомов и частым развитием устойчивости к проводимому лечению [4]. Несмотря на значительный прогресс в изучении данного заболевания, его причины и механизмы развития все еще требуют дальнейшего исследования. В настоящее время розацеа рассматривается как заболевание, развитие которого связано с влиянием разнообразных внешних и внутренних факторов [5]. Проведенные ранее исследования подтвердили, что розацеа представляет собой воспалительный процесс, сопровождающийся активацией неоангиогенеза, расширением сосудов и нарушением эндотелиальной функции. Эти изменения обусловлены экспрессией вазоактивных пептидов под воздействием внешних триггеров [6].
Патогенетически значимым белком в патофизиологии розацеа является фактор роста эндотелия сосудов (vascular endothelial growth factor, VEGF) — цитокин, в 50 тыс. раз превосходящий по активности гистамин. Он способствует вазодилатации, стимулирует ангиогенез и увеличивает сосудистую проницаемость [7]. Синтез VEGF в кератиноцитах активируется провоспалительными цитокинами, которые в свою очередь инициируются экзогенными факторами [8]. Под влиянием VEGF разрушаются волокна дермы посредством матриксных металлопротеиназ, что приводит к снижению тонуса и увеличению ломкости сосудов, усугубляя проявления розацеа [9]. Избыточная продукция VEGF усиливает процессы ангиогенеза и миграцию моноцитов, что приводит к формированию периваскулярных инфильтратов. Эти клетки выделяют провоспалительные цитокины, усиливая воспалительный каскад, запущенный VEGF [10]. Воспаление в коже с участием иммунокомпетентных клеток приводит к дилатации сосудов, образованию новых капилляров, клеточной инфильтрации и хроническому воспалению [11]. Клинически это проявляется эритемой, телеангиэктазиями, папулами и пустулами. На поздних стадиях заболевания происходит разрастание соединительной ткани и гиперплазия желез, формируются фимы, отмечается застой в кровеносных и лимфатических сосудах [12]. Ангиогенез неизменно сопровождает воспалительный процесс, который, даже если не запускает воспаление, значительно усиливает его проявления. Это приводит к переходу воспаления в хроническую форму, а в тяжелых случаях розацеа становится устойчивой к проводимому лечению, что препятствует достижению ремиссии [13].
Современные методы терапии розацеа ориентированы на устранение основных проявлений заболевания, улучшение качества жизни пациентов, предотвращение его прогрессирования и обеспечение стойкой ремиссии [14]. Учитывая хроническую и рецидивирующую природу заболевания, обусловленную ангиопатией, закономерно включение ангиопротекторов в комплексную терапию дерматоза. Их применение позволит снизить проницаемость сосудов, улучшить реологические свойства крови, уменьшить отечность тканей, активировать метаболические процессы в стенках сосудов и контролировать процесс неоангиогенеза [15]. Достижения медицинских технологий открывают возможности для использования лазерной терапии. Одним из хорошо известных методов лазеротерапии является внутривенное лазерное облучение крови (ВЛОК). Этот метод эффективно используют в комплексной терапии различных заболеваний, в том числе и хронических дерматозов, с долгосрочным эффектом. Биохимические изменения в клетках, вызванные лазерным облучением, инициируют запуск реакций в организме, нормализуя функции иммунной и сосудистой систем, активируя метаболические и пролиферативные процессы. Фотобиологические эффекты низкоинтенсивного лазерного излучения свидетельствуют о целесообразности применения этого метода у пациентов с розацеа [16].
Цель исследования: оценить воздействие сочетанной терапии, включающей 1% ивермектин крем, ангиопротектор троксерутин и ВЛОК, на сосудистый и воспалительный компоненты у пациентов с эритематозно-телеангиэктатическим (ЭТР) и папуло-пустулезным (ППР) подтипами розацеа.
Содержание статьи
Материал и методы
Набор пациентов для исследования проводился в период с 2020 по 2023 г. на базе кафедры кожных и венерических болезней ФГБОУ ВО «Российский университет медицины» Минздрава России (Москва), и кожно-венерологического отделения ГБУЗ МО «ДБ» (Долгопрудный).
Пациенты подписывали информированное согласие на участие в исследовании. Работа была одобрена локальным этическим комитетом ФГБОУ ВО «Российский университет медицины», протокол № 11–22 от 17.11.2022.
Критерии включения: мужчины и женщины, достигшие 18 лет; подтвержденный диагноз «розацеа» (эритематозно-телеангиэктатический и папуло-пустулезный подтипы); согласие на участие в исследовании и подписание информированного согласия пациента.
Критерии невключения: наличие тяжелого соматического заболевания в стадии декомпенсации; наличие онкологической патологии; пациенты с признаками выраженного психоза, поражения центральной нервной системы; беременность и период грудного вскармливания; пациенты, длительно использующие местные глюкокортикостероиды для терапии розацеа.
Критерии исключения: добровольное решение пациента прекратить участие в исследовании; наступление беременности в ходе исследования; возникновение аллергических реакций или других нежелательных явлений при использовании исследуемых препаратов.
Пациенты были разделены методом простой слепой рандомизации на три группы:
группа I (n=30): монотерапия ивермектином в лекарственной форме крем 1% 1 р/день вечером с нанесением на очищенную кожу лица в течение 12 нед.;
группа II (n=30): ивермектин в лекарственной форме крем 1% 1 р/день вечером с нанесением на очищенную кожу лица в течение 12 нед. и троксерутин внутрь по 1 капсуле 300 мг 3 р/день в течение 90 дней;
группа III (n=30): ивермектин в лекарственной форме крем 1% 1 р/день вечером с нанесением на очищенную кожу лица в течение 12 нед. и троксерутин внутрь по 1 капсуле 300 мг 3 р/день в течение 90 дней. Также пациентам данной группы проводили ВЛОК с излучающей головкой КЛ-ВЛОК-405 (НИЦ «Матрикс», Россия, Рязань) мощностью 2,5 мВт, длиной волны 0,63 мкм. Катетер-ВЛОК устанавливали в периферическую вену и присоединяли к магистральному световоду. Процедуры проводились курсом из 9 сеансов с экспозицией 30 мин 1 раз в 10 дней.
Состояние пациентов оценивалось по Шкале диагностической оценки розацеа (ШДОР) до и через 12 нед. терапии. Данная шкала предусматривала балльную оценку степени выраженности таких симптомов, как эритема, телеангиэктазии, количество папул и пустул, а также сухость, жжение, покалывание и отечность кожи лица. Максимальное количество баллов, указывающее на тяжелое течение розацеа, составляет 21 балл. Минимальное количество баллов — 0 [17].
До и через 12 нед. после начала лечения оценивали показатели микроциркуляции и системы свертывания крови. Для анализа состояния микроциркуляции применяли аппарат «АнгиоСкан-01 П» (ООО «АнгиоСкан», Россия, Москва), функционирующий на основе измерения частоты сердечных сокращений, определения биологического возраста сосудов, показателя жесткости сосудистой стенки и уровня стресса. Регистрация фотоплетизмограммы осуществлялась в течение 5 мин, после чего данные подвергались компьютерной обработке и анализу.
Для оценки состояния системы свертывания крови применялся тест тромбодинамики (ООО «ГемаКор», Россия, Москва). Метод основан на моделировании процесса тромбообразования в условиях, приближенных к физиологическим. Параметры тромбообразования определяли с помощью лазерной интерферометрии.
Оценка возникновения нежелательных реакций проводилась по 4-балльной шкале: 1 балл — отсутствие нежелательных реакций; 2 балла — легкие нежелательные реакции, не требующие медицинского вмешательства; 3 балла — нежелательные реакции, требующие назначения дополнительных средств для их устранения; 4 балла — выраженные нежелательные реакции, при которых дальнейшее использование метода невозможно.
Статистическая обработка полученных данных проводилась с применением статистической программы Statistica 10. Распределение данных соответствовало нормальному, поэтому для попарного сравнения двух групп использовался t-критерий Стьюдента для независимых выборок. Результаты представлены в виде среднего значения и стандартного отклонения (M±SD). Различия считались статистически значимыми при р<0,05.
Результаты исследования
В исследование были включены 90 пациентов с клинически подтвержденным диагнозом розацеа. Подтип ЭТР был диагностирован у 55 пациентов (61,11%), из которых 15 составляли мужчины и 40 — женщины. Подтип ППР выявлен у 35 (38,89%) пациентов, включая 11 мужчин и 24 женщины.
Средняя продолжительность заболевания составляла 3,55±1,20 года. Из анамнеза пациентов, участвующих в исследовании, были выявлены следующие триггерные факторы, способствующие развитию розацеа и поддержанию клинических проявлений дерматоза: инсоляция у 76 (84,44%), эмоциональный стресс у 71 (78,88%), употребление алкоголя у 67 (74,44%), температурные воздействия у 65 (72,22%), погрешности в диете у 55 (61,11%), интенсивные физические нагрузки у 50 (55,55%) и неправильный уход за кожей у 44 (48,88%). В большинстве случаев розацеа провоцировалась несколькими факторами одновременно: пациенты указывали от 3 до 5 факторов. Кроме того, были зарегистрированы сопутствующие заболевания: сердечно-сосудистые заболевания у 40 (44,44%), варикозная болезнь нижних конечностей у 38 (42,22%), патология желудочно-кишечного тракта у 33 (33,33%), эндокринные заболевания у 28 (31,11%), болезни мочевыделительной системы у 24 (26,665), хронические заболевания ЛОР-органов у 20 (22,22%), хронические заболевания легких у 15 (16,66%), заболевания нервной системы у 14 (15,55%), а также достаточно часто отмечалось сочетание нескольких нозологий.
До начала терапии показатель ШДОР (баллы) в группе I составил 9,83±1,21, в группе II — 9,96±0,85, в группе III — 9,73±0,78. Между группами статистически значимых различий не выявлено (р=0,221 между I и II группами; р=0,264 между I и III; р=0,235 между II и III), что свидетельствует о сопоставимости пациентов на старте исследования.
После 12 нед. терапии во всех группах отмечено статистически значимое снижение индекса ШДОР. В группе I показатель снизился до 8,66±0,75 баллов (р=0,027), однако улучшение было связано преимущественно с регрессом воспалительных элементов (папул и пустул), тогда как эритема, телеангиэктазии, сухость кожи, жжение и отек сохранялись без значимой динамики. В группе II индекс ШДОР снизился до 4,06±0,38 баллов (р=0,003), при этом отмечено улучшение по большинству клинических параметров, за исключением телеангиэктазий. В группе III снижение индекса ШДОР оказалось наиболее выраженным — до 0,83±0,12 баллов (р=0,001), причем улучшение наблюдалось по всем оценочным критериям, включая воспалительные элементы, эритему, телеангиэктазии, сухость кожи, жжение и отек.
После терапии выявлены статистически значимые меж-групповые различия: между группами I и II (р=0,002), I и III (р=0,001), II и III (р=0,001), что указывает на различную эффективность применяемых методов лечения.
Таким образом, до терапии статистически значимых межгрупповых различий не наблюдалось, что подтверждает однородность выборки. Внутригрупповая динамика показала статистически значимое улучшение во всех группах, но степень регресса клинических проявлений различалась. Межгрупповые различия после терапии оказались значимыми, что подчеркивает неодинаковую эффективность применяемых терапевтических подходов.
Оценка динамики средних значений индекса ШДОР в результате лечения в зависимости от подтипа розацеа представлена на рисунках 1 и 2.
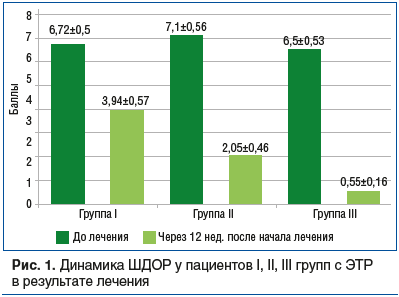
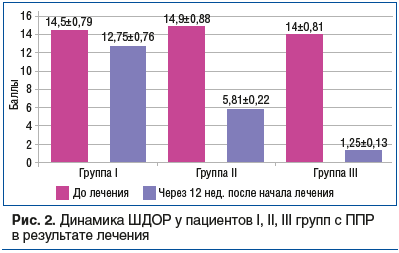
Сравнительная оценка динамики клинических проявлений розацеа в терапевтических группах показала, что включение в комплексную терапию дерматоза ангиопротектора и воздействие лазерного излучения на венозную кровь способствовали наибольшему достижению ремиссии дерматоза. Так, в группе I проведение стандартной наружной терапии привело к снижению средних значений индекса ШДОР через 12 нед. наблюдения на 41,37% при ЭТР и на 50,21% при ППР; в группе II динамика индекса составила 71,13% при ЭТР и 61,01% при ППР; в группе III ШДОР уменьшился на 91,54% при ЭТР и 91,07% при ППР.
Далее была проведена регистрация количества пациентов с обоими подтипами розацеа, достигших показателей ШДОР 0 баллов (полная клиническая ремиссия): в группе I — 4 (13,33%), в группе II — 19 (63,33%) и в группе III — 26 (86,67%) больных.
Обоснованием терапевтической эффективности в различных группах послужили результаты инструментального обследования пациентов. Динамика показателей фотоплетизмографии представлена в таблице 1.
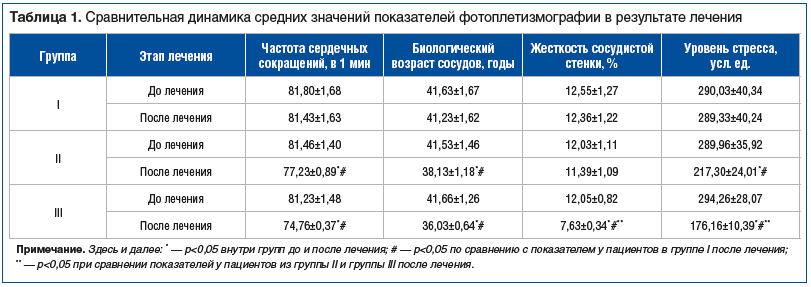
В результате проведенной терапии было установлено положительное ангиопротективное действие троксерутина, что проявлялось не только положительной динамикой показателей функции эндотелия сосудистой стенки после лечения, но и значительным улучшением данных показателей по отношению к таковым в группе I. Однако включение в комплексную терапию ВЛОК привело к нормализации показателей эндотелиальной функции не только относительно первоначальных, но и относительно показателей в группах I и II, что указывало на наилучший клинический эффект.
Сравнительная динамика средних значений параметров тромбодинамики, полученных в результате терапии, представлена в таблице 2.
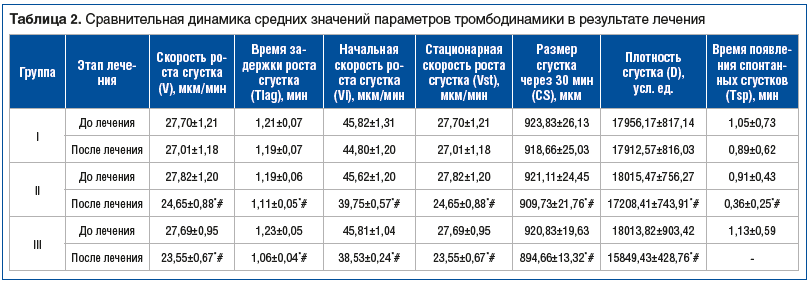
При оценке результатов исследования тромбодинамики наблюдали схожую тенденцию. Применение троксерутина и ВЛОК привело к улучшению реологических свойств крови, устранению склонности к тромбообразованию, снижению плотности и размера сгустка крови, что, безусловно, было причиной формирования более выраженного клинического ответа в группах с комплексной терапией, а также однозначно оказывало положительный эффект на состояние микроциркуляции организма в целом.
Пациенты трех групп хорошо переносили лечение, ни в одной не наблюдалось нежелательных реакций и серьезных нежелательных явлений.
Настоящее исследование продемонстрировало высокую эффективность сочетанной терапии, включающей 1% крем ивермектин, ангиопротектор троксерутин и ВЛОК. Особое значение имеет нормализация эндотелиальной функции сосудов и микроциркуляции, что вносит вклад в уменьшение сосудистого и воспалительного компонентов розацеа. Эти результаты согласуются с данными H. Husein-ElAhmed et al. [18], которые показали, что применение крема ивермектина приводит к значительному уменьшению воспалительных элементов при ППР, а также улучшает барьерную функцию кожи.
Полученные данные подтверждают перспективность применения сочетанной терапии в клинической практике. Ранее схожие методики изучались в работе Л.С. Кругловой и соавт. [19], где было продемонстрировано, что комплексное использование импульсного лазера на красителе (595 нм) и 1% ивермектина эффективно устраняет сосудистые проявления и воспалительные элементы розацеа. Наши результаты дополняют эти данные, показывая, что включение в терапию ангиопротекторов и ВЛОК не только улучшает клинические проявления заболевания, но и способствует нормализации микроциркуляции, улучшению реологических свойств крови и снижению склонности к тромбообразованию. Высокая эффективность предложенного подхода и отсутствие значимых побочных эффектов позволяют рекомендовать его для пациентов с различными подтипами розацеа, особенно с ЭТР и ППР.
Перспективными направлениями будущих исследований являются изучение долгосрочной эффективности и безопасности данной терапии, анализ ее влияния на качество жизни пациентов. Также важно провести исследования с участием большего числа пациентов для подтверждения универсальности подхода.
Среди ограничений исследования следует отметить небольшой размер выборки и отсутствие группы с длительным наблюдением для оценки устойчивости ремиссии. Также отсутствует сравнение с другими современными методами терапии розацеа, что ограничивает возможности критической оценки предложенного метода.
В отличие от предыдущих работ, сосредоточенных на отдельных компонентах терапии (например, применение только ивермектина или лазерных методик), данное исследование подчеркивает синергический эффект сочетанного метода. Полученные результаты значительно превосходят эффективность стандартных методов лечения, что согласуется с ограниченными данными о применении ВЛОК при розацеа [20].
Заключение
Представленное исследование подтверждает высокую клиническую значимость сочетанной терапии, включающей 1% ивермектин крем, ангиопротектор троксерутин и ВЛОК. Данная методика продемонстрировала превосходство в лечении розацеа по сравнению со стандартными подходами, способствуя ремиссии у 86,67% пациентов. Терапия оказывает комплексное воздействие на сосудистый и воспалительный компоненты патогенеза, улучшая микроциркуляцию, реологические свойства крови и снижая склонность к тромбообразованию. Отсутствие побочных эффектов подтверждает ее безопасность. Ограничения исследования указывают на необходимость дальнейшего изучения, включая длительные наблюдения и сравнительные анализы с другими терапевтическими подходами. Однако уже сейчас предложенная терапия может быть рекомендована для широкого применения в клинической практике.
Информация с rmj.ru






