Содержание статьи
Введение
Эндотелиальная дисфункция (ЭД) и окислительный стресс являются важными механизмами формирования и прогрессирования как сердечно-сосудистой, так и бронхолегочной патологии [1, 2]. В частности, это относится к самому распространенному сердечно-сосудистому заболеванию — артериальной гипертензии (АГ), которая в 34,3% случаев сочетается с хронической обструктивной болезнью легких (ХОБЛ) [3]. В связи с этим актуальным является изучение изменений состояния функции эндотелия и перекисного окисления липидов (ПОЛ) под воздействием назначенной терапии, а значит, поиск лекарственных препаратов, положительно влияющих не только на гемодинамические изменения, но и патогенетические механизмы прогрессирования данных заболеваний.
Согласно последним европейским и российским клиническим рекомендациям по АГ [4, 5], одним из основных классов антигипертензивных препаратов считаются тиазидные и тиазидоподобные диуретики. Их польза при сопутствующей ХОБЛ обусловлена тем, что они не нарушают вентиляционно-перфузионное отношение в легких, не влияют на тонус легочных сосудов и бронхов. Однако их использование может вызвать ряд побочных эффектов, таких как гипокалиемия, гипомагниемия, гиперурикемия, повышение уровня глюкозы сыворотки крови, изменение липидного состава крови [4, 5]. В связи с этим актуален поиск наиболее эффективных препаратов из этой группы, положительно влияющих как на состояние сосудистой стенки, так и на течение сопутствующей ХОБЛ, при этом обладающих минимальными побочными эффектами.
Цель исследования: провести сравнительную оценку гипотензивного эффекта, а также влияния на функцию эндотелия, окислительный стресс и давление в легочной артерии хлорталидона и гидрохлортиазида в составе комбинированной антигипертензивной терапии больных АГ в сочетании с ХОБЛ через 6 мес. лечения.
Материал и методы
Проведено проспективное исследование, включавшее 66 пациентов с АГ и ХОБЛ. Исследование одобрено локальным этическим комитетом ФГБОУ ВО НижГМА Минздрава России (протокол № 10 от 25.12.2017).
Критерии включения: эссенциальная АГ 1–3-й степени; ХОБЛ I–III стадии по GOLD вне обострения; добровольное информированное согласие на участие в исследовании. Критерии исключения: возраст младше 18 лет; вторичная АГ; ишемическая болезнь сердца в анамнезе; хроническая сердечная недостаточность со сниженной фракцией выброса и выше III функционального класса; клапанная болезнь сердца с гемодинамически значимыми нарушениями; ХОБЛ в стадии среднетяжелого и тяжелого обострения; тяжелая сопутствующая патология; онкологические заболевания; беременность, лактация; бронхиальная астма; перенесенные острые воспалительные заболевания в течение месяца до начала
исследования.
Диагноз АГ ставили на основании критериев согласно рекомендациям по АГ (ESC/ECH 2018, РКО 2020) [4, 5]. Степень АГ определялась по уровню артериального давления (АД), зарегистрированному у пациента до назначения антигипертензивной терапии. Стратификацию риска развития сердечно-сосудистых осложнений осуществляли на основе шкалы SCORE. Диагноз ХОБЛ устанавливали на основании анамнестических данных, клинической картины заболевания, объективного осмотра и по результатам инструментальных исследований в соответствии с Глобальной инициативой по ХОБЛ (GOLD, 2017, 2020) [6, 7].
Методом свободного конвертирования пациенты были разделены на две группы. В качестве основной гипотензивной терапии пациентам 1-й группы была назначена фиксированная комбинация азилсартана медоксомила 40 мг и хлорталидона 12,5 мг — препарат Эдарби® Кло. Больные 2-й группы получали свободную комбинацию азилсартана медоксомила 40 мг (Эдарби®) и гидрохлортиазида 12,5 мг. Группы были сопоставимы по полу, возрасту, тяжести основной патологии (табл. 1).
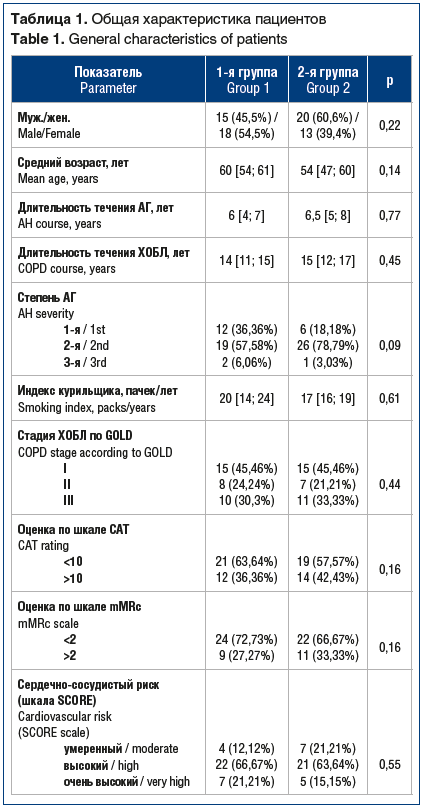
Исходно пациенты получали гипотензивную терапию антигипертензивными препаратами различных классов, в т. ч. ингибиторами ангиотензинпревращающего фермента,
β-адреноблокаторами, однако целевой уровень АД меньше 130/80 мм рт. ст. согласно европейским рекомендациям 2018 г. и российским рекомендациям 2020 г. по АГ не был достигнут, поэтому эти препараты у всех пациентов были отменены. В терапии ХОБЛ согласно клиническим рекомендациям GOLD 2019 г. использовались β2-агонисты, м-холинолитики, ингаляционные глюкокортикостероиды или комбинация указанных классов бронхолитических препаратов. Терапия была эффективной, все больные находились вне обострения ХОБЛ, поэтому дозы препаратов в ходе исследования не менялись.
Обследование включало сбор жалоб, уточнение анамнеза заболевания и жизни, проведение общесоматического осмотра и комплекс лабораторно-инструментальных исследований.
Лабораторное обследование заключалось в определении уровня продуктов ПОЛ (диеновых конъюгатов (ДК), триеновых конъюгатов (ТК), оснований Шиффа (ОШ)) по методу И.А. Волчегорского (1989), содержания оксида азота (NO) по методу П.П. Голикова (2004), уровня эндотелина-1 (ЭТ-1) методом иммуноферментного анализа с помощью коммерческой тест-системы Quantikine ELISA Endotelin-1 (R&D Systems, США) согласно прилагаемой инструкции, интенсивности свободнорадикального окисления методом индуцированной биохемилюминесценции сыворотки крови по методу Е.И. Кузьминой, А.С. Нелюбина, М.К. Щенниковой (1983) (S, Imax).
Инструментальные методы исследования включали: суточное мониторирование АД (СМАД), эхо-допплерокардиографию (ЭхоДКГ), пробу на эндотелийзависимую вазодилатацию (ЭЗВД), оценку функции внешнего дыхания (ФВД). Оценка АД проводилась посредством СМАД на регистраторе «BPLab МнСДП-2» (Россия) с определением суточного профиля и параметров АД. Исследование ФВД выполнено на аппарате «Cestgraph HI-101» (CHEST, Япония). ЭхоДКГ проведена на ультразвуковом аппарате «GEVIVID 7 Pro» (США) с измерением среднего давления в легочной артерии. Для выявления ЭД проводили ультразвуковое исследование с использованием ультразвукового датчика с высоким разрешением по методу D. Celermajer (1992).
Статистическая обработка выполнена при помощи лицензионной программы Statistica 10.0. Количественные данные представлены в виде медианы и интерквартильного размаха (Me [Q25; Q75]), качественные — в виде абсолютных и относительных показателей. Анализ вида распределения проводили с использованием критерия Колмогорова — Смирнова. Различия считали статистически значимыми при р<0,05.
Результаты исследования
Исходно группы были сопоставимы по уровню систолического АД (САД) (р=0,73) и диастолического АД (ДАД) (р=0,13). На фоне лечения в обеих группах через 1 мес. выявлено статистически значимое снижение САД (р<0,001; табл. 2).
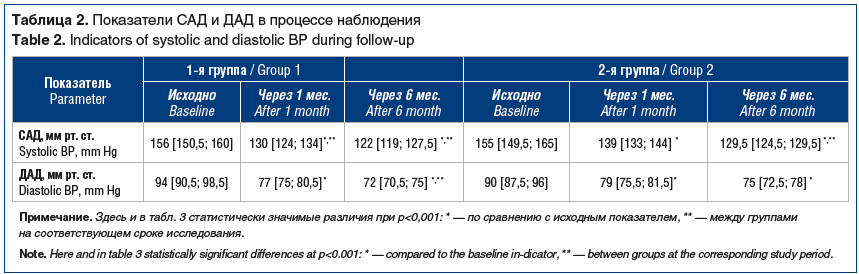
При межгрупповом сравнении медианных значений САД выявлено, что более значимо САД снизилось в 1-й группе пациентов, получавших лечение азилсартана медоксомилом в сочетании с хлорталидоном, так как к концу 1-го мес. лечения САД в этой группе снизилось на 26 [22,5; 30,5] мм рт. ст., а во 2-й группе — на 16 [11,5; 21,5] мм рт. ст.
По показателю ДАД в каждой группе выявлена аналогичная статистически значимая положительная динамика (см. табл. 2). При межгрупповом сравнении статистически значимой разницы не выявлено (р=0,1). В 1-й группе пациентов к концу 1-го мес. лечения среднее ДАД снизилось на 17,5 [14; 20] мм рт. ст., а во 2-й группе — на 11 [9,5; 17] мм рт. ст.
Следует отметить, что целевое АД (меньше 130/80 мм рт. ст.) через 1 мес. исследования было достигнуто у 30 (91%) больных в 1-й группе и у 17 (51,5%) — во 2-й группе.
По результатам СМАД при назначении терапии азилсартана медоксомилом в сочетании с хлорталидоном через 6 мес. лечения показано статистически значимое снижение дневного и ночного САД и ДАД (р<0,001), а также достоверное снижение вариабельности как САД, так и ДАД в дневное и ночное время (р<0,001) и среднего пульсового АД (р<0,001) (табл. 3).
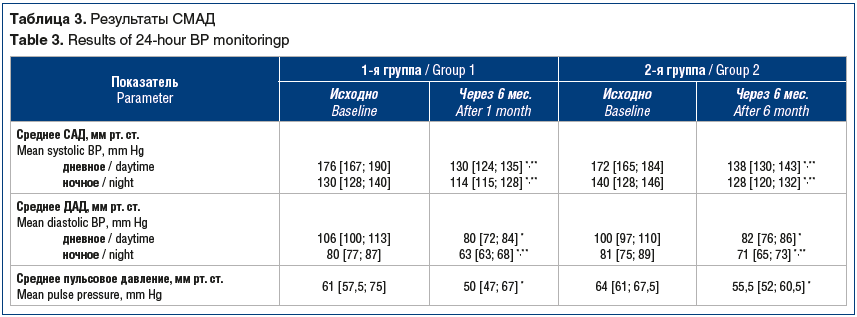
На момент включения в исследование методом СМАД было выявлено 60,6% больных с суточным профилем АД non-dipper, 36,4% — с night-peaker, 3% — с dipper. По прошествии 6 мес. лечения за счет уменьшения числа пациентов с недостаточным снижением АД в ночные часы (night-peaker и non-dipper), количество больных с нормальным суточным типом АД (dipper) составило 78,8%. У остальных 21,2% пациентов суточный профиль АД соответствовал типу non-dipper.
Через 6 мес. исследования всем пациентам удалось достичь целевого АД без повышения дозы препарата. У 12 больных, имевших утреннюю гипертензию, через 6 мес. лечения отмечено уменьшение утреннего САД в среднем на 7,0±2,1% и ДАД — на 10±7,3%.
У всех пациентов, получавших азилсартана медоксомил в сочетании с гидрохлортиазидом, через 6 мес. лечения достигнуты целевые значения АД (см. табл. 3), однако
в 4 наблюдениях пришлось увеличить дозу гидрохлортиазида до 25 мг. Исходно пациентов с недостаточным снижением ночного АД (non-dipper) было 63,6%, с повышенным профилем АД (night-peaker) — 36,4%. Через 6 мес. за счет уменьшения числа пациентов с недостаточным снижением АД в ночные часы (night-peaker и non-dipper) количество больных с нормальным суточным типом АД (dipper) составило 36,4%. В 57,6% наблюдений суточный профиль АД соответствовал типу non-dipper, в 6% — night-peaker. У 13 больных, имевших утреннюю гипертензию, через 6 мес. отмечено уменьшение утреннего САД в среднем на 6,3±5,9% и ДАД — на 4,8±4,6%.
Таким образом, у пациентов, страдающих АГ в сочетании с ХОБЛ, терапия с применением фиксированной комбинации азилсартана медоксомила с хлорталидоном Эдарби® Кло обладает более выраженным антигипертензивным эффектом в отличие от терапии азилсартана медоксомилом с гидрохлортиазидом. Приверженность терапии у пациентов обеих групп была одинаково высокой, так как они находились под наблюдением врача-исследователя, поэтому исключается ее влияние на результаты терапии. Таким образом, разницу в результатах терапии всецело можно связать с разным антигипертензивным эффектом хлорталидона и гидрохлортиазида.
При исследовании показателей ЭД и окислительного стресса были получены следующие результаты (табл. 4).
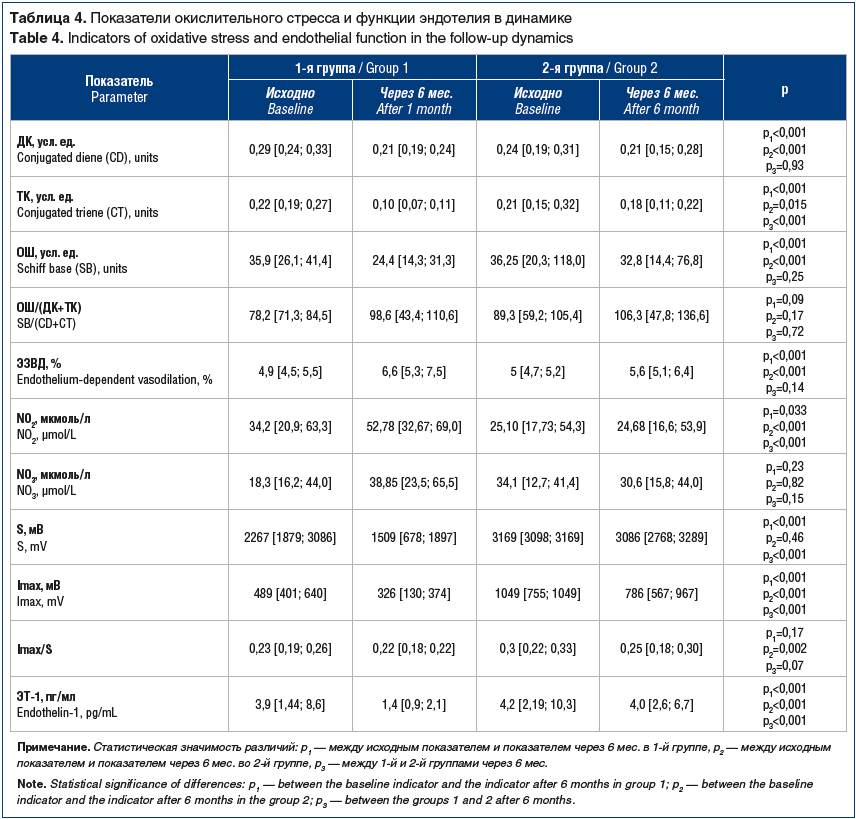
В 1-й группе через 6 мес. лечения достоверная положительная динамика наблюдалась в отношении ДК, ТК, NO2, S, Imax, ОШ, ЭЗВД, ЭТ-1, а во 2-й группе — в отношении ДК, ТК, Imax, ОШ, ЭЗВД, ЭТ-1. В целом более выраженное улучшение лабораторных показателей, характеризующих ЭД и окислительный стресс, отмечалось в 1-й группе. Статистически значимые результаты при сравнении 1-й и 2-й групп получены для ТК, NO2, S, Imax, ЭТ-1 (см. табл. 4).
При выполнении пробы на ЭЗВД исходно дилатационная реакция плечевой артерии была снижена у всех больных 1-й группы и составила в среднем 4,9 [4,5; 5,5] %. Через 6 мес. ЭЗВД возросла и составила 6,6 [5,3; 7,5] % (р<0,001). Во 2-й группе исходно ЭЗВД также была ниже нормы —
5 [4,7; 5,2] % и достоверно увеличилась к концу лечения до 5,6 [5,1; 6,4] % (р<0,001). Однако различия ЭЗВД между группами были статистически незначимыми (р=0,14).
Стоит отметить положительное влияние назначенной терапии в виде уменьшения давления в легочной артерии через 6 мес. лечения в обеих группах, однако в 1-й группе достигнутая положительная динамика статистически значимо отличалась от таковой во 2-й группе (рис. 1). Полученные результаты связаны, по-видимому, с улучшением функции эндотелия в сосудах малого круга кровообращения на фоне лечения.
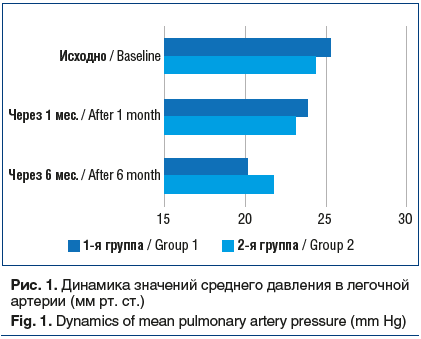
При оценке показателей бронхиальной проходимости по данным ФВД отмечалось статистически значимое улучшение показателя ОФВ1 в обеих группах, однако прирост составил меньше 100 мл, что является клинически незначимым.
Также следует отметить, что комбинация азилсартана медоксомила с хлорталидоном оказалась метаболически нейтральной в отношении электролитов крови, уровня мочевой кислоты и глюкозы сыворотки крови, что говорит о безопасности применения данной комбинации, тогда как при использовании комбинации азилсартана медоксомила с гидрохлортиазидом отмечалось снижение уровня калия с 4,2 [3,9; 4,6] до 3,8 [3,5; 4,3] ммоль/л (p=0,003) и увеличение уровня мочевой кислоты c 236 [211; 327]
до 304 [267; 367] мкмоль/л (p=0,008).
Обсуждение
В лечении больных АГ с ХОБЛ оправдано назначение препаратов, не только эффективно снижающих АД, но и отвечающих ряду требований, таких как: адекватный контроль АД в ночные и ранние утренние часы; совместимость препаратов с базисными средствами лечения ХОБЛ; отсутствие эффектов, ухудшающих вентиляцию легких; положительное влияние на гемодинамику малого круга кровообращения; выраженные кардио- и вазопротективные эффекты [3, 8]. Также необходимо, чтобы выбранный препарат влиял на патогенетические механизмы формирования АГ при ХОБЛ.
В основе развития АГ при ХОБЛ лежит раннее формирование ЭД в малом и большом круге кровообращения, повышение симпатической активности с дисбалансом синтеза катехоламинов, оксидативный стресс, хроническое системное воспаление, дисбаланс в ренин-ангиотензин-альдостероновой системе (РААС) [9, 10]. Блокаторы РААС, прежде всего блокаторы рецепторов ангиотензина II, являются препаратами выбора при лечении АГ у больных ХОБЛ [3–5].
Хорошо известно их положительное воздействие не только на уровень АД, но и на течение ХОБЛ у указанной категории больных [3, 8]. То же самое можно сказать и про антагонисты кальция, прежде всего амлодипин [4, 5]. Таким образом, комбинация блокатора РААС с антагонистом кальция в этой ситуации выглядит наиболее рациональной. Однако нередко гиперволемический тип кровообращения, гиперсимпатикотония, проявляющаяся тахикардией и нарушениями ритма, наличие побочных эффектов у антагонистов кальция (особенно при использовании высоких доз) не позволяют назначить их в составе комбинированной терапии больных АГ с сопутствующей ХОБЛ. Встает вопрос о комбинированной терапии блокатором РААС и диуретиком. Самым популярным у российских докторов является тиазидный диуретик гидрохлортиазид, несмотря на его хорошо известные побочные эффекты, которые становятся более выраженными при увеличении дозы и присутствуют практически у всех пациентов, получающих препарат в дозе выше 12,5 мг/сут [4, 5].
Не так давно на российском рынке появился принципиально отличный от гидрохлортиазида по фармакокинетическим характеристикам диуретик хлорталидон. К сожалению, в России он отсутствует в чистом виде и представлен только в составе фиксированной комбинации с азилсартана медоксомилом — Эдарби® Кло. В различных рандомизированных клинических исследованиях изучены клинические и фармакологические эффекты гидрохлортиазида и хлорталидона [11, 12]. Также имеются сравнительные исследования комбинированной терапии азилсартана медоксомилом с гидрохлортиазидом или с хлорталидоном, которые демонстрируют преимущество последнего по влиянию на АД и безопасности использования [13, 14]. Однако отсутствуют даже единичные работы, которые выявили бы положительное влияние комбинированной терапии АГ с диуретиком хлорталидоном на показатели ПОЛ и ЭД, тем более у больных с сопутствующей ХОБЛ, когда это особенно важно, так как через окислительный стресс и дисфункцию эндотелия происходит прогрессирование заболеваний.
Заключение
Терапия АГ у больных с сопутствующей ХОБЛ фиксированной комбинацией азилсартана медоксомила и хлорталидона — препаратом Эдарби® Кло по сравнению с терапией свободной комбинацией азилсартана медоксомила с гидрохлортиазидом через 6 мес. лечения оказывает более выраженное антигипертензивное действие, положительно влияя при этом на суточный профиль АД, давление в легочной артерии, функцию эндотелия и процессы перекисного окисления липидов.
При назначении больным АГ в сочетании с ХОБЛ диуретиков в составе комбинированной терапии предпочтение следует отдавать хлорталидону ввиду его большей антигипертензивной эффективности и положительного влияния на окислительный стресс, функцию эндотелия, давление в легочной артерии вместо традиционно используемого в российской клинической практике гидрохлортиазида.
Благодарность
Редакция благодарит АО «Нижфарм» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgment
Editorial Board is grateful to JSC Nizhfarm for the assistance in technical edition of this publication.
Сведения об авторах:
Григорьева Наталья Юрьевна — д.м.н., доцент, профессор кафедры, и.о. заведующего кафедрой клинической медицины, Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского, 603950, Россия, г. Нижний Новгород, просп. Гагарина, д. 23; ORCID iD 0000-0001-6795-7884.
Самолюк Марина Олеговна — ассистент кафедры клинической медицины, Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского, 603950, Россия, г. Нижний Новгород, просп. Гагарина, д. 23; ORCID iD 0000-0001-9118-5327.
Шешина Татьяна Владимировна — ассистент кафедры клинической медицины, Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского, 603950, Россия, г. Нижний Новгород, просп. Гагарина, д. 23; ORCID iD 0000-0003-1417-2340.
Королева Наталья Борисовна — студентка 5-го курса лечебного факультета, Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского, 603950, Россия, г. Нижний Новгород, просп. Гагарина, д. 23; ORCID iD 0000-0001-9993-4812.
Королева Татьяна Викторовна — заведующая 2-м кардиологическим отделением, ГБУЗ НО «ГКБ № 5», 603005, Россия, г. Нижний Новгород, ул. Нестерова, д. 34.
Контактная информация: Григорьева Наталья Юрьевна, e-mail: grigoreva28@mail.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 06.07.2020, поступила после рецензирования 20.07.2020, принята в печать 03.08.2020.
About the authors:
Natalia Yu. Grigorieva — Dr. of Sci. (Med.), Associate Professor, Professor and Acting Head of the Department of Clinical Medicine, Lobachevsky State University of Nizhny Novgorod: 23, Gagarina str., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0001-6795-7884.
Marina O. Samolyuk — Assistant Professor of the Department of Clinical Medicine, Lobachevsky State University of Nizhny Novgorod: 23, Gagarina str., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0001-9118-5327.
Tatiana V. Sheshina — Assistant Professor of the Department of Clinical Medicine, Lobachevsky State University of Nizhny Novgorod: 23, Gagarina str., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0003-1417-2340.
Natalia B. Koroleva — 5th year student of the Faculty of General Medicine, Lobachevsky State University of Nizhny Novgorod: 23, Gagarina str., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0001-9993-4812.
Tatyana V. Koroleva — Head of the 2nd Department of Cardiology, City Clinical Hospital No. 5: 34, Nesterova str., Nizhny Novgorod, 603005, Russian Federation.
Contact information: Natalia Yu. Grigorieva, e-mail: grigoreva28@mail.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 06.07.2020, revised 20.07.2020, accepted 03.08.2020.
.
Информация с rmj.ru






