Введение
За время пандемии новой коронавирусной инфекции COVID-19 (НКВИ) накоплено достаточно научных данных, которые свидетельствуют о том, что вирус SARS-CoV-2 поражает не только легкие, но и другие органы. Особенный интерес вызывает поражение сердечно-сосудистой системы, которое реализуется посредством эндотелиальной дисфункции, коагулопатии, гипоксии [1]. Немаловажными являются прямое повреждающее действие вирусной частицы SARS-CoV-2 на миокард с развитием воспалительной реакции, а также активация системного воспалительного ответа с развитием дестабилизации имеющихся атеросклеротических бляшек, что может вызвать атеротромбоз [2]. Пациенты, перенесшие НКВИ, даже с изначально низким кардиоваскулярным риском имеют более высокую вероятность развития сердечно-сосудистых заболеваний [3]. Это свидетельствует о важности учета НКВИ, особенно в случае тяжелых форм заболевания, как потенциального фактора, способствующего развитию атеросклероза и его осложнений. К факторам риска, увеличивающим вероятность развития сердечно-сосудистых осложнений после перенесенной НКВИ, относятся: пожилой возраст, женский пол, наличие сопутствующих заболеваний (таких как ожирение, диабет и гипертензия), объем поражения легких в острый период НКВИ, необходимость госпитализации в реанимацию, длительное пребывание в стационаре, а также повышенные уровни воспалительных биомаркеров (ферритин и С-реактивный белок) и сердечных маркеров (тропонин и натрийуретические пептиды) [3]. Еще одной проблемой НКВИ является так называемый лонг-ковид-синдром, когда клинические проявления заболевания длятся более 4 нед., но менее 12 нед. с начала болезни, а также постковидный синдром, когда клинические проявления заболевания сохраняются более 12 нед. с момента развития [4]. Влияние перенесенной НКВИ на течение основных сердечно-сосудистых заболеваний в настоящее время оценивается в многочисленных регистровых исследованиях [5–7] и требует дополнительной оценки эффектов НКВИ в отношении отдаленных этапов течения основных сердечно-сосудистых заболеваний, включая инфаркт миокарда (ИМ).
Цель исследования: выявление предикторов неблагоприятного (смерть от всех причин) отдаленного исхода у пациентов с ИМ в зависимости от наличия НКВИ.
Содержание статьи
Материал и методы
Проведено одноцентровое регистровое сравнительное исследование. В исследование включена когорта пациентов, поступивших в ГБУЗ «КККБ» (Кемерово) с диагнозом ИМ, подтвержденным в соответствии с действующими клиническими рекомендациями «Острый коронарный синдром без подъема сегмента ST электрокардиограммы»1 и «Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы».
Включение больных в регистр острого коронарного синдрома осуществлялось с 2018 по 2021 г. Необходимо отметить, что группа пациентов с ИМ без НКВИ была включена в регистр в период 2018–2019 гг., группа лиц с ИМ и НКВИ — в 2020–2021 гг. Более подробно дизайн регистра, критерии включения/исключения, клинические характеристики пациентов представлены в ранее опубликованной статье [8]. На базе КККД имени академика Л.С. Барбараша в период пандемии НКВИ было организовано отделение для лечения пациентов с кардиоваскулярной патологией и НКВИ, в котором оказывали помощь пациентам в том числе с сочетанным течением ИМ и НКВИ. НКВИ была диагностирована на основании качественного определения РНК SARS-CoV-2 методом полимеразной цепной реакции. Пациентам с ИМ и НКВИ проводилась компьютерная томография легких, по результатам которой все пациенты были разделены на группы по тяжести проявлений коронавирусной пневмонии (% поражения легочной ткани): от 0 до 25% — 25 (22,1%) пациентов, 25–50% — 5 (4,4%) пациентов, 50–75% — 10 (8,8%) пациентов, 75–100% — 3 (2,65%) пациента. Дыхательная недостаточность (ДН) оценивалась по уровню сатурации (SpO2) и была представлена следующим образом: ДН I (SpO2 94–90%) — 50 (44,4%) пациентов, ДН II (SpO2 89–75%) — 8 (7%), ДН III (SpO2 <75%) – 3 (2,65%) пациента [8]. В стационаре все пациенты с ИМ и НКВИ получали специфическую терапию по поводу НКВИ. В анализ госпитального этапа регистра включен 591 человек с верифицированным диагнозом ИМ, сформированы две группы: 478 (80,9%) пациентов с изолированным ИМ без НКВИ и 113 (19,1%) — с ИМ и сопутствующей НКВИ. Большую часть выборки составили лица мужского пола (399 (67,5%)), женщин было в два раза меньше (192 (32,5%)). Медиана возраста включенных в исследование лиц составила 64,5 [58,0; 72,0] года. В течение 12 мес. после выписки из стационара в обеих группах ретроспективно оценена частота смертельных исходов (показатель общей смертности) и проведен статистический анализ с целью поиска информативных предикторов риска смертельного исхода ИМ в зависимости от наличия перенесенной НКВИ.
Статистический анализ выполнен в программе IBM SPSS Statistics, версия 27 (IBM Corp., США). Проверка на нормальность распределения проведена с использованием критерия Колмогорова — Смирнова с поправкой Лиллиефорса. Для анализа количественных данных с распределением, отличным от нормального, в двух независимых группах применен критерий Манна — Уитни. В зависимости от характера распределения данных показатели представлены как медиана и квартили (Me [Q1; Q3]) или как среднее и стандартное отклонение (M±SD). Качественные показатели представлены в виде n (%). Оценка качественных параметров в двух группах пациентов выполнена с помощью критерия χ2 Пирсона или точного критерия Фишера — в зависимости от минимального предполагаемого числа. Статистически значимыми считали различия при p≤0,05. Использованы возможности статистического анализа факторов риска смерти от всех причин методом бинарной логистической регрессии.
Результаты исследования
Пациенты обеих групп регистра были сопоставимы по основным клинико-анамнестическим характеристикам (табл. 1), за исключением более высокой частоты стенокардии и сердечной недостаточности (СН) в анамнезе у больных с ИМ без НКВИ. С другой стороны, у пациентов с ИМ и диагностированной НКВИ отмечали более высокую частоту ранее выполненных реваскуляризирующих процедур (23,9% против 12,7%, р=0,025), в том числе коронарного шунтирования (7,1% против 2,9%, р=0,049), стентирования (16,8% против 9,8%, р=0,034), и большое число кровотечений (9,8% против 2,7%, р=0,002). Вероятно, это обусловлено более пожилым возрастом данных больных, а также улучшением отбора пациентов с хронической ишемической болезнью сердца для плановой реваскуляризации миокарда с годами.
![Таблица 1. Основные клинико-анамнестические характеристики пациентов с ИМ [8] Таблица 1. Основные клинико-анамнестические характеристики пациентов с ИМ [8]](https://medblog.su/wp-content/uploads/2025/01/Faktory-riska-neblagopriyatnogo-otdalennogo-ishoda-u-patsientov-s-infarktom-miokarda.png)
Исходно пациенты с ИМ и НКВИ не отличались от больных с изолированным ИМ по возрасту, полу и основной коморбидности, при этом эта группа пациентов характеризовалась значимо более высокой частотой ранее проведенной плановой реваскуляризации миокарда. За время госпитализации пациентов с ИМ летальный исход развился у 70 (14,6%) пациентов с ИМ без НКВИ и у 19 (16,8%) пациентов с ИМ и наличием НКВИ без значимых различий по частоте (р=0,562).
В течение 12 мес. наблюдения показатель общей смертности у пациентов с ИМ без НКВИ (n=408) составил 9 (2,2%) пациентов и у пациентов с ИМ и НКВИ (n=94) — 7 (7,4%), что было статистически значимо (р=0,010).
Далее были оценены факторы, ассоциированные с риском развития смерти от всех причин в течение 12 мес. В группе ИМ без НКВИ к таковым были отнесены следующие показатели (табл. 2).
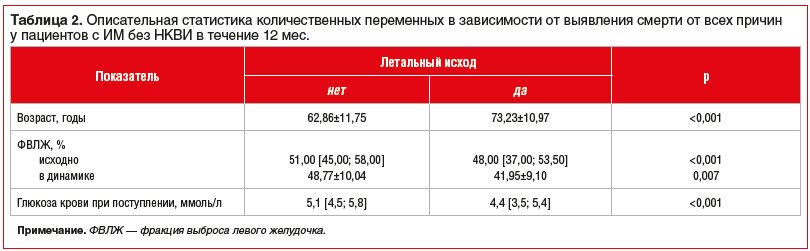
Далее была разработана прогностическая модель для определения вероятности смерти от всех причин при ИМ без НКВИ в течение 12 мес. методом бинарной логистической регрессии. В качестве информативных факторов риска смерти показали себя закономерно возраст и значение ФВЛЖ. Наблюдаемая зависимость описывается уравнением:
P = 1 / (1 + e-z) × 100%
z = -4,149 + 0,076Xвозраст — 0,061XФВЛЖ исходно,
где P — вероятность события, Xвозраст — возраст, XФВЛЖ исходно — ФВЛЖ исходно.
Полученная регрессионная модель является статистически значимой (p<0,001). Исходя из значения коэффициента детерминации Найджелкерка, модель объясняет 21,8% наблюдаемой дисперсии смерти (табл. 3). При увеличении возраста на 1 единицу риск развития смерти от всех причин увеличивался в 1,079 раза. При увеличении ФВЛЖ исходно на 1 единицу шансы развития смерти от всех причин уменьшались в 1,063 раза.

Таким образом, в отношении показателя смерти от всех причин в течение 12 мес. наблюдения значимыми оказались факторы возраста и насосной функции левого желудочка, что было вполне закономерно.
Далее проанализированы факторы риска смертности от всех причин среди пациентов с ИМ и НКВИ в течение 12 мес. (табл. 4).
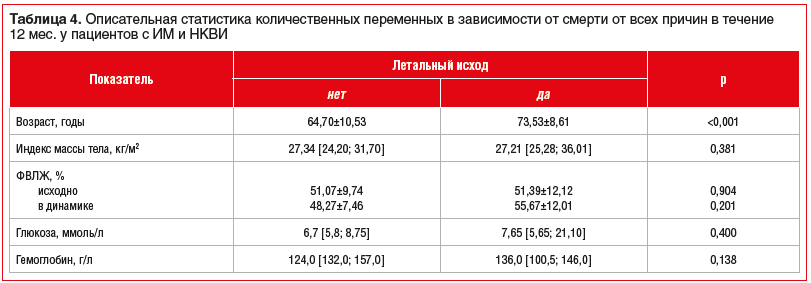
Сформирована прогностическая модель для определения вероятности смертельного исхода от всех причин в течение 12 мес. методом бинарной логистической регрессии. Информативными факторами, ассоциированными с развитием смерти от всех причин в течение 12 мес. у пациентов с ИМ и НКВИ, стали СД в анамнезе и рецидив ИМ во время стационарного лечения. Наблюдаемая зависимость описывается уравнением:
P = 1 / (1 + e-z) × 100%
z = -2,437 + 2,786Xналичие + 2,542Xналичие,
где P — вероятность наступления смерти от всех причин, Xналичие — СД в анамнезе (0 — отсутствие, 1 — наличие), Xналичие — рецидив ИМ (0 — отсутствие, 1 — наличие).
Полученная регрессионная модель является статистически значимой (p<0,001). Исходя из значения коэффициента детерминации Найджелкерка, модель объясняет 42,9% наблюдаемой дисперсии смерти.
При наличии СД шансы летального исхода увеличивались в 16,218 раза. При наличии рецидива ИМ шансы летального исхода увеличивались в 12,705 раза (табл. 5).
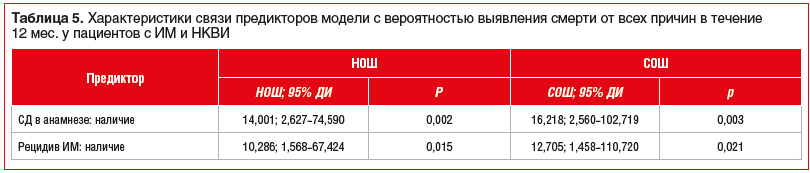
Таким образом, у пациентов с ИМ и НКВИ значимыми предикторами смерти от всех причин в течение 12 мес. оказались рецидивирующее течение ИМ и наличие СД в анамнезе, при этом показатель общей смертности в течение 12 мес. наблюдения после ИМ был статистически значимо выше в группе пациентов с НКВИ, чем в группе с изолированным ИМ (в 3,36 раза, р=0,010).
Обсуждение
В настоящем одноцентровом регистровом исследовании выявлено, что частота развития смерти от всех причин в течение 12 мес. была значимо выше в группе ИМ и НКВИ, чем в группе изолированного ИМ (7,4% против 2,2%, р=0,010). При этом исходные характеристики пациентов с ИМ при поступлении в стационар не отличались. Пациенты с ИМ и НКВИ характеризовались значимо более высокой исходной до развития ИМ и НКВИ частотой использования технологий реваскуляризации миокарда на амбулаторном этапе. Тем не менее наличие перенесенного НКВИ статистически значимо ухудшало отдаленный исход в этой группе больных.
Ранее в регистровых исследованиях также отмечались отрицательные ранние и отдаленные эффекты перенесенной НКВИ. В нашем регистровом исследовании отрицательные эффекты НКВИ реализовались на отдаленном этапе наблюдения после ИМ.
В исследовании Y. Xie et al. [9], направленном на оценку риска и однолетнего бремени сердечно-сосудистых заболеваний у пациентов после пневмонии при НКВИ, авторы выявили высокий риск развития сердечно-сосудистых заболеваний, аритмий, инсульта и тромботических событий в течение 12 мес. после НКВИ, даже у тех, кто не был госпитализирован. Тяжесть пневмонии при НКВИ повышала риск развития сердечно-сосудистых заболеваний.
В небольшом исследовании, проведенном J.F. Wei et al. [10], было показано, что пациенты с НКВИ и острым повреждением миокарда чаще требовали госпитализации в отделение интенсивной терапии, у них была более высокая частота использования искусственной вентиляции легких и вазоактивных препаратов, выше показатели общей смертности, чем у пациентов с НКВИ без повреждения миокарда. Авторы оценили предикторы неблагоприятного исхода у этих пациентов: пожилой возраст, артериальную гипертензию, цереброваскулярные заболевания, низкую скорость клубочковой фильтрации и повышенный уровень прореагировавшего тропонина или С-реактивного белка. W. Wang et al. [11] проанализировали сердечно-сосудистый риск в течение 12 мес. у пациентов, перенесших тяжелую НКВИ. Выявлено, что у пациентов после НКВИ наблюдались более высокие показатели смертности от сердечно-сосудистых причин, чем у пациентов без НКВИ. У женщин, переживших тяжелую НКВИ, отмечали более высокую частоту нарушений ритма сердца, чем в группе пациентов без НКВИ. Т. Kiris et al. [12] изучили исходы пациентов с острым коронарным синдромом до пандемии НКВИ и сравнили их с исходами у пациентов с ИМ в период пандемии НКВИ. Исходно пациенты не отличались по клиническим характеристикам и применяемой терапии, при этом у пациентов с ИМ и НКВИ чаще развивались коронарные тромбозы, а у пациентов с ИМ увеличивалась потребность в применении ингибиторов гликопротеинов IIb/IIIa после коронарных вмешательств. Однако у пациентов с НКВИ и ИМ была более высокая частота смертности и тромбоза стента, что соответствует данным нашего регистрового исследования. Еще одно исследование показало, что пациенты с ИМ в период НКВИ были моложе, имели более низкую ФВ ЛЖ и чаще нуждались в назначении ингибиторов гликопротеина IIb/IIIa, чем больные с ИМ в доковидный период. Наличие перенесенной НКВИ было независимым предиктором частоты больших сердечно-сосудистых событий в отдаленном периоде наблюдения после ИМ, в основном из-за более высокой частоты госпитализаций по поводу декомпенсации СН [13]. Установлено, что пациенты с ИМ и НКВИ характеризуются более обширным некротическим процессом, более высоким уровнем тропонина, а также более тяжелым классом острой СН, чем пациенты с ИМ без НКВИ [14]. Большая склонность пациентов с ИМ и НКВИ к протромботическим реакциям может объяснять более частое развитие рецидивирующего течения ИМ, снижение насосной функции сердца и, как следствие, развитие смерти в отдаленном периоде наблюдения. В нашем исследовании рецидив ИМ оказался значимым предиктором риска смерти при ИМ и НКВИ в течение 12 мес. Еще один установленный предиктор отдаленной смертности — наличие СД, который приводит к более активным процессам системного воспаления, дисгликемии и атерогенеза. Ранее в нашем исследовании [8] мы показали влияние СД на риск развития раннего неблагоприятного исхода у пациентов с ИМ и НКВИ, такое влияние этой коморбидности сохраняется и на отдаленном этапе наблюдения в течение 12 мес., по данным оценки отдаленного периода наблюдения за пациентами с ИМ и НКВИ. В этом отношении наличие у пациента с ИМ и НКВИ СД требует более эффективного контроля на амбулаторном этапе за кардиометаболической коморбидностью для профилактики риска неблагоприятного исхода у этих пациентов.
Ограничение исследования: одноцентровой характер регистрового исследования, выборки разных лет, объем выборок до 1000 пациентов.
Заключение
По данным одноцентрового регистрового исследования выявлены значимые различия показателя смертности от всех причин у пациентов с ИМ и НКВИ — 7,4% и ИМ без НКВИ (2,2%, р=0,010). Наличие СД у пациентов с ИМ и НКВИ повышает риск смерти от всех причин в течение 12 мес., помимо рецидивирующего течения ИМ, что определяет необходимость более эффективного управления коморбидными состояниями у этой когорты больных. У пациентов с изолированным ИМ значимыми в отношении риска смерти от всех причин в течение 12 мес. оказались возраст и низкие значения ФВЛЖ.
Источник финансирования
Исследование выполнено при поддержке Российской Федерации в лице Министерства науки и высшего образования РФ в рамках Соглашения о предоставлении из федерального бюджета грантов в форме субсидий от 30 сентября 2022 г. № 075-15-2022-1202, комплексной научно-технической программы полного инновационного цикла «Разработка и внедрение комплекса технологий в областях разведки и добычи твердых полезных ископаемых, обеспечения промышленной безопасности, биоремедиации, создания новых продуктов глубокой переработки из угольного сырья при последовательном снижении экологической нагрузки на окружающую среду и рисков для жизни населения» (утв. распоряжением Правительства РФ от 11 мая 2022 г. № 1144-р).
Cписок литературы Вы можете найти на сайте http://www.rmj.ru
1Клинические рекомендации. Острый коронарный синдром без подъема сегмента ST электрокардиограммы. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/schema/154_1 (дата обращения: 29.11.2024).
Информация с rmj.ru






