Введение
Распространенность бактериального вагиноза (БВ) в популяции женщин фертильного возраста составляет 23–33% (частота выделения G. vaginalis из влагалища у здоровых и бессимптомных женщин — 45–87%) [1, 2], кандидозного вульвовагинита (КВВ) — 23–49% (частота выделения Candida spp. — 28–60%) [3, 4]. Частота рецидивов у пациенток в течение 12 мес. после лечения варьирует от 50 до 80% и от 14 до 28% соответственно [4, 5], что связывают со снижением доли лактобактерий и инверсией их структуры в пользу Lactobacillus iners, а также образованием биопленок [6, 7].
Было обнаружено, что дисахарид лактулоза наиболее широко и специфично стимулирует вагинальные лактобактерии, в том числе виды L. crispatus, и, что важно, не стимулирует микроорганизмы, ассоциированные с БВ, или C. albicans [8]. Очевидно, что восстановление нормальной микрофлоры влагалища после антибактериального лечения БВ и КВВ является патогенетически обоснованным, однако количество работ, посвященных применению пребиотиков для этой цели, крайне ограниченно [8, 9], что и определяет актуальность выполненного исследования.
Цель исследования: оценить эффективность и безопасность препарата Экорутель форте суппозитории вагинальные (750 мг метронидазола, 200 мг миконазола и 500 мг лактулозы) в сравнении с суппозиториями вагинальными (750 мг метронидазола и 200 мг миконазола) у пациенток с БВ и/или КВВ.
Содержание статьи
Материал и методы
Организация исследования. Работа выполнена на базе шести исследовательских центров Российской Федерации и Республики Беларусь в период с 03.12.2020 по 28.09.2021. При создании протокола исследования учитывали положения Хельсинкской декларации Всемирной медицинской ассоциации (пересмотр 64-й Генеральной ассамблеи WMA, г. Форталеза, Бразилия, 2013 г.) и другие законодательные и нормативные документы РФ и Республики Беларусь. Все пациентки подписали письменное информированное добровольное согласие на участие в исследовании.
Дизайн. Многоцентровое открытое проспективное сравнительное рандомизированное контролируемое исследование в параллельных группах. С целью исключения возможного влияния открытого характера исследования на результаты конечных точек эффективности их оценку проводил заслепленный специалист, которому не сообщалась информация о группе лечебного назначения.
Расчет выборки. Расчет необходимого объема выборки проводили в статистическом пакете R 3.2.2. Для обеспечения 80% мощности при уровне значимости α=0,05 количество пациенток в каждой группе должно составлять не менее 99 (198 во всем исследовании). С учетом 20% пациенток, которые могут досрочно выбыть из исследования, или данных, непригодных для анализа, планировалось рандомизировать 240 пациенток.
Критерии включения: возраст от 18 до 50 лет; диагноз «бактериальный вагиноз» (В96.8 Другие уточненные бактериальные агенты как причина болезней, классифицированных в других рубриках) и/или «кандидозный вульвовагинит» (B37.3 Кандидоз вульвы и вагины); отсутствие беременности, воспалительных и онкологических заболеваний половых органов, тяжелых соматических заболеваний; отрицательные результаты анализов на ВИЧ, гепатиты В и С, сифилис; согласие пациентки следовать процедурам протокола.
Критерии невключения: гиперчувствительность к любому компоненту используемых препаратов; прием системных или местных противогрибковых, антибактериальных, антипротозойных препаратов или антисептиков в течение 2 нед. до визита скрининга; применение внутриматочных устройств; сахарный диабет без достижения целевых значений гликемии в течение 3 мес. до визита скрининга; прием системных или местных глюкокортикостероидов, иммунодепрессантов в течение 1 мес. до визита скрининга; применение любых вводимых во влагалище средств в течение 48 ч до планируемого первого применения опытного препарата / препарата сравнения; первичные и вторичные иммунодефициты, участие в других клинических исследованиях в течение 90 дней до скрининга.
Критерии исключения: отказ пациентки от участия в исследовании; развитие одного из критериев невключения во время участия в исследовании; нарушение процедур протокола; развитие нежелательного явления (НЯ), сопряженного с высоким риском для здоровья пациентки в случае продолжения участия в исследовании; возникновение или обострение сопутствующих соматических заболеваний, не связанных с приемом лекарственных препаратов, требующих изменения курса лечения и назначения процедур, не удовлетворяющих протоколу исследования.
Рандомизация. Скрининг прошли 224 пациентки, из них отобраны 220, которые были разделены на 2 группы методом генерации случайных чисел с использованием программы WinPepi 11.65 (модуль ETCETERA 3.26) (рис. 1). Зачисление участниц и назначение терапии выполнял врач амбулаторного звена, к которому обращались пациентки.
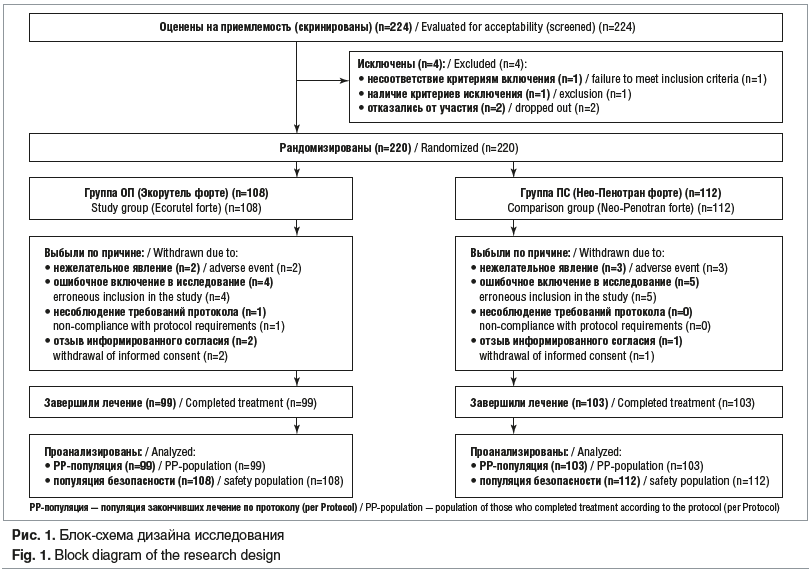
Группу опытного препарата (группа ОП) составили 108 пациенток, которые получали суппозитории вагинальные, содержащие 750 мг метронидазола, 200 мг миконазола и 500 мг лактулозы (Экорутель форте, АО «АВВА РУС», Россия). В группу препарата сравнения (группа ПС) включены 112 пациенток, которым были назначены суппозитории вагинальные, содержащие 750 мг метронидазола и 200 мг миконазола (Нео-Пенотран® форте, «Эксэлтис Илач Сан. ве Тик. А.С.», Турция). В обеих группах пациентки применяли препараты самостоятельно 1 р/сут на ночь в течение 7 дней.
Методы исследования. Выполняли: сбор социальных данных, анамнеза, жалоб, объективный осмотр, измерение жизненно важных параметров (артериальное давление, частота сердечных сокращений, частота дыхательных движений, температура тела), гинекологический осмотр, измерение рН влагалища, аминный тест, лабораторные исследования (клинический и биохимический анализы крови; общий анализ мочи; цитологическое исследование мазка; микроскопия нативного мазка и мазка, окрашенного по Граму, с использованием шкалы Nugent; бактериологическое исследование). ПЦР-исследование отделяемого влагалища на урогенитальные инфекции проводилось на визите 1 (скрининг) для исключения у пациентки инфекций, передаваемых половым путем (вирусных и бактериальных).
В рамках исследования пациентка оценивала удовлетворенность лечением по 4-балльной шкале: 0 баллов — неудовлетворительно, 1 балл — удовлетворительно, 2 балла — хорошо, 3 — отлично. Комплексная оценка состояния, симптомов НЯ (в том числе время их возникновения и выраженность) проводилась ответственным исследователем на каждом визите и во время телефонных контактов с пациенткой со дня получения первой дозы препаратов опытного/сравнения до визита наблюдения. В случае развития НЯ его связь с исследуемым препаратом оценивалась по шкале ВОЗ (определенная, вероятная, возможная, сомнительная, не связанная с препаратом).
Порядок обследования. Дизайном исследования было предусмотрено 6 визитов: визит 1 (дни от -6 до 0) — скрининг; визит 2 (1-й день) — рандомизация / первое введение препаратов исследования; визиты 3–5 (9–11, 14–18 и 21–24-й день соответственно) — промежуточная оценка эффективности и безопасности; визит 6 (30–35-й день) — окончательная оценка эффективности и безопасности.
Критерии эффективности. Первичные конечные точки: доля (%) пациенток, у которых достигнуто клиническое и микроскопическое выздоровление на 14–18-й день (визит 4) и 30–35-й день (визит 6). Клиническое выздоровление: исчезновение клинических проявлений БВ и/или КВВ. Микробиологическое выздоровление: оценка окрашенного по Граму вагинального мазка по шкале Nugent <4 баллов, отсутствие Candida при микроскопии нативного мазка и при культуральном исследовании отделяемого влагалища.
Вторичные конечные точки: удовлетворенность пациентки проводимым лечением на визите 4; изменение содержания лактобактерий при микробиологическом исследовании мазка из влагалища на визите 6 в сравнении с исходными данными.
Анализ эффективности представлен в РР-популяции (Реr-Protocol) пациенток, отвечавших критериям включения, соблюдавших условия протокола и полностью завершивших курс лечения. Параметры безопасности оценивали в популяции безопасности (все пациентки, получившие хотя бы одну дозу препарата).
Статистический анализ. Использовали статистическое программное обеспечение Microsoft R Open версии 3.5.3, пакет TrialSize версии 1.3. Оценку соответствия распределения признаков на нормальность проводили с помощью критерия Колмогорова — Смирнова. Количественные признаки представляли как среднее и среднее квадратичное отклонение (M±SD) — для нормально распределенных показателей и как медиану и первый и третий квартили (Me [Q1; Q3] — для показателей, не соответствовавших нормальному распределению. Сравнение количественных показателей проводили при помощи t-критерия Стьюдента для независимых выборок или критерия Манна — Уитни в зависимости от результатов проверки нормальности распределения данных. Для сравнения категориальных показателей использовали критерий χ2 Пирсона или точный критерий Фишера. Принят уровень значимости р<0,05 при уровнях ошибки первого и второго рода α=5% и β=20% соответственно.
Результаты исследования
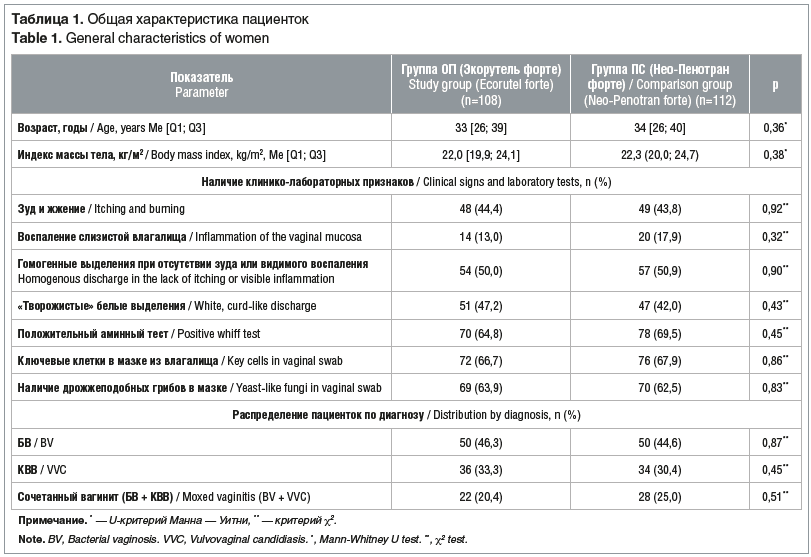
Общая клиническая характеристика пациенток. Базовые социальные, анамнестические и клинические характеристики пациенток представлены в таблице 1. Индивидуальные показатели физикального осмотра по органам и системам, а также жизненно важные параметры у пациенток обеих групп не имели клинически значимых отклонений и были сопоставимы.
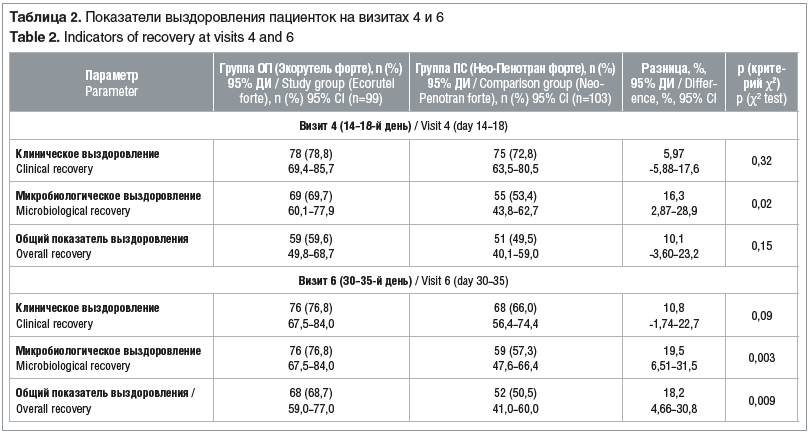
Оценка эффективности лечения. Первичные конечные точки. Как видно из таблицы 2, на визите 4 (14–18-й день от начала лечения) микробиологическое выздоровление наступило у большинства пациенток обеих групп с преимуществом в пользу группы ОП (Экорутель форте). Разность между группами составила 16,3% (95% ДИ 2,87–28,9), что характеризует опытный препарат как более эффективный в отношении микробиологического выздоровления в данной временной точке.
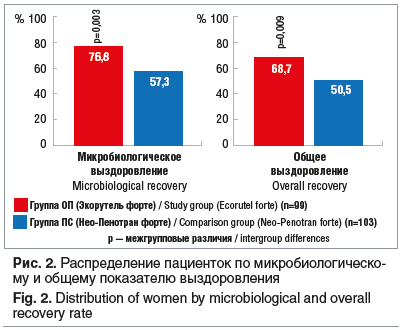
Анализ показателей клинического, микробиологического и общего (клинического и микробиологического) выздоровления на визите 6 (30–35-й день от начала лечения) показал, что по клинической эффективности изученные препараты сопоставимы, а по микробиологическому и общему показателям выздоровления Экорутель форте статистически значимо превосходит препарат сравнения (см. табл. 2, рис. 2).
Анализ результатов обследования в подгруппах пациенток с изолированным БВ в группе ОП и группе ПС показал, что на визите 4 выздоровление (общее) наступило у 41,3% (19/46) и 45,7% (21/46) соответственно, на визите 6 — у 63,0% (29/46) и 41,3% (19/46) соответственно со статистически значимыми различиями (р=0,02) при разности в 21,7% (95% ДИ 1,37–39,7), что свидетельствует о бóльшей эффективности препарата Экорутель форте у пациенток с БВ (рис. 3).
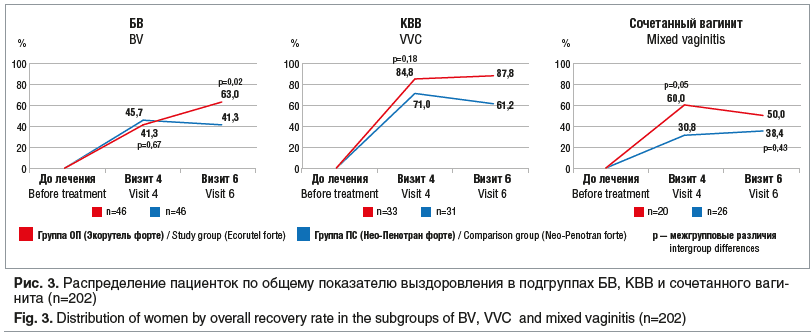
Эффективность лечения по показателю общего выздоровления на визите 4 в подгруппах КВВ в группе ОП и группе ПС была сопоставимой — 84,8% (28/33) против 71,0% (22/31) соответственно (р=0,180),а на визите 6 — более выраженной в группе ОП — 87,8% (29/33) и 61,2% (19/31) соответственно, что свидетельствует о бóльшей эффективности препарата Экорутель форте у пациенток с КВВ (см. рис. 3).
У пациенток с сочетанным вагинитом установлено преимущество опытного препарата в достижении общего выздоровления на визите 4, при этом в группе ОП выздоровело 60% (12/20) пациенток, в группе ПС — 30,8% (8/26) (р=0,05). К визиту 6 различий между группами не установлено (р=0,43) (см. рис. 3).
Вторичные конечные точки. Показатели удовлетворенности пациенток представлены следующим образом: оценки «хорошо» и «отлично» на финальном визите 6 дали 76,8 и 19,2% (суммарно 96,0%) пациенток группы ОП и 75,7 и 20,4% (суммарно 96,1%) — группы ПС (p=0,09). Оценку «удовлетворительно» дали 3,0 и 2,9% пациенток соответственно, «неудовлетворительно» — только по 1 пациентке в каждой группе.
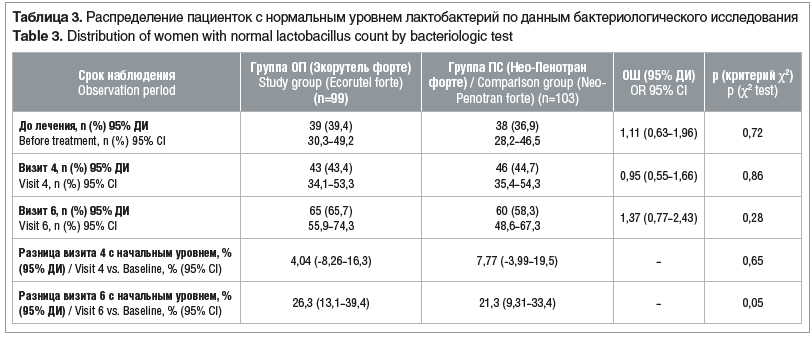
Изменения содержания лактобактерий по данным бактериологического исследования представлены в таблице 3. В обеих группах отмечено увеличение числа пациенток с уровнем лактобактерий 105 КОЕ/мл к визиту 6 без статистически значимой разницы между группами. Так, доля пациенток с нормальным уровнем лактобактерий увеличилась в группе ОП на 26,3% (95% ДИ 13,1–39,4), в группе ПС на 21,3% (95% ДИ 9,31–33,4).
Для выявления влияния лактулозы в составе препарата Экорутель форте на динамику содержания лактобактерий во влагалищном отделяемом пациентки были стратифицированы по нозологическим формам. Доля пациенток с уровнем лактобактерий 105 КОЕ/мл и выше в динамике ото дня скрининга до визита 6 у пациенток с БВ в группе ОП увеличилась на 47,8% (95% ДИ 28,8–66,8, р<0,05), в группе ПС — на 23,9% (95% ДИ 4,49–43,3, р<0,05) (рис. 4). Различия между группами на финальном визите 6 были статистически значимы (р=0,05) при одинаковом исходном уровне (р=0,65).
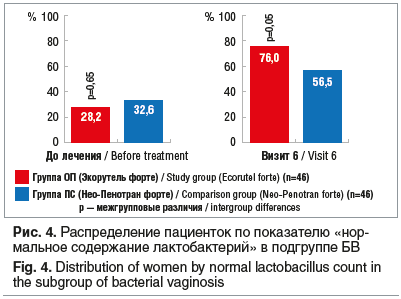
Для пациенток с КВВ и сочетанным вагинитом динамику установить не удалось ввиду небольшого количества наблюдений с указанными нозологиями.
Таким образом, результатами проведенного исследования доказано, что препарат Экорутель форте суппозитории вагинальные (750 мг метронидазола, 200 мг миконазола и 500 мг лактулозы) превосходит по эффективности препарат сравнения суппозитории вагинальные (750 мг метронидазола и 200 мг миконазола) при лечении БВ и/или КВВ у взрослых женщин.
Оценка безопасности. В популяции безопасности в группе ОП (Экорутель форте) НЯ зарегистрированы у 48,2% (52/108) пациенток, в группе ПС (Нео-Пенотран форте) — у 53,6% (60/112) (p=0,42), большинство из них были легкой степени. Серьезные НЯ не наблюдались.
Определенную связь с лечением установили для одного НЯ в группе ОП и для двух НЯ в группе ПС (р=1,0), вероятную — для 6 и 20 НЯ соответственно (р=0,007), возможную — для 32 и 43 НЯ соответственно (р=0,25), сомнительную — для 84 и 68 НЯ соответственно (р=0,007), т. е. в группе ОП у меньшего числа пациенток по сравнению с группой ПС развившиеся НЯ были связаны с применяемым лечением. Установлена статистически значимая разница между группами по такому НЯ, как реакции в месте введения суппозитория — 8,3% (9/108) против 17,9% (20/112), разница 9,5% (95% ДИ 0,5–18,5, р=0,04), что позволяет сделать вывод о более комфортном применении препарата Экорутель форте.
Обсуждение
Оценка микробиологической эффективности в группах продемонстрировала преимущество препарата Экорутель форте на 14–18-й день, а через 30–35 дней от начала лечения бóльшая его эффективность установлена как по микробиологическому выздоровлению, так и по общему показателю выздоровления. Такой результат, вероятно, можно объяснить присутствием в препарате Экорутель форте пребиотика лактулозы — средства, способствующего росту собственных лактобактерий. Действительно, доля пациенток с нормальным уровнем лактобактерий (105 КОЕ/мл и выше) к финальному контрольному визиту у пациенток с БВ в группе ОП увеличилась на 47,8%, в группе ПС — на 23,9% (р=0,05) при отсутствии статистической значимости на исходном уровне (р=0,65).
Лактулоза — пребиотик, который усиливает рост полезных бактерий, таких как бифидобактерии и лактобактерии, способствует подавлению роста потенциально патогенных бактерий (Clostridium spp. и Escherichia coli), что обеспечивает более благоприятный баланс микрофлоры. Ранее проведенные исследования показали, что лактобактерии используют лактулозу в качестве питательного субстрата, что приводит к увеличению количества собственных лактобактерий (генетически «родных»), при этом было показано, что вагинальные лактобактерии подавляют рост и образование гиф C. albicans in vitro и in vivo [10]. S.L. Collins et al. [11] продемонстрировали, что лактулоза наиболее активно и избирательно стимулирует рост лактобактерий, в том числе L. crispatus, при этом C. albicans и анаэробные бактерии не метаболизируют лактулозу, она для них не является питательным субстратом. Восстановление Lactobacillus spp. до уровня выше 90% в структуре представителей микробиоты in vitro происходит в течение 48 ч [11].
Таким образом, нами продемонстрировано положительное влияние комбинированного препарата, содержащего лактулозу, на восстановление пула лактобактерий у пациенток с БВ.
Заключение
Препарат Экорутель форте суппозитории вагинальные, содержащий 750 мг метронидазола, 200 мг миконазола и 500 мг лактулозы, превосходит препарат-компаратор Нео-Пенотран® форте суппозитории вагинальные, содержащий 750 мг метронидазола и 200 мг миконазола, по микробиологической эффективности на 14–18-й день от начала лечения, по микробиологическому и общему показателю излеченности на 30–35-й день при лечении БВ и/или КВВ у взрослых женщин и способствует восстановлению количества лактобактерий у пациенток с БВ.
Сведения об авторах:
Дикке Галина Борисовна — д.м.н., доцент, профессор кафедры акушерства и гинекологии с курсом репродуктивной медицины, ЧОУ ДПО «Академия медицинского образования им. Ф.И. Иноземцева»; 190013, Россия, г. Санкт-Петербург, Московский пр-т, д. 22, литера М; ORCID iD 0000-0001-9524-8962.
Кузьмин Владимир Николаевич — д.м.н., профессор кафедры репродуктивной медицины и хирургии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; ORCID iD 0000-0003-4022-9814.
Ярош Елена Евстафьевна — врач акушер-гинеколог, заведующая женской консультацией УЗ «2-я центральная районная поликлиника Фрунзенского района г. Минска»; 220018, Республика Беларусь, г. Минск, ул. Якубовского, д. 33.
Дегилева Ирина Николаевна — врач акушер-гинеколог, заведующая женской консультацией УЗ «1-я городская клиническая больница г. Минска»; 220013, Республика Беларусь, г. Минск, пр-т Независимости, д. 64.
Лучко Светлана Владимировна — врач акушер-гинеколог, заведующая женской консультацией УЗ «4-я городская поликлиника г. Минска»; 220020, Республика Беларусь, г. Минск, пр-т Победителей, д. 93.
Мавричева Лариса Александровна — заместитель главного врача по медицинской части УЗ «Городская гинекологическая больница г. Минска»; 220007, Республика Беларусь, г. Минск, ул. Сенницкая, д. 53.
Мосько Татьяна Васильевна — врач акушер-гинеколог кабинета патологии шейки матки женской консультации УЗ
«Клинический родильный дом Минской области»; 220114, Республика Беларусь, г. Минск, ул. Ф. Скорины, д. 16.
Контактная информация: Дикке Галина Борисовна, e-mail: galadikke@yandex.ru.
Источник финансирования: исследование проведено при поддержке АО «АВВА РУС», Россия (протокол исследования Metronidazole-Miconazole-supp-III-04/19-AVVA — CSR). Сотрудники компании не участвовали в разработке и проведении исследования; сборе, анализе и интерпретации данных, а также в подготовке, рассмотрении или утверждении рукописи.
Конфликт интересов отсутствует.
Статья поступила 23.01.2024.
Поступила после рецензирования 15.02.2024.
Принята в печать 11.03.2024.
About the authors:
Galina B. Dikke — Dr. Sc. (Med.), Associate Professor, professor of the Department of Obstetrics and Gynecology with the Course of Reproductive Medicine, F.I. Inozemtsev Academy of Medical Education; 22, letter M, Moskovskiy ave., St. Petersburg, 190013, Russian Federation; ORCID iD 0000-0001-9524-8962.
Vladimir N. Kuz’min — Dr. Sc. (Med.), professor of the Department of Reproductive Medicine and Surgery, Russian University of Medicine; 4, Dolgorukovskaya str., Moscow, 127006, Russian Federation; ORCID iD 0000-0003-4022-9814.
Elena E. Yarosh — obstetrician & gynecologist, Head of the Women’s Clinic of the 2nd Central District Polyclinics of the Frunzenskiy District of Minsk; 33, Yakubovskiy str., Minsk, 220018, Republic of Belarus.
Irina N. Degileva — obstetrician & gynecologist, Head of the Women’s Clinic of the 1st City Clinical Hospital; 64, Nezavisimosti ave., Minsk, 220013, Republic of Belarus.
Svetlana V. Luchko — obstetrician & gynecologist, Head of the Women’s Clinic of the 4th City Polyclinics; 93, Pobeditiley ave., Minsk, 220020, Republic of Belarus.
Larisa A. Mavricheva — Deputy Head Doctor of Medical Work, City Gynecological Hospital; 53, Sennitskaya str., Minsk, 220007, Republic of Belarus.
Tatyana V. Mos’ko — obstetrician & gynecologist of the Cabinet of Cervical Disorders of the Women’s Clinic of the Clinical Maternity Hospital of Minsk Region; 16, F. Skorina str., 220114, Republic of Belarus.
Contact information: Galina B. Dikke, e-mail: galadikke@yandex.ru.
Financial Disclosure: the study was supported by AVVA-Rus LLC, Russia (study protocol Metronidazole-Miconazole-supp-III-04/19-AVVA — CSR). It should be noted that company personnel were not involved in any aspect of the study, including the design and conduct of the study, the collection, analysis, and interpretation of data, or the preparation, review, or approval of the manuscript.
There is no conflict of interest.
Received 23.01.2024.
Revised 15.02.2024.
Accepted 11.03.2024.
Информация с rmj.ru