Введение
Опухоли придаточного аппарата глаза по распространенности среди новообразований органа зрения занимают лидирующее место и, соответственно, представляют собой социально значимую проблему в офтальмологии [1–3]. Клиническая картина этих опухолей отличается полиморфностью, в связи с чем их дифференциальная диагностика представляет определенные трудности [4–7]. Правильно установленный первоначальный диагноз играет важную роль, так как тактика лечения и объем хирургического вмешательства при доброкачественных и злокачественных новообразованиях придаточного аппарата глаза кардинально различаются [8, 9]. Особенно важно своевременное выявление злокачественных новообразований, которые представляют угрозу для жизни пациента.
Единственным методом подтверждения доброкачественного или злокачественного характера новообразования придаточного аппарата глаза является патогистологическое исследование уже удаленной опухоли [10]. Но, как известно, опухоли отличаются не только морфологически. В 2000 г. была опубликована основополагающая работа ведущих специалистов в области биологии профессоров D. Hanahan и R. Weinberg, посвященная особенностям метаболизма опухолей. Было показано, что отличительной чертой опухолевого процесса является генетически обусловленный повышенный уровень метаболизма [11]. За последние 20 лет появилось множество работ по изучению энергетического метаболизма опухолевых клеток, но на данный момент точно установлено лишь то, что метаболический профиль опухолей различается, также до конца не были определены метаболические особенности разных типов опухолей [12–14]. Это побудило нас провести поиск и разработку нового метода диагностики для оценки метаболического статуса опухолей придаточного аппарата глаза, который позволил бы установить до операции характер опухолевого процесса.
Анализ литературы показал, что биогенный синтез наночастиц ранее был применен для определения метаболической активности микроорганизмов [15, 16]. Авторами было показано, что имеется четкая корреляция между выходом биогенных наночастиц и уровнем метаболической активности микробных объектов [17]. Методологической основой метода служит генерация биогенных наночастиц de novo путем естественной фундаментальной способности живых метаболически активных клеток к восстановлению катионов [18, 19]. Мы изучили использование биогенного синтеза наночастиц серебра в оценке метаболизма опухолей придаточного аппарата глаза путем определения их восстановительной способности в отношении катионов серебра.
Цель исследования — создание и отработка нового нанобиотехнологического метода и применение его на практике для дифференциальной диагностики опухолей придаточного аппарата глаза.
Содержание статьи
Материал и методы
За период с 2021 по 2023 г. в отделении офтальмоонкологии и радиологии ФГБУ «НМИЦ ГБ им. Гельмгольца» Минздрава России проведено обследование 192 больных (105 женщин, 87 мужчин) с гистологически верифицированным диагнозом опухоли века или конъюнктивы: 79 пациентов со злокачественными новообразованиями век (n=42) и конъюнктивы (n=37) и 113 пациентов с доброкачественными опухолями век (n=54) и конъюнктивы (n=59). По поводу продолженного роста и рецидива опухоли придаточного аппарата поступили 17 (11,05%) пациентов, из них со злокачественными ново-образованиями 14 пациентов. Возраст больных на момент поступления в стационар составил от 5 до 90 лет (средний возраст 48 лет).
Всего исследованы 192 биопсийных материала из опухолей век и конъюнктивы. Контролем служили образцы здоровой ткани из того же глаза.
Все исследования проводились с согласия пациентов и были одобрены локальным этическим комитетом.
Отработка метода. Для регистрации и получения значимых различий генерации биогенных наночастиц серебра in situ требовались подбор и оптимизация основных параметров проведения реакции восстановления катионов серебра.
Генерация de novo биогенных наночастиц серебра. Образцы исследуемых тканей помещали в стерильный раствор источника катионов в асептических условиях. Генерацию наночастиц металлов проводили in situ с использованием стерильного раствора реактива Толленса (Ag(HN3)2NO3).
Были проведены измерения оптической плотности (при λ=410 нм) реакционных смесей с биогенными наночастицами серебра при использовании реактива Толленса в концентрациях 1000, 500, 250, 125, 63, 31 и 16 мкг/мл.
Оборудование. Измерение массы биоптатов проводили с использованием аналитических весов CPA225D (Sartorius, Германия), для минимизации погрешности взвешивания использовали лабораторную центрифугу LMC 4200-R. Восстановление катионов серебра и формирование de novo биогенных наночастиц проводили в термостатируемом шейкере ST-3 (Elmi, Латвия). Спектрофотометрическое определение восстановительной способности проводили на многофункциональном фотометре для микропланшетов Synergy MX (Bio-Tek, США).
Результаты спектрофотометрического определения активности генерации биогенных наночастиц серебра при длинах волн, близких к специфическим для наночастиц серебра, представляли как коэффициент (Ak) — отношение показателя оптической плотности реакционной смеси с биогенными наночастицами, сформированными в присутствии опухолей, к показателю оптической плотности реакционной смеси с биогенными наночастицами, сформированными в присутствии здоровых тканей с учетом оптической плотности раствора Ag(NH3)2NO3.
Статистическая обработка данных. Полученные результаты исследования автоматически сохранялись в виде таблицы Excel на компьютере с программной установкой Windows. Статистическую обработку полученных данных проводили с помощью программного пакета IBM SPSS Statistics 23. Для характеристики статистических рядов распределения использовали средние значения (М) и стандартное отклонение (SD). Для оценки статистической значимости различий между группами применили критерий Стьюдента, различия считались статистически значимыми при p<0,05.
Результаты и обсуждение
Подбор оптимальной концентрации раствора источника катионов серебра. Концентрации катионов серебра в реакционной смеси, в которой генерация наночастиц биологическими объектами происходит in situ, должна быть достаточной для обеспечения формирования детектируемого количества наночастиц серебра. Были проведены измерения оптической плотности (при λ=410 нм) реакционных смесей с биогенными наночастицами серебра при использовании реактива Толленса в различных концентрациях и установлено, что максимальный уровень генерации биогенных наночастиц серебра наблюдался при концентрации раствора нитрата серебра при 31 и 63 мкг/мл. Поскольку статистически значимых различий при использовании этих двух концентраций не было (p>0,05), для дальнейших исследований была выбрана концентрация источника катионов серебра 63 мкг/мл в целях экономии реактива.
Выбор длины волны для спектрометрического определения уровня генерации биогенных наночастиц серебра. Поглощение света наночастицами определяется специфическими оптическими свойствами металла и размером наночастиц в суспензии. Возможность визуализации с помощью спектрометрии биогенных наночастиц серебра определяется рассеянием свободных электронов на поверхности наночастиц, вследствие чего плазмонная частота свободных колебаний электронов наблюдается в видимой области спектра около λ=400 нм. Исследование препаратов биогенных наночастиц серебра, генерируемых клетками биоптатов, проводили при фиксированных длинах волн 395, 400, 405, 410, 415 и 420 нм. Измерение оптической плотности образцов показало, что максимум поглощения наблюдали при длинах волн 395, 400 и 410 нм. Подобные спектральные характеристики препаратов указывают на то, что размер генерируемых de novo наночастиц серебра не превышает 30–50 нм. На основании полученных данных в дальнейшей работе для расчетов сравнительных показателей различных типов тканей была выбрана средняя длина волны 410 нм.
Оценка массы биоптатов. Хотя макроскопически размеры исследуемых биоптатов из опухолей и контрольных тканей были сопоставимы, нам требовалось нормировать образцы по массе и определить их точную массу с помощью электронных весов. Анализ значений уровня генерации наночастиц серебра (определенного спектрометрически при длине волны 410 нм) как опухолей, так и нормальных тканей после нормирования по массе не выявил значимых различий в показателях при разности масс в 2–3 раза.
Подбор времени реакции восстановления катионов клетками биоптатов. Одной из важнейших задач исследования было определение времени реакции, при котором значения оптической плотности генерируемых de novo биогенных наночастиц были бы наиболее показательными. Инкубацию для проведения реакции восстановления проводили от 5 до 40 мин с интервалами измерения уровня генерации биогенных наночастиц серебра по 5 и 10 мин. В исследовании достоверные уровни генерации наночастиц серебра фиксировали уже через 5 мин от начала реакции восстановления катионов. Наиболее показательными явились параметры оптической плотности (измеренные при длине волны 410 нм) в интервале от 10 до 20 мин. При длительности реакции восстановления более 20 мин рост величины показателей становился незначительным, а при проведении реакции восстановления более 30 мин показатели практически не изменялись. При этом после 40 мин мы наблюдали изменение цвета ткани, что могло говорить о ее разрушении. На основании проведенных измерений было определено, что в дальнейших исследованиях реакцию восстановления катионов серебра следует проводить 10 и 20 мин.
Дифференциальная диагностика доброкачественных и злокачественных опухолей век и конъюнктивы на основе нового нанобиотехнологического метода. При оценке клинической картины новообразований у пациентов обращали внимание на их переход в прилежащие структуры. У пациентов с новообразованиями век признаки активности в виде распространения на прилежащие структуры (интермаргинальное пространство) наблюдали у 34 человек, среди которых у 19 был установлен диагноз злокачественного новообразования. Опухоли конъюнктивы (доброкачественные и злокачественные) чаще всего локализовались на бульбарной конъюнктиве, среди таких опухолей распространение на прилежащие структуры (лимб и роговицу) наблюдали у 32 пациентов, из них злокачественные опухоли гистологически верифицировались у 18.
При анализе восстановительной способности опухолей век и конъюнктивы в зависимости от локализации и активности процесса (перехода на прилежащие структуры) не выявлено статистически значимых различий.
В первой части исследования была проведена оценка восстановительной способности всех типов опухолей век и конъюнктивы и восстановительной способности здоровых контрольных тканей. Значения оптической плотности реакционных смесей с биогенными наночастицами, сформированными de novo, в присутствии опухолей придаточного аппарата глаза сравнивали со значениями для соответствующих парных образцов здоровой ткани. На основании того, что уровень генерации биогенных наночастиц серебра за фиксированное время был выше в препаратах с биоптатами опухолей придаточного аппарата глаза, было установлено, что независимо от характера роста опухоли имеют более высокие по сравнению с контрольными здоровыми тканями показатели восстановительной способности.
Далее мы сравнивали восстановительную способность между доброкачественными и злокачественными опухолями придаточного аппарата глаза, так как именно возможность установить характер опухоли имеет наиболее ценную практическую значимость. Показатели восстановительной способности доброкачественных опухолей придаточного аппарата глаза в среднем составили Ak=1,5±0,2 (n=113) и не имели значимых существенных различий в зависимости от локализации опухоли (веки или конъюнктива) и типа (папилломы, невусы и т. д.). Среди злокачественных опухолей конъюнктивы (умеренно тяжелая и тяжелая интраэпителиальная неоплазия конъюнктивы, плоскоклеточный рак, меланома, лимфома) наибольшая восстановительная способность обнаружена у меланомы Ak=3,6±0,6 (n=17) (p<0,05). Среди злокачественных опухолей век не выявили статистически значимых различий разных типов опухоли. Показатели восстановительной способности при базальноклеточном раке Ak=2,9±0,3 (n=22) и при плоскоклеточном раке Ak=3,0±0,2 (n=15) отличались незначительно.
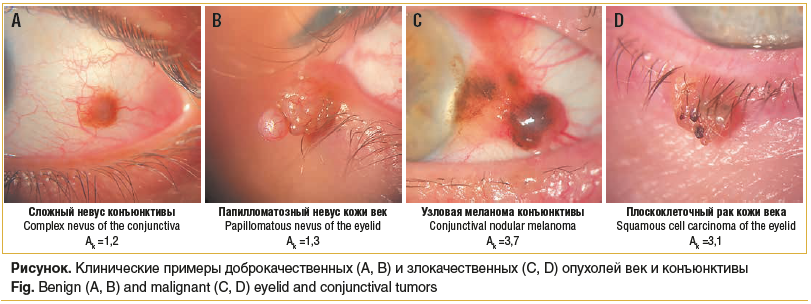
На рисунке представлены клинические примеры доброкачественных и злокачественных опухолей век и конъюнктивы и уровни их восстановительной способности.
В литературе встречается все больше работ по генетически обусловленному изменению энергетического метаболизма опухолевых клеток [9]. Однако до настоящего времени нет конкретных данных о дифференциальной диагностике различных опухолей по уровню их метаболической активности.
Мы разработали новый нанобиотехнологический метод для оценки метаболической активности опухолей придаточного аппарата глаза на основе биогенного синтеза наночастиц серебра [20]. Основой разработки метода послужила способность живых метаболически активных клеток к восстановлению катионов с формированием биогенных наночастиц, доказанная на микробных моделях, где уровень синтеза клеток был пропорционален уровню их метаболической активности. Скорость формирования de novo биогенных наночастиц из катионов отражала общий уровень биосинтеза микробных клеток и служила индикатором уровня их метаболической активности [15–17].
При создании и отработке нового нанобиотехнологического метода для удобства проведения исследований и с целью получения значимых результатов исследования были оптимизированы основные методические параметры: концентрация источника катионов серебра, способ нормирования массы биоптатов, длина волны для оценки уровня генерации наночастиц серебра и время реакции восстановления катионов серебра.
Реакционные смеси, приготовляемые по протоколу нового нанобиотехнологического метода, имеют точно известный состав, за исключением тех компонентов (биогенных доноров электронов, необходимых для восстановления катионов серебра), которые привносят опухолевые клетки. Соответственно, различия при формировании биогенных нанокристаллических структур de novo строго зависели от восстановительных способностей опухолевых клеток и/или от различий биогенных секретируемых восстановителей, что позволяло оценивать метаболическую активность доброкачественных и злокачественных опухолей придаточного аппарата глаза.
С помощью нового нанобиотехнологического метода мы показали, что разные опухоли придаточного аппарата глаза имеют разную восстановительную способность в отношении катионов серебра, определенную по уровню генерации de novo биогенных наночастиц. Было впервые показано, что более высокий уровень генерации биогенных наночастиц de novo определяется у злокачественных опухолей придаточного аппарата глаза по сравнению с доброкачественными. Более того, была обнаружена наибольшая восстановительная способность у меланомы конъюнктивы. Это может объясняться тем, что меланома в качестве основного механизма обмена веществ активнее всех использует глюкозу, которая является одним из основных источников энергии опухоли [21].
Заключение
На основе фундаментальной природной способности метаболически активных клеток генерировать наночастицы серебра мы создали, отработали и использовали новый нанобиотехнологический метод экспресс-диагностики доброкачественных и злокачественных опухолей придаточного аппарата глаза. Полученные данные показали, что данный метод может быть применим для получения информации на одном из важнейших диагностических этапов в офтальмоонкологии — для установления доброкачественного или злокачественного характера опухоли до операции. Ценность указанного метода заключается в возможности проводить дифференциальную диагностику доброкачественных и злокачественных опухолей придаточного аппарата глаза с целью определения тактики ведения пациента и планирования объема хирургического вмешательства.
Сведения об авторах:
Саакян Светлана Ваговна — д.м.н., профессор, член-корр. РАН, начальник отдела офтальмоонкологии и радиологии ФГБУ «НМИЦ ГБ им. Гельмгольца» Минздрава России; 105062, Россия, г. Москва, ул. Садовая-Черногрязская, д. 14/19; ORCID iD 0000-0001-8591-428X.
Складнев Дмитрий Анатольевич — д.б.н., профессор, главный научный сотрудник лаборатории выживаемости микроорганизмов ИНМИ РАН ФИЦ Биотехнологии РАН; 119071, Россия, г. Москва, Ленинский пр-т, д. 33, стр. 2; ORCID iD 0000-0001-6929-6397.
Алексеева Алена Павловна — аспирант отдела офтальмоонкологии и радиологии ФГБУ «НМИЦ ГБ им. Гельм-гольца» Минздрава России; 105062, Россия, г. Москва, ул. Садовая-Черногрязская, д. 14/19; ORCID iD 0000-0002-7568-3016.
Безнос Ольга Валерьевна — врач клинической лабораторной диагностики отдела патофизиологии и биохимии ФГБУ «НМИЦ ГБ им. Гельмгольца» Минздрава России; 105062, Россия, г. Москва, ул. Садовая-Черногрязская, д. 14/19; ORCID iD 0000-0001-7557-4955.
Сорокин Владимир Владиславович — старший научный сотрудник лаборатории выживаемости микроорганизмов ИНМИ РАН ФИЦ Биотехнологии РАН; 119071, Россия, г. Москва, Ленинский пр-т, д. 33, стр. 2; ORCID iD 0000-0002- 4166-3105.
Контактная информация: Алексеева Алена Павловна, e-mail: chonai.94@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 17.07.2023.
Поступила после рецензирования 07.08.2023.
Принята в печать 28.08.2023.
About the authors:
Svetlana V. Saakyan — Dr. Sc. (Med.), Professor, Corresponding Member of the RAS, Head of the Department of Ocular Oncology and Radiology, Helmholtz National Medical Research Center; 14/19, Sadovaya-Chernogryazskaya str., Moscow, 105062, Russian Federation; ORCID iD 0000-0001-8591-428X.
Dmitriy A. Skladnev — Dr. Sc. (Biol.), Professor, senior researcher of the Laboratory of Microorganism Survival, Federal Research Center «Fundamental Basis of Biotechnology»; 33, build. 2, Leninskiy av., Moscow, 119071, Russian Federation; ORCID iD 0000-0001-6929-6397.
Alena P. Alekseeva — postgraduate student of the Department of Ocular Oncology and Radiology, Helmholtz National Medical Research Center; 14/19, Sadovaya-Chernogryazskaya str., Moscow, 105062, Russian Federation; ORCID iD 0000-0002-7568-3016.
Olga V. Beznos — specialist in clinical and laboratory diagnostics of the Department of Pathophysiology and Biochemistry, Helmholtz National Medical Research Center; 14/19, Sadovaya-Chernogryazskaya str., Moscow, 105062, Russian Federation; ORCID iD 0000-0001-7557-4955.
Vladimir V. Sorokin — senior researcher of the Laboratory of Microorganism Survival, Federal Research Center «Fundamental Basis of Biotechnology»; 33, build. 2, Leninskiy av., Moscow, 119071, Russian Federation; ORCID iD 0000-0002- 4166-3105.
Contact information: Alena P. Alekseeva, e-mail: chonai.94@mail.ru.
There is no conflict of interest.
Financial Disclosure: autors have no a financial or property interest in any material or method mentioned.
Received 17.07.2023.
Revised 07.08.2023.
Accepted 28.08.2023.
материал rmj.ru
