Содержание статьи
Введение
В 2017 г. в докладе Dry Eye Workshop II исследовательской группой Tear Film and Ocular Surface Society (TFOS DEWS II) синдром «сухого глаза» (ССГ) было предложено рассматривать как самостоятельное мультифакторное заболевание глазной поверхности, оказывающее существенное влияние на зрительные функции, а также на повседневную деятельность, производительность труда и качество жизни пациентов [1–5].
Среди патогенетических факторов ССГ важную роль играют: нестабильность и гиперосмолярность слезной пленки, воспаление и повреждение поверхности глаза, а также нейросенсорные аномалии [6–8]. Лечение заболевания включает применение комплекса слезозаместительных и противовоспалительных препаратов, различных немедикаментозных методов. С учетом хронического течения ССГ его лечение является длительным, а в ряде случаев и пожизненным, что существенно снижает качество жизни пациентов [9–13]. Сложности лечения ССГ обусловлены как многофакторностью патогенеза самого заболевания, так и наличием сопутствующей глазной патологии, лечение которой зачастую не проводится. Примером такой патологии является хронический периферический увеит (ХПУ), представляющий собой воспаление плоской части цилиарного тела и прилежащих хориоретинальных структур. Заболевание характеризуется длительным, многолетним течением и скудными клиническими проявлениями, среди которых имеются и сходные с ССГ признаки раздражения глазной поверхности [14–16]. Лечение ХПУ проводится с учетом формы заболевания, наличия осложнений и включает как консервативные, так и хирургические способы [17–20]. Однако особенности клинического течения и лечения ССГ на фоне ХПУ остаются недостаточно изученными.
Цель исследования: изучить клинические особенности течения ССГ на фоне ХПУ и разработать комплексный способ лечения, включающий слезозаместительную, противовоспалительную терапию в сочетании с лазеркоагуляцией крайней периферии сетчатки.
Материал и методы
Клиническое исследование выполнено среди 98 пациентов (196 глаз) с ССГ легкой и средней степени тяжести и ХПУ на базах офтальмологической клиники ФГБОУ ВО СибГМУ Минздрава России и ООО «Гранд Ретина» (г. Томск). Протокол клинического исследования утвержден локальным этическим комитетом ФГБОУ ВО СибГМУ Минздрава России от 17.12.2018 (регистрационный номер 6978/1).
Обследование пациентов включало сбор жалоб и анамнеза заболевания, анамнеза жизни, заполнение опросника «Индекс поражения глазной поверхности» (Ocular Surface Disease Index, OSDI). Расчет индекса по опроснику OSDI проводили для каждого пациента по следующей формуле: OSDI = (количество баллов за ответы) × 25 / количество заданных вопросов. Полученный индекс отражает степень выраженности проявлений ССГ: 0–12 баллов — нет проявлений ССГ, 13–22 балла — слабовыраженный ССГ; 23–32 балла — ССГ умеренной степени; 33–100 баллов — ССГ тяжелой степени.
Офтальмологическое обследование включало: визометрию, тест Ширмера I, пневмотонометрию, биомикроскопию переднего отрезка обоих глаз, бинокулярную офтальмоскопию со склерокомпрессией.
Диагноз ССГ выставляли на основании следующих критериев: индекс OSDI>12 баллов, наличие характерных биомикроскопических изменений глазной поверхности, снижение суммарной слезопродукции по результатам теста Ширмера I.
В исследование не включали пациентов с имеющимися в анамнезе признаками клинически значимого неконтролируемого заболевания любого органа или системы органов (активный туберкулез, онкологические заболевания), психическими нарушениями и снижением интеллекта, а также страдающих тяжелой степенью ССГ согласно классификации Е.Е. Сомова, В.В. Бржеского (1998 г., с изменениями).
В зависимости от планируемого лечения пациенты были разделены на 2 группы: основную и сравнения. В основную группу вошло 78 пациентов (156 глаз), из них 58 (74,4%) женщин. Пациентам основной группы проводилось комплексное лечение в виде местной противовоспалительной (инстилляции 0,09% бромфенака 1 раз на ночь в течение 1 мес.) и слезозаместительной терапии в сочетании с лазеркоагуляцией крайней периферии сетчатки. Лазерная манипуляция выполнялась однократно бесконтактным методом на аппарате офтальмохирургическом диодном «АЛОД-01» («Алком», Россия) (лазерный коагулятор совмещен с налобным бинокулярным офтальмоскопом Neitz IQ-α (Япония) с одновременной склерокомпрессией. Под визуальным контролем с использованием асферической линзы 20,0 дптр каждому пациенту в индивидуальном порядке подбиралась мощность лазерного излучения для получения коагулятов II–III степени по LЂEsperance на крайней периферии глазного дна (вблизи зубчатой линии сетчатки). Мощность и длительность импульсов задавались на панели управления лазерного блока. Средние параметры лазеркоагуляции: диаметр пятна — 100–350 мкм, мощность — 0,4–0,6 Вт, экспозиция импульса — 0,2–0,3 с. Частота повторения импульсов составляла 0,2–0,3 Гц. Общее количество коагулятов — 300–360.
Длительность применения и выбор препаратов из группы слезозаменителей осуществляли с учетом степени тяжести ССГ: при легкой степени назначали инстилляции слезозаменителя 3–4 р/сут в течение 1–1,5 мес., при средней тяжести — комплексную терапию в течение 6 мес. в виде инстилляций слезозаменителя 4–5 р/сут и 5% геля с декспантенолом (Корнерегель) на ночь.
Препараты из группы слезозаменителей являются наиболее востребованными средствами лечения ССГ. В связи с этим при средней степени тяжести ССГ был добавлен 5% глазной гель декспантенола (Корнерегель), оказывающий регенерирующее действие за счет ускорения пролиферации эпителиальных клеток роговицы, увеличения количества мигрирующих клеток и скорости их миграции, устраняющий неровности глазной поверхности и стабилизирующий состояние слезной пленки. Преимуществом гелевой формы препарата является его способность удерживаться на глазной поверхности до 4 раз дольше, чем у растворов, обеспечивая более длительное комфортное состояние.
В группу сравнения включены 20 пациентов (40 глаз), из них 14 (70%) женщин, которым проводилась только местная терапия, аналогичная проводимой в основной группе.
В ходе исследования осмотры пациентов обеих групп проводили через 3 и 6 мес. после лечения. Срок наблюдения составил 6 мес. Все пациенты были проинформированы о наличии у них ССГ и ХПУ, необходимости их лечения и были согласны на регулярные контрольные осмотры.
Статистический анализ полученных данных осуществляли общепринятыми методами статистики, включая расчет параметров распределения (среднее значение, ошибка среднего, дисперсия), с помощью программного обеспечения MS Excel 2016 (Microsoft Inc., США), Statistica 12.0 (StatSoft Inc., США). Для оценки статистической значимости различий при сравнении средних величин использовали непараметрические критерии: U-критерий Манна — Уитни (pU) и Т-критерий Уилкоксона (pT). Критический уровень значимости (р) при проверке статистических гипотез принимали меньше 0,05.
Результаты исследования
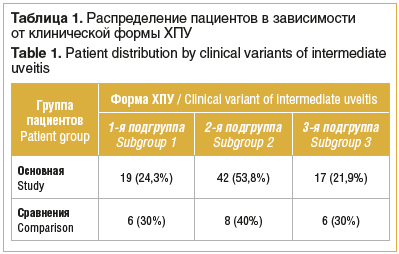
Клиническая картина ССГ у всех (100%) пациентов на момент обращения была сходной: жалобы на ощущение «сухости» в глазах, чувство зрительного дискомфорта, периодическое покраснение глаз и слезотечение. По результатам анкетирования OSDI у пациентов обеих групп перед началом лечения ССГ соответствовал легкой и умеренной степени тяжести. ССГ легкой степени определялся у 77 (78,5%) пациентов основной группы и 15 (75%) пациентов группы сравнения, умеренной степени — у 21 (21,5%) и 5 (25%) пациентов соответственно. Средняя максимальная корригированная острота зрения у всех обследованных пациентов составила 0,9, уровень внутриглазного давления находился в пределах референсных значений (16,8±0,3 мм рт. ст.). При биомикроскопии глазной поверхности у пациентов обеих групп обнаруживались признаки ССГ: тусклость конъюнктивы век и переходных складок, нависание конъюнктивы над задним ребром нижнего века, «вялая» гиперемия конъюнктивы век и глазного яблока, наличие в конъюнктивальной полости скудного отделяемого слизистого характера. Средний показатель теста Ширмера I в основной группе составил 9,0±1,2 мм, в группе сравнения — 9,0±1,4 мм. На крайней периферии глазного дна у пациентов обеих групп определялись признаки хронического воспаления различной степени тяжести. В зависимости от клинической формы ХПУ пациенты основной группы и группы сравнения были разделены на 3 подгруппы: 1-я подгруппа — «Ползучая периферическая дистрофия», 2-я — «Белая сетчатка с давлением или без давления», 3-я — «Пристеночные экссудаты» (табл. 1).
Сравнительный анализ результатов лечения выявил значительную эффективность нового комплексного лечения ССГ на фоне ХПУ. Динамика индекса OSDI у обследованных пациентов свидетельствовала о значительном уменьшении характерных для синдрома жалоб, особенно у пациентов основной группы (табл. 2). Так, например, через 3 мес. после комплексного лечения индекс OSDI у пациентов основной группы снизился на 11, 17,6 и 9,3% в 1-й, 2-й и 3-й подгруппах соответственно (p<0,01), через 6 мес. — на 30,3, 34,8 и 27,8% от исходного уровня соответственно (р<0,05) (см. табл. 2).
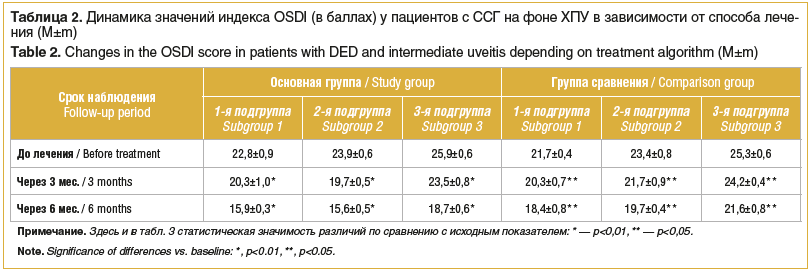
В группе сравнения через 3 мес. после курса местного консервативного лечения индекс OSDI уменьшился на 6,4, 7,2 и 4,3% от первоначального уровня в 1-й, 2-й и 3-й подгруппах соответственно (р<0,05), спустя 6 мес. — на 15,2, 15,8 и 14,6% от исходного уровня соответственно (см. табл. 2).
Необходимо отметить, что в основной группе и группе сравнения до лечения и через 3 мес. после соответствующего лечения не выявлено статистически значимых различий индекса OSDI (р>0,05). Однако через 6 мес. данный показатель во всех 3 подгруппах основной группы был статистически значимо ниже, чем у пациентов 3 подгрупп группы сравнения (р<0,05).
Применение комплексного способа лечения ССГ на фоне ХПУ положительно отразилось и на состоянии глазной поверхности у пациентов основной группы. Так, через 3 мес. после комплексного лечения отмечено статистически значимое уменьшение числа случаев нависания складки конъюнктивы над задним ребром нижнего века на 27,6, 25,7 и 25% в 1-й, 2-й и 3-й подгруппах основной группы соответственно (p<0,01). Встречаемость выраженной «вялой» гиперемии конъюнктивы век и переходных складок статистически значимо уменьшилась на 50% в 1-й и 2-й подгруппах, на 43% — в 3-й подгруппе (р<0,01). Частота выявления скудного вязкого отделяемого снизилась во всех 3 подгруппах основной группы, однако выявлены значимые внутригрупповые различия в итоговом проценте: в 1-й и 2-й подгруппах данный показатель уменьшился на 60%, в 3-й подгруппе — на 20% (р<0,01).
У пациентов группы сравнения через 3 мес. после курса консервативного лечения число случаев нависания конъюнктивальной складки над задним ребром нижнего века статистически значимо (p<0,05) уменьшилось: в 1-й и 3-й подгруппах — на 20%, во 2-й подгруппе — на 21,4%. Значительно снизилось и число случаев выраженной «вялой» гиперемии конъюнктивы: в 1-й и 3-й подгруппах — на 20%, во 2-й подгруппе — на 33,3% (p<0,05). Частота обнаружения скудного отделяемого в полости конъюнктивы сократилась во всех 3 подгруппах группы сравнения, при этом также выявлены значимые внутригрупповые различия: в 1-й и 2-й подгруппах анализируемый показатель уменьшился на 50%, в 3-й подгруппе — лишь на 20% (p<0,05).
Необходимо отметить, что через 6 мес. после комплексного (в сочетании с лазеркоагуляцией сетчатки на крайней периферии глазного дна) лечения у 37,7% пациентов основной группы биомикроскопические признаки ССГ отсутствовали полностью. У остальных 62,3% пациентов данной группы при биомикроскопии глазной поверхности выявлялись признаки ССГ легкой степени. При этом встречаемость нависания складки конъюнктивы над задним ребром нижнего века у пациентов основной группы статистически значимо снизилась по сравнению с исходным уровнем на 51,8% в 1-й и 2-й подгруппах и на 35,7% — в 3-й подгруппе (p<0,05). Частота «вялой» гиперемии конъюнктивы значительно снизилась во всех 3 подгруппах основной группы. При этом выявлены значимые внутригрупповые различия: у всех пациентов 1-й подгруппы конъюнктива век и переходных складок имела здоровую окраску, у пациентов 2-й и 3-й подгрупп уменьшение числа выявленных случаев по сравнению с исходным значением составило 81,3% и 64,3% соответственно (p<0,05). Внутригрупповые различия наблюдались и при оценке частоты скудного конъюнктивального отделяемого в основной группе: у всех пациентов 1-й и 2-й подгрупп отделяемое отсутствовало, у пациентов 3-й подгруппы данный показатель уменьшился на 60% от первоначального уровня (p<0,05).
В группе сравнения через 6 мес. после курса местного консервативного лечения легкая степень ССГ выявлялась у 65% пациентов, умеренная — у 15% пациентов, при этом у 20% биомикроскопические признаки ССГ вовсе отсутствовали. Распространенность случаев нависания конъюнктивальной складки над задним ребром нижнего века статистически значимо уменьшилась от исходного уровня на 35,7% в 1-й и 2-й подгруппах группы сравнения и на 20% — в 3-й подгруппе (p<0,05). При сравнении частоты встречаемости «вялой» гиперемии конъюнктивы у пациентов группы сравнения выявлены внутригрупповые различия: в 1-й и 2-й подгруппах данный показатель уменьшился на 50%, в 3-й подгруппе — на 33,3% (p<0,05). Показатель частоты обнаружения скудного вязкого конъюнктивального отделяемого сократился в 1-й и 2-й подгруппах на 60% (p<0,05), в то время как в 3-й подгруппе остался на прежнем уровне.
В течение всего периода исследования (6 мес.) отмечено постепенное увеличение суммарной слезопродукции у пациентов обеих групп, происходившее, однако, более быстрыми темпами в основной группе (табл. 3). Так, через 3 мес. после комплексного лечения у пациентов основной группы средний показатель теста Ширмера I увеличился от первоначального уровня на 39,7, 39,5 и 25,8% в 1-й, 2-й и 3-й подгруппах соответственно (p<0,05). В группе сравнения через 3 мес. после курса консервативного лечения данный показатель увеличился лишь на 23,5, 17,5 и 12,5% в 1-й, 2-й и 3-й подгруппах соответственно.
Через 6 мес. после лечения в основной группе показатель теста Ширмера I увеличился по сравнению с исходным значением на 46,4, 47,2 и 43,5% соответственно (p<0,05), в группе сравнения — на 34,7, 32,3 и 26,7% соответственно (p<0,05) (см. табл. 3).
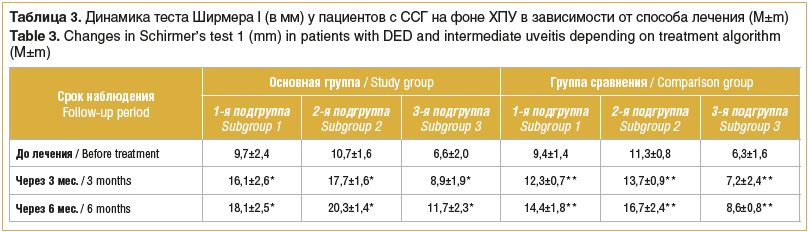
Необходимо отметить, что исходные (до лечения) значения показателя теста Ширмера I у пациентов основной группы и группы сравнения статистически значимо не различались. Однако уже через 3 мес. данный показатель у пациентов каждой из 3 подгрупп основной группы статистически значимо превышал таковой у пациентов всех 3 подгрупп группы сравнения (р<0,05). Выявленная тенденция наблюдалась и через 6 мес. после комплексного лечения (см. табл. 3).
Положительная динамика течения ХПУ в виде постепенного рассасывания экссудатов стекловидного тела, уменьшения отека сетчатки с купированием воспаления и восстановлением прозрачности витреоретинальных структур наблюдалась у большинства (75%) пациентов основной группы уже через 3 мес. после комплексного лечения. К концу периода наблюдения (6 мес.) ни у одного пациента основной группы не выявлено рецидива ХПУ. У всех (100%) пациентов группы сравнения после улучшения состояния хориоретинальных структур на крайней периферии глазного дна в виде уменьшения отека сетчатки и частичного рассасывания преретинальных экссудатов через 3 мес. после консервативного лечения уже спустя 6 мес. диагностирован рецидив ХПУ.
Обсуждение
Согласно общепризнанному мнению [1, 21–23] течение ССГ значительно усугубляется при наличии у пациентов аутоиммунных и аллергических заболеваний, нарушений обмена веществ, инфекционных заболеваний, а также при имеющейся офтальмологической патологии. Так, например, ХПУ, нередко встречающийся у пациентов молодого и среднего возраста, в 28–57% случаев сопровождается признаками раздражения глазной поверхности и симптомами, характерными для ССГ [16, 24].
В ходе настоящего клинического исследования установлено, что выраженность симптомов ССГ прямо коррелирует с активностью воспаления хориоретинальных структур на крайней периферии глазного дна. В частности, легкая степень ССГ в большинстве случаев встречается при таких формах ХПУ, как ползучая периферическая дистрофия сетчатки и белая сетчатка с давлением или без давления, средняя же степень данного синдрома обнаруживается при форме ХПУ в виде периферических экссудатов (см. табл. 2, 3).
Проведение лазеркоагуляции крайней периферии сетчатки в ходе комплексного лечения ССГ на фоне ХПУ обеспечивает стабильный терапевтический эффект в течение длительного времени, что подтверждается результатами проведенного исследования. В частности, у пациентов основной группы выявлено значительное — до 34,8% — уменьшение характерных для ССГ жалоб по данным опросника OSDI, улучшение состояния глазной поверхности в виде снижения числа случаев нависания складки конъюнктивы — до 51,8%, выраженности «вялой» гиперемии конъюнктивы век и переходных складок, уменьшения количества конъюнктивального отделяемого. Кроме того, в основной группе отмечено статистически значимое увеличение суммарной слезопродукции — в 1,7–1,8 раза по сравнению с исходным уровнем. Необходимо отметить, что положительная динамика течения ССГ у пациентов основной группы наблюдалась на фоне постепенного уменьшения отека сетчатки вблизи зубчатой линии, рассасывания экссудатов стекловидного тела и восстановления прозрачности витрео-
ретинальных структур.
Таким образом, комплексный подход к лечению ССГ при ХПУ позволяет достичь существенного уменьшения признаков раздражения глазной поверхности, вплоть до их полного исчезновения на фоне купирования воспаления на крайней периферии глазного дна, в сравнении с традиционной фармакотерапией данного синдрома.
Заключение
Согласно результатам проведенного исследования наличие ХПУ усугубляет течение ССГ: чем активнее воспаление хориоретинальных структур вблизи зубчатой линии, тем более выражены клинико-функциональные изменения глазной поверхности. У пациентов с ССГ, развившимся на фоне ХПУ, рационально проводить комплексное лечение, включающее применение местного противовоспалительного препарата, слезозаменителя, репаранта в случае средней тяжести ССГ (в форме геля с 5% декспантенолом (Корнерегель)) и лазеркоагуляции крайней периферии сетчатки. Последняя способствует быстрому и стабильному купированию воспаления хориоретинальных структур вблизи зубчатой линии, обеспечивает значительное уменьшение субъективных и объективных проявлений ССГ, что позволяет улучшить медико-социальную реабилитацию данной категории пациентов, которая подтверждается результатами проведенного клинического исследования.
Благодарность
Редакция благодарит ООО «Бауш Хелс» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgements
The technical edition is supported by Bausch Health LLC.
Сведения об авторах:
Татарникова Елена Борисовна — заочный аспирант кафедры офтальмологии; ORCID iD 0000-0003-3038-8117.
Кривошеина Ольга Ивановна — д.м.н., профессор, заведующая кафедрой офтальмологии; ORCID iD 0000-0001-7509-5858.
ФГБОУ ВО СибГМУ Минздрава России. 634050, Россия, г. Томск, Московский тракт, д. 2.
Контактная информация: Татарникова Елена Борисовна, e-mail: elenka.morozova.92@inbox.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 17.05.2021.
About the authors:
Elena B. Tatarnikova — distant postgraduate student of theDepartment of Ophthalmology; ORCID iD 0000-0003-3038-8117.
Olga I. Krivosheina — Dr. Sc. (Med.), Professor, Head of the Department of Ophthalmology; ORCID iD 0000-0001-7509-5858.
Siberian State Medical University. 2, Moskovskiy tract, Tomsk, 634050, Russian Federation.
Contact information: Elena B. Tatarnikova, e-mail: elenka.morozova.92@inbox.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 17.05.2021.
.
материал rmj.ru
