Клинический опыт применения рекомбинантной проурокиназы у пациентов с сочетанной патологией глазного дна при сахарном диабете 2 типа
Введение
Пациенты с сахарным диабетом 2 типа (СД2) с диабетической ретинопатией (ДР) разных стадий (непролиферативной, препролиферативной, пролиферативной (ДРI, ДРII, ДРIII)) склонны к геморрагическим осложнениям: преретинальным, ретинальным кровоизлияниям, частичным, субтотальным, тотальным гемофтальмам.
Внутриглазные кровоизлияния, часто рецидивирующие, токсически действующие на сетчатку, являются причиной резкой потери зрения при СД2 и трудно поддаются лечению. Своевременное применение фибринолитической терапии, направленной на резорбцию крови и восстановление прозрачности оптических сред, дает возможность правильного выбора дальнейшего лечения (лазерной коагуляции сетчатки, анти-VEGF-терапии), что широко освещено в современной научной литературе [1–9]. При неэффективности консервативной терапии методом выбора является витрэктомия, которая имеет ряд противопоказаний у соматически тяжелых пациентов с нестабильным течением СД2, склонностью к гипо- и гипергликемическим состояниям. Ферментотерапия как более щадящий вид лечения в последние годы широко используется в офтальмологической практике. В связи с актуальностью проблемы проведен обзор литературных источников разных лет, в которых затрагиваются вопросы консервативного лечения интравитреальных и ретинальных кровоизлияний.
Отечественными биотехнологами совместно с офтальмологами более 20 лет назад был создан генно-инженерный высокоэффективный ферментный препарат для офтальмологии — Гемаза. Его действующим веществом является фермент рекомбинантная проурокиназа человека. Препарат выпускается в форме лиофилизата для приготовления раствора для инъекций в ампулах. Специфическая ферментативная активность препарата Гемаза — 5000 ME в ампуле. Препарат стерилен, нетоксичен и апирогенен. Препарат получают биотехнологическим путем. В качестве вспомогательных веществ препарат содержит декстран и натрия хлорид. Гемаза катализирует превращение плазминогена в плазмин — сериновую протеазу, способную лизировать фибриновые сгустки. Препарат обладает высокой специфичностью действия, которая достигается за счет того, что активируется преимущественно фибринсвязанный плазминоген, имеющий иную конформацию по сравнению с циркулирующим в кровотоке плазминогеном, и трансформируется в плазмин. В области фибринового сгустка Гемаза нечувствительна к специфическим ингибиторам, присутствующим в плазме крови. Одноцепочечная молекула рекомбинантной проурокиназы под воздействием плазмина превращается в двухцепочечную молекулу, которая, в отличие от одноцепочечной проформы, значительно более активна в отношении фибринсвязанного плазминогена. Образуется цепная реакция взаимодействия рекомбинантной проурокиназы с фибринсвязанным плазминогеном, в результате которой фибриновый сгусток разрушается. Препарат относится к фибринолитикам последнего поколения и обладает уникальными свойствами: гипоаллергенностью, низким риском развития кровотечения и, таким образом, показан при гифеме, гемофтальме, преретинальных, субретинальных и интраретинальных кровоизлияниях. Рекомбинантная проурокиназа эффективна при фибриноидном синдроме различного генеза, что подтверждено исследованиями у пациентов с послеоперационным токсическим синдромом [10–12], при окклюзиях центральной артерии сетчатки и ее ветвей и тромбозе центральной вены сетчатки и ее ветвей [13, 14]. Хороший эффект достигается при лечении спаечного процесса в послеоперационном периоде при антиглаукоматозных операциях [15], при травматическом гемофтальме [16, 17]. Сегодня используют форсированные инстилляции, субконъюнктивальные, парабульбарные, субтеноновые инъекции, введение в переднюю камеру. Так, положительный эффект отмечен при инстилляциях раствором препарата в концентрации 330 МЕ в 1 мл 0,9% раствора натрия хлорида непрерывно в течение 10 мин со скоростью 30 капель в минуту. Общий объем инстилляций препарата составил 15 мл (5000 МЕ Гемазы) [18, 19]. Хорошие результаты получают при использовании препарата Гемаза для интравитреального введения. Такая клиническая эффективность объясняется, в том числе, результатами экспериментов на кроликах с использованием метода иммунофлюоресценции, где был изучен процесс транссклерального проникновения фибринолитика. Отмечено, что Гемаза (по современным данным, молекулярная масса фермента составляет 46,0 кДа) способна проникать через все слои сетчатки через 2 ч после интравитреального введения. При лечении субмакулярных кровоизлияний различной этиологии применяют интравитреальное введение 500 МЕ препарата Гемаза (за 1 сут) с последующей пневматической дислокацией субмакулярного кровоизлияния из-под области фовеа пузырем газообразного перфторциклобутана, что позволяет добиться повышения остроты зрения в 80% случаев [20]. Широко используют комбинированные методы лечения, электрофорез, лечебные контактные линзы [18]. В доступной литературе освещены новые подходы к хирургическому лечению массивной субмакулярной геморрагии при «влажной» форме возрастной макулярной дегенерации (ВМД) [21]. Однако недостаточно широко в научной литературе представлены данные о фибринолитической терапии геморрагических осложнений при сочетанной патологии глазного дна: ДР, гипертонической ангиопатии (ГА), гипертонической ретинопатии (ГР), ВМД. Данное исследование было предпринято для проведения клинико-морфофункционального и патогенетического анализа состояния сетчатки при сочетанной патологии глазного дна на фоне фибринолитической терапии.
Цель: оптимизировать лечение рекомбинантной проурокиназой сочетанной патологии глазного дна: ДР, ГР, «влажной» формы ВМД с геморрагическими проявлениями при СД2 с учетом динамики состояния сетчатки и уровня патогенетического биомаркера фактора роста эндотелия сосудов (VEGF-A) в слезной жидкости.
Материал и методы
Под наблюдением находилось 30 пациентов (30 глаз), страдающих СД2, гипертонической болезнью (ГБ). Все пациенты были с сочетанной патологией глазного дна и геморрагическими изменениями на глазном дне: 23 — с пролиферативной ДР (ДРIII), ГР; 7 человек — с «влажной» формой ВМД (AREDS IV) с геморрагическими изменениями, ГР, ДРIII. В группу из 30 человек вошли 20 женщин (66,7%) и 10 мужчин (33,3%). Средний возраст пациентов составил 62,8±1,5 года. Длительность течения СД от 2 до 5 лет была отмечена у 10 (33,3%) пациентов, 6–10 лет — у 14 (46,7%), 11–15 лет — у 5 (16,7%), более 15 лет — у 1 (3,3%) пациента. Пациенты принимали пероральные сахароснижающие препараты (ПССП). Средний по группе уровень гликемии натощак составил 7,02±0,5 ммоль/л. Уровень гликемии натощак у пациентов с длительностью течения СД до 5 лет составил 7,15±0,4 ммоль/л, 6–10 лет — 7,09±0,4 ммоль/л, 11–15 лет — 6,82±0,7 ммоль/л, более 15 лет — 5,7 ммоль/л. Средний по группе уровень гликированного гемоглобина (HbA1c) составил 7,32±0,6%. Уровень HbA1c составил среди пациентов с длительностью течения СД до 5 лет 6,96±0,4%; 6–10 лет — 7,6±0,3%, 11–15 лет — 7,0±0,6%, более 15 лет — 7,0%.
Визометрию вдаль проводили по стандартной методике с использованием проектора знаков OAP 311 (Carl Zeiss, Германия) и стандартного набора стекол; тонометрию осуществляли тонометром Маклакова массой 10,0 г; биомикроскопию переднего отдела проводили на щелевой лампе AIA-12 2S (Appasamy Associates, Индия); биомикроскопию стекловидного тела и офтальмоскопию сетчатки выполняли в условиях медикаментозного мидриаза с помощью бесконтактной линзы +60 D (Ocular Instruments Inc., США) и 3-зеркальной линзы Гольдмана OG3MA (Ocular Instruments Inc., США) на щелевой лампе; ультразвуковое исследование проводили на аппарате Ultrasonic A/B Scanner UD-6000 (Tomey, Япония); фоторегистрацию глазного дна выполняли на цветной фундус-камере NM-1000 (Nidek, Германия); фундус-микропериметрию выполняли при помощи периметра MAIA (CenterVue Spa, Италия) в режиме Fast Expert Exam, позволяющем определять светочувствительность макулярной зоны сетчатки в 37 точках (0–3–5 мм от центральной ямки сетчатки).
Степень выраженности гемофтальма определяли количественно при помощи индекса гемофтальма, который позволяет по состоянию рефлекса глазного дна в условиях медикаментозного мидриаза при биомикроскопии в баллах оценивать выраженность интравитреального кровоизлияния. Оценку проводили по данным непрямой бинокулярной биомикроскопии с линзой +30 дптр по четырем квадрантам: при взгляде вверх направо, вверх налево, вниз направо, вниз налево. В каждом положении видимость деталей сетчатки оценивали в баллах от 0 до 3:
0 — кровь и ее остатки не определяются, видны все детали сетчатки;
1 — незначительное кровоизлияние или его остатки, детали сетчатки в тумане;
2 — слабый розовый рефлекс, детали видны в густом тумане;
3 — розовый рефлекс отсутствует, офтальмоскопия невозможна.
Результаты осмотра в баллах по каждому квадранту складывали и получали индекс гемофтальма, который оценивали у больных с гемофтальмами до лечения, на 1-й и 10-й день курса лечения. Проводя эхографическое исследование, определяли объем гемофтальма и выделяли больных с частичным, субтотальным и тотальным гемофтальмом.
Критерии включения: СД2; терапия СД2 — ПССП; наличие ГБ; наличие одного или более микрососудистых осложнений (ретинопатия, нефропатия, нейропатия); НbА1с на уровне от 5,5 до 12%, геморрагические изменения: преретинальные, ретинальные кровоизлияния, частичный, субтотальный, тотальный гемофтальм у пациентов с сочетанной патологией глазного дна: ДР, ГР, «влажной» формой ВМД. Критерии исключения: тяжелые осложнения СД, хроническая почечная недостаточность, синдром диабетической стопы; НbА1с выше 12%; уровень артериального давления выше 160/100 мм рт. ст.; симптоматическая артериальная гипертензия; инфаркт миокарда, острое нарушение мозгового кровообращения менее 12 мес. давности; пороки сердца, нарушения ритма по типу мерцательной аритмии, атриовентрикулярные блокады II–III степени, сердечная недостаточность.
Все пациенты с геморрагическими изменениями получали препарат Гемаза строго в соответствии с инструкцией по медицинскому применению препарата (регистрационный № 001837/01 от 02.03.2009) в офтальмологии для лечения гемофтальмов, преретинальных, субретинальных и интраретинальных кровоизлияний. По типу геморрагических осложнений 30 человек (30 глаз) с СД2 разделялись на исследовательские группы (ИГ): ИГ1, ИГ2, ИГ3, ИГ4 и контрольную группу из 15 пациентов с СД2, ГБ и сочетанной патологией глазного дна: ГР, ДРIII с преретинальными, ретинальными кровоизлияниями и гемофтальмом, получавших в качестве лечения традиционную терапию (ангиопротекторы, ферментные препараты).
В ИГ1 пациентам с СД2, ГБ и сочетанной патологией глазного дна: ГР, ДРIII с преретинальными, ретинальными кровоизлияниями (n=7) был проведен курс из 10 ежедневных парабульбарных инъекций препарата по 0,5 мл раствора (5000 МЕ).
В ИГ2 пациентам с СД2, ГБ и сочетанной патологией глазного дна: ГР, ДРIII с преретинальными, ретинальными кровоизлияниями (n=8) препарат вводили однократно интравитреально (0,2 мл раствора в дозе 500 МЕ) с последующими ежедневными парабульбарными инъекциями в течение 10 дней по 0,5 мл раствора (5000 МЕ).
В ИГ3 пациентам с СД2, ГБ и сочетанной патологией глазного дна: ГР, ДРIII с гемофтальмом, преретинальными, ретинальными кровоизлияниями (n=8) препарат вводили однократно интравитреально (0,2 мл раствора в дозе 500 МЕ) и парабульбарно по схеме 10 ежедневных парабульбарных инъекций по 0,5 мл раствора (5000 МЕ).
В ИГ4 пациентам с СД2, ГБ, ГР, ДРIII, «влажной» формой ВМД (AREDS IV) с преретинальными и ретинальными кровоизлияниями (n=7) препарат вводили парабульбарно по схеме 10 ежедневных парабульбарных инъекций по 0,5 мл раствора (5000 МЕ).
Согласно инструкции по медицинскому применению препарата, для парабульбарного введения содержимое 1 ампулы препарата Гемаза разводили в 0,5 мл 0,9% раствора натрия хлорида. Полученный раствор, содержащий дозу 5000 ME, вводили 1 р./сут парабульбарно, 10 инъекций на курс.
Для интравитреального введения содержимое 1 ампулы препарата Гемаза (5000 ME лиофилизата) разводили в стерильных условиях в 1,0 мл 0,9% раствора натрия хлорида. Затем из полученного объема брали 0,1 мл (500 ME) и разбавляли 0,1 мл 0,9% раствора натрия хлорида. Полученный объем (0,2 мл) вводили интравитреально. Интрави-
треальное введение препарата Гемаза проводили в условиях стерильной операционной под капельной анестезией при расширенном зрачке. После двукратной обработки операционного поля спиртом и раствором повидон-йода, инстилляции антибиотиков широкого спектра действия, через плоскую часть цилиарного тела в 4,0 мм от лимба вводили иглу в намеченный участок склеры по направлению к центру глазного яблока; препарат вводили в стекловидное тело, затем иглу извлекали. После манипуляции проводили инстилляцию антибиотиков широкого спектра действия. В первые минуты после инъекции происходило повышение уровня внутриглазного давления (ВГД) (пальпаторно), которое купировалось самостоятельно в течение 30 мин. В дальнейшем ВГД не повышалось. В течение 3 дней до манипуляции и 7 дней после нее всем пациентам назначали инстилляции антибиотиков широкого спектра действия из группы фторхинолонов по 1 капле 4 р./сут. В соответствии с инструкцией по медицинскому применению препарата фармакокинетика Гемазы такова, что при парабульбарном введении максимальная концентрация препарата в тканях глаза достигается через 1–2 ч после введения. Затем концентрация препарата постепенно снижается, через 12–24 ч препарат обнаруживается в следовых количествах. Максимальная концентрация препарата определяется во внутриглазных структурах при интравитреальном введении. Период полувыведения препарата составляет 4–6 ч.
В связи с этим динамическую оценку максимально корригированной остроты зрения (МКОЗ), светочувствительность макулы (СМ), индекс гемофтальма при гемофтальме, ВГД, эхографическое исследование проводили до и после лечения во всех группах на фоне фибринолитической терапии в сочетании с традиционным лечением (ангиопротекторы, ферментные препараты).
В те же сроки у всех пациентов стерильной пипеткой забирали слезную жидкость (СЖ) из нижнего конъюнктивального свода в объеме 100 мкл, помещали в микропробирки «Eppendorf» и однократно замораживали при температуре ‑20 °С. После размораживания в образцах СЖ определяли уровень VEGF-А (пг/мл) методом твердофазного иммуноферментного анализа.
Результаты исследования
В ИГ1 средняя МКОЗ возрастала от 0,01±0,003 до 0,02±0,004 через 1 сут (p>0,05), до 0,2±0,01 на 10-е сут курса лечения (p0,05). Уровень патогенетического биомаркера VEGF-A в слезе менялся и до лечения составил 1532,2±123,1 пг/мл, через 1 сут — 2008,4±112,1 пг/мл (p>0,05), на 10-е сут курса лечения — 1645,4±52,9 пг/мл (p>0,05). Положительный результат лечения Гемазой показан на рисунке 1. Представлены данные пациента Б., 63 г., диагноз: СД2, ГБ, ДРIII, ГА, преретинальное кровоизлияние. Пациенту был проведен курс лечения препаратом Гемаза — инъекции по 5000 МЕ парабульбарно ежедневно в течение 10 дней.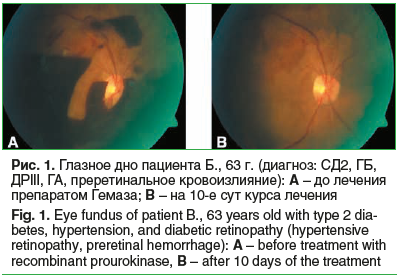
В ИГ2 средняя МКОЗ возрастала от 0,05±0,03 до 0,06±0,01 через 1 сут, до 0,49±0,04 на 10-е сут (p0,05). Уровень патогенетического биомаркера VEGF-A в слезе на фоне лечения изменялся от 1521,8±152,2 пг/мл до начала лечения до 1599,3±73,8 пг/мл через 1 сут после (p>0,05), до 1648,5±115,6 пг/мл — на 10-е сут курса лечения (p>0,05).
В ИГ3 средняя МКОЗ возрастала от 0,06±0,02 до 0,07±0,01 (p>0,05) через 1 сут, до 0,27±0,02 (p0,05); СМ до лечения не определялась, после лечения составила 10 дБ (p0,05), 4,1±0,2 на 10-е сут курса лечения (p0,05). Положительный результат лечения препаратом Гемаза проиллюстрирован на рисунке 2. Пациент И., 64 г., диагноз: СД2, ГБ, ДРIII, ГР, частичный гемофтальм, ретинальное кровоизлияние. Проведено лечение препаратом Гемаза: однократно интравитреально (0,2 мл раствора в дозе 500 МЕ), затем инъекции по 5000 МЕ парабульбарно ежедневно в течение 10 дней. Частичный гемофтальм при пролиферативной ДР через 10 дней лечения значительно уменьшился. Положительный эффект в короткие сроки от начала лечения позволил своевременно приступить к следующему этапу лечения — лазерной коагуляции сетчатки (ЛКС) при пролиферативной ДР, а именно панретинальной лазерной коагуляции в несколько этапов.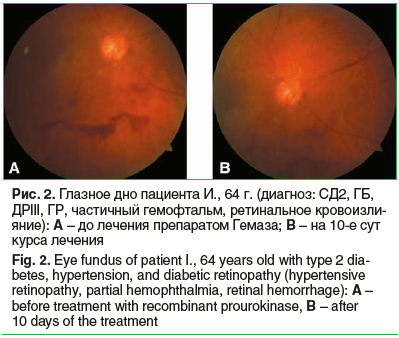
В ИГ4 с преретинальными и ретинальными кровоизлияниями средняя МКОЗ возрастала от 0,01±0,02 до 0,03±0,05 через 1 сут (p>0,05), до 0,21±0,02 на 10-е сут курса лечения (p0,05). Уровень патогенетического биомаркера VEGF-A в слезе на фоне лечения изменялся от 1535,5±91,1 пг/мл до начала лечения до 1587,1±99,2 пг/мл через 1 сут после, до 1621,4±111,85 пг/мл — на 10-е сут курса лечения (p>0,05). Клинический пример пациента из ИГ4 с сочетанной патологией глазного дна представлен на рисунке 3.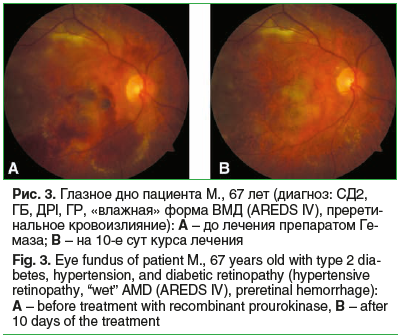
Пациент М., 67 лет, диагноз: СД2, ГБ, ДРI, ГР, «влажная» форма ВМД (AREDS IV), преретинальное кровоизлияние. Проведен курс лечения препаратом Гемаза — инъекции по 5000 МЕ парабульбарно ежедневно в течение 10 дней. Данный клинический пример иллюстрирует выраженный положительный результат лечения препаратом Гемаза у пациента с сочетанной патологией глазного дна: ДР, ГА, «влажной» формой ВМД с выраженным геморрагическим компонентом. На 10-е сут курса лечения препаратом Гемаза острота зрения улучшилась статистически значимо, патогенетический биомаркер в слезе менялся, но недостоверно (до лечения: Vis OD=1/∞ pr. l. certa, ВГД OD=21 мм рт. ст., VEGF-A 1521 пг/мл; после лечения Vis OD=0,2 н/к,
ВГД OD=20 мм рт. ст., VEGF-A 1620 пг/мл).
В контрольной группе средняя МКОЗ возрастала от 0,03±0,02 до 0,05±0,05 через 1 сут (p>0,05), до 0,1±0,02 на 10-е сут курса лечения (p0,05). Уровень патогене-тического биомаркера VEGF-A в слезе на фоне лечениявозрастал и составлял до начала лечения 1545,5±92,2 пг/мл, 1587,1±99,2 пг/мл через 1 сут после начала лечения, 1800,1±111,85 пг/мл на 10-е сут курса лечения (p
Анализ патогенетически значимого биомаркера VEGF-A в слезе в разных группах (ИГ1, ИГ2, ИГ3, ИГ4) позволил выявить, что при преретинальных, ретинальных кровоизлияниях, частичном гемофтальме, субтотальном гемофтальме и тотальном гемофтальме уровень VEGF-A на фоне фибринолитической терапии меняется, но недостоверно (p>0,05). В контрольной группе уровень VEGF-A достоверно возрастает (p
Обсуждение
Изолированно ДР при СД2 встречается редко. В 80% случаев СД2 сопутствует ГБ, а ДР сопутствует ГА или ГР. При полипатии, а именно ДР, ВМД, ГР, которые сопровождаются кровоизлияниями преретинальными, ретинальными и в стекловидное тело, необходимо выбрать правильную тактику ведения пациентов. Первым этапом необходимо восстановить прозрачность стекловидного тела, сетчатки. Оптимальным методом для этого является фибринолитическая терапия с помощью препарата Гемаза, особенно у тяжелой категории больных. Вторым этапом, в зависимости от состояния сетчатки, необходимо проводить ЛКС, или анти-VEGF-терапию, или комбинацию ЛКС и анти-VEGF-терапии.
В данной работе были изучены офтальмологические показатели и уровень патогенетически значимого биомаркера (VEGF-A) в слезной жидкости на фоне лечения Гемазой у таких пациентов. Полученные данные по динамике офтальмологических показателей свидетельствуют о высокой эффективности проведенной фибринолитической терапии в ИГ и позволяют рекомендовать оптимальные схемы лечения. Большое внимание в данной работе было уделено анализу динамики VEGF-A. По нашим данным, у здоровых лиц уровень VEGF-A составляет 214,1±22,2 пг/мл, у пациентов с ДР и ГБ без геморрагических проявлений — 518±4,4 пг/мл. В контрольной группе до лечения уровень
биомаркера был равен 1545,5±92,2 пг/мл, а на 10-е сут курса лечения — 1800,1±111,85 пг/мл (p
Исходя из современных представлений о структуре и функциях фермента проурокиназа, можно полагать, что фибринолитик Гемаза (модифицированная рекомбинантная проурокиназа) не влияет непосредственно на синтез VEGF-А в организме. Наблюдаемая стабилизация уровня VEGF-A представляет собой интересный и обнадеживающий эффект терапии данным фибринолитиком. Фибринолитическая терапия направлена, в первую очередь, на резорбцию кровоизлияний в оптических средах глаза, лизис тромбов в сосудах сетчатки любого калибра и, таким образом, улучшение микроциркуляции в сетчатке. Предполагаем, что улучшение микроциркуляции у пациентов всех ИГ приводило к снижению уровня ишемии сетчатки, уменьшая потребность в патологическом избыточном ангиогенезе, вызывая, таким образом, стабилизацию выработки VEGF-A.
Выводы
Выявлена высокая эффективность лечения гемофтальмов и ретинальных кровоизлияний препаратом Гемаза у пациентов с сочетанной патологией глазного дна (ДР, ГР, «влажной» формой ВМД с выраженными геморрагическими проявлениями) при СД2.
Доказана стабилизация патогенетического процесса при применении фибринолитической терапии при сочетанной патологии глазного дна по статистически незначимому изменению уровня биомаркера VEGF-A в слезе, что позволяет отсрочить прогрессирование заболевания, в сравнении с ростом уровня VEGF-A на фоне традиционной терапии.
Рекомендуется пациентам с гемофтальмом, ретинальными кровоизлияниями однократное интравитреальное введение препарата Гемаза по 0,2 мл раствора в дозе 500 МЕ и далее ежедневное парабульбарное введение Гемазы в дозе 5000 МЕ на 0,5 мл 0,9% раствора натрия хлорида № 10 при СД2 у пациентов с сочетанной патологией глазного дна (ДР, ГР) на 3-и сут от начала заболевания.
Рекомендуется пациентам с преретинальными, ретинальными кровоизлияниями ежедневное парабульбарное введение Гемазы в дозе 5000 МЕ на 0,5 мл 0,9% раствора натрия хлорида № 10 при СД2 у пациентов с сочетанной патологией глазного дна (ДР, ГР, «влажной» формой ВМД с выраженными геморрагическими проявлениями) на 3-и сут от начала заболевания.
Данные рекомендации являются методом выбора для пациентов с тяжелым течением основного заболевания СД2, у которых невозможно проведение хирургических видов лечения из-за тяжести состояния больного при сочетанной патологии глазного дна (ДР, ГР, «влажной» форме ВМД с выраженными геморрагическими проявлениями).
Своевременное применение препарата Гемаза у вышеуказанной категории больных с СД2 и сочетанной патологией глазного дна позволит сохранить зрение и отсрочить прогрессирование заболеваний.
Сведения об авторах:
1Мошетова Лариса Константиновна — академик РАН, д.м.н., профессор, зав. кафедрой офтальмологии, ORCID iD 0000-0002-5899-2714;
1Слонимский Юрий Борисович — д.м.н., профессор кафедры офтальмологии, ORCID iD 0000-0002-5656-4919;
1Воробьева Ирина Витальевна — к.м.н., доцент кафедры офтальмологии, ORCID iD 0000-0003-2707-8417;
1Дгебуадзе Ана — аспирант кафедры офтальмологии, ORCID iD 0000-0002-9518-0459;
2Агафонова Ольга Вячеславовна — к.б.н., научный сотрудник, ORCID iD 0000-0002-7483-7167;
2Дельвер Евгений Петрович — к.б.н., старший научный сотрудник, ORCID iD 0000-0003-2319-7937;
2Белогуров Анатолий Александрович — к.б.н., ведущий научный сотрудник, ORCID iD 0000-0002-7170-9530.
1ФГБОУ ДПО РМАНПО Минздрава России. 125993, Россия, Москва, ул. Баррикадная, д. 2/1.
2Научно-исследовательский институт экспериментальной кардиологии ФГБУ «НМИЦ кардиологии» Минздрава России. 121552, Россия, Москва, ул. 3-я Черепковская, д. 15а.
Контактная информация: Воробьева Ирина Витальевна, e-mail: irina.docent2000@mail.ru Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 15.04.2019.
About the authors:
1Larisa K. Moshetova — MD, PhD, Professor, Academician of the Russian Academy of Sciences, Head of Ophthalmology Department, ORCID iD 0000-0002-5899-2714;
1Yury B. Slonimsky — MD, PhD, Professor of the Department of Ophthalmology, ORCID iD 0000-0002-5656-4919;
1Irina V. Vorobyeva — MD, PhD, Associate Professor of the Department of Ophthalmology, ORCID iD 0000-0003-2707-8417;
1Ana Dgebuadze — postgraduate student of the Department
of Ophthalmology, ORCID iD 0000-0002-9518-0459;
2Olga V. Agafonova — PhD in Biology, Research Scientist, ORCID iD 0000-0002-7483-7167;
2Evgeny P. Delver — PhD in Biology, Senior Research Scientist, ORCID iD 0000-0003-2319-7937;
2Anatoly A. Belogurov — PhD in Biology, Leading Research Scientist, ORCID iD 0000-0002-7170-9530.
1Russian Medical Academy of Continuous Professional Education. 2/1, Barrikadnaya str., Moscow, 125993, Russian
Federation.
2Research Institute of experimental cardiology of the National Medical Research Center of Cardiology. 15а, 3rd Cherepkovskaya str., Moscow, 121552, Russian Federation.
Contact information: Irina V. Vorobyeva, e-mail: irina.docent2000@mail.ru. Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 15.04.2019.
материал rmj.ru
