Введение
Аметропии являются одной из актуальных проблем современной офтальмологии. В общей структуре рефракционной патологии среди аметропий преобладает миопия, которая по распространенности в мире к 2050 г. составит 5 млрд человек, ожидается рост распространенности до 49,8%[1]
[1]. В Европе к 2050 г. более половины населения — 56,2% станут близорукими [1, 2]. В странах Восточной и Юго-Восточной Азии зарегистрировано более широкое распространение данной аномалии рефракции — до 96%, при этом из них на долю миопии высокой степени приходится от 10 до 20% случаев [1, 2].
На сегодняшний день имеется достаточный клинический опыт хирургической коррекции аметропий, разработаны оптимальные протоколы операций, алгоритмы ведения пациентов по предотвращению развития интра- и послеоперационных осложнений с последующим их лечением, подходы к оценке результатов в отдаленном периоде кераторефракционных операций с учетом клинико-функциональных, структурно-морфологических и офтальмоэргономических показателей, оценки состояния глазной поверхности, что отражено во многих исследованиях [4–11]. Кераторефракционные вмешательства проводят пациентам в возрасте от 18 до 45 лет при непрогрессирующей (стационарной) миопии от -0,5 до -12,0 дптр с целью достижения предсказуемого и стабильного рефракционного эффекта и высокой послеоперационной некорригированной остроты зрения (НКОЗ)1.
Для подготовки пациентов к кераторефракционному вмешательству, а также для ведения пациентов в послеоперационном периоде разработаны различные схемы медикаментозной терапии. Наиболее известна следующая медикаментозная схема, которая применяется за 1 сут до операции, в день операции и в послеоперационном периоде: назначаются инстилляции глазных капель 0,5% раствора левофлоксацина по 1 капле 4 р/сут в течение 1 нед. и 0,1% раствора дексаметазона по 1 капле 3 р/сут в течение 1-й недели, затем по 1 капле 2 р/сут в течение 2-й недели и по 1 капле 1 р/сут в течение 3-й недели [12, 13].
Однако известно, что инстилляции 0,1% раствора дексаметазона более 2 нед. могут приводить к повышению внутриглазного давления (ВГД) на 6–15 мм рт. ст. Так, авторы отмечают, что после применения 0,1% раствора дексаметазона в 9,8% случаев у пациентов на фоне синдрома «сухого глаза» через 1 мес. после кераторефракционной операции отмечалось значительное повышение роговично-компенсированного ВГД с 16,9±3,8 до 20,5±7 мм рт. ст., что потребовало отмены глюкокортикостероидов (ГКС) [14].
У пациентов с миопией после ФемтоЛАЗИК в 1-е сутки после операции могут отмечаться болевой синдром [15, 16], светобоязнь, слезотечение, а у 9% пациентов с исходной миопией средней и высокой степени и достигнутым высоким рефракционным результатом, отсутствием синдрома «сухого глаза», идеальным заживлением роговицы отмечаются астенопические жалобы, проявляющиеся в виде снижения остроты зрения вблизи, нечеткости, размытости рассматриваемых объектов, покраснения, слезотечения, периодической или постоянной диплопии на различных расстояниях [4–11].
Для уменьшения или купирования болевого синдрома в раннем послеоперационном периоде авторы предлагают применение, кроме антибактериальной терапии [17], также нестероидных противовоспалительных препаратов (НПВП) [18].
С другой стороны, медикаментозная терапия после кераторефракционных вмешательств может включать не только инстилляции антибактериальных препаратов и ГКС, но и применение слезозаместительных препаратов [19].
Таким образом, по данным разных авторов, до и после кераторефракционной операции требуется медикаментозная терапия, которая направлена на повышение эффективности и безопасности хирургического лечения. Однако возможности современного медикаментозного сопровождения при выполнении данного вида вмешательств, направленного на повышение качества жизни пациентов, исследованы недостаточно.
Для устранения болевого синдрома, повышения качества жизни пациентов в раннем послеоперационном периоде в настоящее время возможно применение комбинированной медикаментозной терапии: Сигницеф® Плюс (кеторолак 0,5% + левофлоксацин 0,5%) и Флоас Моно (0,1% раствор фторметалона). Выбор данных групп лекарственных средств для включения в схему подготовки и ведения пациентов после кераторефракционного вмешательства обусловлен наличием, во-первых, 0,5% раствора кеторолака, который относится к НПВП и обладает выраженным анальгезирующим эффектом. Механизм действия кеторолака связан с неселективным угнетением активности фермента циклооксигеназы 1 и 2, главным образом, в периферических тканях, следствием чего является торможение биосинтеза простагландинов — модуляторов болевой чувствительности, терморегуляции и воспаления. Левофлоксацин является синтетическим антибактериальным препаратом широкого спектра действия из группы фторхинолонов. Сигницеф® Плюс применяется в офтальмологии в качестве средства профилактики и лечения инфекционных осложнений, боли и воспаления в послеоперационном периоде после факоэмульсификации и рефракционных операций [17, 18]. Во-вторых, 0,1% раствора фторметалона (Флоас Моно) обладает выраженным противовоспалительным действием и, в отличие от 0,1% раствора дексаметазона, имеет наименьший риск возможного повышения офтальмотонуса при его применении в течение 3 нед. [20, 21].
Цель исследования: оценить эффективность и безопасность предоперационной подготовки и послеоперационного ведения пациентов кераторефракционного профиля с использованием различных схем медикаментозного сопровождения.
Содержание статьи
Материал и методы
Проспективное сравнительное одноцентровое исследование выполнено в Клинике Волгоградского филиала ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова». Обследованы 80 пациентов (80 глаз) со стабилизированной миопией слабой, средней и высокой степени.
Критерии включения: пациенты со стабилизированной миопией слабой, средней и высокой степени, нуждающиеся в выполнении кераторефракционной хирургии.
Критерии исключения: дистрофические заболевания роговицы, кератоконъюнктивиты, блефариты, отсутствие в анамнезе травм и хирургических операций на глазах, синдром «сухого глаза».
Все пациенты были разделены на 2 группы по 40 человек (40 глаз) в каждой. Основную группу составили 40 пациентов (40 глаз) до и после эксимерлазерной кераторефракционной операции, которым были назначены в виде инстилляций глазные капли за 1 сут до операции, утром в день операции и в послеоперационном периоде ежедневно: Сигницеф® Плюс (кеторолак 0,5% + левофлоксацин 0,5%) по 1 капле 4 р/сут в течение 5 дней и фторметолон 0,1% (Флоас Моно) по 1 капле 3 р/сут в течение 3 нед. Среди пациентов было 13 (32,5%) мужчин, 27 (67,5%) женщин; средний возраст составил 26,8±7,15 (М±σ) года, от 18 до 48 лет.
Контрольную группу составили 40 пациентов (40 глаз) до и после эксимерлазерного кераторефракционного вмешательства, которым была назначена стандартная схема медикаментозного сопровождения в виде инстилляций глазных капель за 1 сут до операции, утром в день операции и в послеоперационном периоде ежедневно: левофлоксацин 0,5% по 1 капле 4 р/сут в течение 5 дней и дексаметазон 0,1% по 1 капле 3 р/сут в течение 1-й недели, затем по 1 капле 2 р/сут в течение 2-й недели и по 1 капле в день в течение 3-й недели. Мужчин было 17 (42,5%), женщин — 23 (57,4%), средний возраст пациентов составил 26,4±7,9 (М±σ) года, от 18 до 40 лет.
Исследование соответствовало принципам Хельсинкской декларации, информированное добровольное согласие получено от всех обследуемых.
Всем пациентам проводилось комплексное офтальмологическое обследование до и через 1 нед. после кераторефракционного вмешательства: визометрия, рефрактометрия, тонометрия, комплексное обследование на фотощелевой лампе Dixon-S350, биомикроофтальмоскопия, оптическая когерентная томография (ОКТ) переднего сегмента глаза, офтальмоскопия, выполнение пробы Ширмера I. При проведении комплексного обследования на щелевой лампе Dixon-S350 определяли толщину слезной пленки, высоту слезного мениска и время разрыва слезной пленки.
С помощью офтальмологического оптического когерентного томографа SOLIX (США) проводили ОКТ переднего сегмента: оценивали количество и высоту палисад Фогта, толщину эпителия роговицы на ее периферии в нижнем квадранте.
У всех пациентов с целью коррекции миопии выполняли ФемтоЛАЗИК по стандартной технологии. Фемтосекундным лазером WaveLight FS 200 (Alcon) формировали роговичный клапан с заданными параметрами: диаметром 9,2 мм, толщиной 110 мкм, положение «ножки» 90°. По завершении формирования клапана автоматически снималась вакуумная фиксация глаза пациента. Подъем роговичного клапана выполняли с использованием шпателя. После этого с помощью эксимерлазерной установки WaveLight EX500 (Alcon), работающей по технологии «летающего пятна» с частотой повторения импульсов 750 Гц, выполняли абляцию стромы роговицы. Диаметр оптической зоны во всех случаях был 6,5–7,0 мм. Во время всех операций была активирована система слежения за движением глаза (eye-tracker system). Во всех случаях целевой рефракцией была эмметропия. Далее выполняли орошение стромального ложа роговицы сбалансированным солевым раствором (BSS) и проводили репозицию клапана. Эпителиально-стромальный лоскут роговицы разглаживали и высушивали на стромальном ложе роговицы стерильными микротупферами. По завершении операции проводили инстилляции в конъюнктивальную полость раствором левофлоксацина 0,5%.
У всех пациентов проводили оценку интенсивности болей по визуальной аналоговой шкале боли (ВАШ) во время операции и в послеоперационном периоде. Интенсивность боли пациент оценивал самостоятельно, ежедневно в течение 7 дней (включая день операции). Шкала представляет собой неградуированную линию длиной 10 см. Левая граница линии соответствует определению «боли нет», правая — «худшая боль, какую можно себе представить». Оценка интенсивности болевого синдрома проводится путем измерения расстояния (мм) между точкой «боли нет» и отметкой пациента в диапазоне от 0 до 100: нет боли — 0–4 мм, слабая боль — до 40% (от 5 до 44 мм), умеренная боль — 40–70% (45–74 мм), сильная боль — более 70% (75–100 мм), нестерпимая боль — 100% (100 мм).
Все полученные результаты обследования с обезличенными данными заносили в электронную базу данных. Результаты исследования обрабатывали в программах Microsoft Excel и Statistica 10.0. Тип распределения количественных данных оценивали с помощью критерия Шапиро — Уилка. Так как распределение данных было отличным от нормального, показатели представлены как медиана и квартили (Me [Q1; Q3]). Значимость различий между группами оценивали по критерию Манна — Уитни. При проведении статистического анализа определяли также показатель Z, который используется для аппроксимации нормального распределения, когда размер выборки достаточно большой (обычно более 30 наблюдений в каждой группе). Он рассчитывается на основе статистики Манна — Уитни и позволяет определить, является ли различие между двумя выборками статистически значимым, путем сравнения полученного значения с критическими значениями стандартного нормального распределения (например,±1,96 для уровня значимости 0,05). Сравнительный анализ внутри каждой группы до и после операции проводили по критерию Уилкоксона. Различие признавали статистически значимым при уровне значимости p<0,05.
Результаты исследования
Исходные показатели пациентов не выявили статистически значимых различий между двумя группами, что указывало на их однородность (табл. 1).
После кераторефракционной операции у всех пациентов отмечалось достоверное повышение НКОЗ и уменьшение субъективной рефракции по сравнению с исходными данными (см. табл. 1). В контрольной группе медиана НКОЗ увеличилась с 0,05 до 0,9 (Z=7,8; p<0,001), в основной группе — с 0,045 до 0,95 (Z=7,7; p<0,001). Значение субъективной рефракции в контрольной группе достоверно изменилось с -4,0 до 0,0 дптр (Z=7,4; p<0,001), в основной группе — с -3,87 до 0,0 дптр (Z=7,69; p<0,001).
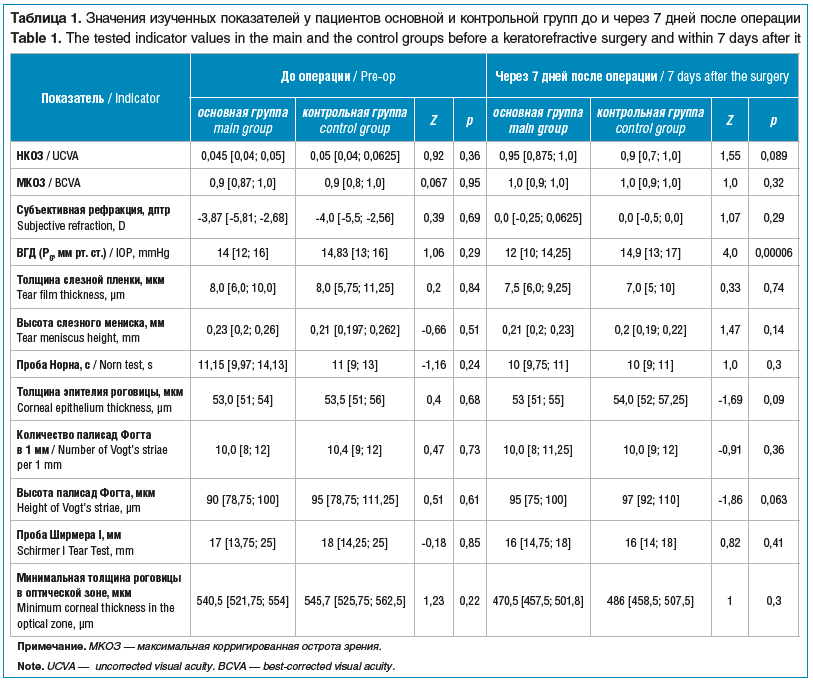
Сравнительный анализ показателей у пациентов основной и контрольной групп через 7 дней после кераторефракционной операции показал, что при применении двух схем послеоперационного медикаментозного лечения не было достоверных различий между группами по показателям НКОЗ, МКОЗ, субъективной рефракции и значениям минимальной толщины роговицы (см. табл. 1), что указывает на сопоставимый эффект повышения остроты зрения в двух группах (р>0,05).
Значения истинного ВГД (P0) через 7 дней после операции у пациентов двух групп находились в пределах среднестатистической нормы. Однако медиана Р0 у лиц контрольной группы была статистически значимо выше, чем у пациентов основной группы (р<0,001).
Значения толщины слезной пленки, высоты слезного мениска и времени разрыва слезной пленки через 7 дней после операции также соответствовали нормативным показателям и не различались между группами (p>0,05).
Значения пробы Ширмера I через 7 дней после операции статистически значимо не различались между группами (p=0,41). Однако при сравнении с исходными данными у пациентов контрольной группы отмечалось статистически значимое снижение слезопродукции c 18 [14,25; 25] до 16 [14; 18] мм (Z=2,17; p=0,029) через 7 дней после операции в отличие от основной группы (Z=1,43; p=0,15).
В таблице 2 представлен сравнительный анализ интенсивности боли в течение 7 дней, включая день операции.
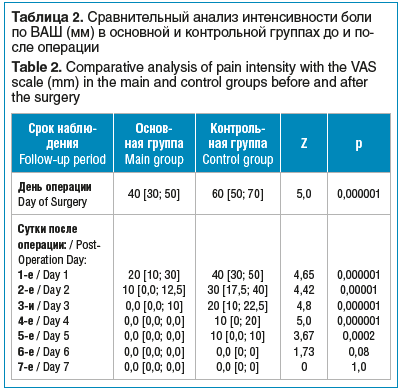
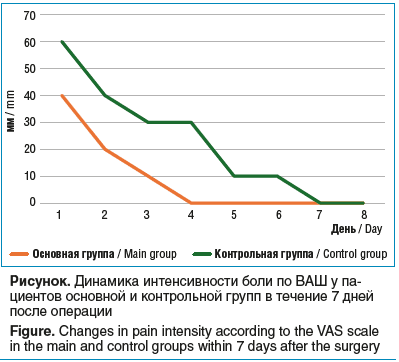
Сравнительный анализ интенсивности болей во время операции и в послеоперационном периоде по ВАШ показал преимущество предложенной медикаментозной схемы послеоперационного ведения. Интенсивность болей в день операции и в течение 5 дней в послеоперационном периоде была достоверно выше у пациентов контрольной группы (p<0,05). У пациентов основной группы в день операции интенсивность боли по ВАШ была достоверно ниже, чем в контрольной группе (р<0,001). Боль отсутствовала у пациентов основной группы уже на 3-й день после кераторефракционного вмешательства. У пациентов контрольной группы исчезновение боли было отмечено только на 6-й день после операции. Наиболее наглядно различия продемонстрированы на рисунке.
Через 1 мес. после операции уровень истинного ВГД статистически значимо повышался с 14,9 до 16 мм рт. ст. (Z=2,4; р=0,016) у пациентов контрольной группы. При этом разброс колебаний P0 соответствовал диапазону среднестатистической нормы: от 12 до 20 мм рт. ст.
У пациентов основной группы, наоборот, отмечалось снижение офтальмотонуса с 14 до 12 мм рт. ст. (Z=3,3; р=0,0009). При этом разброс колебаний P0 также соответствовал диапазону среднестатистической нормы — от 8 до 17 мм рт. ст.
Обсуждение
Таким образом, результаты сравнительного исследования по оценке эффективности и безопасности предоперационной подготовки и послеоперационного ведения пациентов кераторефракционного профиля с использованием различных схем медикаментозного лечения продемонстрировали преимущество предложенной схемы, включающей комбинированный препарат Сигницеф® Плюс (кеторолак 0,5% + левофлоксацин 0,5%) и глазные капли Флоас Моно (фторметолон 0,1%).
Сигницеф® Плюс и Флоас Моно оказывали более выраженное противовоспалительное действие, снижали интенсивность боли в день операции и устраняли боль на 3-и сутки после кераторефракционного вмешательства. Данные о более выраженном противовоспалительном действии указанных лекарственных препаратов согласуются с ранее опубликованными результатами исследований [5, 14, 18, 20, 21].
Учитывая сопоставимое повышение НКОЗ и отсутствие значимого различия между медианами минимальной толщины роговицы в послеоперационном периоде, можно предположить, что снижение слезопродукции у пациентов контрольной группы в послеоперационном периоде было связано с применением стандартной медикаментозной терапии и более значимой болевой реакцией на хирургическое лечение.
Препарат фторметолона 0,1% оказывал выраженный противовоспалительный эффект и при этом не приводил к достоверному повышению уровня ВГД через 1 мес. после операции в отличие от контрольной группы. Полученные результаты согласуются с ранее опубликованными данными [20, 21].
Оба препарата не снижали слезопродукцию в послеоперационном периоде и не вызывали нежелательных местных и системных побочных действий.
Таким образом, комбинированное терапевтическое действие препаратов Сигницеф® Плюс и Флоас Моно соответствует рекомендациям офтальмологической практики по использованию антибиотика, ГКС и НПВП после операций на роговице [22].
Заключение
Использованная медикаментозная схема, включающая препараты с выраженным противовоспалительным и обезболивающим действием, в раннем послеоперационном периоде обусловливает более гладкое течение послеоперационного периода, обеспечивая удовлетворенность пациентов результатом кераторефракционной операции, и может быть рекомендована как предпочтительная схема терапии, используемой в качестве предоперационной подготовки и послеоперационного ведения пациентов кераторефракционного профиля.
Сведения об авторах:
Солодкова Елена Геннадиевна — к.м.н., заместитель директора по научной работе Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0000-0002-7786-5665
Балалин Сергей Викторович — д.м.н., заведующий научным отделом Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0000-0002-5250-3692
Ушакова Лариса Ивановна — к.м.н., заведующая офтальмологическим отделением комплексных методов лечения Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0000-0002-5311-0006
Соколова Марина Владиславовна — врач-офтальмолог офтальмологического отделения комплексных методов лечения Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0000-0002-5739-6777
Мелихова Ирина Александровна — врач-офтальмолог диагностического отделения Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0000-0003-4557-4131
Текеева Асият Альбертовна — врач-офтальмолог офтальмологического отделения коррекции аномалий рефракции Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0009-0005-5305-1877
Бреев Владимир Алексеевич — заведующий офтальмологическим отделением коррекции аномалий рефракции Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0000-0002-3694-7066
Кузнецова Ольга Семеновна — к.м.н., врач-офтальмолог офтальмологического отделения коррекции аномалий рефракции Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0000-0001-8250-1471
Бочарова Анна Анатольевна — врач-офтальмолог офтальмологического отделения коррекции аномалий рефракции Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0009-0008-6658-1166
Сибакин Даниил Дмитриевич — врач-офтальмолог офтальмологического отделения коррекции аномалий рефракции Волгоградского филиала ФГАУ «НМИЦ «МНТК» «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; 400117, Россия, г. Волгоград, ул. Землячки, д. 80; ORCID iD 0000-0002-9880-6867
Контактная информация: Балалин Сергей Викторович, e-mail: s.v.balalin@gmail.com
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 28.08.2025.
Поступила после рецензирования 22.09.2025.
Принята в печать 15.10.2025.
About the authors:
Elena G. Solodkova — C. Sc. (Med.), Deputy Director for Scientific Work, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0002-7786-5665
Sergei V. Balalin — Dr. Sc. (Med.), Head of the Scientific Department, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0002-5250-3692
Larisa I. Ushakova — C. Sc. (Med.), Head of the Ophthalmological Department of Complex Treatment Methods, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal
State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0002-5311-0006
Marina V. Sokolova — Ophthalmologist, Ophthalmological Department of Complex Treatment Methods, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0002-5739-6777
Irina A. Melikhova — Ophthalmologist, Diagnostic Department, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0003-4557-4131
Asiyat A. Tekeeva — Ophthalmologist, Ophthalmological Department of Refractive Abnormality Management, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0009-0005-5305-1877
Vladimir A. Breev — Head of the Ophthalmological Department of Refractive Abnormality Management, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0002-3694-7066
Olga S. Kuznetsova — C. Sc. (Med.), Ophthalmologist, Ophthalmological Department of Refractive Abnormality Management, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0001-8250-1471
Anna A. Bocharova — Ophthalmologist, Ophthalmological Department of Refractive Abnormality Management, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0009-0008-6658-1166
Daniil D. Sibakin — Ophthalmologist, Ophthalmological Department of Refractive Abnormality Management, Volgograd Branch of the S. Fyodorov Eye Microsurgery Federal State Institution; 80, Zemlyachka str., Volgograd, 400138, Russian Federation; ORCID iD 0000-0002-9880-6867
Contact information: Sergey V. Balalin, e-mail: s.v.balalin@gmail.com
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 28.08.2025.
Revised 22.09.2025.
Accepted 15.10.2025.
[1] Клинические рекомендации. Миопия. 2024. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/preview-cr/109_2 (дата обращения: 06.09.2025).
материал rmj.ru
