Введение
За последние 10 лет отмечается рост выявляемости глаукомы на начальных стадиях. Так, в 2011 г., по данным Российского глаукомного общества, более чем в 60% случаев глаукома выявлялась на развитой и далеко зашедшей стадиях [1, 2], а в 2021 г., по данным тех же авторов, количество указанных стадий уменьшилось до 50% [3]. Считается, что в среднем на фоне проводимого лечения переход от одной стадии к другой занимает 4,0±3,2 года [4]. Так, при начальной стадии глаукомы переход на следующую стадию происходит через 3,1–4,5 года, при развитой стадии — через 2,9–4,3 года, а при далеко зашедшей — через 1,8–3,5 года [5–10].
Выявление глаукомы на развитой и далеко зашедшей стадиях и быстрое прогрессирование глаукомного процесса часто требуют раннего назначения комбинированной терапии, уже на старте наблюдения [6], однако стабилизация глаукомного процесса не всегда зависит от выбранной тактики лечения, а зачастую обусловлена самой стадией заболевания, что, в свою очередь, предопределяет выбор агрессивной терапии и ранний переход к максимальной медикаментозной терапии.
Максимальная медикаментозная терапия (MMT) — это терапия, подразумевающая использование трех и более классов местных гипотензивных агентов, что позволяет достичь максимального снижения ВГД при минимизации побочных эффектов и проблем, с соблюдением рекомендаций врача [11, 12]. Несмотря на то, что при отсутствии компенсации ВГД на 2-3-х препаратах рекомендуется рассмотреть вопрос о лазерном или хирургическом лечении, усиление ММТ 4-м препаратом является актуальным для ряда пациентов, которым проведение хирургического лечения невозможно по различным причинам (местные или общие противопоказания, эпидемиологическая обстановка в регионе и т. д.).
В качестве дополнительного гипотензивного агента зачастую используется бримонидин 0,2%. Это селективный α2-адреномиметик, который снижает ВГД за счет уменьшения продукции водянистой влаги и увеличения увеосклерального оттока [13]. По гипотензивной эффективности бримонидин 0,2% сопоставим с тимололом 0,5% [14]. К тому же в исследованиях на лабораторных животных было выявлено, что бримонидин обладает также нейропротективным действием [15].
Так как работ по исследованию эффективности добавления бримонидина в качестве 4-го препарата к ММТ практически нет [16], целью нашего исследования стала оценка аддитивного эффекта снижения ВГД бримонидином 0,2% для достижения давления цели при усилении максимального режима гипотензивной терапии первичной открытоугольной глаукомы (ПОУГ).
Материал и методы
В период с августа 2018 г. по май 2021 г. были обследованы 63 пациента (63 глаза), средний возраст которых составлял 73,0 (64,5; 77,5) года, с развитой стадией ПОУГ. Исследование было проспективным открытым сравнительным в двух параллельных группах.
Критерии включения: развитая стадия ПОУГ; выявленная субкомпенсация ВГД на фоне гипотензивной терапии аналогами простагландинов вместе с фиксированной комбинацией ингибитора карбоангидразы и бета-блокатора; возраст на момент включения в исследование — от 45 до 89 лет; регион проживания — г. Челябинск; клиническая рефракция в диапазоне ±3,0 дптр и астигматизм ±1,5 дптр; толщина роговицы в центральной зоне не учитывалась.
Критерии исключения: любая иная форма глаукомы; помутнение оптических сред, препятствующее выполнению периметрических исследований с помощью стандартной автоматической периметрии; другие заболевания сетчатки (возрастная макулодистрофия, состояния после окклюзий сосудов сетчатки, диабетическая ретинопатия и ее осложнения; наличие в анамнезе осложнений оперативного лечения офтальмопатологии; травмы и заболевания органа зрения и его придаточного аппарата; другие общие заболевания, требующие гормональной терапии.
Все пациенты проходили офтальмологическое обследование, включающее визорефрактометрию, биомикроофтальмоскопию, гониоскопию, тонометрию с помощью портативного офтальмологического тонометра iCare (Icare Finland Оу, Финляндия), эластотонометрию, статическую автоматическую компьютерную периметрию (Octopus 600, Haag-Streit International, Koeniz, Switzerland), оптическую когерентную томографию и пахиметрию на приборе Revo NX (Optopol Technology SA, Zawiercie, Poland).
На момент включения в исследование (визит 1) к имеющемуся режиму ММТ у всех пациентов добавлялся препарат группы α2-адреномиметиков — бримонидин 0,2%. Через 1 мес. пациенты приглашались повторно (визит 2), где после офтальмологического обследования по вышеуказанному плану оценивалась компенсация ВГД. В зависимости от степени снижения ВГД исследуемых делили на 2 группы: в 1-ю группу были включены пациенты, у которых удалось достичь целевого уровня ВГД; во 2-ю группу вошли пациенты с сохраняющейся субкомпенсацией, которым затем была выполнена синустрабекулэктомия (СТЭ). В сроки не ранее чем через 2 мес. от визита 2 пациентам назначалось заключительное обследование (визит 3).
Статистическую обработку полученных данных проводили с использованием программного обеспечения R Core Team (2016). R: A language and environment for statistical computing (Vienna, Austria). Приводимые параметры (нормальность распределения проверяли с помощью теста Шапиро — Уилка, гомогенность дисперсии — с помощью теста Бартлетта) представлены в формате Me (Q25%; Q75%), где Мe — медиана, Q25% и Q75% — квартили. При сравнении нескольких выборок использовали критерий Уилкоксона. Критический уровень значимости при проверке статистических гипотез принимали равным меньше 0,05.
Результаты и обсуждение
Клинико-демографическая характеристика пациентов, включенных в исследование, представлена в таблице 1.
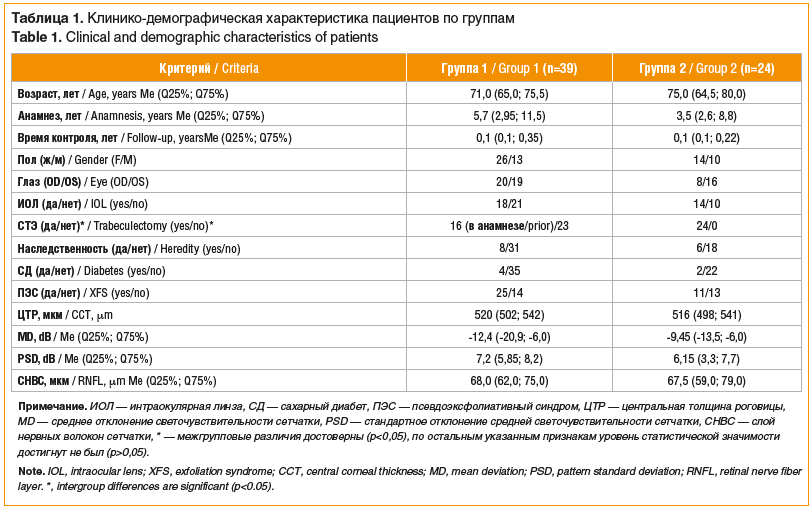
Общая продолжительность наблюдения за пациентами составила 0,2 (0,1; 0,65) года. Напряженная эпидемиологическая обстановка в регионе не позволила провести заключительный визит в фиксированные сроки, в связи с чем длительность наблюдения пациентов варьировала: в 1-й группе она составила 0,1 (0,1; 0,5) года, во 2-й — 0,4 (0,17; 0,7) года (р>0,05).
После разделения пациентов на группы стало возможным оценить ретроспективно средний по обеим группам уровень ВГД на визите 1: у пациентов группы оперативного лечения уровень офтальмотонуса оказался значимо выше, чем в группе консервативного лечения, но только по данным тонометра iCare (табл. 2).
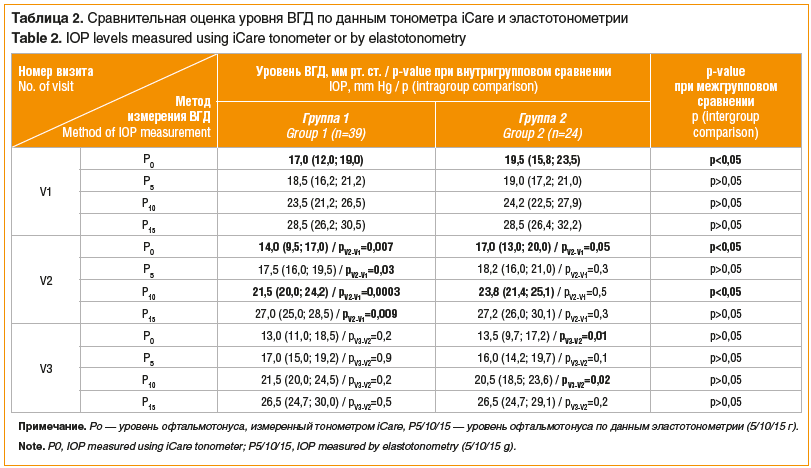
Через 1 мес. после усиления гипотензивного режима бримонидином 0,2% в обеих группах наблюдалось статистически значимое снижение офтальмотонуса: по данным всех тонометров в группе консервативного лечения и только по данным тонометра iCare в группе оперативного лечения (см. табл. 2).
На заключительном обследовании у пациентов 1-й группы отмечалось сохранение достигнутого уровня истинного ВГД в пределах целевых значений, значимых различий с показателями ВГД, полученными на визите 2, выявлено не было. У пациентов же 2-й группы отмечалось статистически значимое снижение ВГД в сравнении с показателями на визите 2 по данным тонометров iCare и Маклакова 10 г (см. табл. 2).
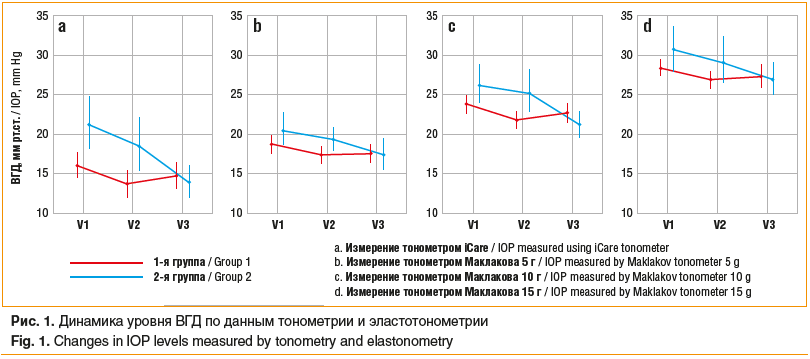
Сравнительный анализ показателей офтальмотонуса в течение всего периода наблюдения наглядно отражает схожую динамику по данным использованных методов измерения ВГД (рис. 1). В обеих группах был достигнут целевой уровень ВГД с сопоставимыми показателями. Однако были выявлены значимые межгрупповые различия в итоговом проценте снижения офтальмотонуса: в 1-й группе снижение ВГД по усредненным для всех тонометров данным составило 5,4% (-7,1%; 17,6%), а во 2-й — 20,7% (4,4%; 30,7%) (p<0,05). Различия по данным только тонометра iCare были наиболее выраженными и составили 8,3% (-11,8%; 28,6%) для группы консервативного лечения и 33,3% (13,9%; 50,7%) для группы оперативного лечения. В группе 1 через 1 мес. применения бримонидина среднее P0 снизилось с 16,1±5,0 до 13,8±5,7 мм рт. ст., т. е. на 14,3%, что является хорошим результатом для 4-го гипотензивного препарата.
На сегодняшний день проведен целый ряд исследований, посвященных оценке гипотензивной эффективности бримонидина 0,2%. Так, эффективность монотерапии бримонидином 0,2% для снижения ВГД, по данным метаанализа 24-часового контроля уровня офтальмотонуса, проведенного Stewart et al. еще в 2007 г., составляет 14% [17]. В свою очередь, по данным Zimmerman et al., которые упоминаются в публикации, посвященной ММТ, гипотензивная эффективность латанопроста при его добавлении для усиления ММТ в качестве четвертого гипотензивного агента не превышает 1–2 мм рт. ст. [11]. При этом в исследовании Schwartzenberg и Buys при назначении бримонидина 0,2% пациентам с максимальным режимом гипотензивной терапии офтальмотонус снижался в среднем на 20%, около 50% пациентов продолжали терапию через 9 мес. при хорошей переносимости препарата [16]. В нашем же исследовании у пациентов с субкомпенсированным офтальмотонусом на ММТ дополнительное назначение бримонидина 0,2% дало снижение уровня истинного ВГД на 8,3%. Вероятным объяснением такой разной гипотензивной эффективности максимального медикаментозного режима гипотензивной терапии в нашем исследовании и по данным Schwartzenberg и Buys является характер отбора пациентов.
Разница между показателями офтальмотонуса, полученными разными методами тонометрии, обусловлена особенностями взаимодействия тонометров с биомеханическими свойствами фиброзной оболочки глаза. Это объясняет полученную в процессе измерения разницу в проценте снижения офтальмотонуса по данным тонометра iCare и эластотонометрии [16]. В нашем исследовании средние значения ВГД, измеренного тонометром Маклакова (10 г), были не менее 20,5 (18,5; 23,6) мм рт. ст., а при измерении ВГД тонометром iCare среднее значение составило 13,0 (11,0; 18,5). Меньшая разница в динамике офтальмотонуса в послеоперационном периоде по данным эластотонометрии, вероятнее всего, обусловлена ограничением метода тонометрии по Маклакову, которое выражается в том, что идентифицировать офтальмотонус меньше 20 мм рт. ст. таким методом у большого числа пациентов невозможно (это можно увидеть на примере многоцентровых исследований). Так, по данным многочисленных исследований группы «Научный авангард», в клинической практике крайне редко фиксируются значения среднего уровня офтальмотонуса по данным тонометрии по Маклакову (10 г) менее 20 мм рт. ст. [7–10, 18–34].
Заключение
Проведенное исследование демонстрирует аддитивный эффект бримонидина 0,2% при усилении максимального режима гипотензивной терапии развитой стадии ПОУГ. При достижении целевого уровня ВГД в раннем периоде аддитивной терапии отмечается стойкое сохранение достигнутого результата. Если аддитивный эффект бримонидина 0,2% недостаточен, проведение дополнительно антиглаукомной операции позволяет снизить офтальмотонус до целевого уровня. При этом получаемые показатели ВГД сопоставимы в обоих случаях (р>0,05).
Таким образом, при добавлении к ММТ 4-го гипотензивного препарата — бримонидина 0,2% необходимо учитывать предполагаемый гипотензивный эффект — дополнительное снижение истинного ВГД в среднем на 8%, и, если это снижение не позволяет достичь целевого уровня, планировать оперативное вмешательство. При терапии субкомпенсированного ВГД у пациентов на ММТ предпочтительнее проводить измерение тонометром iCare как более чувствительным к небольшим перепадам офтальмотонуса.
Сведения об авторах:
1Дорофеев Дмитрий Александрович — врач-офтальмолог; ORCID iD 0000-0003-3352-8170.
2Балухтина Виолетта Петровна — студентка; ORCID iD 0000-0001-7986-9726.
1Еськова Марина Владиславовна — оператор ОКТ; ORCID iD 0000-0001-8321-276X.
1Ефимова Ксения Алексеевна — оператор ОКТ, ORCID iD 0000-0001-6492-7743.
1Кирилик Елена Викторовна — врач-офтальмолог; ORCID iD 0000-0002-0189-9586.
1Лукьянова Ксения Олеговна — врач-офтальмолог; ORCID iD 0000-0002-6781-3343.
1МАУЗ «ГКБ № 2». 454090, Россия, г. Челябинск, ул. Российская, д. 200.
2ФГБОУ ВО ЮУГМУ. 454092, Россия, г. Челябинск, ул. Воровского, д. 64.
Контактная информация: Дорофеев Дмитрий Александрович, e-mail: dimmm.83@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 15.06.2021.
About the authors:
1Dmitry A. Dorofeev — ophthalmologist; ORCID iD 0000-0003-3352-8170.
2Violetta P. Balukhtina — student; ORCID iD 0000-0001-7986-9726.
1Marina V. Es’kova — OCT operator; ORCID iD 0000-0001-8321-276X.
1Kseniya A. Efimova — OCT operator; ORCID iD 0000-0001-6492-7743.
1Elena V. Kirilik — ophthalmologist; ORCID iD 0000-0002-0189-9586.
1Kseniya O. Luk’yanova — ophthalmologist; ORCID iD 0000-0002-6781-3343.
1City Clinical Hospital No. 2, Polyclinic № 1; 200, Rossiiskaya St., Chelyabinsk, 454090, Russian Federation.
2South Ural State Medical University; 64, Vorovskiy str., Chelyabinsk, 454092, Russian Federation.
Contact information: Dmitry A. Dorofeev, e-mail: dimmm.83@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 15.06.2021.
.
материал rmj.ru
