Содержание статьи
Исследование эффективности, переносимости и безопасности
гиалуроновой кислоты у пациентов с остеоартрозом коленных суставов
С. Г. Аникин, кандидат медицинских наук
Л. И. Алексеева, доктор медицинских наук
Е. М. Зайцева, кандидат медицинских наук
Н. Г. Кашеварова
Т. А. Короткова, кандидат медицинских наук
Е. П. Шарапова, кандидат медицинских наук
ФГБНУ НИИР им В. А. Насоновой, Москва
Остеоартроз (ОА) представляет собой заболевание суставов, которое
характеризуется клеточным стрессом и деградацией экстрацеллюлярного матрикса,
возникающих при макро- и микроповреждениях, которые активируют ненормальные
адаптивные процессы восстановления, включая провоспалительные реакции иммунной
системы, костного ремоделирования и образования остеофитов [1]. ОА является
одним из самых распространенных заболеваний костно-мышечной системы. В целом
частота ОА коленных суставов у лиц в возрасте 55 лет и старше достигает 10%, из
них в 25% случаев ОА протекает с частыми обострениями и выраженной клинической
симптоматикой [2]. Основными проявлениями ОА являются боль, преимущественно
механического, стартового характера, непродолжительная скованность до 30 минут и
нарушение функции сустава. Клиническая картина может сопровождаться крепитацией
при активных движениях, умеренным выпотом и костными разрастаниями. В терапии ОА
применяется комплексный подход с использованием как медикаментозных, так и не
медикаментозных методов лечения: физиотерапия, лечебная физкультура и другие
методы реабилитации. При упорном течении заболевания, сопровождающемся
выраженной болевой симптоматикой, тяжелыми функциональными нарушениями и
значительным снижением качества жизни, применяются хирургические методы лечения.
ОА является хроническим заболеванием, требующим длительной терапии. Большинство
пациентов, страдающих первичным ОА, — это лица старших возрастных групп, как
правило, имеющих целый ряд сопутствующих заболеваний. В последних рекомендациях
от 2014 г. по нехирургическому лечению ОА коленных суставов Международной
организации по изучению остеоартроза (Osteoarthritis Research Society
International, OARSI) проблеме коморбидности уделяется особое внимание [3].
Экспертный совет этой организации оценил разные методы не только исходя из их
эффективности, но и с позиции степени риска развития нежелательных явлений. На
основании решения экспертного совета были сделаны выводы об обоснованности
применения того или иного терапевтического подхода. Для купирования боли при ОА
применяют нестероидные противовоспалительные препараты (НПВП) и внутрисуставное
введение глюкокортикоидов. Эти методы лечения позволяют существенно уменьшать
боль и улучшать функциональные показатели. Однако их применение может
ограничиваться сопутствующими заболеваниями желудочно-кишечного тракта,
сердечно-сосудистой системы, почек, печени, эндокринной системы и целым рядом
других заболеваний. При терапии НПВП и глюкокортикоидами для внутрисуставного
введения, необходимо учитывать возможные нарушения функции внутренних органов,
при этом продолжительность такой терапии должна быть короткой с использованием
минимальных эффективных доз препаратов [3, 4]. Другая группа лекарственных
средств, широко применяемая для лечения ОА, — это препараты с медленным
развитием симптоматического эффекта (ПМРЭ). До настоящего времени сохраняются
споры об их роли и месте в терапии ОА. Это связано с большой неоднородностью
полученных данных в различных клинических исследованиях. В целом можно отметить,
что ПМРЭ обладают умеренным симптоматическим эффектом и хорошей переносимостью.
Практически во всех исследованиях отмечалась очень низкая частота нежелательных
лекарственных реакций, которые, как правило, не имели существенного клинического
значения. Эти особенности ПМРЭ позволяют их широко применять у пациентов с
высокой степенью коморбидности и в разных возрастных группах.
Гиалуроновая кислота (ГНК) является типичным представителем ПМРЭ и широко
применяется в комплексном лечении ОА. ГНК оказывает симптоматический эффект,
уменьшая боль, скованность и улучшая функциональные показатели пораженного
сустава. В некоторых исследованиях имеются указания на структурно-модифицирующий
эффект ГНК [5]. Согласно последним рекомендациям OARSI от 2014 г. препараты ГНК
применяются для терапии пациентов с ОА коленных суставов по решению лечащего
врача в зависимости от конкретной клинической ситуации [3].
Целью исследования было оценить эффективность, переносимость и безопасность
внутрисуставного введения ГНК (Синокром) у пациентов с первичным ОА коленных
суставов.
Материалы и методы исследования
В годовое проспективное когортное исследование были включены 30 человек с
диагнозом первичного ОА коленных суставов, из них 93% составляли женщины и 7% —
мужчины. Диагностика ОА проводилась с использованием классификационных критериев
Американской коллегии ревматологов (American College of Rheumatology, ACR) 1986
г. [4].
Критерии включения: мужчины и женщины в возрасте 45–70 лет, подтвержденный,
согласно критериям Американской коллегии ревматологов, диагноз первичного
тибиофеморального ОА, выраженность боли при ходьбе не менее 40 мм по визуальной
аналоговой шкале (ВАШ), вторая или третья рентгенологические стадии по Kellgren–Lawrence,
потребность в приеме НПВП длительностью не менее 30 дней за предшествующие 3
месяца и подписанное информированное согласие.
Критерии исключения: лица с диагнозом вторичного гонартроза, пациенты,
которым проводилась терапия другими симптоматическими средствами и препаратами с
медленным развитием эффекта за последние 6 месяцев, внутрисуставное введение
иных препаратов за последние 6 недель до включения в исследование, случаи:
хондрокальциноза, асептического некроза мыщелков бедренных и большеберцовых
костей, оперативного вмешательства на коленном суставе, а также пациентов,
имеющих в анамнезе указание на повышенную чувствительность к ГНК и тяжелые
сопутствующие заболевания, включая системные ревматические заболевания.
Разрешалось использование НПВП, которые пациенты принимали на момент
включения в исследование. Не допускалось проведение других внутрисуставных
инъекций, включая глюкокортикоиды и иные препараты ГНК, и физиотерапевтических
процедур.
Клиническая характеристика больных
В исследовании приняли участие лица в возрасте от 48 до 74 лет, 28 (93%)
женщин и 2 (7%) мужчин в возрасте 62 лет (± 6,9 года), рост — 1,62 (± 0,06)
метра, вес — 80,9 (± 10,8) кг, индекс массы тела (ИМТ) — 31 (± 4,3) кг/м2,
медиана длительности заболевания — 8 лет (25-й, 75-й процентили — 6 и 10 лет),
длительности обострения — 3,5 месяца (± 2,1).
Наиболее выраженная симптоматика на момент включения в исследование несколько
чаще отмечалась в правом коленном суставе — 53%, по сравнению с левым — 47%.
Большинство участников исследования (70%) было с ОА второй рентгенологической
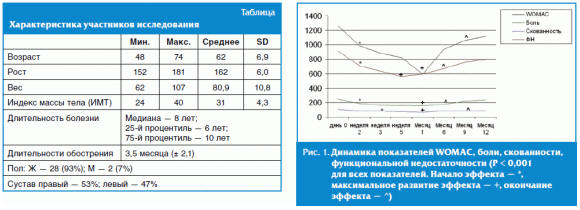
стадии и 30% с ОА третьей стадии. Характеристика участников исследования
представлена в таблице.
Показатели эффективности. В качестве показателей эффективности
использовалась динамика индекса WOMAC и отдельных его параметров: суммарный
показатель боли (при ходьбе по ровной поверхности, при спуске/подъеме по
лестнице, в ночное время, в положении сидя/лежа, в положении стоя), скованности
и функциональной недостаточности. Оценивалась потребность в НПВП на протяжении
исследования и общая оценка эффекта пациентом в конце исследования.
Показатели безопасности. Изучалась частота и характер нежелательных
лекарственных реакций (НЛР) и их связь с исследуемой терапией.
Терапия. Всем пациентам проводилось внутрисуставное введение ГНК
один раз в неделю, всего было выполнено 5 инъекций. В случае необходимости
пациенты принимали НПВП, назначенный ранее, до включения в программу. При этом
замена одного НПВП на другой на протяжении исследования не допускалась.
Статистическая обработка данных проводилась с помощью программы SPSS 16.0.
Результаты представлены в виде среднего значения и стандартного отклонения или
указывалась медиана и 25-й и 75-й процентили. Нормальность распределения
оценивалась с помощью теста Колмогорова–Смирнова.
Результаты исследования
Все 30 больных полностью завершили исследование, комплаентность составила
100%.
Терапия Синокромом была эффективна у большинства включенных больных. Было
выявлено улучшение показателей WOMAC в целом, боли, скованности и функциональной
недостаточности (ФИ). Динамика показателей представлена на рис. 1.
Отмечалось статистически значимое уменьшение общего индекса WOMAC спустя
неделю после первой инъекции. Клинически значимое уменьшение, рассматриваемое
как снижение показателя на 20% и более, наблюдалось через 2 недели от начала
терапии. Общий индекс WOMAC при этом уменьшился на 277 мм — 22% (95% ДИ 154 мм,
401 мм, р < 0,001). Этот эффект сохранялся до 6 месяцев, снижение на 434 мм —
27% (95% ДИ 262 мм, 606 мм, р < 0,001). Максимальное снижение общего индекса
WOMAC было выявлено через месяц после окончания курса внутрисуставных инъекций
или через 8 недель после начала лечения, снижение на 460 мм — 36% (95% ДИ 297
мм, 622 мм, р < 0,001).
На фоне терапии Синокромом было выявлено статистически значимое уменьшение
боли в анализируемом суставе также спустя неделю после первой инъекции. Этот
показатель достигал клинической значимости начиная со 2-й недели курсового
лечения. Отмечалось снижение боли на 59 мм — 24% (95% ДИ 32 мм, 87 мм, р <
0,001), которое сохранялось до 6 месяцев после прекращения терапии — 71 мм, 20%
(95% ДИ 44 мм, 99 мм, р < 0,001). Максимальное уменьшение боли наблюдалось
спустя 1 месяц после последней, пятой инъекции — снижение боли на 91 мм, 37%
(95% ДИ 58 мм, 124 мм, р < 0,001).
Скованность в оцениваемом коленном суставе статистически значимо уменьшалась
спустя неделю после первой инъекции и становилась клинически значимой на 3-й
неделе терапии — снижение на 24 мм, 23% (95% ДИ 10 мм, 38 мм, р = 0,002), этот
эффект сохранялся до девятого месяца после прекращения лечения — снижения
показателя скованности на 23 мм, 21% (95% ДИ 14 мм, 31 мм, р < 0,001).
Максимально выраженное уменьшение скованности было выявлено спустя 1 месяц после
курса инъекций — 40 мм, 37% (95% ДИ 27 мм, 53 мм, р < 0,001).
Статистически значимое уменьшение значений показателя функциональной
недостаточности (ФН) тоже выявлялось после первой инъекции и достигало
клинически значимого уровня на 2-й неделе — снижение на 200 мм, 22% (95% ДИ 114
мм, 286 мм, р < 0,001). Эффект сохранялся до 6 месяцев — снижение на 255 мм, 28%
(95% ДИ 160 мм, 350 мм, р < 0,001). Максимальный эффект наблюдался спустя 5
недель после начала терапии (неделя после окончания курса), достигавший 354 мм,
39% (95% ДИ 216 мм, 491 мм, р < 0,001).
Полностью прекратили прием НПВП 10% пациентов, уменьшили дозу препарата в два
раза или стали принимать НПВП не чаще одного раза в три дня — 40%. Сохранялась
потребность в приеме НПВП у 50% лиц. Из них 30%, тем не менее, отмечали
улучшение состояния, хотя дозу препарата не меняли.
Анализ оценки эффективности проводился у всех пациентов, принимавших участие
в исследовании. Наступление эффекта пациентами в большинстве случаев отмечалось
на 23-й день, наиболее раннее наступление эффекта у 25% лиц было на 20-й день, а
наиболее позднее наступление эффекта у 25% лиц было на 34-й день от начала
терапии.
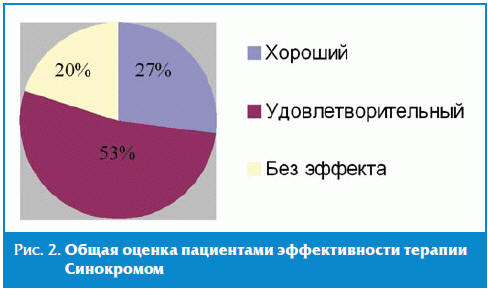
Хороший эффект Синокрома отметили 27% пациентов, удовлетворительный — 53% и
20% больных отметили отсутствие эффекта (рис. 2).
НЛР, связанных с проводимой терапией, не выявлено.
Обсуждение
ГНК относится к группе препаратов замедленного действия для симптоматической
терапии ОА. ГНК облает большим спектром биологической активности, оказывая
влияние на самые разные ключевые моменты патогенеза ОА. В литературе имеется
большое число работ, включая крупные метаанализы, в которых оценивался
симптоматический эффект ГНК. В некоторых из них был выявлен клинически значимый
эффект ГНК [6–10]. R. R. Bannuru и соавт. [10] провели метаанализ 54
плацебо-контролируемых рандомизированных клинических исследований (РКИ), в
которых принимало участие 7545 больных ОА. При оценке динамики симптоматического
эффекта его максимальное значение отмечалось на 8-й неделе терапии и достигало
коэффициента — 0,46 (95% ДИ 0,28, 0,65). Согласно общепринятому подходу, уровень
эффекта 0,2 соответствует небольшому размеру эффекта, 0,5 — среднему, а 0,8 и
выше говорит о выраженном эффекте. V. Strand и соавт. [9] выполнили
интегрированный анализ пяти двойных слепых РКИ эффективности внутрисуставного
введения ГНК в коленные суставы. В общей сложности в них было включено 1155
больных ОА. Длительность наблюдения составила более трех месяцев. Имея доступ к
индивидуальным картам больных, авторам удалось существенно снизить
гетерогенность данных и провести максимально полный анализ полученных
результатов. Интегрированный анализ в основной группе выявил значительно более
выраженное снижение индекса Лекена, чем в группе плацебо (соответственно на 2,68
и на 2,0, p < 0,001), при этом размер эффекта ГНК достигал 0,2. В других работах
результаты были более скромными. G. H. Lo и соавт. [6] при анализе 22 РКИ
выявили силу эффекта влияния ГНК на боль, достигавшую 0,32, но при исключении
выступающих крайних значений она снижалась до небольшого уровня — 0,19 (95% ДИ
0,10–0,27). В некоторых работах авторы не выявили значимого смптоматического
эффекта. Так, в метаанализе, проведенном J. Arrich и соавт. [11], отмечалось
лишь незначительное снижение боли в исследуемом суставе, в том числе и во время
ходьбы: –3,8 мм (95% ДИ –9,1 до 1,4 мм) после 2–6 недели, 4,3 мм (95% ДИ –7,6 до
–0,9 мм) после 10–14 и 7,1 мм (95% ДИ –11,8 до –2,4 мм) после 22–30 недели
наблюдения. В нашем исследовании мы выявили клинически значимый симптоматический
эффект при введении ГНК в коленные суставы, который развивался спустя 2 недели
после начала терапии, при этом 80% пациентов отметили эффект от внутрисуставного
введения Синокрома как хороший или удовлетворительный. Максимальное снижение
боли достигало 37%, скованности — 37%, ФН — 39% и общего индекса WOMAC — 36%.
Динамика изменения симптоматики после проведения курса терапии ГНК изучалась
в целом ряде работ. Так, A. Modawal и соавт. [8] провели метаанализ 12 двойных
слепых плацебо-контролируемых РКИ, в которых оценивалась динамика боли по
визуальной аналоговой шкале (ВАШ). Клинически значимые изменения были отмечены
на 5–7 неделе — 17,7 мм (7,5–28) и сохранялись до 8–12 недели — 18,1 мм
(6,3–29,9). Как и в большинстве других метаанализов, авторами была отмечена
высокая гетерогенность групп больных, включенных в исследования. В метаанализе,
цитируемом выше, R. R. Bannuru и соавт. [10] оценивали динамику боли на
протяжении 6 месяцев после введении ГНК в коленные суставы. Согласно полученным
данным, размер эффекта к 4-й неделе составил 0,31 (95% ДИ 0,17, 0,45), достигая
максимального значения на 8-й — 0,46; (95% ДИ 0,28, 0,65) и с последующим
снижением до 0,21 (95% ДИ 0,10, 0,31) к 24-й неделе. В нашем исследовании мы
использовали как отдельные суммированные показатели боли, скованности, ФН, так и
общее значение WOMAC.
Мы выявили развитие клинически значимого эффекта для большинства показателей,
начиная со второй недели терапии: снижение значений на 22%, 24%, 22% для
суммарного WOMAC, боли и ФН соответственно и с третьей недели для скованности —
23%. При этом длительность эффекта сохранялась до 6 месяцев для общего значения
WOMAC, боли и ФН (уменьшение на 27%, 29% и 28% соответственно (р < 0,001)), а
для скованности — на протяжении 9 месяцев (уменьшение на 21% (р < 0,001)). И
хотя мы не можем напрямую сравнивать наши результаты с приведенными выше
исследованиями из-за использования разных систем оценки эффективности терапии,
тем не менее прослеживается четкая динамика клинического эффекта при
внутрисуставном введении ГНК: развитие симптоматического эффекта спустя 2–4
недели и его сохранение до 6–9 месяцев.
В целом применение препаратов ГНК считается относительно безопасным, и
серьезные НЛР возникают редко. В нашем годовом исследовании мы не выявили НЛР,
связанных с внутрисуставным введением ГНК. Согласно последним рекомендациям
OARSI 2014 г. [3], ГНК может применяться у пациентов с ОА коленных суставов, при
этом решение о таком лечении принимается лечащим врачом совместно с больным.
В настоящее время имеются убедительные данные об умеренно выраженном
симптоматическом эффекте ГНК у пациентов с ОА. Он развивается не сразу, а
начинает проявляться со 2–4 недели после внутрисуставного введения и может
сохраняться до полугода, а у некоторых пациентов и дольше. По данным ряда
исследований применение ГНК сопровождается небольшим числом НЛР, среди которых
основное значение имеет небольшая постинъекционная реакция в виде болезненности
в месте введения препарата. В нашем исследовании НЛР не отмечено.
Таким образом, внутрисуставное введение Синокрома:
- уменьшает боль в суставах;
- уменьшает скованность;
- улучшает функцию суставов;
- снижает суточную потребность НПВП;
- обладает высокой безопасностью;
- эффективность терапии сохраняется в течение 6 месяцев.
Литература
-
Lane N. E., Brandt K., Hawker G. и соавт. OARSI-FDA initiative:
defining the disease state of Osteoarthritis // Osteoarthritis Cartilage.
2011; 19 (5): 478–482. -
Peat G., McCarney R., Croft P. Knee pain and osteoarthritis in
older adults: a review of community burden and current use of primary health
care // Ann Rheum Dis. 2001; 60 (2): 91–97. -
McAlindony Т. E., Bannuruy R. R., Sullivany M. C. и соавт. OARSI
guidelines for the non-surgical management of knee Osteoarthritis //
Osteoarthritis and Cartilage. 2014, 22: 363–388. - Клинические рекомендации. Ревматология. Под ред. акад. РАМН Е. Л.
Насонова. М.: Гоэтар-Медиа. 2010. С. 326. -
Аникин С. Г., Алексеева Л. И. Применение препаратов гиалуроновой
кислоты при остеоартрозе коленных суставов // Научно-практическая
ревматология. 2013, 4: 439–445. -
Lo G. H., LaValley M., McAlindon T., Felson D. T. Intra-articular
hyaluronic acid in treatment of knee osteoarthritis: a meta-analysis // JAMA.
2003; 290 (23): 3115–3121. -
Wang C. T., Lin J., Chang C. J. и соавт. Therapeutic effects of
hyaluronic acid on osteoarthritis of the knee. A meta-analysis of randomized
controlled trials // J Bone Joint Surg Am. 2004; 86 (3): 538–545. -
Modawal A., Ferrer M., Choi H. K., Castle J. A. Hyaluronic acid
injections relieve knee pain // J Fam Pract. 2005; 54: 758–767. -
Strand V., Conaghan P. G., Lohmander L. S. и соавт. An integrated
analysis of five double-blind, randomized controlled trials evaluating the
safety and efficacy of a hyaluronan product for intraarticular injection in
osteoarthritis of the knee // Osteoarthritis Cartilage. 2006; 14 (9): 859–866. -
Bannuru R. R., Natov N. S., Dasi U. R. и соавт. Therapeutic
trajectory following intra-articular hyaluronic acid injection in knee
osteoarthritis — meta-analysis // Osteoarthritis Cartilage. 2011; 19 (6):
611–619. -
Arrich J., Piribauer F., Mad P. и соавт. Intra-articular
hyaluronic acid for the treatment of osteoarthritis of the knee: systematic
review and meta-analysis // CMAJ. 2005; 172 (8): 1039–1043.
Статья опубликована в журнале
Лечащий Врач
материал MedLinks.ru






