Содержание статьи
Введение
Синдром Дауна — одна из наиболее распространенных хромосомных аномалий, возникающая в результате мутации 21-й пары хромосом с формированием ее дополнительной копии в геноме человека. Впервые данный синдром был описан Д. Дауном в 1866 г. 21-я хромосома — самая маленькая хромосома человека, которая содержит 200–300 генов (127 известных генов, 98 предсказанных и 59 псевдогенов) [1]. Пациенты с синдромом Дауна имеют большее количество копий генов 21-й хромосомы. Сами по себе гены нормальны, аномалия заключается в том, что происходит выработка повышенного количества продуктов гена на данной хромосоме в результате избыточной экспрессии в клетках и тканях, что приводит к формированию фенотипических аномалий [2].
Частота встречаемости составляет 1 случай на 800 новорожденных [3]. Распространенность синдрома не зависит от расы, национальности и социально-экономического статуса. В России общая частота синдрома Дауна увеличилась с 15,53 на 10 000 в 2011 г. до 19,93 на 10 000 в 2017 г. В то же время частота синдрома Дауна только среди новорожденных за этот период времени снизилась с 9,91 до 7,54 на 10 000 рождений [4].
В последнее время благодаря улучшению ухода и раннему лечению осложнений общая продолжительность жизни больных с синдромом Дауна значительно возросла, они начинают попадать в поле зрения терапевтов, кардиологов. В данной статье приведено клиническое наблюдение пациентки 59 лет с синдромом Дауна, у которой развились приобретенный порок сердца, тяжелые нарушения проводимости, приведшие к летальному исходу.
Клиническое наблюдение
В отделение кардиореанимации многопрофильной больницы поступила пациентка 59 лет с критическим истощением источника питания электрокардиостимулятора (ЭКС). Жалоб при поступлении не предъявляла по тяжести состояния.
По данным медицинской документации, у пациентки в течение более 10 лет имели место гипертоническая болезнь, ишемическая болезнь сердца, стенокардия напряжения, осложненные хронической сердечной недостаточностью. В 2013 г. выполнена имплантация ЭКС по поводу атриовентрикулярной блокады 3-й степени. Также в анамнезе хронический пиелонефрит, хроническая болезнь почек С4, цирроз печени класса B по Чайлд — Пью (9 баллов), металлоостеосинтез по поводу закрытого перелома левой бедренной кости.
На догоспитальном этапе выявлено истощение источника питания, в связи с чем пациентка госпитализирована бригадой скорой медицинской помощи в отделение реанимации и интенсивной терапии.
При поступлении общее состояние тяжелое. Кома I. Кожные покровы бледные. Отеки голеней и стоп. Число дыханий 5 в 1 мин, ритм неправильный. Перкуторный звук ясный легочный. Аускультативно дыхание ослаблено над нижними отделами легких, хрипов нет. Проведена интубация трахеи трубкой 8 мм, начата искусственная вентиляция легких аппаратом Drager в режиме Bipap. Тоны сердца приглушены, выслушивается систолический шум над точкой проекции аортального клапана, проводящийся на сосуды шеи. Ритм неправильный. Частота сердечных сокращений (ЧСС) 12–20 в 1 мин с паузами до 15 с (приступы Морганьи — Адамса — Стокса). Дефицита пульса нет. Артериальное давление не определяется. Язык чистый, увеличен в размере. Живот обычной формы, мягкий, безболезненный. Симптомов раздражения брюшины нет. Печень при пальпации безболезненна, увеличена на 3 см, симптом «головы медузы». Селезенка перкуторно не увеличена, не пальпируется, безболезненна. Мочеиспускание свободное.
На электрокардиограмме (см. рисунок) выявлена полная атриовентрикулярная блокада с паузами по монитору до 15 с. Постановка временного ЭКС не увенчалась успехом. По экстренным показаниям проведена замена постоянного ЭКС.
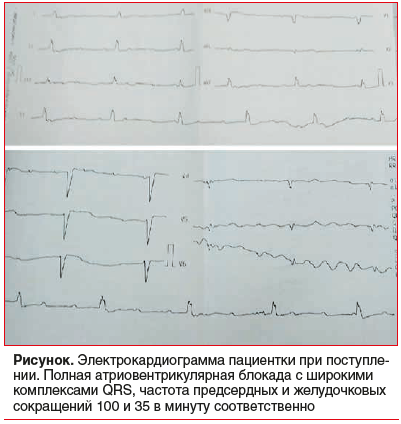
В общем анализе крови выявлялась умеренная нормохромная нормоцитарная анемия: концентрация гемоглобина 84 г/л (норма 112–153 г/л), количество эритроцитов 2,94×1012/л (норма 3,8–5,15×1012/л), гематокрит 30% (норма 34,9–45,6%), средний объем эритроцитов 86 фл (норма 82–98 фл), среднее содержание гемоглобина в эритроците 28,0 пг (норма 26,7–33 пг), средняя концентрация гемоглобина в эритроците 325 г/л (норма 314–349 г/л), цветовой показатель 0,86 (норма 0,82–1,1), лейкоциты 12×109/л (норма 4,5–11×109/л), нейтрофилы 10,84×109/л (норма 1,8–6,98×109/л). Данные биохимического анализа крови и коагулограммы при поступлении и в динамике представлены в таблице 1.
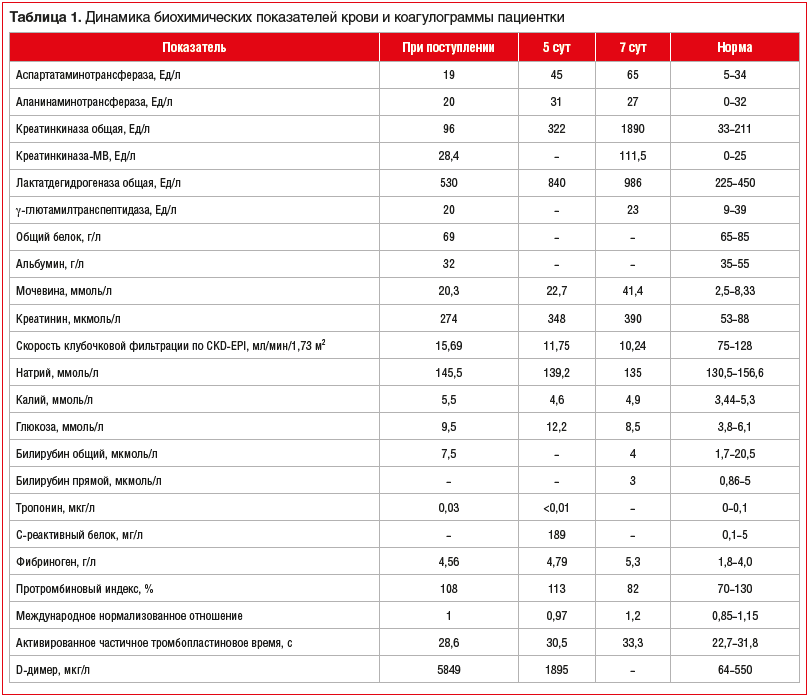
При компьютерной томографии головного мозга данных за острое нарушение мозгового кровообращения не получено. При рентгенографии органов грудной клетки выявлены застойные явления, двухсторонний гидроторакс.
По данным эхокардиографии (ЭхоКГ) корень аорты уплотнен, кальцинирован, пульсация аорты ритмичная, диаметр аорты на уровне синусов Вальсальвы 26 мм. Кальциноз аортального клапана с формированием стеноза устья аорты легкой степени выраженности (градиент 33/17 мм рт. ст., скорость кровотока через аортальный клапан 2,91 м/с) [5] и легкой недостаточности (небольшой центральный поток регургитации, слабая плотность, ширина струи регургитации 2 мм) [6], количество створок достоверно не определяется. Пролапс митрального клапана: систолическое пролабирование передней створки до 2 мм, раскрытие не нарушено. Гипертрофия миокарда левого желудочка (144 г/м2): толщина межжелудочковой перегородки (МЖП) в диастолу 11 мм, толщина задней стенки левого желудочка (ЛЖ) в диастолу 11 мм. Расширение полости левого предсердия: максимальный переднезадний размер левого предсердия 43 мм, объем 74 мл. ЛЖ не расширен: конечно-диастолический размер ЛЖ 38 мм, конечно-диастолический объем ЛЖ 60 мл. Фракция выброса ЛЖ 50%. Локальная сократимость не нарушена. Диссинхрония МЖП. Правый желудочек не расширен: конечно-диастолический размер 34 мм, площадь правого предсердия 16 см2. Расхождение листков перикарда до 6 мм за задней и боковой стенками ЛЖ. В правых отделах электрод ЭКС. Расчетное систолическое давление в легочной артерии 30 мм рт. ст.
Несмотря на проведенную терапию (в том числе инотропную и респираторную поддержку, смену ЭКС по экстренным показаниям), на 8-й день госпитализации зарегистрирована неэффективная кардиостимуляция, асистолия, проведены реанимационные мероприятия без эффекта, констатирована биологическая смерть.
Патологоанатомический диагноз совпал с клиническим:
«Основное заболевание: клапанный аортальный стеноз: периметр аортального клапана 6,5 см, диаметр отверстия 0,8 см, обызвествление створок аортального клапана, гипертрофия миокарда (сердце массой 381 г, толщина стенок левого желудочка 1,7 см).
Фоновое заболевание: синдром Дауна: гидронефроз почек с двух сторон, гипоплазия левой почки.
Осложнения: нарушение проводимости сердца: атриовентрикулярная блокада 2–3-й степени. Имплантация двухкамерного ЭКС «ЭКС-460-DR» от 2013 г. Критическое истощение источника питания ЭКС. Смена ЭКС «ЭКС-460-DR» на ЭКС «ЭКС-460-DR» от 15.10.2020. Отек легких. Двусторонний гидроторакс (слева 300 мл, справа 800 мл). Асцит 200 мл. Острое венозное полнокровие. Некроз эпителия извитых канальцев почек. Отек головного мозга.
Реанимационные мероприятия и интенсивная терапия: пункция и катетеризация правой яремной вены от 15.10.2020. Оротрахеальная интубация от 15.10.2020. Искусственная вентиляция легких с 15.10.2020 по 23.10.2020.
Сопутствующие заболевания: атеросклероз аорты (1-й степени, II стадии). Хронический пиелонефрит. Хронический простой бронхит. Диффузный пневмосклероз. Спайки плевральных полостей с двух сторон. Цирроз печени класса B по Чайлд — Пью (9 баллов). Умеренная нормохромная нормоцитарная анемия».
Синдром Дауна
Синдром Дауна обусловлен мутацией 21-й пары хромосом с формированием ее дополнительной копии в геноме человека. К факторам, повышающим риск появления ребенка с трисомией 21, относят возраст матери. Так, женщина имеет риск 1:1925 в возрасте 20 лет, 1:885 — в 30 лет, 1:365 — в 35 лет, 1:110 — в 40 лет и 1:50 — в 45 лет. Также роль играют наследственность и нарушение формирования гамет [7].
Выделяют 3 формы синдрома Дауна: простую трисомию по 21-й хромосоме, транслокационную трисомию и мозаичный вариант. В случае простой трисомии геном клеток представлен 47 хромосомами и включает 3 хромосомы в 21-й паре. Наиболее часто данный тип возникает при образовании репродуктивных клеток (в 95% случаев — ооцитов, реже — сперматозоидов) и связан с нарушением разделения хромосом во время первого или второго мейотического деления клеток, что ведет к появлению дополнительной копии 21-й хромосомы. Кариотипы детей: представители женского пола — 47, ХХ, +21, представители мужского пола — 47, XY, +21. Встречается в 90–95% случаев заболевания. Транслокационный вариант подразумевает перенос фрагмента хромосомы на другую (чаще между 14-й и 21-й, 21-й и 22-й, 22-й и 21-й хромосомами) и составляет 5–6% всех случаев синдрома Дауна. Кариотипы для девочек — 46, XX, der (21, 21) +21 или 46, XX, der (14, 21) +21, для мальчиков — 46, XY, der (21, 21) +21 или 46, XY, der (14, 21) +21. Мозаичная форма поражает только некоторые клетки организма, поэтому является наиболее сложной для диагностики. Частота встречаемости — 2–3% всех случаев синдрома Дауна [8]. Выделяют несколько типов мозаичной трисомии: клеточный, тканевой и химеризм. В первом случае представлен чередованием нормальных и трисомных клеток, во втором — пораженными трисомией тканями, последний вариант образуется при слиянии двух оплодотворенных яйцеклеток, одна из которых или обе поражены мозаицизмом, с формированием одного зародыша [4, 5].
При синдроме Дауна масса при рождении обычно снижена, прибавка роста, веса и окружности головы ниже нормы вследствие гипотонии, небольшой полости рта и сопутствующих заболеваний желудочно-кишечного тракта и сердечно-сосудистой системы. С возрастом пациенты имеют тенденцию к набору массы тела из-за гипотиреоза, высокого уровня лептина и низкого уровня базального метаболизма. Также наблюдается переменная степень задержки умственного развития пациентов. Коэффициент интеллекта (Intelligence Quotient) колеблется в диапазоне от умеренного (50–70) до низкого (35–50). Такие дети хуже приспособлены к жизни и медленно адаптируются. Типичная модель поведения подобных пациентов подразумевает ласкового, заботливого и довольно общительного человека, но все чаще среди них становятся распространенными аутистические черты характера, наблюдающиеся уже в возрасте 2–3 лет [6, 7].
«Золотым стандартом» диагностики заболевания служит хромосомный анализ, который позволяет обнаружить дополнительную копию хромосомы. Молекулярно-генетические методы, такие как количественная флуоресцентная полимеразная цепная реакция и межфазная гибридизация in situ, обеспечивают быструю диагностику и могут быть использованы у недоношенных детей [9].
Антенатальный скрининг на синдром Дауна позволяет определить вероятность рождения ребенка с данной патологией, рекомендован к проведению у женщин всех возрастных групп в I и II триместрах беременности. Скрининг в I триместре проводится с использованием статистических программ (Astraia и др.) и включает в себя оценку трех составляющих: возрастного риска родителей, биохимического риска (показатели сывороточного человеческого гонадотропина + белок PAPP + PIGF) и ультразвукового риска (по толщине воротникового пространства), затем подсчитывается суммарный риск. Выявляемость синдрома при проведении скрининга составляет 80–82% при ложноположительном показателе 3% [10]. В настоящее время во II триместре проводится только ультразвуковой скрининг — в 19–21 нед. беременности оцениваются более 10 маркеров синдрома Дауна. Скрининг II триместра, проводившийся ранее в виде тройного или квадротеста (включал определение уровня сывороточного человеческого гонадотропина, неконъюгированного эстриола, альфа-фетопротеина и ингибина А или 17-гидроксипрогестерона на сроке 15–19 нед.), в настоящее время отменен ввиду низкой экономической и клинической эффективности. Синдром Дауна обнаруживался в 80% случаев [11]. При превышении порогового уровня суммарного риска по результатам первого скрининга более 1:250 применяется биопсия ворсин хориона на 11–12-й неделях или более безопасный и не менее достоверный амниоцентез на 16–18-й неделях беременности [10] для точной верификации диагноза.
У детей с синдромом Дауна часто имеются пороки развития сердечно-сосудистой системы, дыхательной, нервной, иммунной, эндокринной, мочеполовой систем и опорно-двигательного аппарата. Наибольший интерес представляют врожденные пороки сердца (ВПС) и сосудов в связи с тем, что они являются основной причиной гибели людей с синдромом Дауна. По статистическим данным, среди таких пациентов умирают от кардиологических причин 13% детей и 24% взрослых [12]. Кроме ВПС, уменьшают выживаемость пациентов респираторные инфекции и лейкоз. В последнее время благодаря улучшению ухода и раннему лечению осложнений общая продолжительность жизни больных с синдромом Дауна значительно возросла [12].
Врожденные пороки сердца при синдроме Дауна
У 40–50% новорожденных с синдромом Дауна имеются ВПС [9, 10, 13–15]. Они являются основной причиной смерти пациентов в первые 2 года жизни [16]. Наиболее частыми из ВПС являются полный или неполный атриовентрикулярный канал (или так называемый атриовентрикулярный септальный дефект (АВСД)), дефект межжелудочковой перегородки (ДМЖП), дефект межпредсердной перегородки (ДМПП), открытый артериальный (Боталлов) проток и тетрада Фалло [10, 15]. АВСД и ДМЖП являются типичными пороками развития при синдроме Дауна [17]. Самым часто встречающимся пороком у новорожденных является АВСД, на его долю приходится 40% от всех случаев ВПС. Вторым по частоте является ДМЖП — 35% от всех случаев ВПС [9, 13].
Мутация, способствующая развитию АВСД при синдроме Дауна, находится в 21-й хромосоме [18]. К настоящему времени идентифицированы два специфических генетических локуса для АВСД. Один из них — локус AVSD1, присутствующий на хромосоме 1p31-p21 [19]. Другой локус присутствует на хромосоме 3p25 и соответствующем гене, богатом цистеином, — EGF-подобный домен 1 (CRELD1) [20, 21]. АВСД — это ВПС, при котором сливаются ДМЖП, ДМПП и имеется патология атриовентрикулярных клапанов [22]. Выделяют полный или неполный АВСД [23]. Неполный АВСД характеризуется наличием отдельных атриовентрикулярных клапанов, ДМПП типа «ostium primum», ДМЖП входного типа и расщелины митрального клапана. Он обусловлен неполным слиянием эндокардиальных подушек [24].
Полный АВСД характеризуется общим предсердно-желудочковым клапаном, ДМПП типа «ostium primum» и ДМЖП входного типа. Он обусловлен полным неслиянием эндокардиальных подушек [25]. При полном АВСД общий атриовентрикулярный клапан имеет 5 больших створок: 3 латеральные (прилежащие к свободным стенкам) и 2 мостовидные (перегородочные) [26]. При АВСД наблюдается диспропорция выходного и входного размеров левого желудочка, причем первый из них больше второго по сравнению с нормальным сердцем, где они одинаковы.
При рутинном антенатальном ультразвуковом сканировании АВСД лучше всего виден на четырехкамерной позиции сердца в виде общего атриовентрикулярного клапана [27]. Однако чувствительность антенатального ультразвука при АВСД очень низка [28]. Послеродовая диагностика АВСД проводится с помощью электрокардиографии, рентгенографии органов грудной клетки, ЭхоКГ. Данные ЭхоКГ включают аномальную конфигурацию атриовентрикулярного клапана, потерю нормального смещения атриовентрикулярного клапана, аномальное положение папиллярных мышц, диспропорцию входного и выходного отделов ЛЖ, ДМПП типа «ostium primum», ДМЖП входного типа и другие сопутствующие ВПС [19, 22].
Обычно это тяжелый, гемодинамически значимый порок, однако он совместим с жизнью, и при небольшой выраженности нарушений пациенты могут доживать до 20 лет и более [22]. АВСД подлежит хирургической коррекции. Целью ее является закрытие ДМЖП, ДМПП и восстановление атриовентрикулярных клапанов [27]. Пациенты, подвергшиеся хирургическому лечению, имеют 15-летнюю выживаемость около 90%. От 9% до 10% из них нуждаются в повторной операции в течение 15 лет [29].
ДМЖП — это ВПС, при котором имеется сообщение (отверстие) между левым и правым желудочком со сбросом крови слева направо и развитием легочной гипертензии [22, 30]. Цветовое допплеровское картирование при трансторакальной ЭхоКГ является наиболее высокочувствительным методом диагностики. Примерно от 85% до 90% небольших изолированных ДМЖП спонтанно закрываются в течение первого года жизни. Хирургическое закрытие ДМЖП показано при средних и больших дефектах с дисфункцией ЛЖ, в случаях прогрессирующей аортальной недостаточности или после эпизода эндокардита [31].
ДМПП — это ВПС, при котором имеется сообщение (отверстие) между левым и правым предсердием, через него происходит сброс крови [22, 32]. ДМПП часто не приводит к появлению клинической симптоматики [33]. Диагностическая визуализация важна для определения размера дефекта и имеет решающее значение для определения тактики ведения. Трансторакальная ЭхоКГ является «золотым стандартом» визуализации [32]. ДМПП размерами менее 5 мм часто спонтанно закрываются в течение первого года жизни. ДМПП размером более 1 см чаще всего требуют хирургического закрытия дефекта [34].
Кроме того, необходимо отметить возможность развития у пациентов с синдромом Дауна сердечно-сосудистых осложнений ВПС, включающих легочную гипертензию, аритмию и нарушение проводимости, наличие которых является предиктором неблагоприятного прогноза для пациента [35].
Приобретенные ССЗ у пациентов с синдромом Дауна
Анатомия сердца у людей с трисомией 21-й хромосомы без явных ВПС не является полностью нормальной. Сообщалось об укорочении МЖП и увеличении ее перепончатой части у новорожденных с синдромом Дауна без ВПС [36]. Кроме того, в 64% случаев выявлялась клапанная дисплазия. Также при оценке состояния сердца у случайной группы взрослых с синдромом Дауна было выявлено большое количество пациентов с пролапсом митрального клапана или с аортальной регургитацией [37–39]. Систолическая функция у подростков с синдромом Дауна без ВПС [40] и результаты оценки кардиореспираторного теста (тредмил-теста с оценкой функции внешнего дыхания) [41] были адекватными, что позволяет предположить у них возможность нормальной физической активности, хотя отмечена сниженная работоспособность [42].
У пациентов с синдромом Дауна описаны преждевременное старение и тенденция к ожирению. У них не только дегенеративные изменения внешнего вида, например кожи и волос, появляются раньше, чем у умственно отсталых людей без синдрома Дауна, но и симптомы болезни Альцгеймера отмечаются раньше, чем у населения в целом. К 45 годам практически у всех людей с синдромом Дауна появляются старческие бляшки, нейрофибриллярные клубки и грануловакуолярная дегенерация нервных клеток. У людей с синдромом Дауна продолжительность жизни короче, чем у населения в целом [43]. Также при синдроме Дауна более высокая вероятность избыточной массы тела и ожирения, чем у людей без этой болезни, более частое развитие заболеваний щитовидной и паращитовидной желез, остеопороза, метаболического синдрома, сахарного диабета 2 типа [44–46]. Среди женщин с синдромом Дауна ожирение встречается чаще, чем среди мужчин. Вероятные детерминанты ожирения включали повышенный уровень лептина, снижение расхода энергии в покое, сопутствующие заболевания, неблагоприятное питание и низкий уровень физической активности. Ожирение положительно ассоциировалось с обструктивным апноэ сна, дислипидемией, гиперинсулинемией и нарушением походки [47, 48].
Согласно данным E. Vianello et al. [49] у взрослых с синдромом Дауна редко развивается атеросклероз, артериальная гипертензия и ишемическая болезнь сердца (табл. 2). В исследовании [50] было обнаружено, что у взрослых с синдромом Дауна меньше толщина интима-медиа сонных артерий, систолическое и диастолическое артериальное давление, а также более высокие уровни С-реактивного белка, триглицеридов и общее содержание жира в организме, чем в контрольной группе. Взрослые люди с синдромом Дауна могут быть защищены от атеросклероза, несмотря на повышенный уровень общего жира в организме и повышенные факторы риска ССЗ. Эта тенденция объясняется сверхэкспрессией защитных антиатеросклеротических факторов за счет генов, расположенных в 21-й хромосоме [51]. Более того, было высказано предположение, что более высокий уровень адипонектина [52] и белков, связывающих жирные кислоты [49], может играть роль в защите взрослых с синдромом Дауна от атеросклероза.
![Таблица 2. Частота коморбидных заболеваний при синдроме Дауна (по C.G. Sobey et al. [53] с модификацией), % Таблица 2. Частота коморбидных заболеваний при синдроме Дауна (по C.G. Sobey et al. [53] с модификацией), %](https://medblog.su/wp-content/uploads/2022/12/1672325760_987_sindrom-dauna-i-serdechno-sosudistaya-patologiya-klinicheskoe-nablyudenie-i-obzor-literatury-reznik-e-v-nguen-t-l-ilina-t-s-tokmakova-e-s-dzhobava-e-m-goluhov-g-n.png)
Также сообщается, что сердечно-сосудистая система пациентов с синдромом Дауна характеризуется измененным вегетативным контролем сердечной деятельности и вегетативной дисфункцией. Пациенты с синдромом Дауна без ВПС демонстрируют снижение ЧСС и артериального давления в ответ на изометрические упражнения с хватом, тилт-тест и тестирование холодного пресса [54, 55]. У пациентов с синдромом Дауна наблюдается меньшее парасимпатическое торможение и симпатическое возбуждение в ответ на пассивный вертикальный наклон. Эти эффекты могут быть опосредованы меньшим изменением чувствительности барорефлекса у людей с синдромом Дауна [55]. Вегетативная дисфункция также может частично объяснять недостаточное увеличение ЧСС во время тредмил-теста с максимальной нагрузкой у таких больных [54].
Статистики по продолжительности жизни пациентов с синдромом Дауна в нашей стране нет. Согласно зарубежным данным [3] средняя продолжительность жизни при этом заболевании в последние годы возросла с 25 до 53–58 лет. В представленном наблюдении пациентка дожила до 59 лет и скончалась от полиорганной недостаточности на фоне несвоевременной замены ЭКС, острой декомпенсации сердечной недостаточности.
Заключение
В представленном нами клиническом наблюдении у пациентки с подтвержденным в детстве диагнозом «синдром Дауна» не было данных за наличие ВПС, в 52 года развились тяжелые нарушения проводимости, потребовавшие установки ЭКС, в 59 лет был диагностирован дегенеративный стеноз устья аорты легкой степени и недостаточность аортального клапана.
Таким образом, в связи с увеличением продолжительности жизни пациентов с синдромом Дауна они начинают попадать в поле зрения терапевтов, кардиологов, реаниматологов, оказывающих помощь взрослому населению. В настоящее время ведение таких больных осуществляется с позиций общих рекомендаций. Необходимо изучение особенностей течения ССЗ у данной категории больных для оказания им адекватной медицинской помощи. В будущем возможна разработка отдельных клинических рекомендаций или включение отдельных разделов в общие рекомендации по особенностям ведения таких больных.
Информация с rmj.ru





