Содержание статьи
Синдром раздраженного кишечника: современные представления о
заболевании и перспективы терапии
И. Б. Хлынов*, доктор медицинских наук
Е. Б. Фрезе**, кандидат медицинских наук
О. А. Рябинина***
М. В. Чикунова*, кандидат медицинских наук
О. М. Хромцова*, доктор медицинских наук
Р. И. Акименко*
* ГБОУ ВПО УГМУ МЗ РФ, Екатеринбург
** МЦ «Уральский», Екатеринбург
*** МУ ГКБ № 40, Екатеринбург
Синдром раздраженного кишечника одно из самых распространенных функциональных
гастроэнтерологических заболеваний в клинической практике. Определение синдрома
раздраженного кишечника (СРК), данное Всемирной гастроэнтерологической
организацией (World Gastroenterology Organisation, WGO) в 2009 г., характеризует
рассматриваемую патологию как функциональное расстройство кишечника, при котором
абдоминальная боль или дискомфорт ассоциируется с дефекацией и/или изменением в
его схеме [1].
Распространенность СРК в популяции колеблется от 2,9% до 22%, что приводит к
высокой доле пациентов с данной патологией в практике семейного врача и
врача-гастроэнтеролога, а также значительным косвенным и прямым затратам систем
здравоохранения во всем мире [1–3].
Эпидемиологическими особенностями СРК являются преобладание заболеваемости
среди женской популяции, а также первое обращение пациента к врачу в возрасте до
50 лет. В ряде случаев симптомы развиваются в детском возрасте, причем частота
распространенности СРК среди детей соответствует взрослой популяции. Описана
тенденция по уменьшению частоты развития СРК в старших возрастных группах [1].
Важнейшими общими характеристиками СРК являются, с одной стороны, отсутствие
данных о связи патологии с повышенным риском развития колоректального рака или
воспалительных заболеваний кишечника [3]. С другой стороны, длительное
перстистирование заболевания и значительное снижение качества жизни пациентов
заставляет их прибегать к повторным консультациям врача, многократным
исследованиям и длительной, часто не имеющей доказательной базы терапии.
Этиология СРК до настоящего времени не определена, несмотря на выделение СРК
в качестве нозологической формы в соответствии с Международной классификацией
болезней. С академической точки зрения, рассматриваемая патология принадлежит
больше к «клиническому синдрому», чем определенной нозологии.
Патогенетические механизмы формирования СРК, очевидно, разнообразны при
различных клинических формах данного заболевания. Особое место отводится
моторной дисфункции кишечника и в значительной степени феномену висцеральной
гиперчувствительности [4, 5]. Висцеральная гиперчувствительность как
патогенетический механизм СРК считается универсальным и релевантным для данной
патологии [3]. Соответственно, наиболее перспективными терапевтическими
стратегиями в современной терапии СРК считается поиск и получение доказательств
клинической эффективности препаратов, влияющих на моторику кишечника и
висцеральную чувствительность. Важное место в ряду последних достижений науки и
практики отводится изучению и применению короткоцепочечных жирных кислот (КЦЖК),
в частности масляной кислоты [6, 7].
Исследования продемонстрировали влияние КЦЖК на выработку регуляторного
пептида PYY, который, в свою очередь, замедляет моторику толстой и тонкой кишки,
модулирует илеотолстокишечное торможение и колоподвздошный рефлюкс [8–10].
Функция масляной кислоты определяется ее взаимодействием с рецепторами на
мембранах колоноцитов (GPR41, GPR43, 5-HT-4). Бутират, в отличие от других КЦЖК,
также способен усиливать моторику кишки путем повышения ацетилирования
Н3-гистонов в нейронах кишечника. Выявленные эффекты бутирата на моторику кишки,
что особенно важно, являются дозозависимыми [9, 11–15].
Наиболее интересным и перспективным, в рамках терапевтического применения,
безусловно, является выявленный феномен влияния масляной кислоты на висцеральную
чувствительность у здоровых добровольцев. Данный эффект объясняется увеличением
порога чувствительности висцеральных механорецепторов, увеличением высвобождения
серотонина (5-НТ), модификацией уровня продукции YY-гормона [16, 17].
Согласно действующему международному соглашению — Римским критериям III от
2006 г. [4], диагноз СРК устанавливают при наличии рецидивирующей абдоминальной
боли или дискомфорта в области живота в течение трех дней каждого месяца за
последние три месяца в сочетании с двумя или более из следующих признаков:
улучшение состояния после дефекации; ассоциация с изменением частоты и формы
стула. Дополнительными симптомами в диагностике СРК являются: патологическая
частота стула (< 3 раз в неделю или > 3 раз в день); патологическая форма стула
— комковатый/твердый или жидкий/водянистый стул; натуживание при дефекации;
императивный позыв или чувство неполного опорожнения, выделение слизи и вздутие
живота.
Классификация СРК, в соответствии с Римскими критериями III, выделяет:
1) СРК с преобладанием запора (IBS-C);
2) СРК с преобладанием диареи (IBS-D);
3) смешанный СРК (IBS-M);
4) неклассифицируемый СРК (IBS-U).
Поскольку в разные периоды времени может преобладать запор, сменяющийся
поносом, и наоборот, предлагается использовать термин «перемежающийся СРК» (IBS-A).
Также могут быть использованы другие классификации, основанные на наличии
отягощающих факторов (ВГО, 2009): постинфекционный СРК (ПИ-СРК); СРК, связанный
с определенными пищевыми продуктами; СРК, связанный со стрессом.
Диагностические мероприятия при СРК проводят в рамках стратегии «диагноза
исключения», основой которой является исключение других заболеваний кишечника, в
первую очередь представляющих угрозу здоровью и жизни пациента.
Комплекс обязательных исследований включает: общий анализ крови, общий анализ
мочи, биохимическое исследование (общий билирубин, ACT, АЛТ, щелочная фосфатаза,
γ-глутаматтранспептидаза, глюкоза, креатинин), копрограмму, анализ кала на
скрытую кровь. Целесообразно определение уровня тканевой трансглютаминазы,
концентрации тиреотропного гормона и фекального кальпротектина. К перечню
инструментальных методов исследования относятся: ректороманоскопия, колоноскопия
с биопсией, ультразвуковое исследования органов брюшной полости и малого таза,
электрокардиограмма, эзофагогастродуоденоскопия.
Лечение больных СРК включает нормализацию образа жизни, соблюдение диеты
(выбор пищевых продуктов зависит от клинической формы СРК), применение методов
психотерапии, назначение лекарственных средств.
В основу выбора лекарственной терапии СРК, согласно рекомендациям Римских
критериев III, положена симтоматическая терапия ведущего клинического синдрома.
В частности, для купирования абдоминальной боли, с учетом зарегистрированных в
Российской Федерации препаратов, предлагается назначать пациентам с СРК
лекарственные средства из группы спазмолитиков, трициклических антидепрессантов
и селективных ингибиторов обратного захвата серотонина. При варианте СРК с
диареей в терапию предлагается включать лоперамид, а при СРК с запором —
слабительные препараты (псиллиум, лактулозу, макрогол).
Важно отметить что, с учетом национальных особенностей организации
медицинской помощи в Российской Федерации, терапия СРК на основании Приказа
Министерства здравоохранения России от 15.06.15 г. «Об утверждении критериев
оценки качества медицинской помощи» должна соответствовать национальным
клиническим рекомендациям и Федеральным стандартам медицинской помощи.
Национальные рекомендации диагностики и лечения взрослых пациентов с СРК
опубликованы на сайте Российской гастроэнтерологической ассоциации (www.gastro.ru).
Федеральные стандарты ведения больных СРК утверждены Приказами Министерства
здравоохранения России № 774н от 09.11.2012 г. и 1420н от 24.12.2012 г.
Существующие международные и национальные соглашения по терапии СРК дают
практическому врачу определенный комплекс терапевтических возможностей курации
больных СРК, который, как показывают многочисленные исследования, демонстрирует
определенную, но не достаточную эффективность. Указанное побуждает
исследователей к поиску и доказательству эффективности новых схем терапии
пациентов с СРК.
Проведено собственное проспективное, рандомизированное, контролируемое,
открытое исследование, целью которого явилось изучение эффективности и
безопасности комбинированной терапии с включением спазмолитика (тримебутина) и
масляной кислоты с инулином (Закофалька) у больных СРК.
Материалы и методы исследования
Критериями включения в исследование явились: установленный диагноз СРК,
возраст от 18 до 50 лет, информированное согласие. Критерии исключения из
исследования: суб- и декомпенсированная соматическая патология, операции в
анамнезе на органах брюшной полости и малого таза, онкологические заболевания, в
том числе ранее перенесенные, прием антибактериальных препаратов и препаратов
для лечения СРК до 3 месяцев до начала исследования.
Пациенты были рандомизированы методом конвертов в две группы. В 1-ю
(контрольную) группу вошли 35 пациентов (24 женщины и 11 мужчин), получающие в
течение 4 недель тримебутин (Тримедат) 200 мг 3 раза в день. Во 2-ю (основную)
группу вошли 35 пациентов (24 женщины и 11 мужчин), получающие также 28 дней
тримебутин 200 мг 3 раза в день и масляную кислоту в комбинации с инулином (Закофальк)
по 1 табл. 3 раза в день. Возраст больных 1-й группы составил 39,5 (33,0 ± 49,0)
года, 2-й группы — 38,0 (32,0 ± 49,0) лет. Исследование в 1-й группе завершил 31
больной, во 2-й группе 34 пациента. Причиной исключения пациентов из
исследования стала неявка на контрольный визит.
Пациенты после информированного согласия заполняли опросник, включающий
информацию о симптомах СРК, которые испытывал пациент до и во время лечения.
Критериями оценки эффективности явились следующие показатели:
- Показатель «Длительность болевого симптома» рассчитывался по количеству
дней, в течение которых пациент испытывал абдоминальную боль на фоне терапии. - Показатель «Интенсивность болевого симптома до лечения» вычислялся как
среднее значение баллов, набранных больным за 7-дневный период до начала
терапии по десятибалльной визуально-аналоговой шкале. - Показатель «Интенсивность болевого симптома после лечения» вычислялся как
среднее значение баллов, набранных больным за 7-дневный период после терапии
по десятибалльной визуально-аналоговой шкале. - Показатель «Длительность вздутия живота» рассчитывался как количество
дней, на протяжении которых пациент испытывал этот симптом на фоне терапии. - Показатель «Длительность чувства неполного опорожнения кишечника»
рассчитывался как количество дней, на протяжении которых пациент испытывал
этот симптом на фоне терапии. - Показатель «Удовлетворенность терапией» определялся в виде субъективной
оценки пациентом эффективности терапии, в процентах (от 0 до 100).
Статистическая обработка проведена с использованием прикладных программ
Statistica 6.0. Нормальность распределения данных проверялась критерием согласия
распределений Шапиро–Уилкса (W). Значения всех изучаемых признаков достоверно
отличались от нормального по W-критерию (р < 0,05), вследствие чего
использовались непараметрические критерии. Непрерывные величины были
представлены в виде медианы (Ме) и 25-й и 75-й процентилей (25 ± 75).
Достоверный уровень значимости определялся при значении р < 0,05.
Результаты и их обсуждение
Анализ рассматриваемых параметров у пациентов контрольной группы, получающих
монотерапию спазмолитиком, установил, что болевой симптом сохранялся в течение
17,0 (13,0 ± 18,0) дней, вздутие живота на протяжении 10,0 (4,0 ± 16,0) дней и
чувство неполного опорожнения кишечника в течение 11,0 (5,0 ± 17,0) дней.
Интенсивность болевого симптома до лечения пациенты оценивали в 3,4 (1,9 ± 4,0)
балла, а после курса терапии в 2,0 (0,6 ± 2,0) балла. Подтверждена положительная
и достоверная динамика интенсивности болевого симптома после монотерапии
спазмолитиком (р < 0,01). Показатель «удовлетворенность терапией» у пациентов
контрольной группы составил 53% (17 ± 63).
В основной группе, где пациентам назначалась комбинированная терапия,
длительность болевого симптома составила 13,5 (8,0 ± 15,0) дней, вздутие живота
и чувство неполного опорожнения кишечника фиксировались пациентами 5,0 (3,0 ±
14,0) и 9,0 (7,0 ± 14,0) дней соответственно. Интенсивность болевого симптома до
лечения пациенты оценивали в 3,0 (2,6 ± 3,1) балла, а после курса терапии
показатель снизился до 0,55 (0,3 ± 1,0) балла. Подтверждена положительная и
достоверная динамика интенсивности болевого симптома после комбинированной
терапии спазмолитиком и масляной кислотой с инулином (р < 0,01). Показатель
«удовлетворенность терапией» у пациентов основной группы составил 67% (57 ± 72).
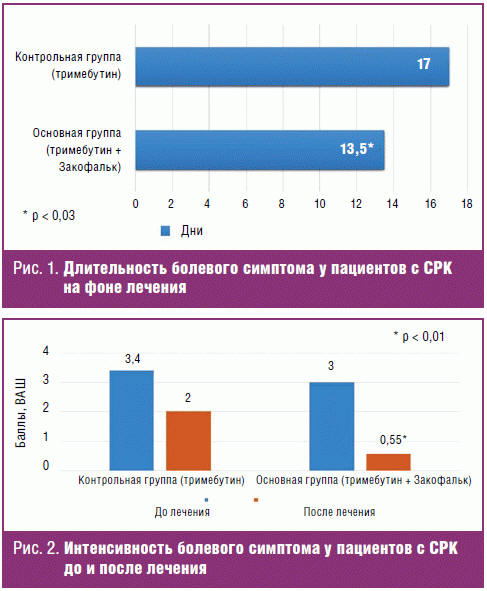
Сравнительный анализ изучаемых показателей установил, что длительность
болевого симптома на фоне комбинированной терапии наблюдалась достоверно меньше
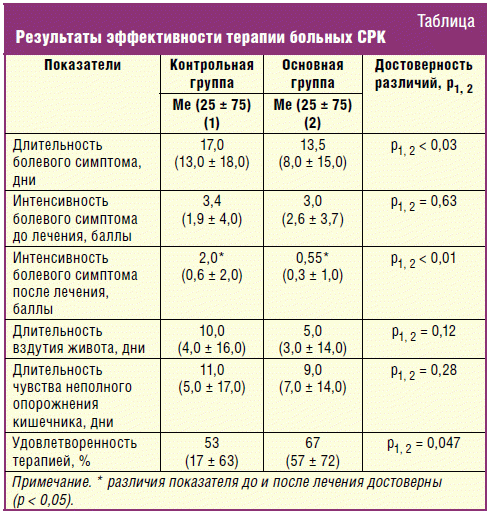
(р < 0,03) (рис. 1). При этом если показатель «интенсивность болевого симптома
до лечения» в контрольной и основной группах достоверных отличий не имел, то
после лечения он был достоверно ниже в группе пациентов, получающих
комбинированную терапию (р < 0,01) (рис. 2). Такие симптомы, как вздутие живота
и чувство неполного опорожнения кишечника не имели достоверных различий в
сравниваемых группах. Статистический анализ различий показателя
«удовлетворенность терапией» был достоверно выше в группе пациентов, получающих
комбинированную терапию, включающую спазмолитик и масляную кислоту с инулином (р
= 0,047). Результаты исследования представлены в таблице. Нежелательных
лекарственных реакций во время проведения терапии в основной и контрольной
группе, потребовавших отмены лечения, не выявлено.
Заключение
Проведенное исследование демонстрирует положительное влияние монотерапии
спазмолитиком (тримебутин в дозе 200 мг 3 раза в день) на интенсивность болевого
симптома у пациентов с СРК. Однако при использовании комбинированной терапии (тримебутин
в дозе 200 мг 3 раза и масляной кислоты с инулином (Закофальк) по 1 табл. 3 раза
в день) наблюдается как сокращение продолжительности абдоминальной боли в
процессе терапии, так и интенсивности абдоминальной боли.
Исследование не выявило различий между сравниваемыми группами в показателях,
оценивающих такие симтомы СРК, как вздутие живота и чувство неполного
опорожнения кишечника. Субъективная оценка удовлетворенности терапией больными
СРК была выше в группе пациентов, в лечение которых включался препарат масляной
кислоты с инулином (Закофальк).
На фоне проведения комбинированной терапии (тримебутин и масляная кислота с
инулином) нежелательных лекарственных реакций не зарегистрировано.
Литература
- www.worldgastroenterology.com/guideline-ibs/irritable-bowel-sindrome-ibs-russian.
-
Longstreth G. F., Wilson A., Knight K. et al. Irritable bowel
syndrome, health care use, and costs: a U. S. managed care perspective // Am J
Gastroenterol. 2003; 98: 600–607. - www.worldgastroenterology.com/guideline-ibs/irritable-bowel-sindrome-ibs-english.
-
Drossman D. A. The Functional Gastrointestinal Disorders and the
Rome III Process // Gastroenterology. 2006; 130 (5): 1377–1390. -
Lembo T., Naliboff B., Munakata J. et. al. Symptoms and visceral
perception in patients with pain-predominant irritable bowel syndrome // Am J
Gastroenterol. 1999; 94: 1320–1326. -
Cummings J. Y., Rombeau J. L., Sakata T. (eds). Physiological and
Clinical Aspects of Short-Chain Fatty Acids. Cambridge University Press. 2004.
596 p. -
Hu S., Dong T. S., Dalai S. R., Wu F., Bissonnette M., Rwon J. H.
et al. The microbe — derived short chain fatty acid butyrate targets
miRNA-dependent p21 gene expression in human colon cancer // PLoS ONE. 2011; 6
(1): е16221. -
Cherbut C. Lactulose and colonic motility // Annales de
Gastroenterologie et d’Hepatologie. 1998; 34 (2): 85–94. -
Cherbut C., Aube A. C., Blottiere H. M., Galmiche J. P. Effects
of short-chain fatty acids on gastrointestinal motility // Scand. J.
Gastroenterology. 1997; 32 (Supp. 222): 58–61. -
Nieuwenhuijs V. B., Verheem A., Van
Duijvenbode-Beumer H. et al. The role of interdigestive small bowel
motility in the regulation of gut micro? ora, bacterial overgrowth, and
bacterial translocation in rats // Annals of Surgery. 1998; 228 (2): 188–193. -
Ардатская М. Д. Масляная кислота и инулин в клинической практике:
теоретические аспекты и возможности клинического применения [пособие]. М.:
Форте принт. 2014. С. 64. -
Canani R. B., Di Costanzo M., Leone L., Pedata M., Meli R., Calignano
A. Potential benecial effects of butyrate in intestinal and
extraintestinal diseases // World J Gastroenterol. 2011; 17 (12): 1519–1528. -
MacFabe D. F. Short-chain fatty acid fermentation products of the
gut microbiome: implications in autism spectrum disorders // Microb Ecol.
Health Dis. 2012; 23. DOI: 10.3402/mehd.v23 i0.19260. -
Soret R., Chevalier J., De Coppet P. et al. Short-chain fatty
acids regulate the enteric neurons and control gastrointestinal motility in
rats // Gastroenterology. 2010; 138 (5): 1772–1782. -
Tazoe H., Otomo Y., Kaji I. et al. Roles of short-chain fatty
acids receptors GPR41 and GPR43 on colonic functions // J Physiol Pharmacol.
2008; 59 (Suppl 2.): 251–262. -
Kilkens T. O., Honig A., van Nieuwenhoven M. A., Riedel W. J., Brummer
R. J. Acute tryptophan depletion affects braingut responses in irritable
bowel syndrome patients and controls // Gut. 2004; 53 (12): 1794–1800. -
Vahoutvin S. A., Troost F. J., Kilkens T. O. et al. The effects
of butyrate enemas on visceral perception in healthy volunteers //
Neurogastroenterol Motil. 2009; 21 (9): 952-e76.
Статья опубликована в журнале
Лечащий Врач
материал MedLinks.ru






