Патология желудочно-кишечного тракта при сахарном диабете
Д.м.н., проф. Т.Е. Полунина
ГОУВПО «Московский государственный медико-стоматологический университет» Минздравсоцразвития России
В настоящее время особое внимание клиницистов привлечено к проблеме патологии желудочно-кишечного тракта (ЖКТ) при сахарном диабете (СД). Это связано с тем, что благодаря более глубокому изучению патофизиологии и классификации симптомов СД была определена патогенетическая связь этого заболевания с желудочно-кишечной симптоматикой. Проявление симптомов меняется в широких пределах и затрагивает весь ЖКТ.
Большинство исследователей чаще всего связывают желудочно-кишечную симптоматику СД с диабетической автономной нейропатией (ДАН) [3]. Наиболее частыми проявлениями гастроэнтерологической формы ДАН являются заболевания пищевода, желудка, тонкой и толстой кишки [3, 20]. В последнее время к гастроэнтерологическим осложнениям СД стали относить и изменение липидного обмена, которое приводит к возникновению таких заболеваний, как неалкогольная жировая болезнь печени (НАЖБП), цирроз, гепатоцеллюлярная карцинома, острая печеночная недостаточность (ОПН) [4,20].
Заболевания пищевода
Проявляются в виде моторной дисфункции пищевода, гастроэзофагеального рефлюкса, изжоги. У больных СД заболевания пищевода встречаются чаще по сравнению с контрольными группами. Это обусловлено ДАН, которая приводит к следующим нарушениям:
■ снижению давления желудочного сфинктера (гипергликемия увеличивает время «переходных расслаблений» сфинктера пищевода);
■ уменьшению амплитуды и частоты перистальтических волн и возрастанию асинхронных и неэффективных волн пищеводных сокращений;
■ запаздыванию желудочной секреции.
Признаки и симптомы:
■ изжога — ощущение жжения в загрудинной области, чаще всего возникающее после приема пищи;
■ регургитация — появление желудочного содержимого во рту или носоглотке, также возникающее после приема пищи;
■ другие симптомы — боль за грудиной, дисфагия, тошнота, хронический кашель.
Проводимые исследования:
■ эзофагогастродуоденоскопия с биопсией, если симптомы являются тяжелыми или постоянными, даже при проведении терапии;
■ анализ биопсийного материала для исключения метаплазии (дисплазии) при пищеводе Барретта;
■ 24-часовая рН-метрия для подтверждения диагноза у больных с симптомами пищеводных нарушений;
■ измерение времени поддержания рН на уровне < 4,0;
■ манометрия пищевода для исследования нарушения подвижности и исключения склеродермии или ахалазии до проведения хирургического вмешательства;
■ двойное рентгеноконтрастное исследование с использованием бария для определения язв или эрозий в пищеводе.
Лечение
Изменение образа жизни:
■ сон в положении с приподнятой верхней частью тела;
■ принятие вертикального положения после приема пищи;
■ исключение из рациона питания жирных продуктов, шоколада, чрезмерного потребления алкоголя, кислых напитков;
■ исключение тесной одежды и тугого затягивания ремня на талии;
■ снижение массы тела для грузных или страдающих ожирением пациентов;
■ прекращение курения.
Медикаментозная терапия — ингибиторы протонной помпы (пантопразол, эзомепразол и др.); блокаторы Н2-рецепторов гистамина (фамотидин).
Хирургический метод лечения — фундопластика: часть желудка фиксируется вокруг нижней части пищевода для дополнительной! поддержки нижнего сфинктера пищевода.
Заболевания желудка
Диабетический гастропарез — состояние, при котором секреция желудка при приеме пищи осуществляется с задержкой, что приводит к застою пищи в желудке. Возникает из-за сниженной иннервации желудочной функции при наличии гипергликемии. Гипергликемия приводит к расслаблению мышечных тканей желудка, уменьшению частоты, распространения и амплитуды сокращения антральных волн, I возникающих после приема пищи, и стимулирует фазу пилорических волн. Все это замедляет желудочную секрецию и двигательную функцию желудка.
Признаки и симптомы:
■ изжога или рефлюкс;
■ тошнота и рвота непереваренной пищей;
■ неконтролируемый уровень сахара в крови;
■ раннее насыщение;
■ вздутие живота;
■ плохой аппетит и потеря массы тела.
Диагноз диабетического гастропареза основывается на следующих критериях:
■ клинические проявления (раннее насыщение, тошнота, рвота, вздутие живота);
■ отсутствие коррекции гликемического профиля, несмотря на проводимую терапию;
■ снижение секреторной функции желудка;
■ отсутствие обструкции в желудке или тонкой кишке, подтвержденной эндоскопией или радиографией с использованием бария.
Лечение
Терапия направлена на устранение симптомов и включает:
1) диетическое питание — обезжиренная пища, частые дробные приемы пищи, гомогенизированная жидкая пища, насыщенная витаминами, энтеральное питание, парентеральное питание при нарушении моторики;
2) контроль гликемического профиля;
3) медикаментозную терапию — стимуляторы моторно-эвакуаторной функции верхних отделов желудочно-кишечного тракта (прокинетики): итоприд, домперидон и метоклопрамид;
4) хирургические методы — желудочная электростимуляция; имплантируемое устройство для желудочной стимуляции (выбор для пациентов с тяжелым гастропарезом, не поддающимся лечению другими методами).
Заболевания тонкой кишки
Могут быть обнаружены более чем у 80% пациентов с длительным анамнезом СД. Наиболее частым (23% пациентов в большинстве исследований) и общим нарушением является замедление кишечного транзита.
Длительная гипергликемия тонкой кишки при автономной невропатии (вагусной и симпатической) приводит к нарушению подвижности тонкой кишки, снижению секреции или уменьшению всасывания. Нарушенная подвижность тонкого кишечника ведет к слабому перемещению пищи, вызывает усиленное размножение бактерий, полную мальабсорбцию, способствует слабому ионному обмену, что заканчивается увеличением внутриполостной осмолярности, пассивным передвижением жидкости в полости кишечника и поносом.
Симптомы:
■ водянистый, безболезненный ночной понос;
■ боль в животе;
■ нейропатия тонкой кишки;
■ вздутие живота.
Лабораторные и инструментальные исследования — копрология, анализ кала на дисбактериоз, колоноскопия, гастроинтестинальная эндоскопия с биопсией (гистология и бактериология).
Диагноз обычно основывается на исключении других причин диареи, таких как лекарственные (метформин, антибиотики широкого спектра действия) или глютеновая болезнь.
Лечение
Неотложная помощь — повторная гидратация и коррекция электролитных нарушений, кишечные антисептики, антидиарейные средства (Лоперамид, Смекта). Длительное лечение: постоянный контроль за гликемическим профилем и диабетической энцефалопатией.
Заболевания толстой кишки
Связаны с:
■ наличием ДАН;
■ снижением желудочно-ободочного рефлекса;
■ уменьшением основного давления внутреннего анального сфинктера (автономная иннервация);
■ дисфункцией внешнего анального сфинктера и лонноректальных мышц, приводящей к снижению расслабляющей способности;
■ нарушением гликемического профиля;
■ уровнем субстанции Р, которая стимулирует панкреатическую секрецию, секрецию электролита и кишечную подвижность.
Клинические проявления:
■ запоры;
■ усиление потребности в слабительных средствах;
■ недержание кала.
Лабораторные и инструментальные исследования:
■ копрология;
■ ректороманоскопия;
■ исключение других причин запора (например, гипотиреоидной или лекарственной этиологии);
■ аноректальная манометрия.
Лечение
Терапия запора включает в себя:
■ гидратацию;
■ регулярную физическую активность;
■ увеличение количества пищи с содержанием грубой клетчатки;
■ прием лактулозы;
■ применение осмотических слабительных средств в более тяжелых случаях.
Неалкогольная жировая болезнь печени
Термин «неалкогольная жировая болезнь печени» (НАЖБП) используется для описания состояния печени у пациентов с патологией, характерной для алкогольного поражения печени, но не имеющих в анамнезе значительного употребления алкоголя. Этиология неизвестна, но заболевание часто связывают с СД 2 типа и ожирением. В некоторых случаях НАЖБП проявляется в виде неалкогольного стеатогепатита (НАСГ) с различной степенью воспаления. В очень редких случаях это может привести к циррозу печени. Данные о распространенности НАЖБП у пациентов с СД противоречивы и имеют существенный диапазон колебаний — от 34 до 78%, а при сочетании с ожирением — до 100%. При этом морфологически стеатогепатиты составляют 50%, а циррозы- 19% [6]. Поскольку НАЖБП часто сочетается с нарушениями углеводного и липидного обмена, ее все чаще стали считать компонентом метаболического синдрома (МС). Распространенность МС у больных НАЖБП составляет более 40%. МС является предиктором НАЖБП. В последние годы к проблеме МС привлечено особое внимание клиницистов. МС представляет собой комплекс многих взаимосвязанных между собой нарушений (инсулинорезистентность (ИР) с относительной гиперинсулинемией, нарушение углеводного обмена, абдоминальное висцеральное ожирение, артериальная гипертензия, атерогенная дислипидемия, микропротеинурия, гиперкоагуляция, гиперурикемия или подагра, НАЖБП) (рис. 1).
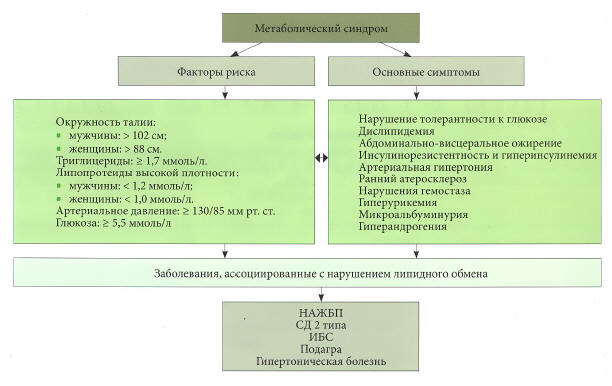
Рис. 1. Основные составляющие метаболического синдрома
Современное понятие НАЖБП охватывает широкий спектр поражений печени и включает две ее основные формы: жировую дистрофию печени и НАСГ. Взаимосвязь патогенеза НЖБП с ИР позволяет считать это заболевание одним из независимых компонентов МС, клиническая значимость которого заключается в значительном прогрессировании атеросклеротического поражения сосудов (рис. 2). В некоторых случаях возможна трансформация НАСГ в цирроз, что требует проведения трансплантации печени. Жировая инфильтрация печеночных клеток лежит в основе жировой дистрофии печени. Морфологическим критерием жировой дистрофии является содержание триглицеридов в печени более 5-10%. При прогрессировании НАСГ в печени выявляются воспалительно-некротические изменения, которые больше напоминают гепатит, вследствие чего при обнаружении подобного поражения печени устанавливается диагноз «НАСГ». В связи с этим большинство исследователей сходятся во мнении, что НАЖБП является печеночной составляющей МС. Снижение чувствительности к инсулину проявляется в жировой, печеночной, мышечной тканях, в надпочечниках. В жировой ткани ИР характеризуется нарушением чувствительности клеток к антилиполитическом действию инсулина, что приводит к накоплению свободных жирных кислот и глицерина, которые выделяются в портальный кровоток поступают в печень и становятся источником формирования атерогенных ЛПНП. Кроме этого, ИР гепатоцитов снижает синтез гликогена и активирует гликогенолиз и глюконеогенез.
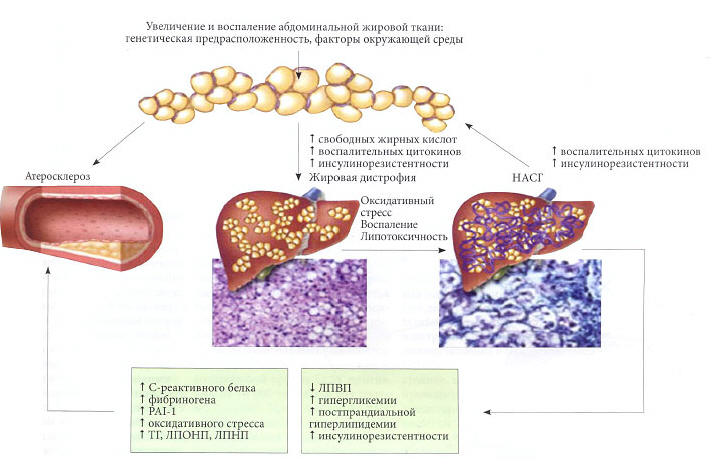
Примечание. PAI-1 — ингибитор активаторов плазминогена-1; ЛПНП и ЛПОНП — липопротеиды низкой и очень низкой плотности.
Рис. 2. Основные формы НАЖБП. Адаптировано по [21]
На рисунке 3 представлена схем «двойного удара» в развитии жировой болезни печени. На ранних стадиях повреждения печени усиливается воздействие TNF-α на гепатоциты, одновременно он инициирует различные клеточные сигналы, повышающие проницаемость митохондриальной мембраны, что приводит к высвобождению реактивных форм кислорода и способствует апоптозу гепатоцитов — «первый удар». Однако болыпинство здоровых гепатоцитов использует потенциально «летальные» сигналы для активации множественных адаптивных разнонаправленных ответов, что позволяет клеткам выжить. «Второй удар» подавляет эту адаптационную способность и также приводит к апоптозу. Даже в том случае, когда адаптация к «первому удару» успешна и гепатоцитам удается выжить, они становятся очень уязвимыми к отрицательным воздействиям. Это приводит к частичной деполяризации внутренней митохондриальной мембраны, и в случае нарушения трансмембранных ионных градиентов происходит некроз клетки.
Лечение
У большинства пациентов НАЖБП характеризуется длительным, стабильным бессимптомным течением. Поэтому, по современным представлениям, специальная фармакотерапия показана только больным с прогрессирующим течением этого заболевания или высоким риском его прогрессии. Ожирение, СД 2 типа, гиперлипидемия — основные состояния, ассоциируемые с развитием НАЖБП. Фармакотерапия НАЖБП представлена в таблице 1. Необходимыми условиями для устранения ИР — главного патогенетического фактора НАЖБП — также являются мероприятия, направленные на снижение массы тела: изменение образа жизни, уменьшение калорийности питания, увеличение двигательной активности. Для лиц с избыточной массой тела и ожирением реально достижимая цель — ее снижение примерно на 7-10% за 6-12 месяцев. Снижение массы тела должно сочетаться с физической активностью умеренной интенсивности (минимум 30 минут в день).
Таблица 1. Фармакотерапия НАЖБП
| Класс лекарственных средств |
Препараты |
| Пероральные сахароснижающие средства | Бигуаниды — метформин (Метфогамма) |
| Антиоксиданты | α-липоевая (тиоктовая) кислота (Тиогамма) |
| Гиполипидемические препараты | Аторвастатин, орлистат |
| Желчегонные средства | Силибинин, силимарин, Хофитол |
| Гепатопротекторы | Урсодезоксихолевая кислота, S-адеметионин |
| Антимикробные препараты | Метронидазол, нифуроксазид, рифаксимин, полимиксин В |
| Пребиотики, пробиотики, эубиотики | Лактулоза (Дюфалак), Эубикор |
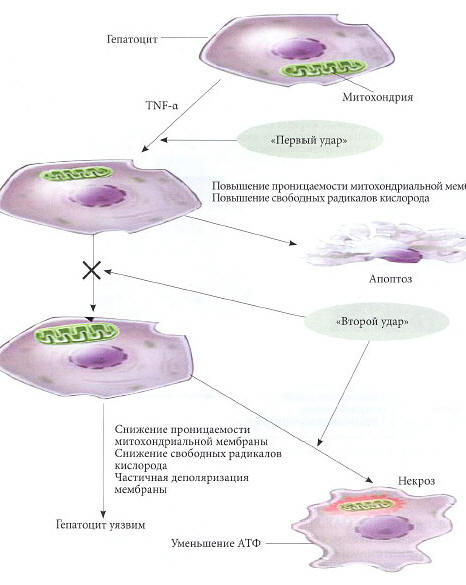
Примечание. TNF-α — фактор некроза опухоли α.
Рис. 3. Схема «двойного удара» в развитии жировой болезни печени. Адаптировано по [21]
Регулярная мышечная активность приводит к метаболическим изменениям, снижающим ИР. Многочисленные данные о влиянии снижения массы тела на состояние печени весьма противоречивы. Показано, что быстрая потеря массы тела закономерно приводит к нарастанию активности воспаления и прогрессии фиброза. В то же время ее снижение на 11-20 кг/год положительно влияет на выраженность стеатоза и воспаления, степень фиброза печени. Безопасной считается потеря массы до 1600 г в неделю для взрослых и до 500 г — для детей. Это достигается при суточном калораже пищи 25 ккал/кг и активных физических упражнениях или применении ингибитора кишечной липазы орлистата. На фоне нормализации биохимических показателей печени отмечается достоверное уменьшение стеатоза, воспаления, повреждения и фиброза печени. Ранняя диагностика НАЖБП и определение факторов риска неблагоприятного течения заболевания являются важными в выборе адекватного метода лечения, способного предотвратить дальнейшее прогрессирование НАЖБП. В связи с этим все пациенты с МС и высокой вероятностью НАЖБП, и особенно НАСГ, должны быть обследованы с целью оценки состояния печени. Наиболее информативным методе оценки состояния печени является биопсия.
Основным в лечении НАЖБП является снижение массы тела за счёт изменения образа жизни, а также лечение ИР и других компонента МС. Предложенные фармакологические препараты для лечени НАЖБП могут быть использованы врачами в своей практике.
Цирроз печени
Цирроз — это конечная стадия хронических заболеваний печени различной этиологии, его главные отличительные черты — узловая перестройка паренхимы и распространенный фиброз. Различают две формы цирроза печени:
■ макроузловой — большинство узелков больше 3 мм в диаметра
■ микроузловой — большинство узелков меньше 3 мм в диаметре
На ранней стадии цирроз проявляется потерей аппетита, тошнотой снижением массы тела, усталостью слабостью, истощением; на стадии декомпенсации — отеком ног и асцитом, гематомами, кожным зудом желтухой, печеночной энцефалопатией.
Лабораторные и инструментальные исследования — компьютерная томография (КТ), ультразвуковое исследование (УЗИ), биопсия печени («золотой стандарт»).
Лечение
Терапия цирроза печени основывается на приеме гепатопротекторов легких слабительных средств, бета-адреноблокаторов (для коррекции портальной артериальной гипертензии), мочегонных средств, уменьшении содержания белка в пище.
Гепатоцеллюлярная карцинома
Является наиболее частой первичной опухолью печени. Ее распространенность в западных страна: составляет 4 случая на 100 000 населения. Большинство больных этим заболеванием умирают в течение 1 года после установления диагноза. Частота встречаемости гепатоцеллюлярной карциномы у пациентов с СД в 4 раза превышает частоту в общей популяции. Вероятная последовательность событий, приводящих возникновению гепатоцеллюлярной карциномы у пациентов с СД, включает гиперинсулинемию, ускоренный липолиз, аккумуляцию липидов в гепатоцитах, оксидативный стресс с формированием избытка свободных радикалов. Результатом оксидативного стресса является повреждение ДНК и некроз гепатоцитов. Восстановление структуры ткани происходит с пролиферацией клеток и фиброзом. Однако в ходе этого процесса велика вероятность возникновения хромосомной нестабильности и появления генетических дефектов, что и предрасполагает к злокачественной трансформации. Важным фактором, участвующим в канцерогенезе, является инсулиноподобный фактор роста 1, который способствует пролиферации клеток, активируя субстрат 1 инсулинового рецептора. В свою очередь, высокая концентрация субстрата 1 инсулинового рецептора оказывает туморостимулирующий эффект за счет усиления пролиферации клеток, в ходе которой происходит потеря части информации ДНК, включая гены, подавляющие опухолевый рост. Больным с высоким риском развития рака печени целесообразно проведение скрининговых исследований и определение маркера опухоли — альфа-фетопротеина (АФП). Цель подобного наблюдения — выявление карциномы на стадии, когда она может быть удалена. Частота проведения исследований должна определяться гистологическим типом опухоли. Скрининговые исследования АФП и УЗИ печени через каждые 6 месяцев необходимо начинать в возрасте 35 лет.
Острая печеночная недостаточность
Острая печеночная недостаточность (ОПН) — это развитие печеночно-клеточной недостаточности с энцефалопатией в течение 8 недель после появления первых признаков при отсутствии поражений печени в анамнезе. ОПН возникает при резком нарушении функции печени, вызванном поражением ткани органа вследствие разнообразных причин. ОПН характеризуется высокой смертностью, обусловленной в основном отеком мозга и инфекционными осложнениями. Частота развития ОПН у пациентов с СД почти в два раза выше, чем в контрольной группе (2,31 против 1,44 на 10 000 человек в год соответственно). При этом риск ОПН остается значительным даже после исключения из анализируемой группы пациентов с заболеваниями печени и подвергавшихся лечению троглитазоном (пероральным гипогликемическим препаратом с доказанной гепатотоксичностью). В то время как механизмы взаимосвязи СД и ОПН остаются неясными, гепатотоксический эффект пероральных сахароснижающих препаратов не вызывает сомнений. При анализе медицинской документации 171 264 пациентов с СД удалось установить, что в 35 случаях (1 на 10 000 человек в год) ОПН не имела других причин, кроме применения инсулина, производных сульфонилмочевины, метформина и троглитазона.
Вторичная гипогликемия, возникающая из-за снижения глюконеогенеза вследствие дефицита гликогена и увеличения циркулирующего уровня инсулина, — характерное для ОПН состояние, требующее интенсивного лечения. Исследование глюкозы крови должно проводиться достаточно часто (например, каждые 4 часа), возникшая гипогликемия эффективно купируется 10% или большей концентрации раствором декстрозы.
Наиболее частыми нарушениями электролитного баланса являются гипомагнезиемия и гипофосфатемия. ОПН — это катаболическое состояние, в связи с чем необходимо проводить зондовое питание для предотвращения истощения. Пациентам с быстротекущей ОПН требуется назначение коллоидов и вазопрессоров (например, норэпинефрина). Невосприимчивая к терапии гипотензия обычно вызвана претерминальной печеночной недостаточностью, сепсисом или панкреатитом, который может осложнить течение ОПН, особенно при передозировке ацетаминофена. Схемы ведения пациентов с ОПН в зависимости от осложнений представлены в таблице 2.
Таблица 2. Схемы ведения пациентов с ОПН в зависимости от осложнений
| Осложнения | Диагностика | Лечение | Комментарий |
| Энцефалопатия | Оценка клинических признаков | L-орнитин-аспартат, лактулоза | Увеличивается эффективность лечения ОПН |
| Отек мозга | Оценка клинических признаков. КТ. Контроль ВЧД | Интубация. Увеличение подъема подголовника кровати на 20-30°. Гипервентиляция. Мониторинг внутричерепного давления. Маннитол. Барбитураты. Гипотермия | Перед интубацией необходим лидокаин. При использовании мониторинга внутричерепного давления риск кровотечений составляет около 5% |
| Инфекция | Наличие лихорадки, лейкоцитоз. Выделение культуры микроорганизмов | Антибиотики. Противогрибковые препараты | Наиболее часто определяются стафилококки и грамотрицательные микроорганизмы |
| Кровотечение | Клинический анализ крови: определение гематокрита | Свежезамороженная плазма. Тромбоциты. Криопреципитат | Протромбиновое время — важный прогностический маркер |
| Метаболические нарушения (гипогликемия, электролиты) | Лабораторные исследования | Поддерживающая терапия | Гипокалиемия и гипофосфатемия встречаются чаще других |
| Гипотензия | Оценка показателей жизненно важных функций | Вазопрессоры | Норэпинефрин |
Коррекция гастроэнтерологических осложнений при СД включает использование препаратов из группы антиоксидантов, к которым относится альфа-липоевая (тиоктовая) кислота (Тиогамма). Тиоктовая (альфа-липоевая) кислота, открытая и изученная в 1948-1952 гг., является неотъемлемой частью клеток организма, высвобождающих энергию аэробным путем. Физиологическое действие альфа-липоевой кислоты многообразно, что в первую очередь связано с ее центральной ролью в дегидрогеназных комплексах, прямо или косвенно влияющих на многие стороны обмена веществ [1]. Препарат Тиогамма:
■ обладает гепатопротективным эффектом, который заключается в стимулировании глюконеогенеза в печени;
■ препятствует процессу накопления липидов в печени;
■ оптимизирует белковый и углеводный обмен;
■ участвует в окислении жирных кислот и ацетата, предупреждает развитие жирового стеатоза печени;
■ подавляет синтез оксида азота гепатоцитами (профилактика и купирование реологических расстройств и сосудистых нарушений).
Тиогамма — лекарственный препарат меглюминовой соли тиоктовой кислоты — выпускается немецкой фармацевтической компанией «Вёрваг Фарма». Тиогамма — единственное лекарственное средство, которое выпускается в форме готового раствора для инфузий. Флакон препарата содержит 600 мг меглюминовой соли тиоктовой кислоты.
Проведение инфузий непосредственно из флакона более удобно и безопасно, что также сокращает время введения, так как не требует предварительного разведения. К каждому флакону прилагается светонепроницаемый пластиковый пакет, который надежно защищает препарат от воздействия солнечного света во время процедуры инфузий. Следует отметить, что только Тиогамма производится в данной форме. При лечении НАЖБП (стеатоз печени) препарат Тиогамма назначают внутривенно в дозе 600 мг (1 флакон Тиогаммы в сутки) в течение 2-3 недель. При выраженных клинико-лабораторных проявлениях НАЖБП (стеатогепатит и цирроз) внутривенные инфузий проводят до 3-4 недель. После окончания инъекционного курса рекомендован прием таблетированной формы препарата Тиогамма по 1 таблетке в день (600 мг) в течение 2-3 месяцев. Тиогамма играет важную роль в утилизации углеводов, белков, липидов, окислении жирных кислот, влияет на основной обмен и потребление кислорода клетками головного мозга, снижает уровень глюкозы и содержание холестерина в крови. Имеются данные о ее способности повышать секреторные возможности (3-клеток под-1 желудочной железы. Кроме того, Тиогамма играет роль антиоксиданта, что очень важно для клинической практики [2].
Основные механизмы действия Тиогаммы
1. Влияние на энергетический метаболизм, обмен глюкозы и липидов:
■ участие в окислительном декарбоксилировании α-кетокислот с активацией цикла Кребса;
■ усиление захвата и утилизации глюкозы клеткой, потребления кислорода;
■ повышение основного обмена;
■ нормализация глюконеогенеза и кетогенеза;
■ торможение образования холестерина.
2. Цитопротективное действие:
■ повышение антиоксидантной активности (прямое и опосредованное через системы витаминов С/Е, цистин/цистеин и глютатионовую систему);
■ стабилизация митохондриальных мембран.
3. Влияние на реактивность организма:
■ стимуляция ретикулоэндотелиальной системы;
■ иммунотропное действие (снижение уровня интерлейкина-1 и TNF-α);
■ противовоспалительная и обезболивающая активность, связанная с антиоксидантным действием.
4. Нейротропные эффекты:
■ стимуляция роста аксонов;
■ положительное влияние на аксональный транспорт;
■ уменьшение вредного влияния свободных радикалов на нервные клетки;
■ нормализация аномального поступления глюкозы к нерву;
■ предупреждение и уменьшение повреждения нервов при экспериментальном диабете.
5. Дезинтоксикационное действие (при отравлении фосфорорганическими соединениями, свинцом, мышьяком, ртутью, сулемой, цианидами, фенотиазидами и др.).
Литература
1. Городецкий В.В. Лечение диабетической полиневропатии и других дистрофически-дегенеративных и воспалительных заболеваний периферической нервной системы метаболическими препаратами: методические рекомендации. М., 2004.
2. Воробьев С.В., Кириченко Д.А., Паленый AM. Препараты Тиогамма и Мильгамма в терапии гастроинтестинальной формы автономной нейропатии при сахарном диабете типа 2 // Врач. 2007. № 11. С. 27-30.
3. Лейтес Ю.Г., Галстян Г.Р., Марченко Е.В. Гастроэнтерологические осложнения сахарного диабета // Consilium Medicum. 2007. № 2.
4. Кособян Е.П., Смирнова О.М. Современные концепции патогенеза неалкогольной жировой болезни печени // Сахарный диабет. 2010. № 1. С. 55-64.
5. Abell T.L., Bernstein R.K., Cutts Т. et al. Treatment of gastroparesis: a multidisciplinary clinical review // Neurogastroenterol. Motil. 2006. Vol. 18 (4). P. 263-283.
6. Adams L.A., Sanderson S., Lindor K.D., Angulo P. The histological course of nonalcoholic fatty liver disease: a longitudinal study of 103 patients with sequential liver biopsies // J. Hepatol. 2005. Vol. 42 (1). P. 132-138.
7. Anand C, Al-Juburi A., Familoni B. et al. Gastric electrical stimulation is safe and effective: a long-term study in patients with drug-refractory gastroparesis in three regional centers // Digestion. 2007. Vol. 75 (2-3). P. 83-89.
8. Angelico E, Burattin M., Alessandri C, del Ben M., Lirussi E. Drugs improving insulin resistance for non-alcoholic fatty liver disease and/or non-alcoholic steatohepatitis // Cochrane Database Syst. Rev. 2007. № 1: CD005166.
9. Angulo P. et al. Non-alcoholic fatty liver disease // N. Engl. J. Med. 2002. Vol. 346 (16). P. 1221-1231.
10. American Gastroenterological Association. American Gastroenterological Association medical position statement: non-alcoholic fatty liver disease // Gastroenterology. 2002. Vol. 123 (5). P. 1702-1704.
11. Bujanda L. The effects of alcohol consumption upon the gastrointestinal tract // Am. J. Gastroenterol. 2000. Vol. 95 (12). P. 3374-3382.
12. Camilleri M. Clinical practice. Diabetic gastroparesis [published correction appears in N. Engl. J. Med. 2007. Vol. 357 (4). P. 427] // N. Engl. J. Med. 2007. Vol. 356 (8). P. 820-829.
13. Degen L., Matzinger D., Merz M. et al. Tegaserod, a 5-HT4 receptor partial agonist, accelerates gastric emptying and gastrointestinal transit in healthy male subjects // Aliment. Pharmacol. Then 2001. Vol. 15 (11). P. 1745-1751.
14. Ebert E.C. Gastrointestinal complications of diabetes mellitus // Dis. Mon. 2005. Vol. 51 (12). P. 620-663.
15. Galligan J.J., Vanner S. Basic and clinical pharmacology of new motility promoting agents // Neurogastroenterol. Motil. 2005. Vol. 17 (5). P. 643-653.
16. Gupte P., Amarapurkar D., Agal S., Baijal R., Kulshrestha P., Pramanik S., Patel N., Madan A., Amarapurkar A., Hafeezunnisa. Non-alcoholic steatohepatitis in type 2 diabetes mellitus // J. Gastroenterol. Hepatol. 2004. № 19. P. 854-858.
17. Jones M.P., Maganti K. A systematic review of surgical therapy for gastro-paresis // Am. J. Gastroenterol. 2003. Vol. 98 (10). P. 2122-2129.
18. Lluch L, AscasoJ.E, Mom E etal. Gastroesophageal reflux in diabetes mellitus // Am. J. Gastroenterol. 1999. Vol. 94 (4). P. 919-924.
19. Parkman H.R., Hasler W.L., Fisher R.S. et al. American Gastroenterological Association technical review on the diagnosis and treatment of gastro-paresis // Gastroenterology. 2004. Vol. 127 (5). P. 1592-1622.
20. Shakil A., Church R.J., Rao S.S. Gastrointestinal Complications of Diabetes // Am. Fam. Physician. 2008. Vol. 15. № 77 (12). P. 1697-1702.
21. Targher G. Non-alcoholic fatty liver disease and cardiovascular disease risk // Curr. Cardio Risk. Rep. 2010. № 4. P. 32-39.
22. Targher G., Bertolini L., Padovani R., Rodella S., Tessari R., Zenari L. et al. Prevalence of non-alcoholic fatty liver disease and its association with cardiovascular disease among Type 2 diabetic patients // Diabetes Care. 2007. Vol. 30. P. 1212-1218.
23. Tilg H., Diehl A.M. Cytokines in alcoholic and nonalcoholic steatohepatitis // N. Engl. J. Med. 2000. Vol. 343. P. 1467-1476.
24. Tolman K.G., Fonseca V, Dalpiaz A., Tan M.H. Spectrum of liver disease in type 2 diabetes and management of patients with diabetes and liver disease // Diabetes Care. 2007. Vol. 30 (3). P. 734-743.
25. Tougas G., Chen Y., Coates G. et al. Standardization of a simplified scintigraphic methodology for the assessment of gastric emptying in a multicenter setting // Am. J. Gastroenterol. 2000. Vol. 95 (1). P. 78-86.
26. Virally-Monod M., Tielmans D., Kevorkian J.P. et al. Chronic diarrhoea and diabetes mellitus: prevalence of small intestinal bacterial overgrowth // Diabetes Metab. 1998. № 24 (6). P. 530-536.
Статья опубликована на сайте http://www.gastroscan.ru
материал MedLinks.ru





