Особенности диагностики аллергии к яду перепончатокрылых насекомых
Содержание статьи
Введение
Инсектная аллергия — одна из актуальных и сложных проблем современной клинической аллергологии. Насекомые (Insecta), являющиеся причиной инсектной аллергии, — это представители наиболее многочисленного по видовому составу подтипа членистоногих (Arthropoda), в настоящее время насчитывающего более миллиона видов [1].
Отряд перепончатокрылых (Hymenoptera) объединяет насекомых, способных к ужалению, и насчитывает более 100 тыс. видов [2, 3].
Для человека значение перепончатокрылых положительно, многие из них являются опылителями растений и естественными регуляторами численности вредных насекомых. Некоторые виды используются для биологической защиты сельскохозяйственных культур и разводятся в промышленных масштабах на биофермах. Очевидно значение медоносных пчел как производителей пищевых (мед), лекарственных (пчелиное молочко, прополис, пчелиный яд) и технических (воск) продуктов [4]. Однако отрицательной стороной является высокая вероятность развития аллергических и других гиперергических реакций при контакте с ними. Наибольшую клиническую значимость представляют реакции на яд перепончатокрылых, что связано с тяжестью и стремительностью развития угрожающих жизни симптомов после ужаления.
Эпидемиология
По существующим эпидемиологическим данным, 56,6–94,5% взрослого населения нашей планеты хотя бы однократно были ужалены представителями отряда Hymenoptera [5]. В России распространенность аллергии к яду насекомых составляет 0,4–8% [6]. В Европе число переживших выраженные местные реакции на ужаления насекомыми составляет 2,4–26,4% населения Европы в целом. Распространенность же системных реакций на ужаления перепончатокрылыми в странах ЕС составляет 0,3–8,9%, в США — 0,5–3,3% общей популяции [7]. По данным исследований, проводимых лабораторией молекулярных механизмов аллергии ФГБУ «ГНЦ Институт иммунологии» ФМБА России, частота системных реакций достигает 5,3% случаев реакций на ужаления [8]. В педиатрической практике, по результатам исследований, распространенность инсектной аллергии среди детей Московского региона составляет 2–6% [9]. Частота смертельных случаев при аллергии к яду перепончатокрылых достигает 0,03–0,48% на 1 млн жителей в год [10].
Диагностика аллергии к яду перепончатокрылых насекомых
Согласно отечественным и зарубежным клиническим рекомендациям диагноз «аллергия к яду перепончатокрылых насекомых» выставляется на основании данных анамнеза и специализированного аллергологического обследования, а именно кожного тестирования, определения специфических IgE и уровня базальной сывороточной триптазы у пациентов с тяжелыми системными реакциями. Диагностический поиск должен проводиться у всех пациентов с перенесенной системной аллергической реакцией после ужаления перепончатокрылыми для выявления сенсибилизации. Дополнительные тесты in vitro проводятся в случае выявления негативных или сомнительных результатов обследования [11]. Диагностические мероприятия при аллергии к яду перепончатокрылых направлены на определение не только этиологического фактора, но и вероятных патогенетических механизмов, что позволяет выбрать наиболее верный лечебный алгоритм. По современным понятиям аллергия к яду перепончатокрылых относится к неатопической IgE-опосредованной гиперчувствительности [12].
Анамнез
Сбор анамнеза является наиболее важным аспектом диагностики в целом и аллергии к яду перепончатокрылых в частности. В большинстве случаев на основании анамнеза удается установить факт аллергической реакции и степень ее тяжести, выявить и оценить потенциальные факторы риска. Основными факторами риска являются: повышенный уровень сывороточной триптазы, мастоцитоз. У больных без диагностированного мастоцитоза, но с повышенным уровнем сывороточной триптазы при укусе перепончатокрылыми регистрируются более тяжелые анафилактические реакции. Сопутствующие сердечно-сосудистые заболевания утяжеляют течение анафилаксии [13]. Применение β-блокаторов и ингибиторов ангиотензинпревращающего фермента (АПФ) также влияет на течение аллергического процесса: β-блокаторы не увеличивают риск системных аллергических реакций, но могут утяжелить их проявления; ингибиторы АПФ могут увеличить частоту системных аллергических реакций, в т. ч. при аллерген-специфической иммунотерапии (АСИТ) [13, 14].
Но наиболее сложной проблемой является установление вида «виновного» насекомого. Многие пациенты не различают пчел, шмелей, ос, полист и шершней, нередко складываются ситуации, что пациент и вовсе не видел ужалившее его насекомое [15]. Частично в таких ситуациях помогают косвенные признаки. Так, пчелы относятся к виду перепончатокрылых, которые всегда оставляют жало в коже жертвы. Шмели заметно крупнее и имеют более интенсивную окраску, чем пчелы. Осы и полисты очень похожи, но имеют различия на стыке грудной клетки и брюшной полости. У ос есть усеченное соединение, в то время как тело полисты более овальной формы. Шершни встречаются реже и являются самыми крупными представителями осиных. Кроме того, при сборе анамнеза следует обратить внимание на информацию о количестве и дате реакции на ужаление, тяжесть симптомов и время, прошедшее между укусом и появлением симптомов.
Кожные тесты
К сожалению, отечественным аллергологам недоступны диагностические аллергены ядов насекомых для проведения кожного тестирования. При этом в Европе и США данные методики распространены как основные диагностические инструменты. Кожные пробы выполняются в виде прик-теста или внутрикожного теста с экстрактом яда по крайней мере через 2 нед. после реакции на укус во избежание возможных ложноотрицательных результатов во время латентного периода [16].
Чувствительность прик-теста ниже, чем внутрикожного теста (до 1,0 мкг/мл), который применяется для подтверждения отрицательного результата прик-теста.
Так, в исследовании у 301 пациента с аллергией к яду ос прик-тест был диагностически значимым в 49% случаев, а комбинация прик-теста и внутрикожного теста идентифицировала аллерген в 94% случаев [17].
Стандартные аллергены перепончатокрылых коммерчески доступны во многих странах, кроме России. Они являются смесями экстрактов яда клинически значимых видов пчел (Apis mellifera), ос (Vespula vulgaris, V. flavopilosa,
V. germanica, V. maculifrons, V. pensylvanica, V. squamosa), а также полист (Polistes annularis, P. exclamans, P. fuscatus, P. metricus). Рекомбинантные аллергены яда перепончатокрылых для кожных проб пока коммерчески недоступны.
Также в ходе многочисленных исследований не выявлено корреляции между тяжестью клинической картины после ужаления и реактивностью кожи [18]. Действительно, резко положительные кожные тесты встречаются у пациентов с легкими локальными реакциями, тогда как почти у 25% пациентов с тяжелыми системными реакциями на ужаление прик-тесты дают отрицательный ответ, а положительный внутрикожный тест наблюдается только при максимальной концентрации аллергена.
Диагностика in vitro
В нашей стране отсутствуют зарегистрированные лечебно-диагностические аллергены ядов перепончатокрылых для кожного тестирования, вследствие чего лабораторная диагностика приобретает ведущую роль.
Общий IgE. Исследование общего IgE, как правило, малоинформативно. Однако R.G. Hamilton сообщает об информативности индекса sIgE/tIgE — отношения уровня специфических иммуноглобулинов класса Е (sIgE) к уровню общего иммуноглобулина класса Е (tIgE). Так, у 54% лиц, сенсибилизированных к яду пчел, соотношение sIgE/tIgE составило >4% [19].
Специфические IgE. Для определения sIgE к аллергенам ядов перепончатокрылых наиболее распространенными и доступными являются метод иммуноферментного анализа (ELISA) и его усовершенствованные современные модификации (хемилюминесцентный и флюоресцентный анализы). Данные иммунологические методики основаны на взаимодействии определенного аллергена с определяемыми sIgE сыворотки крови пациента. Аллерген чаще всего адсорбирован на твердой фазе (полистерол, стрептавидин или целлюлоза), и при взаимодействии с sIgE пациента комплекс аллергена и sIgE соединяется с мечеными анти-IgE. В результате химического взаимодействия изменяются цветовой спектр или свечение, что фиксируется соответствующим регистратором (колориметром, люминометром или флюориметром).
В последние годы для клинической лабораторной диагностики разработана технология определения концентрации sIgE в сыворотке крови человека методом двухстадийного «capture»-варианта иммуноферментного анализа (ИФА) [20]. Отличие данного вида анализа от классических вариантов состоит в том, что для выявления sIgE используется двухстадийная последовательность их связывания. Вначале исследуемые образцы с sIgE инкубируют с растворами биотинилированных аллергенов, поверхность которых покрыта мышиными моноклональными антителами к IgE человека. Если в пробе имеется sIgE, специфичный биотинилированному аллергену, то происходит одновременное связывание IgE с аллергеном и моноклональными антителами к IgE человека. Затем добавляется конъюгат стрептавидина с пероксидазой хрена. Конъюгат стрептавидин-пероксидаза связывается с биотинилированным аллергеном. Далее во время инкубации с раствором хромогена (тетраметилбензидин) в субстратном буфере происходит окрашивание раствора. Интенсивность окраски прямо пропорциональна количеству sIgE.
Преимущество данной технологии по сравнению с классическим ИФА заключается в том, что в отличие от методики связывания аллергена на твердой фазе реакция связывания аллергена и sIgE происходит в жидкой среде, что увеличивает степень доступности аллергена для связи с IgE. Кроме того, данная жидкофазная методика легко адаптируется к автоматизированным системам постановки иммунологических анализов. К примеру, анализаторам Alisei Q.S. не требуются, как в случае с постановкой исследований на твердофазных дисках, специальные вошеры для процедуры промывки, они позволяют измерять оптическую плотность пробы на спектрофотометре при длине волны как 450 нм, так и 405 нм, что повышает точность анализа и расширяет диапазон определяемых концентраций sIgE [20]. Классический ИФА и «capture»-технология определения sIgE имеют наибольшую актуальность для исследовательских и клинических лабораторий с невысокой проходимостью, а также для проведения скрининговых обследований населения ввиду относительной простоты выполнения и невысокой стоимости исследований.
Определение sIgE проводят чаще всего с использованием водно-солевых экстрактов аллергенов. Использование экстрактов аллергенов зачастую приводит к увеличению как ложноположительных результатов из-за присутствия компонентов с перекрестной реактивностью, так и ложноотрицательных — из-за отсутствия или деградации основных аллергенных белков в экстракте. По опубликованным данным, чувствительность этих тестов составляет 60–95%, а специфичность — 30–95% [21].
В настоящее время активно развивающимся направлением лабораторной аллергологии является компонентная, или молекулярная, аллергодиагностика. Развитие и внедрение данного направления обусловлено прежде всего современными достижениями в области изучения точного аллергенного состава, в т. ч. состава различных ядов перепончатокрылых. Например, в яде Apis mellifera исследовано 12 различных аллергенов, в яде ос — 6, а в яде полист —
5 аллергенов. Актуальный и обновляемый аллергенный состав представлен на ресурсах WHO/IUIS Allergen Nomenclature Sub-Committee. Молекулярно-биологические подходы позволили подробно охарактеризовать отдельные молекулы различных ядов. Доказано, что аллергенная активность большинства ядов зависит от их третичной структуры (рис. 1).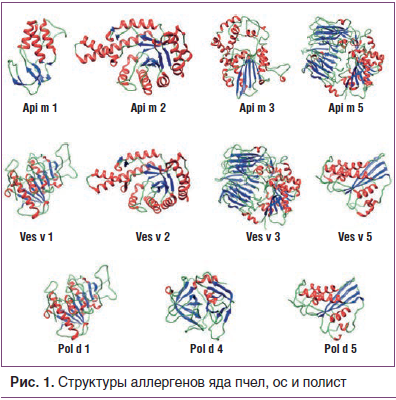
В яде пчел идентифицировано более 100 белков и пептидов [22]. Состав яда подвержен сезонным колебаниям [23]. Молекулярная диагностика позволила провести грань между истинной аллергией и клинически незначимой реактивностью к перекрестным углеводным детерминантам (CCD) [24, 25]. Влияние отдельных молекул на тяжесть симптомов до конца еще не изучена [26]. В то же время доказано, что если в лечебных аллергенах для АСИТ не представлены некоторые молекулы, то эффективность подобной АСИТ будет минимальной в связи с интерференцией IgE-антител к клинически незначимым аллергенам. Это особенно важно в тех случаях, когда пациент не смог однозначно идентифицировать «виновное» насекомое [26]. Правильный диагноз не всегда возможен из-за ограничений кожных тестов.
В последние годы достигнут значительный прогресс в идентификации аллергенов яда ос. Аллергены яда ос включают фосфолипазу A1 (Ves v 1), гиалуронидазу (Ves v 2.0101) и антиген 5 (Ves v 5), белок неизвестной функции, но в значительном количестве содержащийся в яде [27]. Недавно в яде ос была идентифицирована вторая неактивная гиалуронидаза (Ves v 2.0201), несущая инактивирующие мутации в активном участке фермента, и, по-видимому, она является преобладающим аллергеном [25, 28]. Достигнут значительный прогресс в изучении белковых последовательностей минорных аллергенов. Недавно были идентифицированы гены дипептидилпептидазы IV (DPP IV) в яде пчел (Api m 5) и ос (Ves v 3). DPP IV (молекулярный вес 100 кДа) — новый класс гомологичных и перекрестно-реактивных ферментов перепончатокрылых [29]. Кроме того, виллогенонины Api m 12 и Ves v 6 (молекулярный вес 200 кДа) были описаны как новая пара кросс-реактивных паналлергенов яда пчел и ос.
В настоящее время рекомбинантные стратегии позволяют правильно выявить аллергены, лишенные перекрестной реактивности к углеводным детерминан-
там [26]. Кроме того, доказано, что комбинация 6 аллергенов (Api m 1–5, 10) позволила повысить диагностическую чувствительность приблизительно до 95% для пациентов с аллергией к яду пчел. Выявлено, что 74% пациентов сенсибилизированы более чем к одному аллергену [26]. В недавнем исследовании молекулярная диагностика с использованием аллергенов Api m 1,
Api m 2 и Api m 4 выявила высокую распространенность сенсибилизации к Api m 4 среди пациентов с аллергией к яду пчел, у этих пациентов наблюдались системные реакции во время проведения АСИТ с применением яда пчел [30]. Последующее проспективное исследование стратифицировало пациентов с аллергией к яду пчел в соответствии с их sIgE к Api m 4 на 2 группы (0,98 KUA/л, кило-единиц на литр) и подтвердило более высокие уровни системных реакций во время проведения АСИТ в последней группе. Кроме того, эта группа характеризовалась высокой исходной кожной реактивностью, повышенными уровнями sIgE и более стойкими ответами при внутрикожном тестировании во время АСИT [31].
При обследовании пациентов с аллергией на аллерген ос rVes v 6 был найден у 39% пациентов. Диагностическая чувствительность рекомбинантных аллергенов rVes v 5 и rVes v 1 достигает 92–98% [17, 32]. Поскольку rVes v 5 и rVes v 1 являются коммерчески доступными во многих странах, эта комбинация может быть полезной для исключения перекрестной чувствительности к углеводным детерминантам CCD. Тем не менее rVes v 1 и rVes v 5 не смогли диагностировать у 2–8% пациентов с установленной аллергией [32].
Комбинации рекомбинантных антигенов (rVes v 1, 2, 3, 5) могут дополнительно увеличивать чувствительность обычных анализов к яду ос до 100% [33]. Исследование, использующее систему ImmunoCAP, в случае двойной позитивности к яду пчел и ос показало, что ни один из 27 пациентов с убедительным анамнезом анафилаксии к осам, но уровнем sIgE ниже 0,35 МЕ/л не проявил сенсибилизацию к рекомбинантным аллергенам ос rVes v 1, 2, 5 и только у одного пациента выявили сенсибилизацию к rVes v 3, скорее всего, из-за перекрестной реактивности к Api m 5 [34].
У пациентов c подтвержденным анамнезом, но с отрицательными лабораторными тестами добавление рекомбинантного аллергена Ves v 5 к экстракту яда позволило повысить диагностическую значимость теста с 42,1 до 84%
[17, 33, 35]. Этот rVes v 5 на платформе ImmunoCAP был введен для рутинной диагностики с 2012 г. В случае двойной позитивности к яду пчел и ос обнаружение IgE к рекомбинантным аллергенам Api m 1, Ves v 1 и Ves v 5 позволит разграничить первичную сенсибилизацию и перекрестную сенсибилизацию к углеводным детерминантам [32, 35].
Латентная сенсибилизация
Распространенность сенсибилизации (выявляется положительным кожным тестом и/или обнаружением sIgE в сыворотке) у пациентов без предшествующих клинических симптомов достигает 9,3–28,7% [5]. Надежные данные о бессимптомной сенсибилизации к рекомбинантным аллергенам ядов пока не получены. Однако риск развития системных реакций у пациентов с бессимптомной сенсибилизацией невелик (5,3% в недавнем исследовании [36] и 10–15% в более ранних исследованиях [37]). Кроме того, увеличение сывороточных уровней sIgE после ужаления не является показателем риска развития клинически значимой гиперчувствительности.
Наиболее широкое распространение в нашей стране молекулярная аллергодиагностика получила благодаря внедрению непрямой иммунофлуоресценции (технология UniCAP System) с применением отдельных очищенных или полученных рекомбинантным путем аллергенных молекул и скрининговой полуколичественной коммерческой системе анализа ImmunoCAP ISAC (Швеция) [38]. ISAC — технология чипов с иммобилизированными аллергенами и их компонентами на твердой фазе. Однако следует отметить, что в настоящее время активными разработками в области молекулярной аллергологии занимаются и отечественные производители. Так, для диагностики аллергии к яду перепончатокрылых группой российских компаний разработаны и внедрены в клиническую практику аллергенные компоненты яда Apis mellifera k203 nApi m1 Фосфолипаза А2 и i12 nApi m 4 Мелиттин для применения совместно с тест-системой «АллергоИФА- sIgE».
Функциональные тесты in vitro
Определение sIgE к аллергенам ядов перепончатокрылых является важнейшим, но не единственным диагностическим решением. Известно, что содержание IgE в сыворотке не всегда коррелирует с истинным содержанием специфических антител в организме вследствие высокой тропности молекул IgE к эффекторным клеткам. В сенсибилизированном организме IgE могут находиться в периферической крови в свободном виде или фиксироваться на тучных клетках и базофилах. Контакт антитела с клеткой осуществляется путем связывания молекулы IgE с высокоаффинным клеточным мембранным рецептором FcεRI. При перекрестном реагировании FcεRI с IgE и соответствующим аллергеном в клетке запускается каскад биохимических реакций, в результате которых наступает ее активация. При этом происходит дегрануляция клетки с выбросом наружу биологически активных веществ, что вызывает развитие воспалительной реакции и приводит к формированию клинических признаков аллергии.
Дополнительным направлением диагностики является проведение провокационных клеточных тестов in vitro с определением медиаторов аллергического воспаления или маркеров активации и дегрануляции эффекторных клеток. Данные методы позволяют не только более углубленно изучить IgE-опосредованную реактивность, но и выявить другие типы аллергического ответа.
Для оценки реакции клеток-эффекторов на специфический аллерген используются тест активации базофилов и система проточной цитофлуориметрии.
При IgE-специфической дегрануляции базофилов происходит встраивание мембраны гранул в поверхностную мембрану клетки, что отражается в появлении в плазмалемме молекул CD63, а также повышается экспрессия поверхностных активационных молекул CD203c [39]. Добавление аллергена к клеткам крови в условиях in vitro имитирует процессы, происходящие в сенсибилизированном организме, и, пользуясь методом проточной цитофлуориметрии, можно зарегистрировать экспрессию маркеров дегрануляции или активации на базофилах [40].
Анализ содержания CD203c позволяет охарактеризовать интактные и активированные базофилы при IgE-независимом ответе у сенсибилизированных пациентов. Таким образом, данным методом может оцениваться вероятное наличие не-IgE-опосредованной реакции, т. е. активации базофилов и неспецифической либерации медиаторов посредством триггерных механизмов.
Частота встречаемости не-IgE-опосредованной реакции на яд Hymenoptera, по разным источникам, варьирует от 6 до 18%. Так, при обследовании 307 жителей Европы с анамнестическими данными аллергии к яду Hymenoptera
у 99 пациентов были отрицательные кожные тесты, и у 56 из них не выявлены специфические IgE. То есть, вероятнее всего, у 18% (n=307) имеет место не-IgE-опосредованная реактивность [41]. По нашим собственным данным, в группе пациентов (n=55) с анамнестическими данными аллергических реакций к яду перепончатокрылых у 29% больных не обнаружены специфические IgE, а при проведении теста базофильной активации выявлена только слабая экспрессия активационной молекулы CD203c и отсутствие экспрессии CD63. Это позволило предположить у данной группы развитие не-IgE-опосредованной реактивности [42].
Заключение
Молекулярная аллергодиагностика позволяет лучше понять сложность сенсибилизации и перекрестной реактивности при гиперчувствительности к яду насекомых. Кроме того, компонентная аллергодиагностика позволяет идентифицировать биомаркеры, которые могут использоваться для стратификации риска при АСИТ. Знание молекулярного состава различных лечебных аллергенов позволит подобрать препараты для АСИТ в соответствии с индивидуальными профилями сенсибилизации, по принципу персонализированной медицины. Но, несмотря на значительные достижения в области аллергодиагностики, в т. ч. молекулярной, верификация аллергии к яду перепончатокрылых остается не до конца решенной проблемой, требуется дальнейшее совершенствование и более широкое внедрение методов лабораторной диагностики.
Перспективным направлением является совмещение молекулярных и клеточных методов, т. е. использование натуральных и рекомбинантных компонентов аллергенов для стимуляции эффекторных клеток. Также необходима разработка единых унифицированных алгоритмов и протоколов обследования пациентов с аллергией к яду перепончатокрылых.
Информация с rmj.ru