Введение
Рак яичников (РЯ) — одна из наиболее агрессивных опухолей женской репродуктивной системы, ежегодно в России более 7000 женщин умирают от этого заболевания [1]. Заболевание характеризуется хроническим рецидивирующим течением, у большинства пациенток развиваются рецидивы [2]. Несмотря на некоторые успехи в молекулярно-направленной терапии, рецидивы РЯ остаются неизлечимым состоянием, и цели лечения пациенток включают увеличение продолжительности и улучшение качества жизни за счет сдерживания прогрессирования опухолевого процесса и контроля симптомов болезни [3, 4].
«Золотым стандартом» оценки эффективности различных терапевтических опций при злокачественных новообразованиях является показатель общей выживаемости (ОВ). В то же время в ряде случаев оценка ОВ может быть значительно затруднена вследствие разных причин: необходимости более длительного периода наблюдения за пациентками, влияния последующей противоопухолевой терапии или применения иных методов лечения. По этой причине в лечении злокачественных опухолей в настоящее время широко используются так называемые суррогатные конечные точки — маркеры эффективности терапии, основанные на оценке более быстро достижимых показателей, таких как частота объективного ответа (ЧОО), выживаемость без прогрессирования (ВБП) или частота контроля заболевания [5].
Цель исследования: оценка информативности использования различных маркеров эффективности противоопухолевой терапии платинорезистентных рецидивов РЯ.
Содержание статьи
Материал и методы
Для оценки эффективности различных вариантов противоопухолевой терапии платинорезистентных рецидивов РЯ был проведен систематический поиск в базе данных PubMed/MedLine. Отобраны исследования, опубликованные в период с 01.01.2000 по 01.07.2019. Поисковый запрос для экстракции данных включал: (ovarian*[Title] OR OVARIAN NEOPLASMS [MESH]) AND (RESISTANT OR RECURRENT OR PLATINUM-RESISTANT OR REFRACTORY OR PLATINUM-REFRACTORY). Если в опубликованном исследовании результаты применения того или иного агента были представлены в виде двух различных групп, они включались в систематический обзор и последующий метаанализ как самостоятельные исследования.
Краткие критерии включения: 1) пациентки с морфологически верифицированным эпителиальным РЯ с платинорезистентными рецидивами (интервал ≤6 мес.); 2) проведение стандартной платиносодержащей или неплатиновой химиотерапии (ХТ); 3) отсутствие сопутствующей терапии таргетными препаратами, экспериментальными препаратами или высокодозной ХТ; 4) наличие опубликованных данных по частоте достижения объективного ответа и критериев, использованных для оценки (RECIST [6], ВОЗ или методы оценки, основанные на определении динамики онкомаркера CA-125 [7]); 5) наличие данных по ОВ и ВБП. Результаты поиска литературы просмотрены двумя специалистами, исключены повторы, исследования с промежуточными результатами.
Исключались исследования, использовавшие нестандартные или неопределенные критерии платинорезистентности, нестандартные варианты противоопухолевой терапии для рецидивов РЯ, работы без опубликованных данных по ЧОО, а также исследования, посвященные целенаправленному изучению редких гистологических подтипов РЯ, равно как и публикации с описанием клинических случаев, обзорные статьи, доклинические исследования.
Из отобранных исследований проводилась экстракция данных об авторах и годе публикации работы, режиме терапии, использовании платиновых агентов, количестве пациенток, критериях оценки ответа, показателе ЧОО, медиане возраста, линиях ранее проведенной ХТ, проценте пациенток с серозным РЯ, медианах ВБП и ОВ.
Статистический анализ данных проведен при помощи программного обеспечения R и RStudio. Для проведения анализа было использовано arcsin-преобразование исходных данных по ЧОО на терапию, так как при оценке распределения ЧОО, выраженной в процентах, нами было отмечено значительное смещение влево в сторону 0. Преобразование осуществлялось по следующей формуле: _______ arcsin (ЧОО, %) = arcsin √(ЧОО, %) — 0,2854.
Проводился линейный регрессионный анализ для оценки влияния ЧОО на ВБП, ОВ, а также влияния ВБП на ОВ. Каждое исследование включалось в регрессионный анализ в качестве отдельного наблюдения. Расчеты проводились после логарифмического преобразования медиан соответствующих показателей. Относительный вес исследования в регрессионной модели определялся в соответствии с количеством включенных в него пациентов.
Результаты исследования
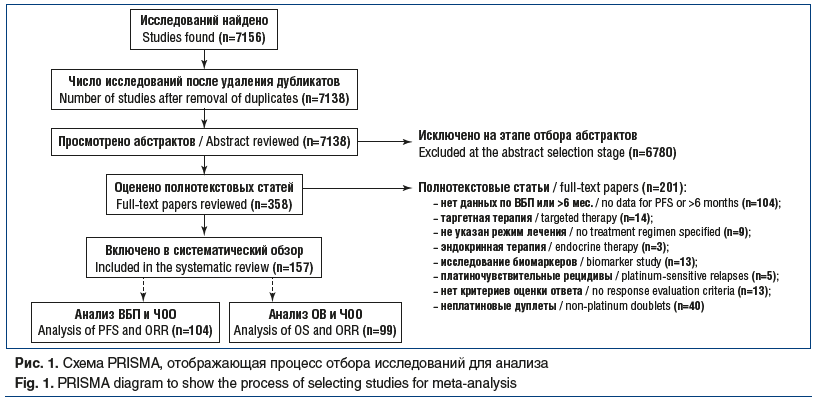
Суммарно нами было проанализировано 7156 исследований, опубликованных за вышеуказанный период времени, для дальнейшего анализа было отобрано 157 исследований, соответствующих критериям включения, из них эффективность платиновой и неплатиновой терапии была оценена в 44 (n=1055) и 113 (n=5272) исследованиях соответственно. На рисунке 1 представлена схема PRISMA (The Preferred Reporting Items for Systematic Reviews and Meta-Analyses) отбора исследований для проведения анализа.
Анализ показателей ЧОО и ВБП
Данные ВБП были представлены в 104 исследованиях, в которые в общей сложности включена 5081 женщина, краткие характеристики исследований суммированы в таблице 1.
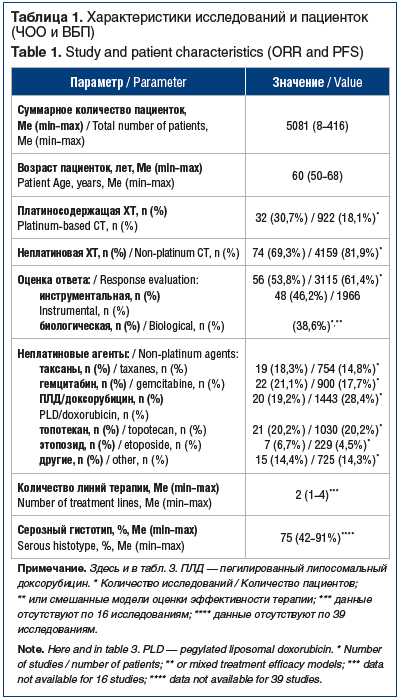
В целом усредненный показатель ЧОО составил 17,2%, на фоне бесплатиновой ХТ — 13,6% (95% ДИ), платиносодержащей ХТ — 36,7% (95% ДИ) (p<0,001). Усредненная медиана ВБП составила 3,68 мес. (95% ДИ 3,40–3,90), для бесплатиновой и платиносодержащей ХТ данный показатель составил 3,38 мес. (95% ДИ 3,18–3,60) и 5,37 мес. (95% ДИ 4,36–6,61) соответственно (p<0,001). Была выявлена достоверная корреляция между ЧОО и ВБП (r=0,62; p<0,001). Для оценки влияния вероятности достижения объективного ответа на ВБП пациенток был проведен регрессионный анализ с поэтапным включением в регрессионную модель различных переменных. По результатам проведенного анализа было выявлено достоверное увеличение медианы ВБП при увеличении ЧОО, репортированной в исследованиях. Было выявлено, что при увеличении показателя ЧОО на каждые 10% медиана ВБП увеличивалась на ≈0,5 мес. (p<0,001), регрессионное уравнение можно представить следующим образом: log(PFSмес.) = 0,87 + arcsin(ORR%) × 1,0065
или (использование нетрансформированных данных)
PFSмес. = 2,91 + ORR% × 5,13.
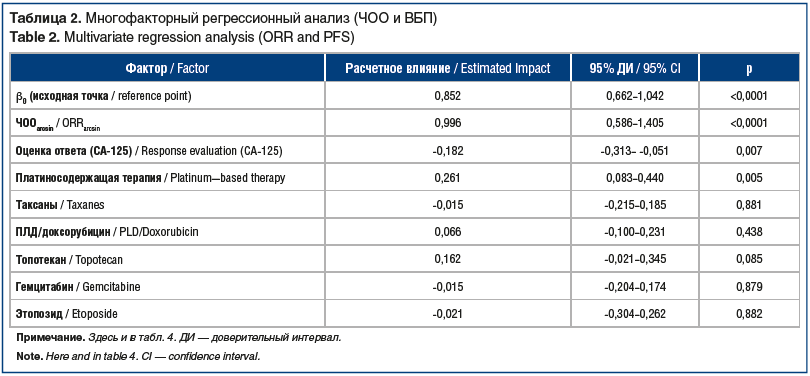
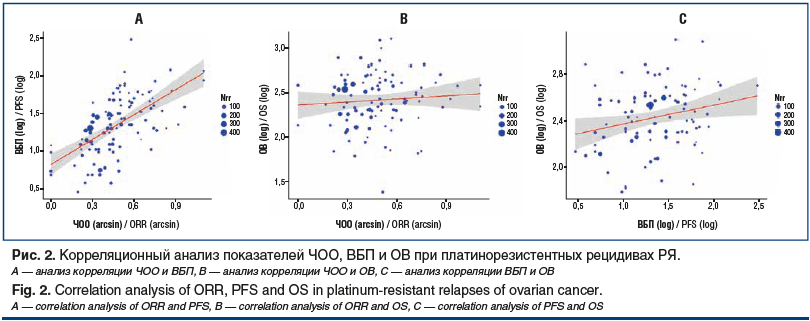
Данные графически отображены на рисунке 2А. Дополнительно был проведен многофакторный линейный регрессионный анализ с изучением влияния других факторов на ВБП (log) пациенток, результаты которого суммированы в таблице 2.
Анализ показателей ЧОО и ОВ
Данные ОВ были представлены в 99 исследованиях, в которые суммарно было включено 5089 пациенток (табл. 3).
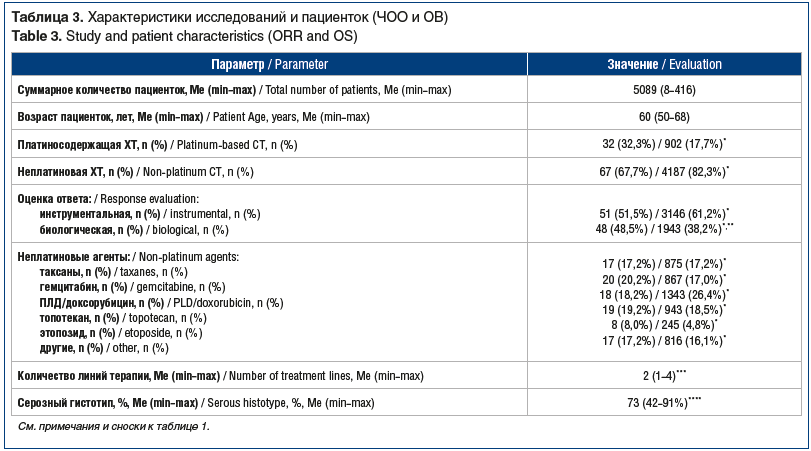
В целом усредненный показатель ОВ составил 11,4 мес. Корреляция между ЧОО и ОВ не отмечена (r=0,07; p=0,45). Для более точной оценки влияния вероятности достижения объективного ответа на ОВ был проведен регрессионный анализ, по результатам которого не было отмечено значимого увеличения медианы ОВ при увеличении ЧОО (p=0,648). Данные графически отображены на рисунке 2B. Дополнительно был проведен многофакторный линейный регрессионный анализ с изучением влияния других факторов на ВБП (log), результаты которого суммированы в таблице 4. Мы не выявили факторы, оказывающие достоверное влияние на ОВ.
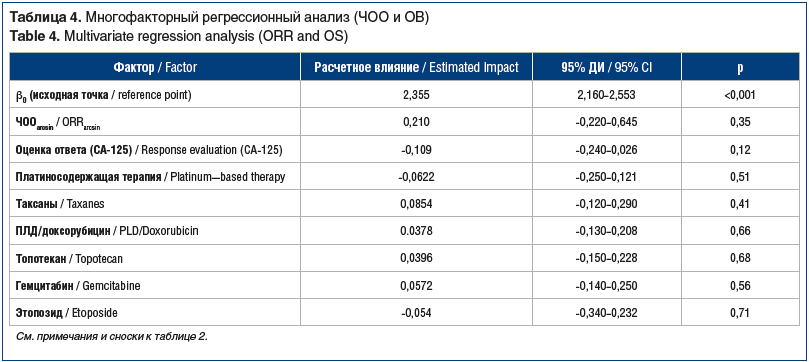
При помощи аналогичной методологии был проведен анализ взаимосвязи ВБП и ОВ (рис. 2C). Отмечено достоверное увеличение ОВ на ≈0,5 мес. за каждый месяц увеличения ВБП (p=0,021), при этом уровень корреляции был низким (r=0,24).
Обсуждение
Представленные результаты систематического обзора и метаанализа посвящены использованию суррогатных биомаркеров при платинорезистентных рецидивах РЯ. Данные литературы по этой проблеме представляются противоречивыми. P.G. Rose et al. [8] в 2010 г. опубликовали результаты анализа 11 исследований (n=407), в которые включались пациентки с платинорезистентными рецидивами РЯ. Авторы исследования не выявили значимой корреляции между ЧОО и ВБП (r=0,477; p=0,0042), ЧОО и ОВ (r=0,404; p=0,086). В 2017 г. M.K. Siddiqui et al. [3] представили результаты более крупного метаанализа по изучению рецидивов РЯ, в который вошли 39 исследований (n=9223). Результаты показали увеличение ВБП на 1,2 мес., ОВ — на 2,83 мес. на каждые 10% повышения ЧОО. При этом из 39 включенных работ всего 10 исследований были посвящены платинорезистентным рецидивам РЯ.
Результаты нашего метаанализа продемонстрировали выраженную корреляцию между непосредственной эффективностью терапии — ЧОО — и показателем ВБП при платинорезистентных рецидивах РЯ. Мы отметили достоверную корреляцию между ВБП и ЧОО, и при регрессионном анализе выявили, что при увеличении показателя ЧОО на каждые 10% медиана ВБП увеличивалась на ≈0,5 мес.; различия были статистически значимыми (p<0,001). Явным преимуществом этой работы является анализ большого количества исследований, посвященных изучению различных терапевтических опций при платинорезистентных рецидивах РЯ — по нашим данным, эта работа является наиболее крупным исследованием в данной области.
При этом стоит подчеркнуть, что в нашей работе оценивалась только эффективность ХТ. Мы целенаправленно исключали исследования с применением каких-либо вариантов таргетной терапии, в первую очередь антиангиогенных препаратов. Кроме того, мы не учитывали влияние наличия мутаций в генах BRCA1/2 и других генетических маркеров на результаты лечения пациенток, которые могут существенным образом влиять на непосредственные и отдаленные результаты лечения [9, 10]. В то же время в контексте отсутствия специального отбора пациенток в исследование в зависимости от BRCA-статуса представляется маловероятным, что данный фактор мог внести существенный дисбаланс.
Отдельно отметим, что в многофакторном линейном регрессионном анализе ВБП была подтверждена превосходящая эффективность платиносодержащей ХТ по сравнению с неплатиновой моно-ХТ (β=0,261; p=0,005), что подтверждает целесообразность повторного назначения платиносодержащей ХТ у пациенток с рецидивами РЯ вне зависимости от сроков их развития. Это согласуется с консенсусом ESMO-ESGO 2019, в соответствии с которым при выборе терапии следует учитывать ряд факторов, включающих токсичность ранее проведенной терапии, наличие противопоказаний к назначению платиновых агентов, необходимость контроля симптомов заболевания и другие критерии [11].
С другой стороны, несмотря на стойкую корреляцию между ЧОО и ВБП, в нашем исследовании не отмечено аналогичной взаимосвязи между ЧОО и ОВ. Именно ОВ считается наиболее важным параметром эффективности терапии. В то же время исходные недостатки дизайна работы — отсутствие сбора данных по предшествующей и последующей терапии, длительности периода наблюдения за пациентками — могут резко снижать информативность анализа ОВ. По этой причине мы можем предположить, что оценка ОВ может быть значительно искажена вследствие ряда систематических ошибок. Следовательно, по нашему мнению, будет корректнее ориентироваться именно на результаты оценки ВБП.
Наше исследование имеет ряд других ограничений и недостатков: в первую очередь ретроспективную природу проводимого сравнения эффективности терапии, нерандомизационный дизайн включенных исследований, а также значительный временной интервал. Как и при проведении любого другого непрямого сравнения, нельзя полностью исключить наличие ряда нераспознанных факторов, которые могли оказать влияние на полученные результаты.
Заключение
Результаты проведенного метаанализа позволяют уточнить роль суррогатных биомаркеров при платинорезистентных рецидивах РЯ. В исследованиях платинорезистентных рецидивов РЯ показатель ЧОО является надежным предиктором ВБП.
Сведения об авторах:
Румянцев Алексей Александрович — к.м.н., старший научный сотрудник онкологического отделения лекарственных методов лечения (химиотерапевтического) № 4 отдела лекарственного лечения НИИ клинической онкологии им. академика РАН и РАМН Н.Н. Трапезникова ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России; 115438, Россия, г. Москва, Каширское ш., д. 23; ORCID iD 0000-0003-4443-9974.
Тюляндина Александра Сергеевна — д.м.н., заведующая отделением лекарственных методов лечения (химиотерапевтического) № 4 отдела лекарственного лечения НИИ клинической онкологии им. академика РАН и РАМН Н.Н. Трапезникова ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России; 115438, Россия, г. Москва, Каширское ш., д. 23; профессор кафедры онкологии института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0002-6104-7473.
Исраелян Эдгар Рудикович — ординатор кафедры онкологии ФДПО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-6666-549X.
Федянин Михаил Юрьевич — д.м.н., старший научный сотрудник онкологического отделения лекарственных методов лечения (химиотерапевтического) № 2 отдела лекарственного лечения НИИ клинической онкологии им. академика РАН и РАМН Н.Н. Трапезникова ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России; 115438, Россия, г. Москва, Каширское ш., д. 23; руководитель химиотерапевтической службы ГБУЗ «ММКЦ «Коммунарка» ДЗМ»; 108814, Россия, г. Москва, пос. Сосенское п. Коммунарка, ул. Сосенский стан, д. 8; научный консультант ФГБУ «НМХЦ им. Н.И. Пирогова» Мин-здрава России; 105203, Россия, г. Москва, ул. Нижняя Первомайская, д. 70; ORCID iD 0000-0001-5615-7806.
Гуторов Сергей Львович — д.м.н., ведущий научный сотрудник онкологического отделения лекарственных методов лечения (химиотерапевтического) № 4 отдела лекарственного лечения НИИ клинической онкологии им. академика РАН и РАМН Н.Н. Трапезникова ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России; 115438, Россия, г. Москва, ш. Каширское, д. 23; ORCID iD 0000-0001-5912-1155.
Тюляндин Сергей Алексеевич — д.м.н., профессор, главный научный сотрудник отделения лекарственных методов лечения (химиотерапевтического) № 2 отдела лекарственного лечения НИИ клинической онкологии им. академика РАН и РАМН Н.Н. Трапезникова ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России; 115438, Россия, г. Москва, Каширское ш., д. 23; ORCID iD 0000-0001-9807-2229.
Контактная информация: Румянцев Алексей Александрович, e-mail: alexeymma@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 15.03.2022.
Поступила после рецензирования 07.04.2022.
Принята в печать 04.05.2022.
About the authors:
Alexey A. Rumyantsev — Dr. Sc. (Med.), Senior Research Associate, Department of Chemotherapy No. 4 of the N.N. Trapeznikov Research Institute of Clinical Oncology, N.N. Blokhin National Medical Research Center of Oncology; 23, Kashirskoe road, Moscow, 115478, Russian Federation; ORCID iD 0000-0003-4443-9974.
Alexandra S. Tyulyandina — Dr. Sc. (Med.), Head of Department of Chemotherapy No. 4 of the N.N. Trapeznikov Research Institute of Clinical Oncology, N.N. Blokhin National Medical Research Center of Oncology; 23, Kashirskoe road, Moscow, 115478, Russian Federation; Professor, Oncology Department of the N.V. Sklifosovskiy Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8 Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0002-6104-7473.
Edgar R. Israelyan — Clinical Resident, Department of Oncology, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-6666-549X.
Mikhail Yu. Fedyanin — Dr. Sc. (Med.), Senior Research Associate, Department of Chemotherapy No. 2 of the N.N. Trapeznikov Research Institute of Clinical Oncology, N.N. Blokhin National Medical Research Center of Oncology; 23, Kashirskoe road, Moscow, 115478, Russian Federation; Head of the Chemotherapy Service, Moscow Clinical Research Center «Kommunarka»; 8, Sosensky stan, Sosenskoye village Kommunarka, Moscow, 108814, Russian Federation; Scientific Consultant, N.I. Pirogov National Medical and Surgical Center; 70, Nizhnyaya Pervomayskaya str., Moscow, 105203, Russian Federation; ORCID iD 0000-0001-5615-7806.
Sergey L. Gutorov — Dr. Sc. (Med.), Leading Research Associate, Department of Chemotherapy No. 4 of the N.N. Trapeznikov Research Institute of Clinical Oncology, N.N. Blokhin National Medical Research Center of Oncology; 23, Kashirskoe road, Moscow, 115478, Russian Federation; ORCID iD 0000-0001-5912-1155.
Sergey A. Tjulandin — Dr. Sc. (Med.), Chief Scientific Associate, Department of Chemotherapy No. 2 of the N.N. Trapeznikov Research Institute of Clinical Oncology, N.N. Blokhin National Medical Research Center of Oncology; 23, Kashirskoe road, Moscow, 115478, Russian Federation; ORCID iD 0000-0001-9807-2229.
Contact information: Alexey A. Rumyantsev, e-mail: alexeymma@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 15.03.2022.
Revised 07.04.2022.
Accepted 04.05.2022.
Информация с rmj.ru
