Введение
Хроническая спонтанная крапивница — заболевание, характеризующееся развитием ежедневных, проходящих в течение 24 ч волдырей и/или ангиоотеков, общей длительностью более 6 нед. [1]. Хроническая спонтанная крапивница диагностируется у 5% взрослого населения [2]. Женщины болеют чаще мужчин, среди детей различия по полу не были выявлены [3]. Около 2/3 пациентов страдают хронической крапивницей больше года, а 1/5 часть — более 5 лет [4].
Главным механизмом возникновения волдырей и ангиоотеков служит дегрануляция тучных клеток с последующим выбросом провоспалительных медиаторов, таких как гистамин, серотонин, интерлейкины, фактор некроза опухоли α, фактор активации тромбоцитов и др. Дегрануляцию вызывает связывание с высокоаффинными рецепторами (FcεRI) иммуноглобулинов: IgE, аутореактивных IgE, аутореактивных IgG к IgE и к FcεRI [5, 6]. Дегрануляцию также могут вызвать компоненты комплемента, некоторые лекарственные средства, физические воздействия и неизвестные механизмы [7].
Для оценки контроля над симптомами крапивницы используют стандартизированные опросники, такие как UCT-тест или UAS-7. UCT-тест состоит из 4 вопросов, ответы на которые оцениваются в баллах от 0 до 4, максимальный балл за 4 вопроса — 16. Итоговые значения считают по сумме баллов за все вопросы, 11 баллов и менее оценивают как отсутствие контроля, с 12 до 15 баллов — как хороший контроль, 16 баллов — как полный контроль [1, 7].
Согласно клиническим рекомендациям по лечению крапивницы на первом этапе лечения используют антигистаминные препараты в стандартных и кратно увеличенных дозировках. На второй ступени, при отсутствии клинического улучшения рекомендовано добавить к лечению генно-инженерный биологический препарат омализумаб [8, 9]. Стандартная дозировка препарата омализумаб — 300 мг п/к 1 раз в 4 нед.[1]
[10]. Длительность лечения в настоящее время не определена, однако, как правило, составляет не менее 6 мес.
Представляем наш опыт применения препарата омализумаб в лечении хронической спонтанной крапивницы.
Содержание статьи
Клиническое наблюдение
Пациент С., 40 лет, впервые поступил в стационар в октябре 2022 г. с жалобами на ежедневные зудящие высыпания сливного характера на коже туловища, рук, ног, лица, гениталий, ладоней и подошв, периодические отеки лица, шеи и век (рис. 1).
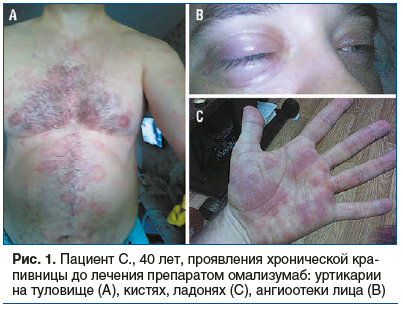
Высыпания впервые появились в 2013 г. Начало заболевание ни с чем не связывал. С тех пор отеки и уртикарии беспокоили ежедневно. Как правило, отеки и уртикарии возникали спонтанно, иногда появлялись в местах сдавления кожи (после ношения тесной обуви, поднятия сумки), отмечал появление уртикарий после бани, пребывания на солнце. В ночное время высыпания сопровождались сильным зудом, что приводило к нарушениям сна, раздражительности, разбитости после пробуждения. С 2014 г. стали беспокоить отеки в местах в/в и в/м введений лекарственных препаратов. В 2014 г. впервые обратился к аллергологу, дерматологу по месту жительства. Ранее аллергическими заболеваниями пациент не страдал. Семейный анамнез не отягощен. При аллергологическом обследовании установлен низкий уровень специфических IgE к пыльцевым аллергенам (полыни, подорожника, 1-й класс), проведен иммунологический скрининг — без особенностей. Консультирован гастроэнтерологом, выставлен диагноз: хронический гастрит, ассоциированный с H. pylori. С 2014 г. с целью купирования симптомов крапивницы ежедневно принимал антигистаминные препараты до 4 таблеток в сутки, системные глюкокортикостероиды (ГКС) (преднизолон 15 мг/сут) без стойкого улучшения состояния. В том же году проведен курс эрадикации H. pylori, профилактический курс противогельминтной терапии (празиквантел), выполнена двусторонняя тонзиллэктомия, проведен курс иммунокорригирующей терапии азоксимера бромидом.
С учетом отсутствия эффекта от проводимой терапии в 2015 г. направлен на обследование и лечение в ФГБУ ГНЦ Институт иммунологии ФМБА России. При обследовании выявлено: общий анализ крови без особенностей, уровень С-реактивного белка повышен до 19 мг/л (норма 0–5 мг/л), при повторном исследовании не изменен — 0 мг/л, антитела к ВИЧ не обнаружены, HBsAg, HCV — отрицательно. Общий IgE 94,5 МЕ/мл, тиреотропный гормон, Т3 и Т4 в норме, антитела к тиреопероксидазе 0,33 МЕ/мл, отрицательно, ревматоидный фактор отрицательный, антистрептолизин О 12 Ед/мл отрицательно, антинуклеарные антитела, LE-клетки, антитела к двуспиральной ДНК не обнаружены. Проведено исследование компонентов комплемента — патологии не выявлено. При иммунологическом исследовании отмечено незначительное увеличение доли CD3+CD8+ T-клеток в процентном и абсолютном значениях. При аллергологическом обследовании была установлена сенсибилизация к полыни, 3-й класс (без клинических проявлений), плесневым грибам — Cladosporium herbarum, 2-й класс, Penicillum notatum, 2-й класс, Alternaria alternate, 1-й класс. Выявлена хроническая цитомегаловирусная инфекция, хроническая герпетическая инфекция (вирус простого герпеса 1-го и 2-го типа), хроническая ВЭБ-инфекция. При проведении провокационных тестов достоверных данных за индуцированный характер крапивницы получено не было. По данным фиброгастродуоденоскопии: гастрит, дуоденогастральный рефлюкс, H. pylori ++++. Осмотрен оториноларингологом: хронический тонзиллит, декомпенсированная форма, рецидивы ангин. Диагностировано тревожно-депрессивное расстройство на фоне тяжелого течения крапивницы.
На основании жалоб, анамнеза, данных обследования был выставлен диагноз: хроническая спонтанная крапивница, тяжелое течение. Пациенту было рекомендовано проведение курса биологической терапии препаратом омализумаб, от которой он отказался (2015 г.)
В дальнейшем заболевание носило непрерывно-рецидивирующий характер, стали ежедневно появляться отеки мягких тканей, максимальные дозы антигистаминных препаратов (до 6 таблеток в сутки) эффекта не давали, от применения системных ГКС пациент отказался ввиду их плохой переносимости (боли в эпигастрии), нарастали тревожно-депрессивные расстройства, нарушение сна. Повторное исследование уровня ингибитора C1-эстеразы в крови и определение функциональной активности С1-эстеразного ингибитора в крови не выявили изменения показателей.
На момент поступления при осмотре диагностированы сливные уртикарии в области спины, шеи, рук. При оценке контроля крапивницы по шкале UCT-теста — 0 баллов (отсутствие контроля). Пациент невротизирован, тревожен. При лабораторном исследовании общий IgE 213 МЕ/мл, эозинофилия крови 210 кл/мкл, общий анализ крови и биохимические показатели без особенностей.
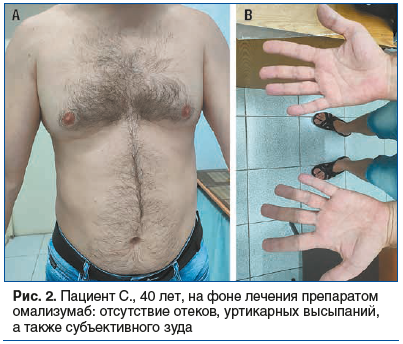
С учетом тяжелого, непрерывно-рецидивирующего течения заболевания, отсутствия эффекта от проводимого лечения в октябре 2022 г. вновь рекомендован курс генно-инженерной терапии препаратом омализумаб, на проведение которого пациент дал согласие. Мы использовали раствор для подкожного введения, дозировка препарата, согласно инструкции, 300 мг п/к 1 раз в 4 нед1. Инициация и все последующие введения препарата проводили в условиях дневного стационара. Осложнений после введения препарата не было. Через 1 нед. после введения препарата отмечено значимое улучшение состояния: уртикарии, зуд не беспокоили, отеков не было, улучшилось настроение и сон, UCT-тест повысился с 0 до 16 баллов (контролируемое течение). Потребности в лекарственной терапии не было. Через 4 мес. после начала терапии на фоне ОРВИ отмечено 2 эпизода высыпаний без ангиоотека, купировавшихся самостоятельно. В дальнейшем высыпаний не наблюдалось. Через 9 мес. терапии высыпания отсутствовали, зуд не беспокоил, ангиоотеков не было (рис. 2). Побочных реакций на введение препарата не отмечалось. Потребность в антигистаминных препаратах не возникала.
Обсуждение
В представленном клиническом наблюдении применение омализумаба привело к довольно быстрому и стойкому ответу на терапию, что согласуется с полученными ранее результатами [10–12]. Несмотря на 9-летний анамнез хронической крапивницы у данного пациента, был получен быстрый результат: в течение 1 нед. после первой инъекции очистилась кожа, снизился зуд, тест контроля над крапивницей UCT составил 16 баллов, т. е. заболевание приобрело контролируемое течение.
Исходный уровень IgE не влияет на дозировку препарата, которая, по данным многих исследований, для достижения оптимального результата составляет 300 мг п/к каждые 4 нед.1 [10, 12]. В то же время отмечен факт более быстрого и полного ответа на биологическую терапию пациентов с изначально более высоким уровнем IgE [11].
Согласно Федеральным клиническим рекомендациям применение препарата омализумаб у пациентов с хронической крапивницей не отменяет назначение антигистаминных препаратов. В представленном наблюдении самостоятельный отказ пациента от применения антигистаминных препаратов не привел к ухудшению, заболевание продолжало оставаться контролируемым.
Заключение
Таким образом, применение омализумаба у пациентов со среднетяжелым и тяжелым течением хронической крапивницы, у которых не удается достигнуть контроля на фоне традиционной фармакотерапии, обеспечивает купирование симптомов заболевания и позволяет достичь длительной ремиссии.
Информация с rmj.ru