Для цитирования: Аляев Ю.Г., Шпоть Е.В., Мосякова К.М. Наблюдение из практики: лечение ангиомиолипомы почки спорадического генеза // РМЖ. 2016. №8. С. 495-497
Представлен клинический случай лечения ангиомиолипомы почки спорадического генеза
Для цитирования. Аляев Ю.Г., Шпоть Е.В., Мосякова К.М. Наблюдение из практики: лечение ангиомиолипомы почки спорадического генеза // РМЖ. 2016. No 8. С. 495–497.
Введение
На сегодняшний день существуют различные виды лечения ангиомиолипомы (АМЛ) почки: хирургическое – резекция почки, нефрэктомия, а также малоинвазивные методы, включающие ангиоэмболизацию почечных сосудов, крио- и радиочастотную абляцию, лапароскопическую резекцию, нефрэктомию, и консервативное лечение. Хирургическое лечение (резекция почки или нефрэктомия) показано больным с крупными опухолями, когда риск разрыва АМЛ и забрюшинного кровотечения очень высок. Другим показанием к хирургическому лечению являются клинические проявления или интенсивный рост опухоли. Необходимо отметить, что лапароскопическая резекция почки по поводу АМЛ требует более деликатной работы, нежели при почечно-клеточном раке, в связи с высоким риском разрыва опухоли интраоперационно. Повреждение ангиомиоматозного узла до пережатия кровотока может привести к массивному внутреннему кровотечению, а грубые, поспешные манипуляции при мобилизации опухоли – к нарушению целостности капсулы, что снижает радикальность данного метода и повышает риск рецидива. Несмотря на немалые технические сложности, лапароскопическая резекция почки ведет к сохранению функциональной паренхимы почки, менее агрессивна, сопровождается меньшей частотой осложнений и легче переносится пациентами, однако при множественном характере образований не всегда является целесообразным выбором лечения данной группы пациентов. Имеются сведения о медикаментозном лечении АМЛ, ассоциированных с туберозным склерозом (ТС), генетически детерминированным заболеванием, характеризующимся поражением нервной системы, кожи и наличием доброкачественных опухолей (гамартом) в различных органах. Food and Drug Administration (Управление по контролю за продуктами и лекарствами, США) разрешило применять для лечения АМЛ, ассоциированной с ТС, таргетный препарат эверолимус – ингибитор mTOR. В 2012 г. были представлены результаты III фазы международного проспективного рандомизированного двойного слепого плацебо-контролируемого исследования по применению mTOR-ингибитора эверолимуса у больных с ТС. В исследование были включены 118 пациентов с ТС в возрасте 3–34 лет. Пациенты рандомизированы на 2 группы: с назначением эверолимуса (N=79) и плацебо (n=39). На 24-й неделе исследования в группе эверолимуса у 54,9% пациентов отмечено уменьшение АМЛ в размерах, в группе плацебо изменений не наблюдалось. По окончании лечения в группе эверолимуса и в группе плацебо улучшение наступило у 80,3 и 3,0% больных соответственно. У 41,8% больных в 1-й группе зарегистрировано уменьшение размеров опухоли, которое сохранялось как минимум 5 мес [1]. Уменьшение АМЛ более чем на 50% от начального уровня произошло только у больных, принимающих эверолимус. Среди пациентов с уменьшением опухоли более чем на 50% на 12-й и 24-й неделе лечения эверолимусом редукция составила 56,5 и 78,3% соответственно [1].
За 40 мес у 56% больных в группе эверолимуса зарегистрировано уменьшение размеров опухоли. Уменьшение АМЛ более чем на 50% от начального уровня произошло только у больных, принимающих эверолимус, – 63% пациентов. Наиболее частым побочным проявлением был назофарингит – у 45% исследуемых [2].
Клиническое наблюдение
Пациент Б., 23 года. И/б № 48377/2015 (с 05.10.15 по 14.10.15).
Диагноз: множественные ангиомиолипомы почек.
Клинические проявления заболевания: периодически возникающая тянущая боль в поясничной области слева.
Краткие данные анамнеза: при профилактическом обследовании по месту жительства в марте 2014 г. по данным УЗИ и мультиспиральной компьютерной томографии (МСКТ) с контрастированием выявлены множественные АМЛ обеих почек (максимальный размер образования левой почки – 60×45 мм, правой – 60×14 мм). При генетическом исследовании крови выявлена мутация в четвертом экзоне гена TSC2: с.С32ОA:p.A1O7Д. Состояние расценено как туберозный склероз (множественные АМЛ обеих почек). Консультирован в клинике урологии Первого МГМУ им. И.М. Сеченова, госпитализирован для обследования и определения дальнейшей тактики лечения.
При поступлении: состояние удовлетворительное, температура тела нормальная, кожные покровы и слизистые бледно-розовой окраски. Пульс 60 уд/мин, удовлетворительного наполнения, АД – 130/80 мм рт.ст. Живот при пальпации мягкий, безболезненный. Почки не пальпируются. Симптом поколачивания отрицательный с обеих сторон. Мочеиспускание безболезненное. Моча визуально не изменена.
Данные лабораторных исследований, функциональное состояние почек
Общий анализ крови: лейкоциты – 4,9×109/л, эритроциты – 4,61×1012/л, Hb – 133 г/л, СОЭ – 9 мм/ч. Биохимический анализ крови: азот мочевины – 4,6 ммоль/л, креатинин – 0,56 мг/дл, глюкоза – 4,6 ммоль/л.
Коагулограмма: активированное частичное тромбопластиновое время (нормализованное отношение) – 1,1, протромбиновый индекс по Квику –104%, фибриноген – 4,09 г/л.
Анализ мочи: рH – 5,0, лейкоциты – 0–1 в п/зр, эритроциты – 0 в п/зр.
При УЗИ: правая почка с четким, неровным контуром, размерами 115×56 мм. Паренхима толщиной до 18 мм, однородная. Чашечно-лоханочная система не расширена. В проекции среднего сегмента визуализируется объемное гиперэхогенное образование без акустической тени размерами 35×30 мм. Подвижность почки сохранена.
Левая почка с четким, ровным контуром, размерами 112×54 мм. Паренхима толщиной до 18 мм, однородная. Чашечно-лоханочная система не расширена. Подвижность почки сохранена.
В проекции среднего сегмента визуализируется объемное гиперэхогенное образование без акустической тени размерами 50×45 мм. Лимфатические узлы забрюшинного пространства не увеличены. Признаков тромбоза почечных вен и нижней полой вены не выявлено.
Мочевой пузырь с четким ровным контуром. Толщина стенки 3 мм. Содержимое анэхогенное. Патологических включений не обнаружено. Остаточной мочи нет.
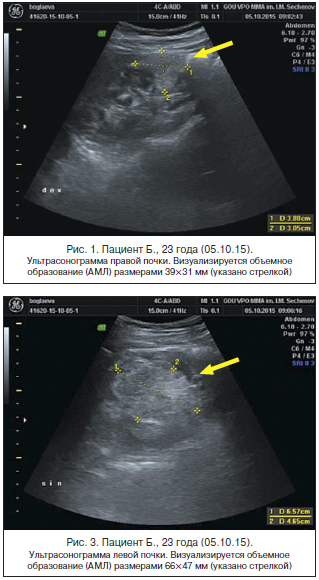
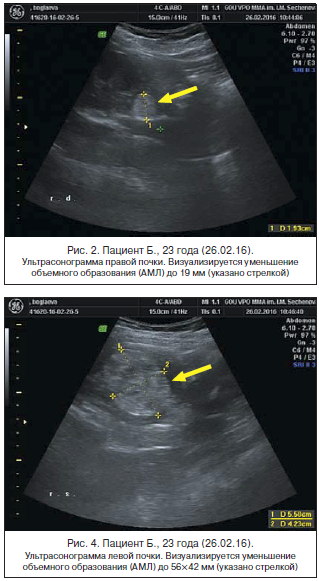
Пациенту по поводу множественных АМЛ почек проводится лечение препаратом эверолимус 10 мг/сут (1 упаковка в месяц по 10 мг) с июля 2015 г. Переносимость препарата удовлетворительная. В начале лечения пациент предъявлял жалобы на стоматит, лечение которого проводилось местно с положительным эффектом. При контрольном обследовании отмечается положительная динамика. По данным УЗИ и МСКТ с контрастированием, субкапсулярно в правой почке определяются АМЛ размерами от 2 мм до 18×22 мм (первоначальные размеры образования – 39×31 мм) (рис. 1, 2). В левой почке, деформируя синус, с линейным тяжем в центральной зоне визуализируется АМЛ размерами 56×42 мм (размеры опухоли от октября 2015 г. – 66×47 мм) (рис. 3, 4). В контрольных анализах крови – без существенных отклонений от нормы.
Заключение
У пациента, принимающего эверолимус 10 мг/сут в течение 8 мес., зарегистрировано уменьшение размеров образований. По данным УЗИ органов мочеполовой системы и МСКТ органов брюшной полости с контрастированием выявлено уменьшение АМЛ обеих почек в среднем на 48,1%. Единственным нежелательным побочным эффектом был стоматит, лечение которого проводилось местно с положительным результатом.
Таким образом, медикаментозное лечение АМЛ приводит к уменьшению опухоли до параметров, при которых риск разрыва снижается и соответственно исчезает необходимость проводить хирургическое лечение, или по крайней мере позволяет подготовить пациента к малоинвазивному хирургическому лечению (крио- и радиочастотной абляции или лапароскопической резекции), при котором размер опухолевого узла является определяющим фактором.
Литература
1. Michael Frost, Klemens Budde, J. Chris Kingswood et al. ЕXIST-2 Examining everolimus in a study of TSC.
2. Bissler J.J. Urol. 2015. Vol. 193(4S). e763(abs.PD35-10).
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
Предыдущая статья
Следующая статья
материал с сайта https://www.rmj.ru/