Введение
Геморрагический синдром является одним из наиболее грозных патологических состояний в неонатологии и педиатрии, учитывая потенциально высокий риск развития осложнений, что в ряде случаев может приводить к неблагоприятному исходу [1–5].
Витамин К: физиологическая роль в гемостазе и патогенез приобретенной коагулопатии при его дефиците у новорожденных и младенцев
Особое место среди различных геморрагических нарушений у детей занимает коагулопатия, развивающаяся из-за дефицита витамина К. При этом необходимо подчеркнуть, что в основе этого лежат различные этиологические факторы, что во многом и определяет время манифестации геморрагического синдрома у детей. В то же время, независимо от причины дефицита витамина К в организме детей, формирующаяся при этом коагулопатия имеет единый патогенез. Это обусловлено тем, что одной из многочисленных биологических ролей витамина К (нем.: Koagulations vitamin — витамин коагуляции) в организме является его участие в γ-карбоксилировании остатков глутаминовой кислоты концевых фрагментов витамин К-зависимых факторов гемостаза. К последним относятся такие факторы свертывания, как: протромбин — фактор II, проконвертин — фактор VII, антигемофильный глобулин В — фактор IX, фактор Стюарта — Прауэра — фактор Х, а также антикоагулянтные белки С и S. Витамин К является кофактором γ-глутамилкарбоксилазы, осуществляющей γ-карбоксилирование всех этих факторов. В результате этой ферментативной реакции во II, VII, IX и Х факторах свертывания крови создаются высокоаффинные сайты связывания для кальция, что обусловливает их функциональную активность и обеспечивает адекватное участие в процессах гемостаза. В тех же случаях, когда в организме развивается недостаток витамина К, нарушаются процессы γ-карбоксилирования, в связи с чем не происходит активации витамин К-зависимых факторов свертывания [6–9]. При этом неактивные факторы свертывания II, VII, IX, X (их принято обозначать факторами PIVKA — Protein Induced by Vitamin K Absence or Antagonism) не способны обеспечить нормальный плазменный гемостаз, что приводит к развитию коагулопатии. Учитывая, что в основе данного варианта коагулопатии лежит глубокая недостаточность витамина К, ее принято обозначать термином «витамин К-дефицитная коагулопатия» (ВКДК) [10–14]. Ключевые моменты участия витамина К в процессах активации II, VII, IX, X факторов свертывания крови, причины дефицита указанного витамина у новорожденных и младенцев, а также патогенез ВКДК, развивающейся при этом, схематично представлены на рисунке 1.
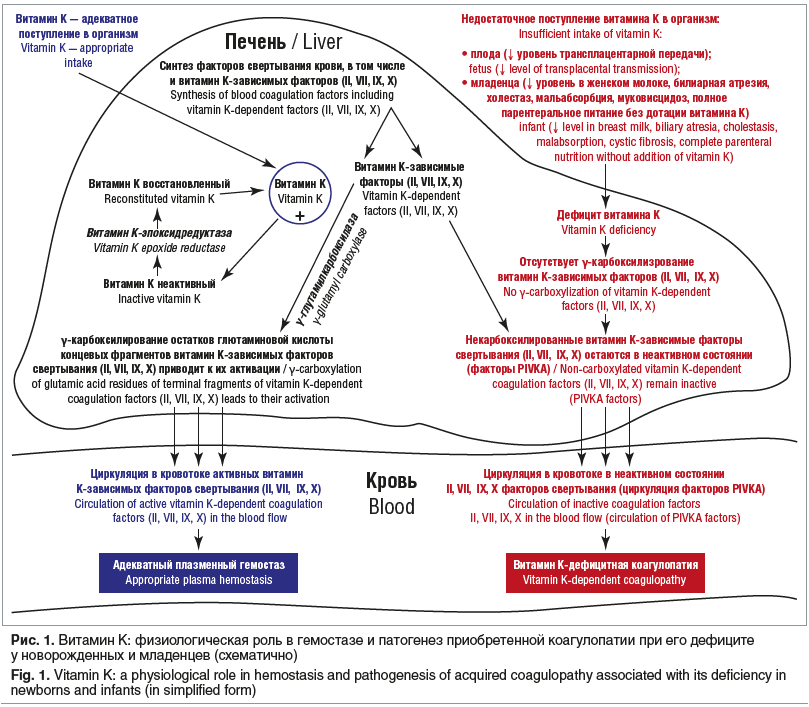
Содержание статьи
Причины ВКДК у новорожденных и младенцев
Следует отметить, что в основе ВКДК у детей лежат различные причины, часть которых имеют четкие возрастные особенности. Так, только в ранний неонатальный период ВКДК обусловлена физиологически ограниченным трансплацентарным поступлением витамина К от матери, что приводит к развитию ранней и классической форм геморрагической болезни новорожденного. Антенатальные геморрагические нарушения и ранняя (в первые часы и сутки жизни) манифестация кровоточивости у новорожденного ребенка могут быть обусловлены также пренатально развившимся дефицитом витамина К из-за приема матерью антагонистов витамина К (производные кумарина, индандиона) [1, 2, 5, 11–13, 15–17]. В свою очередь, только у детей первых месяцев жизни, находящихся исключительно на грудном вскармливании, из-за критически малого содержания витамина К в женском молоке может развиться так называемая поздняя геморрагическая болезнь новорожденного (ГрБН) [4, 11–13, 17–20]. В тех же случаях, когда дефицит витамина К обусловлен нарушением его кишечного всасывания, развитие ВКДК не зависит ни от возраста, ни от характера вскармливания. Так, если у ребенка имеются синдром мальабсорбции, муковисцидоз или различные по генезу патологические состояния, приводящие к нарушению поступления желчи в кишечник (билиарная атрезия, внутрипеченочный холестаз при различных наследственных поражениях печени и метаболических синдромах и др.), то существенно снижается всасывание жирорастворимых веществ, к которым относится и витамин К [1, 2, 5, 13, 17].
Учитывая, что витамин К, в отличие от других жирорастворимых витаминов, практически не накапливается в тканях, глубокий его дефицит в условиях недостаточного поступления с пищей или недостаточного всасывания в кишечнике может сформироваться в течение 1–2 нед. При этом особо следует отметить, что катастрофически быстро дефицит витамина К развивается в ранний неонатальный период. Это обусловлено исходно низким уровнем витамина К в организме новорожденного из-за физиологически ограниченного трансплацентарного его перехода от матери, что усугубляется недостаточным поступлением указанного витамина с пищей в первые дни жизни ребенка (из-за низкого содержания в женском молоке и малого объема грудного молока в период становления лактации), а также транзиторным отсутствием эндогенного синтеза витамина К кишечной микрофлорой (этот процесс сформируется у ребенка только к 4–6-му месяцу жизни и то при условии нормального становления микробиоценоза кишечника). В результате этого глубокий дефицит витамина К в организме ребенка после рождения может развиться очень быстро — от нескольких часов до нескольких дней, — что и определяет высокий риск ВКДК в ранний неонатальный период [1, 2, 5, 13]. Геморрагический синдром у новорожденных детей, обусловленный ВКДК, в Международной классификации болезней и проблем, связанных со здоровьем, 10-го пересмотра (МКБ-10) нозологически рубрицируется как «Р53 Геморрагическая болезнь плода и новорожденного»[1]. При этом на практике ВКДК с клинической симптоматикой, появившейся в первые сутки жизни, принято называть ранней формой ГрБН, а манифестацию заболевания в последующие 2–7 сут жизни — классической формой ГрБН [1, 2, 13].
Клинические проявления ВКДК
Клинически ВКДК проявляется повышенной кровоточивостью слизистых (носовые, желудочно-кишечные и легочные кровотечения) и/или кровоизлияниями в слизистые, кровоточивостью из мест инъекций и хирургических вмешательств, кожными геморрагическими симптомами (петехии, экхимозы), гематомами, в том числе и небольшими подкожными гематомами по типу «нодулярной пурпуры», а в тяжелых случаях — внутричерепными кровоизлияниями и кровоизлияниями во внутренние органы [1, 2, 4, 5, 11–13, 21–25]. Некоторые авторы указывают на возрастные особенности геморрагического синдрома, развивающегося при дефиците витамина К. При этом обращается внимание на то, что у детей раннего неонатального периода клинические симптомы ВКДК чаще представлены кожным геморрагическим синдромом, кровоточивостью пупочной ранки, носовыми, легочными и желудочно-кишечными кровотечениями, в то время как для детей более старшего возраста в дебюте заболевания более характерны внутричерепные кровоизлияния [13, 25]. Однако мы считаем необходимым обратить внимание на другие возможные причины указанного феномена. Так, учитывая, что новорожденный ребенок в течение первых дней после рождения, как правило, находится под постоянным наблюдением неонатолога, то становится понятно, что даже минимальные геморрагические проявления будут своевременно выявлены, их причины уточнены, а адекватная терапия незамедлительно проведена. Все это позволяет своевременно устранить дальнейшее прогрессирование дефицита витамина К, что предупреждает развитие тяжелых форм заболевания, в том числе и манифестацию в виде внутричерепного кровоизлияния. Однако после выписки из роддома ребенок осматривается педиатром значительно реже, только в декретируемые сроки. А родители, даже если и отмечают так называемые малые геморрагические проявления ВКДК (появление скудного кровянистого отделяемого при туалете носовых ходов, кровоточивость пупочной ранки, единичные геморрагические элементы на коже), в подавляющем большинстве не придают этому значения и не обращаются за медицинской помощью. Необходимо подчеркнуть и тот факт, что в ряде случаев указанные симптомы пропускаются и врачами-педиатрами. При этом в целом, по нашим данным, в большинстве случаев ВКДК с внутричерепными кровоизлияниями имели место пропуск или недооценка малых геморрагических проявлений, которые отмечались еще до развития тяжелых форм заболевания [26]. Следует подчеркнуть, что это согласуется с результатами исследований других авторов, которые также отмечают, что у многих детей внутричерепным кровоизлияниям предшествовали различные малые геморрагические симптомы [13, 27].
Геморрагическая болезнь новорожденного: дискуссионные вопросы
После того как стало ясно, что причиной ГрБН является дефицит витамина К, в повседневную практику было внедрено обязательное профилактическое введение витамина К в первые часы жизни всем детям, не имеющим противопоказаний. Благодаря этому удалось добиться значительного, более чем в 100 раз, снижения частоты ГрБН [1, 2, 5, 13, 15]. Однако дальнейшие наблюдения показали, что однократное введение новорожденным витамина К сразу после рождения не предупреждает развитие ВКДК в последующие недели и месяцы жизни. При этом геморрагический синдром из-за дефицита витамина К, клинически проявившийся у младенцев после 7-х суток жизни, на практике стали называть поздней формой ГрБН (синонимы: поздняя ГрБН, ГрБН с поздней манифестацией). Особо при этом следует отметить, что, несмотря на единый патогенез (дефицит витамина К → нарушение γ-карбоксилирования остатков глутаминовой кислоты концевых фрагментов II, VII, IX, X факторов свертывания крови → накопление в плазме неактивных II, VII, IX, X факторов свертывания (PIVKA) → ВКДК) всех форм ГрБН, в основе поздней ГрБН лежат причины, принципиально отличающиеся от этиологических факторов ранней и классической ГрБН. Так, установлено, что основными причинами ГрБН с поздней манифестацией являются вскармливание ребенка исключительно женским молоком, билиарная атрезия, наследственные заболевания печени с холестазом, а также различные нарушения обмена веществ с внутрипеченочным холестазом, дефицит α1-антитрипсина, муковисцидоз, синдром мальабсорбции, полное парентеральное питание и др. [1, 2, 5, 13, 17–21, 25–27]. При этом попытка на практике объединить, без учета этиологии и провоцирующих факторов, все варианты ВКДК, развившиеся как в неонатальный, так и в постнеонатальный период, в одну нозологическую единицу под названием ГрБН, привело к существенной терминологической путанице. Так, ранее нами при анонимном анкетировании 348 врачей-педиатров было установлено, что подавляющее большинство респондентов не могли дать корректных ответов на вопросы о том, что такое поздняя ГрБН, чем она отличается от ранней и классической форм и каковы ее диагностические критерии [20]. Кроме этого, 2/3 анкетируемых считали, что витамин К-дефицитные состояния развиваются только у новорожденных детей и не встречаются в постнеонатальном периоде. Особого внимания заслуживает тот факт, что практически у 100% опрошенных имела место недооценка этиологического значения исключительно грудного вскармливания в развитии ВКДК у детей первых недель и месяцев жизни. Также в подавляющем большинстве случаев респонденты не были информированы о высокой профилактической эффективности дополнительного назначения витамина К1 (фитоменадиона) в виде перорального приема для предупреждения ВКДК у детей, вскармливаемых исключительно женским молоком [20].
Все это стало основанием поддержать профессора Д.О. Иванова, предложившего пересмотреть классификацию ГрБН, используемую в настоящее время на практике [12]. Так, ранее нами было предложено использовать термин «геморрагическая болезнь новорожденного» исключительно для обозначения ранней и классической форм ВКДК [20, 26]. В качестве аргумента нами был использован тезис о том, что ранний неонатальный период четко ограничен первыми 168 часами жизни, и поэтому применять термин «геморрагическая болезнь новорожденного» у детей в возрасте старше 7 дней некорректно. Это четко согласуется с МКБ-10, в которой ГрБН представлена в разделе XVI «Отдельные состояния, возникающие в перинатальном периоде (P00-P96)»1. Следует при этом подчеркнуть, что временные рамки перинатального периода также ограничены первыми 168 часами постнатальной жизни. В связи с этим, учитывая существенные различия в причинах развития ВКДК в ранний неонатальный период и в последующие периоды младенчества, геморрагический синдром, обусловленный дефицитом витамина К и развившийся у детей старше 7 сут жизни, целесообразно рубрицировать как «D68.4 Приобретенный дефицит фактора свертывания» в разделе Нарушения свертываемости крови, пурпура и другие геморрагические состояния (D65–D69)»1. Указанный подход позволит быстрее переломить привычные, но ошибочные представления о том, что развитие у детей дефицита витамина К в разные возрастные периоды имеет одни и те же причины и обусловлено исключительно перинатальными факторами. При этом на практике необходимо как можно быстрее уходить от обобщенного термина «поздняя геморрагическая болезнь новорожденного». Целесообразно при этом использовать нозологический принцип верификации различных по этиологии вариантов ВКДК, развившихся в постнеонатальный период. Так, например, геморрагические нарушения из-за дефицита витамина К у ребенка, находящегося исключительно на грудном вскармливании и не имеющего других причин для развития ВКДК, рубрицируемые под шифром «Приобретенный дефицит факторов свертывания вследствие недостаточности витамина К (D68.4»), четко высвечивают проблему, которой в отечественной педиатрической практике по-прежнему не уделяют должного внимания. Это определило необходимость включения указанных вопросов в образовательные программы проводимых нами циклов повышения квалификации врачей-педиатров и неонатологов, а также активно освещать результаты собственных исследований на страницах профессиональных изданий [20, 26]. При этом наш опыт показывает, что наиболее высокий образовательный эффект достигается в тех случаях, когда теоретические вопросы разбираются в тесной привязке с клиническими примерами.
Разбор клинических наблюдений. Авторы обращают внимание на то, что неотложная помощь при ВКДК в представленных случаях включала применение витамина К3 (менадион натрия бисульфит), так как на тот момент в России еще не был зарегистрирован более эффективный препарат — витамин К1 (фитоменадион).
Клиническое наблюдение 1
Мальчик Г. (возраст 1 мес. 9 дней) доставлен бригадой скорой помощи в ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ», в состоянии средней тяжести с жалобами на повышение температуры тела до 39 °С, отсутствие эффекта от применения антипиретиков (ибупрофен per os, парацетамол per os), затруднение носового дыхания, насморк.
Анамнез жизни. Ребенок от 1-й нормально протекавшей беременности. Роды I, в срок, самостоятельные, в головном предлежании, родился с массой 3700 г, длиной тела 52 см. Закричал сразу, оценка по шкале Апгар 9/10. К груди приложен сразу после рождения, грудь взял активно. Витамин К3 (менадиона натрий бисульфит) введен в/м в первые часы жизни. Против гепатита В и туберкулеза вакцинирован в роддоме, выписан под амбулаторное наблюдение на 4-е сутки жизни. Неонатальный период протекал без осложнений. Находится исключительно на грудном вскармливании с рождения. Лактация достаточная, прибавка массы тела за 1-й месяц жизни — 830 г.
Анамнез заболевания: болеет 1 день, когда появились: повышение температуры тела до 39 °С, затруднение носового дыхания, насморк. В семье есть больные ОРВИ. Обратились к участковому врачу-педиатру, который диагностировал ОРВИ и назначил рекомбинантный интерферон α-2b (интраназально) и симптоматическую терапию (антипиретик — ибупрофен в разовой дозе 10 мг/кг, топический деконгестант — оксиметазолин 0,01%, туалет носовых ходов с использованием физиологического раствора, теплое питье). Несмотря на проводимую терапию, ребенок продолжал фебрильно лихорадить, эффект от применения ибупрофена был краткосрочным и незначительным, что стало основанием для перехода на прием парацетамола (разовая доза 10 мг/кг). Из-за сохраняющейся фебрильной лихорадки была вызвана бригада скорой помощи и ребенок был госпитализирован.
При поступлении состояние средней тяжести, температура тела 38,8 °С (через 1,5 ч после последнего приема парацетамола), ЧСС 153 в 1 мин, частота дыхательных движений 45 в 1 мин. Масса тела — 4750 г. Сознание не нарушено. Дыхание через нос затруднено. Одышки нет. Кожные покровы обычной окраски, ладони и стопы теплые, влажные. Симптом «белого пятна» отрицательный. Небные миндалины и задняя стенка глотки гиперемированы. Периферические л/у не увеличены. Перкуторно над легкими звук легочный, аускультативно — пуэрильное дыхание. Границы сердца не расширены. Тоны сердца звучные, громкие. Живот мягкий, доступен глубокой пальпации, печень +1,0–1,5 см, селезенка не пальпируется. Наружные половые органы сформированы по мужскому типу, правильно, яички в мошонке. Стула во время осмотра не было, диурез сохранен. В приемном отделении выполнен клинический анализ крови (Hb 116 г/л, эритроциты 3,6.1012, MCV 87 фл, MCH 26,9 пг, лейкоциты 10,8×109/л (лейкоцитарная формула: п. 1%, с. 33%, л. 56%, м. 7%, э. 2%, б. 1%), тромбоциты 360,0×109/л, СОЭ 5 мм/ч). Диагноз при поступлении: ОРВИ, средней тяжести. Назначенную амбулаторно терапию решено было продолжить. В течение первых 45 мин пребывания ребенка в стационаре отмечено нарастание гипертермии до 39,2 °С, что стало основанием для в/м введения метамизола (расчетная доза 5 мг/кг). Температура тела через 1 ч после введения метамизола снизилась до 38,3 °С, однако в дальнейшем (через 3,5 ч) вновь повысилась до 39,0 °С, что одновременно сопровождалось ухудшением состояния — наросли бледность, тахикардия. В связи с этим было решено начать инфузионную терапию и повторить введение метамизола в дозе 5 мг/кг. При этом было отмечено продолжающееся кровотечение из места предыдущей инъекции и возникновение кровотечения из места только что выполненной инъекции (рис. 2). Наличие геморрагического синдрома стало основанием для проведения по cito! комплексного лабораторного (клинический анализ крови, коагулограмма, биохимический анализ крови, группа крови и резус-фактор) и инструментального обследования (нейросонография (НСГ), УЗИ внутренних органов). Среди возможных причин геморрагического синдрома рассматривались нарушения первичного (тромбоцитопения) и вторичного гемостаза (наследственные коагулопатии, в первую очередь гемофилия, учитывая пол ребенка, и приобретенные коагулопатии), а также ДВС-синдром и побочное действие медикаментов, так как повторно использовались антипиретики-анальгетики (ибупрофен, парацетамол, метамизол). Параллельно детализировали данные анамнеза, при этом семейной предрасположенности к повышенной кровоточивости выявлено не было.
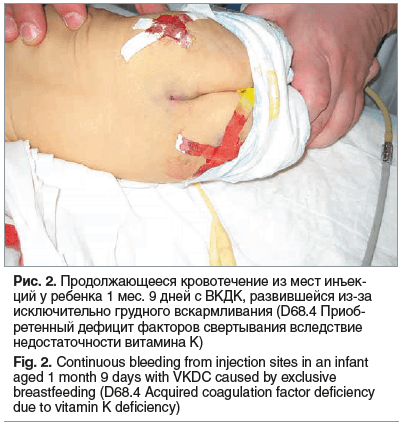
На основании результатов проведенного обследования было сделано заключение о том, что у ребенка имеет место остро возникшая тяжелая постгеморрагическая анемия (клинический анализ крови: Hb 68 г/л, эритроциты 3,1×1012/л, MCV 87 фл, MCH 26,1 пг, ретикулоциты 4,1%, лейкоциты 11,5×109/л (лейкоцитарная формула: п. 1%, с. 29%, л. 56%, м. 10%, э. 3%, б. 1%), тромбоциты 347,0×109/л, СОЭ 12 мм/ч), развившаяся из-за выраженных нарушений плазменного гемостаза (протромбиновый индекс не определяется (нет коагуляции), протромбиновое время не определяется (нет коагуляции), АЧТВ не определяется (нет коагуляции), тромбиновое время 14 с, фибриноген 2,5 г/л, D-димеры 310 нг/мл). При этом, учитывая, что лабораторные признаки гипокоагуляции были выявлены в системе как внутреннего пути свертывания (АЧТВ — нет коагуляции), так и внешнего (протромбиновый индекс — нет коагуляции, протромбиновое время — нет коагуляции) при нормальных значениях конечного этапа свертывания (тромбиновое время 14 с, фибриноген 2,9 г/л), стало ясно, что в основе геморрагического синдрома лежит ВКДК (рис. 3, 4). Особо следует подчеркнуть, что корректная интерпретация показателей стандартной коагулограммы в этом случае позволила исключить гемофилию, при которой, в отличие от ВКДК, имела бы место только гипокоагуляция по внутреннему пути свертывания (АЧТВ в этом случае было бы удлинено или вообще не было бы коагуляции) при нормальных значениях показателей внешнего пути (протромбиновый индекс, протромбиновое время, МНО). Все показатели биохимического анализа крови, общего анализа мочи, копрограммы были в пределах референтных значений. Результаты НСГ и УЗИ внутренних органов, выполненные по cito, свидетельствовали об отсутствии сонографических признаков патологии. Проведенная неотложная терапия (в/в введение свежезамороженной плазмы в дозе 10 мл/кг однократно; эритроцитная взвесь лейкоредуцированная, одногруппная, с индивидуальным подбором донора в дозе 10 мл/кг однократно) позволила купировать геморрагический синдром и анемию, состояние ребенка было стабилизировано. Одновременно для ликвидации дефицита витамина К использовали в/м введение менадиона натрия бисульфита (витамин К3) в дозе 4 мг на 1 введение, несмотря на то, что его терапевтический эффект развивается только через 24 ч. Препарат вводили 1 раз в сутки, ежедневно в течение 3 дней, до нормализации показателей коагулограммы. При катамнестическом наблюдении за ребенком рецидивов геморрагического синдрома отмечено не было.
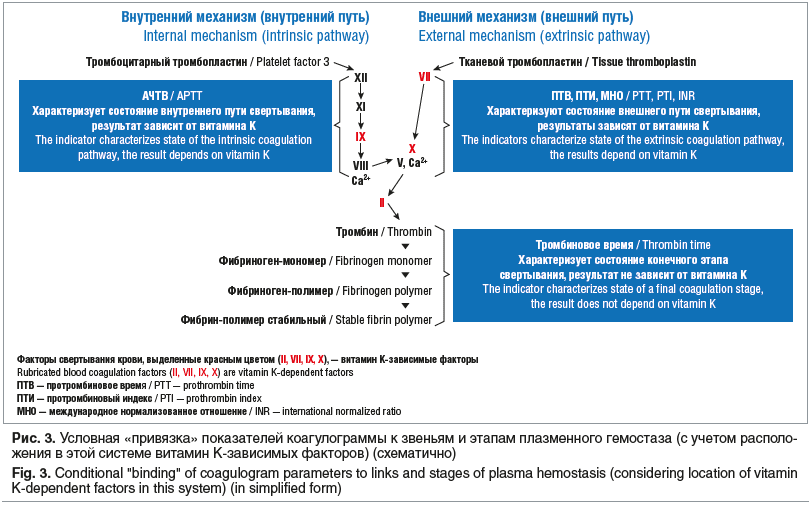
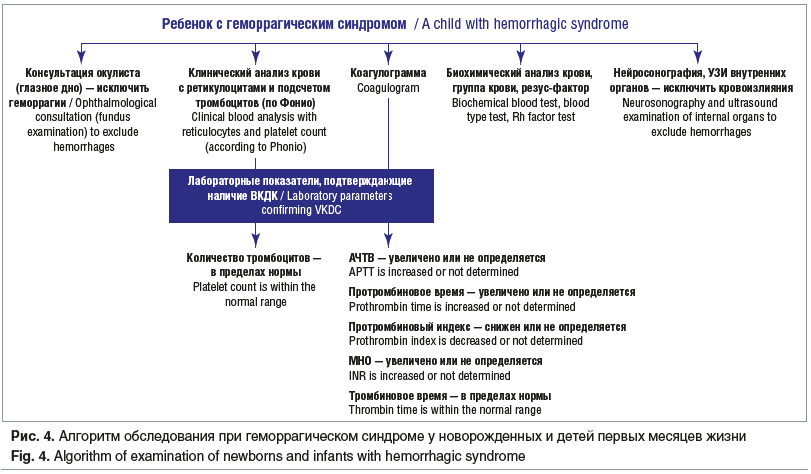
Принимая во внимание, что у ребенка не было клинических, лабораторных и инструментальных признаков билиарной атрезии, холестаза, мальабсорбции и других патологических состояний, приводящих к дефициту витамина К в организме, был сделан вывод, что причиной развившейся витамин К-зависимой коагулопатии является исключительно грудное вскармливание.
Клиническое наблюдение 2
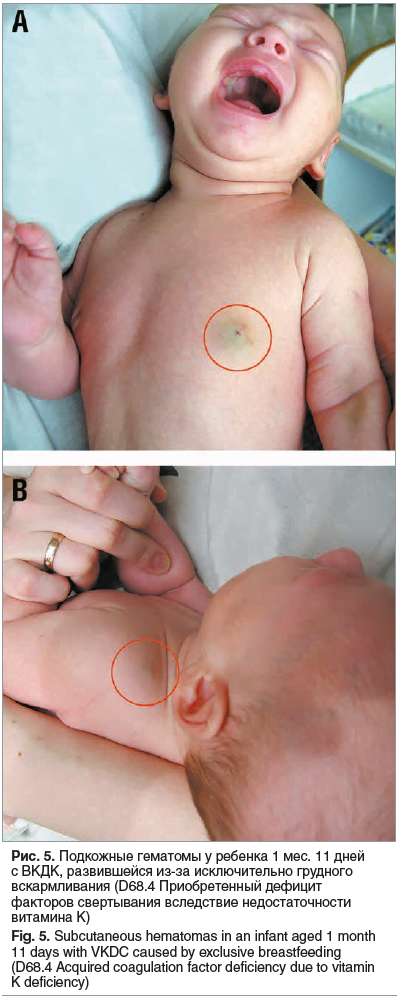
Аналогичный диагноз был верифицирован и у другого ребенка (девочка, 1 мес. 11 дней), госпитализированного в связи с синдромом срыгиваний. Обратили внимание на прожилки крови в рвотных массах, кровоточивость из мест забора крови для лабораторных исследований, а также на кожный геморрагический синдром — подкожные гематомы в виде «нодулярной пурпуры» (рис. 5). Из анамнеза: девочка от здоровой, молодой женщины. Беременность 1-я, в 1-м триместре — токсикоз. Роды I, на 38-й неделе, физио-логические. Девочка родилась в головном предлежании с массой 3100 г, длиной тела 51 см, с оценкой по шкале Апгар 8/9 баллов. К груди приложена сразу после рождения. Грудь взяла активно. Против гепатита В и туберкулеза вакцинирована. Выписана в удовлетворительном состоянии на 4-е сутки жизни. Находится на грудном вскармливании (режим вскармливания свободный). За 1-й месяц жизни прибавила 1100 г. С первых дней жизни необильные срыгивания после кормления, усилившиеся к месячному возрасту, что стало основанием для госпитализации.
При экстренном обследовании выявлена гипохромная гиперрегенераторная анемия средней степени тяжести (Нb 88 г/л, эритроциты 3,4×1012, MCH 23,1 пг, ретикулоциты 4,3%, лейкоциты 7,9×109(лейкоцитарная формула: п/я 2%, с/я 31%, л. 59%, м. 7%, э. 1%), тромбоциты 407×109/л, СОЭ 17 мм/ч). В коагулограмме отмечены нарушения по внутреннему (АЧТВ — нет коагуляции) и внешнему (протромбиновое время — нет коагуляции, протромбиновый индекс — нет коагуляции) путям свертывания, при нормальных показателях конечного этапа свертывания (фибриноген 3,81 г/л, тромбиновое время 15,1 с). Данные НСГ и УЗИ внутренних органов позволили исключить кровоизлияния. Таким образом, отсутствие нарушений со стороны первичного гемостаза (тромбоциты в пределах нормы) и конечного этапа плазменного гемостаза (нормальные значения тромбинового времени) при одновременной выраженной гипокоагуляции по внутреннему и внешнему путям свертывания, функциональная активность которых определяется витамином К, позволили верифицировать витамин К-зависимую коагулопатию (рис. 3, 4). Учитывая, что из всех возможных причинно-значимых факторов дефицита витамина К у девочки имело место только исключительно грудное вскармливание, именно оно и было верифицировано в качестве этиологии данного геморрагического синдрома. Однократное внутривенное введение свежезамороженной плазмы (10 мл/кг) позволило сразу купировать кровоточивость, а ежедневное парентеральное введение витамина К3 (менадион натрия бисульфит 4 мг на введение, 1 р/сут № 3) — полностью нормализовать показатели коагулограммы к 4-м суткам проводимой терапии.
При этом следует отметить, что эффект водорастворимого витамина К3 (менадиона натрия бисульфит) развивается медленно и начинает действовать только через 24 ч после введения. Это связано с тем, что он действует через метаболиты, пройдя путь превращения в печени до витамина К1, который и является активной формой данного витамина, в то время как витамин К1 (фитоменадион) эффективно проявляет свою активность уже в первые часы после введения, обеспечивая тем самым профилактику ранней формы ГрБН.
В связи с этим целесообразно рассмотреть необходимость быстрейшего внесения изменений в рекомендации по оказанию неотложной медицинской помощи при ВКДК, обозначив в них витамин К1(фитоменадион) в качестве препарата выбора вместо витамина К3 (менадиона натрия бисульфит).
Представленные клинические наблюдения свидетельствуют о том, что своевременная диагностика ВКДК и адекватно оказанная при этом экстренная медицинская помощь позволяют быстро купировать геморрагические нарушения и эффективно предупреждают грозные осложнения (интракраниальные кровоизлияния и др.). Особо при этом следует подчеркнуть, что на практике недооценка ранних, так называемых малых геморрагических проявлений ВКДК, и поздняя диагностика имеют место в 40–70% случаев тяжелого дефицита витамина К, приводящего к внутричерепным кровоизлияниям [11, 13, 16, 19, 26, 28, 29]. В связи с этим стоит еще раз подчеркнуть, что появление у новорожденных и младенцев даже минимальных геморрагических симптомов (сукровичные выделения при адекватно проведенном туалете носовых ходов, единичные прожилки крови при срыгиваниях или в каловых массах, незначительно кровоточащая пупочная ранка, единичные кожные геморрагии и др.) требует обязательного срочного уточнения причин для своевременного выбора адекватной тактики ведения таких пациентов.
Современные возможности специфической профилактики и терапии ВКДК
Специфическая профилактика ранней и классической ГрБН в отечественной неонатологии давно разработана, широко и повсеместно внедрена в практику и подкреплена высокой результативностью. Так, многолетний отечественный опыт использования однократного введения витамина К3 (менадион натрия бисульфит) в первые часы жизни всем новорожденным детям, не имеющим противопоказаний, свидетельствует о достоверной эффективности данного метода для профилактики классической формы ГрБН. Однако, учитывая имеющиеся ограничения к применению (гемолитическая болезнь новорожденного, гиперкоагуляция, дефицит глюкозо-6-фосфатдегидрогеназы), менадион натрия бисульфит в ряде случаев не может быть использован. Решить эту проблему позволило появление в арсенале отечественных неонатологов с 2023 г. витамина К1 (фитоменадион) под торговым названием Канеовит[2], который может быть использован для без-опасной профилактики всех форм ГрБН у новорожденных, в том числе и при гемолитической болезни новорожденного[3]. При этом рекомендован следующий режим дозирования 1% эмульсии фитоменадиона:
новорожденным детям (при внутриутробном возрасте плода не менее 36 нед.) — однократно, в дозе 1 мг путем в/м введения при рождении или сразу после рождения;
недоношенным детям (внутриутробный возраст плода менее 36 нед., масса тела не менее 2,5 кг) и новорожденным из группы повышенного риска развития кровотечений (незрелость, асфиксия при рождении, застойная желтуха, расстройство глотания, введение матери антагонистов витамина K, противоэпилептических препаратов) — однократно, в дозе 1 мг путем в/м или в/в введения при рождении или сразу после рождения;
недоношенным детям (внутриутробный возраст плода менее 36 нед., масса тела менее 2,5 кг) — однократно в дозе 0,4 мг/кг путем в/м или в/в введения при рождении или сразу после рождения.
Рассматривая актуальные вопросы специфической профилактики ГрБН, нельзя не отметить, что в последние годы увеличивается число новорожденных детей, родители которых отказываются от введения менадиона натрия бисульфита, так как они являются категорическими противниками инъекций, а пероральный прием этого препарата в неонатальный период не регламентирован. При этом наши наблюдения свидетельствуют о том, что у детей, не получивших в первые часы жизни менадион натрия бисульфит из-за отказа родителей от парентерального введения витамина К, существенно повышался риск развития ГрБН (неопубликованные данные). Решение этой проблемы возможно благодаря тому, что витамин К1 (фитоменадион) на протяжении ряда десятилетий с успехом применяется перорально для профилактики ГрБН во многих экономически развитых странах [19]. При этом доказанная высокая профилактическая эффективность и безопасность использования per os препарата витамин К1 (фитоменадион) у новорожденных детей позволяют рекомендовать внедрение данного метода профилактики ГрБН в отечественную практику. Так, в федеральных клинических рекомендациях «Геморрагическая болезнь плода и новорожденного»3 указано, что витамин К1 (фитоменадион) может быть использован в качестве профилактики ГрБН не только парентерально, но и per os в тех случаях, когда родители отказываются от инъекции витамина К1 (фитоменадион). При этом подчеркивается, что родителям в этом случае может быть предложен альтернативный способ профилактики ГрБН — пероральный прием витамина К1 (фитоменадион) off lable («применение вне инструкции»). Следует особо отметить, что использование лекарственных препаратов off lable возможно только тогда, если это назначение оформлено врачебной комиссией (не менее 3 членов) и подтверждено подписанным добровольным информированным согласием официального представителя ребенка. В том случае, когда родители письменно подтвердили свое согласие на пероральное использование витамина К1 (фитоменадион) для профилактики ГрБН, врачебная комиссия оформляет письменное заключение о назначении препарата в следующем режиме дозирования трехкратно внутрь:
2 мг после рождения (первая доза);
2 мг в период 4–6 дней после рождения (вторая доза);
2 мг в период 4–6 нед. после рождения (третья доза).
Необходимо отметить, что в случае развития рвоты или срыгивания в течение 1-го часа после приема витамина К1 (фитоменадион) per os необходимо повторить прием препарата внутрь в той же дозе3.
Регистрация в Российской Федерации препарата витамин К1 (фитоменадион) позволяет решить еще одну проблему, долгие годы недооцениваемую отечественной педиатрией. Речь идет о ВКДК, развивающейся у детей первых недель и месяцев жизни из-за исключительно грудного вскармливания [1, 13, 20, 26]. Актуальность данной проблемы обусловлена тем, что активная санитарно-просветительская работа по поддержке грудного вскармливания и увеличение за счет этого процента детей, вскармливаемых исключительно материнским молоком, может привести к увеличению среди этих младенцев частоты геморрагического синдрома, обусловленного витамин К-дефицитным состоянием. Дело в том, что у этих детей имеются высокие риски развития ВКДК, так как женское молоко, в отличие от коровьего, из которого готовят смеси, характеризуется низким содержанием витамина К. Так, содержание витамина К в женском молоке составляет 2,5 мг/л, а в смесях, приготовленных на основе коровьего молока, — 24–175 мг/л [19, 29, 30]. Кроме этого, у детей первых месяцев жизни нормальная микрофлора кишечника находится в стадии становления и еще не может компенсировать развивающийся дефицит витамина К эндогенным образованием данного витамина. Поэтому у детей, вскармливаемых исключительно материнским молоком, к возрасту 3–12 нед. возникают условия для глубокого дефицита витамина К с развитием ВКДК. Однако отмечено, что не у всех детей, находящихся исключительно на грудном вскармливании и имеющих за счет этого предпосылки для развития геморрагического синдрома из-за дефицита витамина К, ВКДК проявляется клинически. Среди причин этого феномена обсуждаются индивидуальные особенности метаболизма витамина К, в том числе и наследственная предрасположенность, обусловленная мутациями в генах VKORC1, GGCX, CYP4 F2 и др. [13, 28, 31].
Доказано, что у детей, вскармливаемых только материнским молоком, однократное введение витамина К при рождении не предупреждает развитие ВКДК в постнеонатальный период. В то же время установлена высокая профилактическая эффективность дополнительного введения витамина К1 (фитоменадион) в последующие недели жизни (чаще всего применяют методики дополнительного назначения витамина К1 на 2, 4 и 6-й неделях жизни, используя внутрь препарат витамина К1 (фитоменадион)) [19, 29]. Следует отметить, что отсутствие до недавнего времени в России препаратов витамина К, разрешенных к пероральному применению у младенцев, не позволяло проводить специфическую профилактику ВКДК у детей, вскармливаемых исключительно грудным молоком. Регистрация в Российской Федерации витамина К1 (фитоменадион)2 позволит решить данную проблему. При этом можно воспользоваться мировым опытом и внедрить в отечественную практику наиболее широко используемую методику, при которой витамин К1 (фитоменадион) назначается per os в виде 3 доз. При этом первая доза 2 мг внутрь назначается ребенку при рождении, вторая доза 2 мг внутрь применяется в возрасте 4–6 сут жизни и третья доза 2 мг внутрь назначается в возрасте 4–6 нед. Указанная схема позволяет эффективно компенсировать дефицит витамина К, возникающий у ребенка в результате недостаточного его поступления при вскармливании исключительно грудным молоком [19, 29].
Обсуждая основные принципы лечения неотложных состояний при ВКДК, следует отметить появивившуюся на современном этапе возможность существенно сократить частоту применения свежезамороженной плазмы при этих патологических состояниях за счет витамина К1 (фитоменадион), при внутривенной инфузии которого геморрагический синдром удается контролировть уже через 1–2 ч после введении[4]. Кроме того, учитывая, что терапевтический эффект витамина К1 (фитоменадион) достигается значимо быстрее, чем при использовании витамина К3 (менадион натрия бисульфит), необходимо предусмотреть внесение изменений в неонатологические и педиатрические рекомендации по оказанию неотложной медицинской помощи при геморрагических нарушениях, обусловленных дефицитом витамина К, заменив витамин К3 (менадион натрия бисульфит) на витамин К1 (фитоменадион) в качестве препарата выбора при лечении ВКДК.
Заключение
Витамин К-дефицитные коагулопатии, развивающиеся в раннем неонатальном периоде и в последующие периоды жизни ребенка, несмотря на сходный патогенез, имеют существенные этиологические различия. В связи с этим следует признать некорректным использовать обобщенный термин «геморрагическая болезнь новорожденного», включая в него и те геморрагические нарушения, дефицит витамина К при которых у детей развился после окончания раннего нео-натального периода. В этих случаях правильнее говорить о геморрагическом синдроме, обусловленном приобретенным дефицитом витамина К (D68.4 по МКБ-10). При этом в каждом конкретном случае необходимо уточнять причину (например, приобретенный дефицит витамина К в результате исключительно грудного вскармливания). Термин «геморрагическая болезнь новорожденного» при этом целесообразно использовать только в тех случаях, когда витамин К-дефицитная коагулопатии развивается у ребенка в первые 168 ч его жизни (Р53 по МКБ-10).
Учитывая высокий риск развития ВКДК у детей, находящихся исключительно на грудном вскармливании, для профилактики геморрагических проявлений целесообразны введение витамина К1 сразу после рождения, а также дополнительный прием витамина К1 (фитоменадион) в виде перорального назначения по 2 мг в возрасте 4–6 сут и в возрасте 4–6 нед. Указанная схема позволяет компенсировать дефицит витамина К, возникающий у ребенка в результате недостаточного его поступления при вскармливании исключительно грудным молоком.
СВЕДЕНИЯ ОБ АВТОРАХ:
Заплатников Андрей Леонидович — д.м.н., профессор, заведующий кафедрой неонатологии имени профессора В.В. Гаврюшова, профессор кафедры педиатрии имени академика Г.Н. Сперанского ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0000-0003-1303-8318
Дмитриев Андрей Владимирович — д.м.н., профессор, заведующий кафедрой детских болезней с курсом госпитальной педиатрии ФГБОУ ВО РязГМУ им. акад. И.П. Павлова Минздрава России; 390023, Россия, г. Рязань, ул. Высоковольтная, д. 9; профессор кафедры нео-натологии имени профессора В.В. Гаврюшова ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0000- 0002-8202-3876
Бабаев Бобо Домулаевич — д.м.н., профессор, заведующий кафедрой анестезиологии, реаниматологии и токсикологии детского возраста ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0000-0002-2063-0240
Дементьев Александр Анатольевич — к.м.н., доцент кафедры неонатологии имени профессора В.В. Гаврюшова ФГБОУ ДПО РМАНПО Минздрава России; 123993, Россия, г. Москва, ул. Баррикадная, д. 2/1 стр. 1; ORCID iD 0000-0002-7640-1172
Чабаидзе Жужуна Лазаревна — к.м.н., доцент кафедры неонатологии имени профессора В.В. Гаврюшова ФГБОУ ДПО РМАНПО Минздрава России; 123993, Россия, г. Москва, ул. Баррикадная, д. 2/1 стр. 1; ORCID iD 0000-0002-2192-796X
Майкова Ирина Дмитриевна — к.м.н., заместитель главного врача по лечебной работе ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ»; 125373, Россия, г. Москва, ул. Героев Панфиловцев, д. 28; ORCID iD 0000-0003-2700-2607
Лешик Мария Владимировна — ассистент кафедры педиатрии имени академика Г.Н. Сперанского ФГБОУ ДПО РМАНПО Минздрава России; 123993, Россия, г. Москва, ул. Баррикадная, д. 2/1 стр. 1; ORCID iD 0000-0002-9331-1419
Смирнов Дмитрий Николаевич — к.м.н., ассистент кафедры неонатологии имени профессора В.В. Гаврюшова ФГБОУ ДПО РМАНПО Минздрава России; 123995, Россия, г. Москва, ул. Баррикадная, д. 2/1 стр. 1; ORCID iD 0000-0002-7840-2881
Контактная информация: Заплатников Андрей Леонидович, e-mail: zaplatnikov@mail.ru
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 09.10.2025.
Поступила после рецензирования 05.11.2025.
Принята в печать 28.11.2025.
ABOUT THE AUTHORS:
Andrey L. Zaplatnikov — Dr. Sc. (Med.), Professor, Head of the Prof. V.V. Gavryushov Department of Neonatology, Professor of the Acad. G.N. Speransky Department of Pediatrics, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0003-1303-8318
Andrey V. Dmitriev — Dr. Sc. (Med.), Professor, Head of the Department of Pediatric Diseases with a Course in Hospital Pediatrics, Ryazan State Medical University named after academician I.P. Pavlov; 9, Vysokovoltnaya str., Ryazan, 390023, Russian Federation; Professor of the Department of Neonatology named after Professor V.V. Gavryushov, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000- 0002-8202-3876
Bobo D. Babaev — Dr. Sc. (Med.), Professor, Head of the Department of Pediatric Anesthesiology, Intensive Care Medicine and Toxicology, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0002-2063-0240
Alexander A. Dementiev — C. Sc. (Med.), Assistant Professor of the Department of Neonatology named after Professor V.V. Gavryushov, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0002-7640-1172
Zhuzhuna L. Chabaidze — C. Sc. (Med.), Assistant Professor of the Department of Neonatology named after Professor V.V. Gavryushov, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0002-2192-796X
Irina D. Maikova — C. Sc. (Med.), Deputy Chief Physician for Medical Work, Z.A. Bashlyaeva Children’s City Clinical Hospital; 28, Geroev Panfilovtsev str., Moscow, 125373, Russian Federation; ORCID iD 0000-0003-2700-2607
Maria V. Leshik — Teaching Assistant at the Department of Pediatrics named after academician G.N. Speransky, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0002-9331-1419
Dmitryi N. Smirnov — C. Sc. (Med.), Teaching Assistant of the Department of Neonatology named after Professor V.V. Gavryushov, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0002-7840-2881
Contact information: Andrey L. Zaplatnikov, e-mail: zaplatnikov@mail.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 09.10.2025.
Revised 05.11.2025.
Accepted 28.11.2025.
[1] Геморрагическая болезнь плода и новорожденного. Международная классификация болезней и проблем, связанных со здоровьем; 10-й пересмотр. Всемирная организация здравоохранения, Женева, 1995: пер. с англ., в 3 т. М.: Медицина; 1995.
[2] Канеовит, 10 мг/мл, эмульсия для внутривенного и внутримышечного введения. РУ № ЛП-№(001428)-(РГ-RU) от 18.11.2022. (Электронный ресурс.) URL: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=7b83ba6a-7cdc-4657-ae73-2ff3b0c78fef (дата обращения: 15.10.2025).
[3] Клинические рекомендации Минздрава России. Геморрагическая болезнь плода и новорожденного. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/view-cr/906_1 (дата обращения: 15.10.2025).
[4] Phytonadione. The American Society of Health-System Pharmacists. (Electronic resource.) URL: https://www.drugs.com/monograph/phytonadione.html (access date: 15.10.2025).
Информация с rmj.ru




