Уровень таурина в сыворотке крови в сочетании с офтальмоскопическим обследованием как ранний маркер диабетической ретинопатии (реферат)
Содержание статьи
Введение
В настоящее время принципы дифференциации диабета у детей несовершенны и основаны на таких клинических характеристиках, как степень тяжести, применение инсулина, возраст появления, диабетический кетоацидоз и семейный анамнез диабета [1–4]. У больных СД1 и СД2 часто встречаются хронические сосудистые осложнения — микро- и макрососудистые. Наиболее распространенными микроваскулярными осложнениями, связанными с диабетом, являются ретинопатия, нефропатия и невропатия [5], макрососудистыми — сердечные, периферические артериальные и цереброваскулярные заболевания [6].
Эпидемиологические исследования показали, что у больных диабетом выше риск заболеть онкологическими заболеваниями. Механизмы, с помощью которых это может произойти, изучены недостаточно хорошо [7]. В 2010 г. проводилось исследование, целью которого было изучение связи между диабетом и онкологическими заболеваниями, факторов риска для обоих заболеваний, их возможных биологических связей и определение того, влияют ли некоторые методы лечения диабета на риск развития онкологических заболеваний [8].
Диабетическая ретинопатия (ДР) является распространенным специфическим микрососудистым осложнением СД, приводящим к потере зрения у взрослых в трудоспособном возрасте в развитых странах мира [9]. Клиническими признаками ДР являются микроаневризмы, кровотечение, микрососудистые нарушения и неоваскуляризация сетчатки глаза [10]. Микроаневризмы являются первым клиническим признаком ДР, они представляют собой ослабление стенок капилляров. Повреждение кровеносных сосудов может происходить в глубоких слоях сетчатки и распространяться в слой нервных волокон сетчатки [11]. Несмотря на успехи в лечении ДР, отек макулы, возникающий у 14% больных СД, остается основной причиной слепоты среди больных СД [12]. Офтальмоскопическое обследование играет важную роль в скрининге, мониторинге ДР и является точным и объективным методом диагностики этого заболевания. Онo позволяет получить трехмерные или поперечные изображения, подобные получаемым при гистологическом исследовании сетчатки [13]. По офтальмоскопическому изображению ретинопатию делят на непролиферативную (НПДР) и пролиферативную (ПДР). НПДР подразделяется на легкую, умеренную и тяжелую. Данная классификация помогает выделить стадии ретинопатии, для которых характерно значительное снижение остроты зрения или высокий риск развития ретинопатии до стадий, которые, в свою очередь, требуют проведения определенных мероприятий и вмешательств [10]. Сосудистый эндотелиальный фактор роста (vascular endothelial growth factor — VEGF) — ангиогенный фактор с селективной митогенной активностью эндотелиальных клеток, является ключевым медиатором изменений сосудов сетчатки, связанных с развитием и прогрессированием ДР [14–16].
VEGF играет важную роль в неоваскуляризации при ПДР и преодолении гематоретинального барьера, что приводит к повышению проницаемости сосудов сетчатки [17]. Также было установлено, что его уровень заметно повышен в стекловидном теле и водных средах у пациентов с ПДР [18]. Треть больных с ДР составляют больные с поздней стадией тяжелой ретинопатии или ПДР [19]. Необходимо увеличение частоты обследований и осмотра пациентов с риском развития ПДР [20]. Три основных модифицируемых фактора риска, включая гипергликемию, гипертонию и дислипидемию, играют важную роль в лечении ДР. Снижение уровня гликозилированного гемоглобина (HbA1c) на 1% благодаря интенсивному гликемическому контролю уменьшает риск возникновения ДР на 15–40% [21].
Таурин (2-аминоэтансульфоновая кислота) — производное незаменимой аминокислоты цистеин, которая вырабатывается в печени в результате метаболизма метионина и цистеина, содержится в миллимолярной концентрации в тканях человека. Основным источником таурина являются мясо и морепродукты. Таурин оказывает большое положительное влияние на организм человека: модулирует клеточные функции, ионный обмен, осморегуляцию и передачу нервных импульсов [22], играет важную роль в инициировании и развитии иммунного ответа [23], защищает от гипергликемии [24], гипертонии [25], эндотелиальной дисфункции [26] и неоплазии [27].
Таурин вовлечен во многие механизмы гомеостаза сетчатки. Он находится в высокой концентрации в наружном слое, палочковидных клетках, пигментном эпителии сетчатки и фоторецепторах [28].
Более того, за счет модуляции мембранных ионных каналов таурин повышает Са2+ до уровня, способствующего передаче зрительных сигналов от сетчатки к мозгу, играет важную роль в регенерации поврежденных клеток сетчатки [29].
Материал и методы
В исследование были включены 80 пациентов в возрасте 18–60 лет, принимающих пероральные сахароснижающие препараты. 10 из них не страдали диабетическими осложнениями и составили контрольную группу. Пациенты с тяжелой невропатией, нефропатией, диабетической стопой и цереброваскулярными или сердечно-сосудистыми заболеваниями были исключены из участия. У всех пациентов натощак собирали образцы венозной крови для оценки уровня сывороточных триглицеридов (ТГ), холестерина, липопротеидов высокой плотности (ЛПВП), липопротеидов низкой плотности (ЛПНП), HbA1c и таурина. Измерение уровней АСТ, АЛТ, VEGF, мочевины крови, креатинина, альбумина и микроальбумина в сыворотке крови проводилось не натощак. После полного клинического обследования пациенты были разделены на 5 групп в зависимости от стадии ДР по результатам офтальмоскопического обследования: 10 человек — с легкой НПДР, 10 — с умеренной НПДР, 20 — с тяжелой НПДР, 30 — с ПДР. 20 здоровых волонтеров составили контрольную группу. В исследовании применялись комплекты для микроколоночной хроматографии HbA1c производства Biosystems (Испания), сывороточный таурин определяли методом высокоэффективной жидкостной хроматографии посредством экстракции и предколоночной дериватизации по методу McMahon et al. Корреляция между полом и тяжестью или прогрессированием ДР отсутствовала. Исследования показывают, что пол и возраст не влияют на распространенность ДР, но могут влиять на продолжительность заболевания [30]. Значимость различий оценивали t-тестом для парных выборок или дисперсионным анализом (ANOVA). Связь между переменными оценивали методом простого корреляционного анализа. Данные выражены в виде среднего значения ± стандартное отклонение SD, значение p
Результаты
В исследование включили 70 пациентов с СД, у которых наблюдалась только размытость зрения, 10 пациентов с СД без диабетических осложнений и 20 здоровых волонтеров. Данные липидного профиля (табл. 1): целевое значение общего холестерина 240 мг/дл. У всех обследованных больных СД наблюдалась легкая гиперхолестеринемия без существенных различий (p>0,05) между группами пациентов с СД, но с существенным увеличением по сравнению с группой контроля. Уровни TГ между группами значительно не отличались. Уровень ЛПВП был значительно снижен у всех больных СД независимо от стадии ретинопатии (p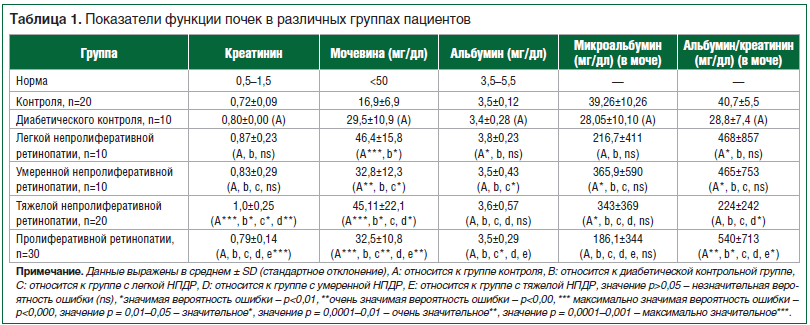
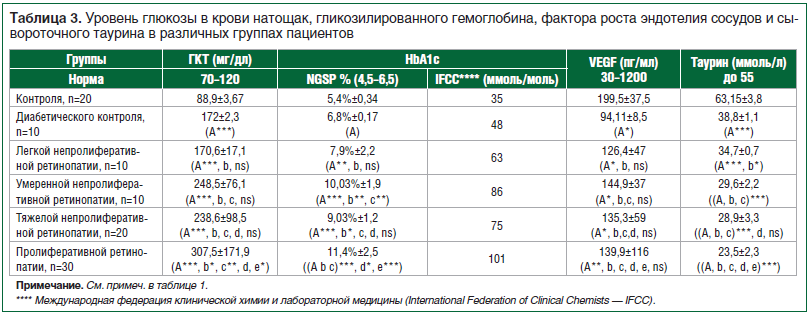
Из таблицы 2 видно, что уровень креатинина в сыворотке крови у здоровых людей колеблется в пределах 0,5–1,5 мг/дл, поэтому патологических изменений между контрольной группой (0,72+0,09) и диабетической группой не зарегистрировано, поскольку все значения были ниже 1,5 мг/дл. То же самое наблюдается в уровне мочевины крови. У здоровых добровольцев значение составляло 16,9±6,9 мг/дл, в контрольной диабетической группе этот показатель увеличился до 29,5±10,9 мг/дл и достигал 46,4±15,8 мг/дл в группе с легкой НПДР против очень значительного (p0,05). В таблице 3 представлен уровень (p0,05) — 48 ммоль/моль. Сывороточный VEGF был незначительно ниже у всех больных СД по сравнению с таковым в группе контроля. Интересно, что уровень таурина в сыворотке крови был заметно (p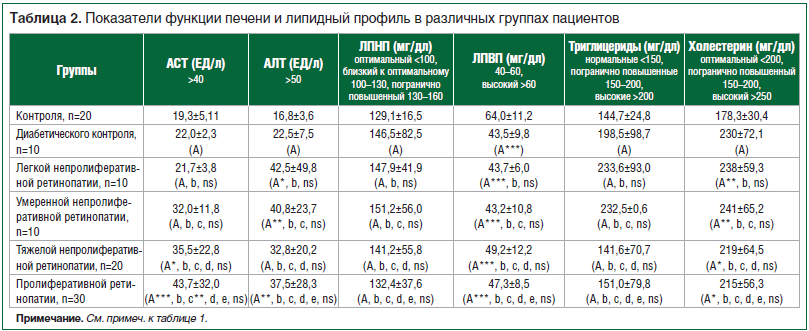
Обсуждение
У всех обследованных пациентов не обнаружили существенных изменений в липидном профиле, особенно ТГ и ЛПНП. Напротив, уровни ЛПВП и холестерина значимо отличались во всех группах больных СД от показателей группы контроля. Значимые различия были зарегистрированы в функциях печени, особенно на поздних стадиях ДР. Установлено, что аномальные функциональные тесты печени у больных СД могут быть индикаторами сопутствующей неалкогольной жировой болезни печени [31]. Имеются доказательства того, что экспрессия VEGF снижается у больных с СД, что способствует задержке заживления ран [32]. В нашем исследовании этот показатель был снижен несущественно по сравнению с таковым в контрольной группе, т. к. кровоснабжение диабетической сетчатки снижено, и показатель VEGF находится в широком диапазоне нормы (30–1200 пг/мл). Во всех группах пациентов с ДР наблюдались значительные изменения показателей мочи по сравнению с таковыми в группе контроля. У всех пациентов, включая контрольную диабетическую группу, выявлено раннее появление альбумина в моче в количестве 1–30 мг/дл, микро- (от 30 до 300 мг/дл) и макроальбуминурии (>300 мг/дл), что считается ранним признаком диабетической нефропатии [33]. Уровни глюкозы в крови натощак (ГКТ) и HbA1c были максимально значимо увеличены у всех пациентов по сравнению с таковыми в группе контроля (p
Наиболее интересным результатом данного исследования является заметно сниженный уровень таурина в сыворотке крови (38,8±1,1 ммоль/л) у пациентов контрольной диабетической группы, несмотря на нормальную офтальмоскопическую картину и небольшое увеличение уровней ГКТ и HbA1c (p>0,05) по сравнению с таковыми в контрольной группе (63,15±3,8 ммоль/л). Этих пациентов регулярно обследуют, и они не имеют диабетических осложнений. Таким образом, снижение уровня таурина в сыворотке крови у больных СД приводит к патологическим изменениям в сетчатке глаза. Это можно считать ранним признаком ДР и непосредственным поводом начать лечение. Полученные данные согласуются с другими исследованиями, опубликованными в 2007 г., которые доказали, что уровень таурина в плазме у пациентов с СД2 заметно ниже, чем у здоровых людей [34]. Таурин действует как гипогликемический препарат как при инсулинзависимом, так и инсулиннезависимом СД [35, 36].
В представленном исследовании наблюдалось снижение уровня сывороточного таурина (34,7±0,7, 29,6±2,2, 28,9±3,3 ммоль/л) параллельно прогрессированию непролиферативной ДР (легкой, средней и тяжелой), соответственно, по мере увеличения тяжести состояния. В сетчатке содержится чрезвычайно большое количество таурина, а у некоторых видов животных уровень таурина в сетчатке самый высокий из всех тканей [37, 38]. Установлено, что таурин выполняет в сетчатке несколько функций, включая регуляцию переноса Ca2+, защиту фоторецепторов и регуляцию трансдукции сигнала [39].
Более того, установлено, что таурин уменьшает вызванное высоким содержанием глюкозы нарушение поглощения и деградации глутамата в культивируемых клетках Мюллера [40]. Подтверждалось также, что таурин играет важную роль в защите нервных клеток сетчатки глаза [41], уменьшает электрофизиологические изменения сетчатки при диабете [42]. В 2015 г. было высказано предположение, что таурин играет важную роль в процессе регенерации родопсина и в защите клеток сетчатки от осмотических, механических и вызванных действием света повреждений [43].
Обычно наблюдение всех хронических больных СД ограничивается измерением уровня глюкозы крови, гемоглобина и глюкозы в моче. Предложены многочисленные методы диагностики ДР, было показано, что средние уровни окиси азота в сыворотке крови (NO), растворимого рецептора интерлейкина-2 (sIL2R), интерлейкина-8 (IL-8) и фактора некроза опухоли альфа (TNF-альфа) увеличиваются у пациентов по мере развития ПДР [44].
Установлено, что у пациентов с НПДР и ПДР также повышен сывороточный уровень хемерина — многофункционального пептида, участвующего в метаболизме липидов и глюкозы [45, 46].
В больнице NIDE пациентам — участникам исследования диагноз в основном ставили на основании биохимического анализа (ГКТ, HbA1c, уровень глюкозы после приема пищи) и офтальмоскопии.
Дальнейшие исследования показали положительную роль таурина при ДР. Это предполагает, что таурин может нормализовать сосудистую функцию сетчатки у больных диабетом [47]. Таурин препятствует повышению содержания глутамата в сетчатке и снижению уровня белков, участвующих в поглощении и деградации глутамата у крыс с диабетом, получавших стрептозотоцин (Streptozotocin) [47]. Известно, что повышение глутамата в сетчатке связано с развитием ДР [47].
В данном исследовании у пациентов из группы ПДР уровень таурина (около 23,5±2,3 ммоль/л) был чрезвычайно низким (р
В соответствии с результатами настоящего исследования было высказано предположение, что концентрации таурина в сыворотке крови не зависят от возраста и пола пациентов [50].
В представленном исследовании в офтальмологическую клинику обратились 50 больных СД с поздней стадией ДР. Пациенты с СД нерегулярно наблюдаются и чаще всего обращаются за помощью на поздней стадии ДР [20]. Вызывают беспокойство высокая частота ПДР и недостаточное внимание к тяжести осложнений заболевания. Таким образом, каждому пациенту с СД1 или СД2 с ранним снижением зрения необходимо проходить регулярный офтальмоскопический осмотр и измерять уровень таурина в сыворотке крови. Уровень таурина может служить высокочувствительным маркером ухудшения состояния пациента.
Содержание таурина в сыворотке не ниже 50 ммоль/л
можно считать запасом прочности для пациентов, страдающих СД. Пациенты с СД с более низкими значениями (
Мы рекомендуем новую классификацию ДР в соответствии с уровнем таурина в сыворотке крови наряду с результатами офтальмоскопии для всех больных СД, регулярное обследование в качестве превентивной меры для ранней диагностики любых микрососудистых осложнений и предлагаем поддерживать уровень таурина в сыворотке крови выше 50 ммоль/л в качестве запаса прочности. Уровень таурина 40–50 ммоль/л мы считаем зоной риска, поскольку у больных СД такой уровень связан с риском серьезных осложнений. При уровне таурина ниже 40 ммоль/л пациенты начинают страдать от микрососудистых осложнений. Уровень ниже 30 ммоль/л связан с большим риском развития новообразований у пациентов с СД [48, 49].
Заключение
Регулярное офтальмоскопическое обследование всех больных СД и измерение уровня таурина в сыворотке крови в соответствии с новой классификацией может быть использовано в качестве раннего маркера микроваскулярных осложнений, особенно ДР.
Реферат подготовлен редакцией «РМЖ» по материалам статьи: I.M. El Agouza, A.H. Saad, A.A. Mahfouz, K. Hamdy. Serum Taurine Level in Relation to Ophthalmoscopic Examination as Early Marker for Diabetic Retinopathy. Clin Med Biochemistry. 2017;3(1):124. DOI: 10.4172/2471–2663.1000124.
Информация с rmj.ru





