Введение
Эозинофильные заболевания желудочно-кишечного тракта (ЖКТ) — группа болезней, характеризующихся плотной эозинофильной инфильтрацией тканей различных органов ЖКТ, приводящей к морфологическим и функциональным нарушениям. Их подразделяют на эозинофильный эзофагит, эозинофильный гастрит, эозинофильный гастроэнтерит и эозинофильный колит в зависимости от локализации поражения [1]. Примером необычно обширного эозинофильного поражения ЖКТ может служить следующее наблюдение.
Клиническое наблюдение
Пациент С., 17 лет, житель Республики Казахстан, госпитализирован в клинику Европейского Медицинского Центра 27.02.2020 с жалобами на снижение аппетита, общую слабость, рвоту съеденной пищей до 3 раз в сутки, неоформленный стул до 7 раз в день.
Ранее у врачей не наблюдался, аллергические реакции отрицает. В январе 2019 г. впервые на фоне полного благополучия возникла рвота съеденной пищей, не приносящая облегчения, диарея до 10–12 раз в сутки, боли в животе спастического характера, преимущественно в эпигастрии. Температура тела не повышалась. Больной был обследован по месту жительства, выполнена эзофагогастродуоденоскопия (ЭГДС), которая выявила признаки рефлюкс-эзофагита 1-й степени, картину катарального гастрита, бульбита, язвы антрального отдела желудка. Уреазный тест положительный. Проводилось лечение: амоксициллин 1 г 2 р/сут, кларитромицин 500 мг 2 р/сут, висмута трикалия дицитрат 240 мг 2 р/сут, омепразол 20 мг/сут в течение 14 дней. На фоне терапии отмечалась положительная динамика: рвота и диарея прекратились. Ухудшение состояния возникло в июле 2019 г., когда возобновились вышеуказанные симптомы.
При обследовании 20.07.2019 в клиническом анализе крови впервые выявлены лейкоцитоз 12×109/л, эозинофилия до 24,9%. Выявлены антитела IgG к лямблиям. Антител к гельминтам не обнаружено. Проведено лечение нифурателом по 400 мг 2 р/сут в течение 7 дней, на фоне которого рвота и диарея снова прекратились.
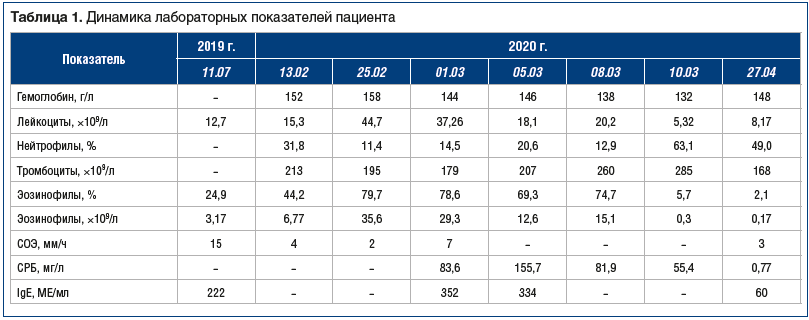
В феврале 2020 г. отмечено возобновление симптомов. При обследовании 13.02.2020 в клиническом анализе крови: лейкоцитоз 15,3×109/л с эозинофилией 44,2% (абсолютное число — 6,77×109/л). Эти и последующие лабораторные данные представлены в таблице 1. Госпитализирован в стационар Европейского Медицинского Центра 27.02.2020.
При поступлении при осмотре отмечено, что живот слабоболезненный в эпигастрии, в остальном данные физикального обследования без особенностей. В клиническом анализе крови от 27.02.2020: лейкоцитоз 49,8×109/л, эозинофилия 82,7%, СОЭ 5 мм/ч. Уровни антигена маннана и антиманнановых антител (признаки инвазивного кандидоза) — в пределах референсных значений. Отмечено повышение уровня С-реактивного белка (СРБ) до 83,6 мг/л, IgE — до 352 (норма — до 87 МЕ/мл). Назначена терапия: кетотифен 1 мг 2 р/сут, омепразол.
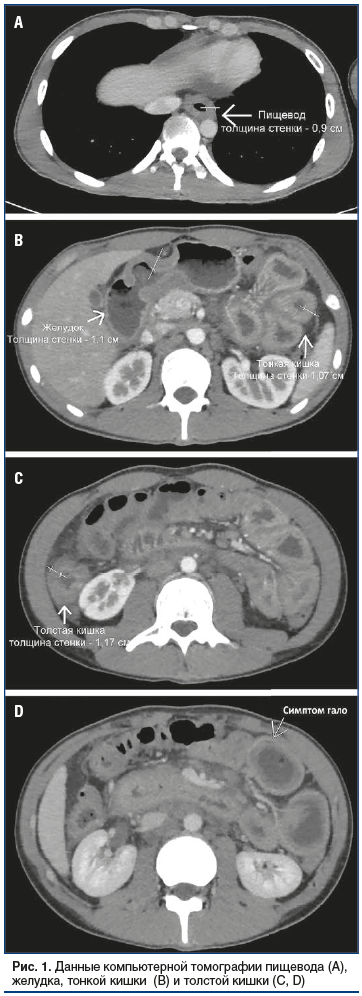
При компьютерной томографии брюшной полости с внутривенным контрастированием стенки нижней трети пищевода равномерно циркулярно утолщены до 0,9 см, в просвете пищевода газ (рис. 1А). Равномерное циркулярное утолщение стенок антрального отдела желудка до 1,1 см (рис. 1B). Стенки тонкой кишки, проксимального отдела толстой кишки равномерно циркулярно утолщены до 1,1 см, с ранним контрастированием внутреннего слоя (рис. 1B, 1C). Отмечается положительный симптом «гало» (рис. 1D). Жировая клетчатка брюшной полости уплотнена за счет отека. Выпот в брюшной полости в небольшом количестве — по латеральным каналам и в полости малого таза. Лимфатические узлы не увеличены.
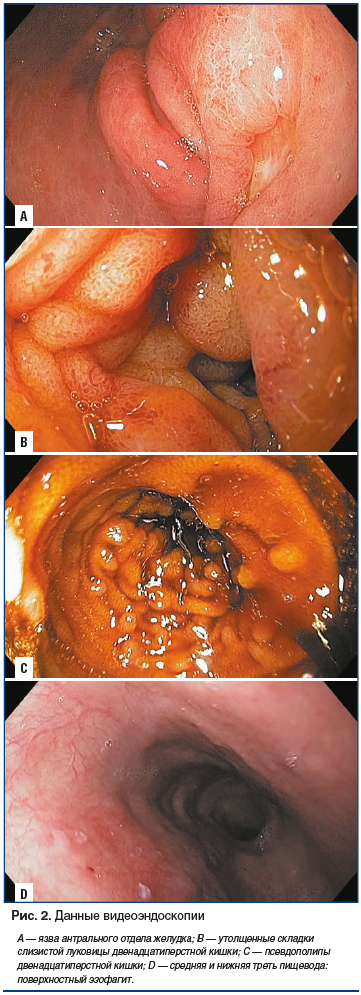
По данным ЭГДС и колоноскопии выявлен кандидоз пищевода, очаговый эзофагит, выраженный диффузный гастрит, эрозии в антральном отделе желудка, язва антрального отдела желудка в подострой фазе, диффузный эрозивный бульбит и дуоденит; лимфофолликулярная гиперплазия слизистой терминального отдела подвздошной кишки на фоне эрозивного терминального илеита, очаговый эрозивный тифлит, диффузный колит с единичными эрозиями (рис. 2).
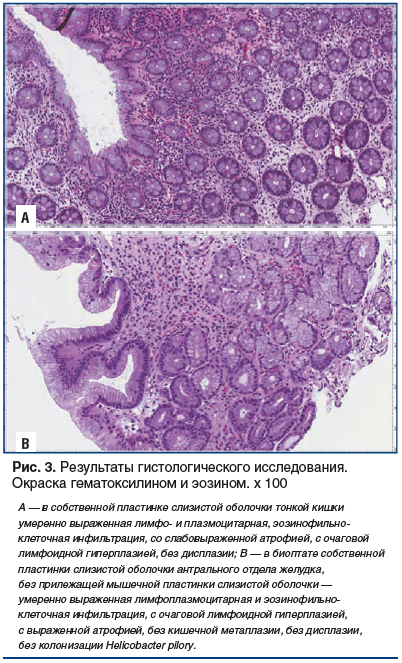
По данным гистологического исследования в биоптатах собственной пластинки слизистой оболочки тонкой кишки — умеренно выраженная лимфоплазмоцитарная, эозинофильно-клеточная инфильтрация, со слабовыраженной атрофией, очаговой лимфоидной гиперплазией, без дисплазии (рис. 3А); в биоптатах собственной пластинки слизистой оболочки толстой кишки, с прилежащей пластинкой слизистой оболочки — умеренно выраженная лимфоплазмоцитарная и эозинофильно-клеточная инфильтрация, со слабовыраженной атрофией, очаговой лимфоидной гиперплазией; в биоптате собственной пластинки слизистой оболочки антрального отдела желудка — умеренно выраженная лимфоплазмоцитарная и эозинофильно-клеточная инфильтрация, с очаговой лимфоидной гиперплазией, выраженной атрофией (рис. 3B); в биоптате слизистой оболочки пищевода, выстланного многослойным плоским эпителием, без атипии, с прилежащей мышечной оболочкой, на всем протяжении фрагмента отмечена умеренно выраженная лимфоплазмоцитарная и эозинофильно-клеточная инфильтрация.
Пациенту поставлен диагноз: Эозинофильный эзофагит. Эозинофильный гастродуоденит. Эозинофильный колит. Кандидоз пищевода. Асцит. Хроническая язва желудка. Рекомендована диета c элиминацией сои, пшеницы, яиц, молока, арахиса, орехов, рыбы, моллюсков. Начата терапия: кетотифен 1 мг 3 р/сут, фексофенадин 180 мг 1 р/сут, фамотидин 20 мг 2 р/сут до еды, висмута трикалия дицитрат 120 мг 3 р/сут до еды 10 дней, флуконазол 200 мг внутривенно капельно 1 р/сут 7 дней.
На фоне терапии отмечена положительная динамика: боли в животе полностью регрессировали, стул нормализовался, рвоты не было, лейкоцитоз и эозинофилия с тенденцией к снижению от 05.03.2020 (табл. 1).
Однако, несмотря на клиническое улучшение и стихание желудочно-кишечной симптоматики, 06.03.2020 у пациента развился эпизод лихорадки до 38 °С, без озноба, видимый глазом отек левой шейной области, отмечено нарастание уровня СРБ до 174 мг/л, уровень прокальцитонина — 0,06 нг/мл (норма — менее 0,1 нг/мл).
При физикальном обследовании пальпировался болезненный мягкоэластический узел надключичной локализации. По данным УЗИ на фоне выраженного отека мягких тканей надключичной области и шеи слева лоцировались множественные лимфатические узлы гипоэхогенной гетерогенной структуры от 5×4 мм до 11×18 мм, признаки организованного окклюзирующего тромбоза дистального сегмента внутренней яремной и подключичной вены с переходом на плечеголовную вену слева с перифлебитом.
Состояние было расценено как лимфаденит, осложнившийся региональным флебитом. К лечению был добавлен эноксапарин 60 мг подкожно каждые 12 ч и цефтриаксон по 1 г 2 р/сут. На фоне проводимой терапии отек шеи регрессировал, температура нормализовалась, СРБ снизился до нормы.
Однако по мере стихания явлений лимфаденита 08.03.2020 вновь отмечен рост лейкоцитоза и абсолютного числа эозинофилов (20,1×109/л и 15,1×109/л соответственно). Доля эозинофилов составила 74,7%. Была начата терапия метилпреднизолоном 16 мг/сут внутрь.
Через 2 дня (10.03.2020) число лейкоцитов снизилось до нормы (5,32×109/л, эозинофилия полностью регрессировала — 0,3×109/л (5,7%). Пациент выписан на амбулаторный этап лечения с рекомендацией последующего постепенного снижения дозы метилпреднизолона (на 2 мг/сут каждую неделю).
На амбулаторном этапе лечения сохранялась выраженная положительная динамика: боли в животе полностью прекратились, стул оформленный, 1 раз в сутки, коричневого окраса, устойчивая нормотермия. Тромбоз внутренней яремной вены с признаками реканализации. В клиническом анализе крови — умеренный лейкоцитоз без эозинофилии (см. табл. 1).
Обсуждение
Эозинофильный гастроэнтерит (ЭГЭ) был впервые описан Kaijser [1] в 1937 г. Позже морфологически сходное поражение было описано и в пищеводе, и в толстом кишечнике. Выделяют 3 клинико-морфологических варианта: мукозальный (слизистый), мускулярный и субсерозный [2].
Эозинофильные заболевания ЖКТ (ЭЗЖКТ) считаются довольно редкими. Так, распространенность эозинофильного эзофагита, оцененная по результатам эндоскопий, составила 20 на 100 000 [3], а встречаемость ЭГЭ в США, по объединенным данным нескольких исследований, — 28 на 100 000 населения [4]. Заболевание поражает пациентов обоих полов, любого возраста, самый частый возраст дебюта — между третьей и пятой декадой жизни, пик заболеваемости — в третьей декаде.
Патогенез ЭЗЖКТ остается не вполне ясным. Заболевания считаются мультифакторными. В качестве предрасполагающих факторов описаны пищевая аллергия и другие атопические заболевания (бронхиальная астма, аллергический риносинусит, экзема). В некоторых исследованиях отмечена ассоциация с аутоиммунными заболеваниями (целиакия, язвенный колит, системная красная волчанка). Триггером заболевания является перенесенная инфекция либо экспозиция какого-то аллергена, либо факторы окружающей среды [2, 3].
В основе патогенеза болезни лежит дефектный ответ Th2-лимфоцитов, которые активируются после экспозиции пищевого фактора, происходит увеличение экспрессии интерлейкина (ИЛ)-5, что запускает механизмы гиперпродукции эозинофилов и эозинофильной инфильтрации тканей. Показана роль эотаксина в рекрутинге эозинофилов и развитии тканевой эозинофилии в ответ на презентацию антигена, к которому имеется сенсибилизация. Эозинофилы, инфильтрирующие ткани, высвобождают пул цитокинов (ИЛ-3, ИЛ-5 и гранулоцитарный макрофагальный колониестимулирующий фактор), а также выбрасывают основной эозинофильный белок, цитотоксический катионный белок, что приводит к повреждению инфильтрированных тканей и развитию локального воспаления [2].
Основным морфологическим признаком ЭЗЖКТ является тканевая эозинофилия. В норме эозинофилы представлены в слизистой оболочке ЖКТ всех отделов, за исключением пищевода. Выраженность эозинофилии, которую можно рассматривать как подтверждение диагноза ЭЗЖКТ, для желудка и тонкой кишки рекомендуется определить как по крайней мере 20 клеток в поле зрения большого увеличения [5]. Для пищевода, в соответствии с рекомендациями Российской гастроэнтерологической ассоциации, это 15 и более клеток [6].
Важно отметить, что менее выраженная тканевая эозинофилия не позволяет исключить ЭЗЖКТ, так как результаты подсчета клеток определяются и клиническим вариантом болезни, и глубиной взятия образцов для биопсии.
В лабораторных анализах у пациентов с ЭГЭ наблюдается эозинофилия периферической крови, ускорение СОЭ. У 2/3 пациентов повышены уровни IgE. При развитии асцита в перитонеальной жидкости преобладают эозинофилы (до 90% от всех лейкоцитов).
При эндоскопии может выявляться как нормальная слизистая, так и поверхностная гиперемия, язвы, полипы и псевдополипы. Ничто из перечисленного не является специфичным для ЭГЭ, однако такие находки могут определить краткосрочные цели для терапии и профилактики осложнений. Однократная биопсия позволяет выявить тканевую эозинофилию не более чем в 60% случаев, однако проведение повторной эндоскопии с биопсией повышает чувствительность гистологического исследования.
При проведении МСКТ картина в целом неспецифична, демонстрирует утолщение стенки ЖКТ и отек подслизистого слоя. При выраженном воспалении могут наблюдаться отек окружающей жировой клетчатки и выпот в брюшной полости. Характерным, хотя и не специфическим, признаком является симптом «гало» («halo sign»), который представляет собой инфильтрацию подслизистой оболочки кишки жиром между собственной мышечной оболочкой и слизистой оболочкой. Он характеризуется внутренним (слизистая оболочка) и наружным (собственно мышечная и серозная оболочка) кольцом контраст-усиливающей стенки кишки с неусиливающим средним слоем (подслизистая оболочка).
Предложены следующие диагностические критерии, позволяющие считать диагноз ЭЗЖКТ вероятным [5]: симптомы со стороны ЖКТ, гистологически подтвержденная тканевая эозинофилия одной или нескольких областей пищеварительного тракта, исключение других причин тканевой эозинофилии.
Из-за относительно небольшого количества исследований и проведения работ на сравнительно небольших группах пациентов естественное течение заболевания определено недостаточно. Известны случаи самопроизвольной спонтанной ремиссии без терапии, однако у большинства пациентов заболевание прогрессирует с исходом в синдром мальабсорбции и недостаточность питания. У нелеченых пациентов могут быть такие осложнения, как обструкция кишки и перфорация, формирование стриктуры или хронической глубокой язвы. Часто возникают обострения с периодами от месяцев до лет после эффективного лечения первичной атаки, и, таким образом, возникает необходимость длительного поддерживающего лечения [4].
В лечении эозинофильных заболеваний используется элиминационная диета, подобранная соответственно профилю сенсибилизации пациента. В нетяжелых случаях она позволяет купировать атаку заболевания вплоть до формирования ремиссии.
В педиатрической практике может быть полезна также длительная элементная диета с использованием аминокислотных смесей [7, 8]. Однако показано, что даже при успешном купировании первой атаки такой подход не позволял предупреждать обострения. Кроме того, во взрослой практике такая диета едва ли применима.
В лечении эозинофильного эзофагита нашли применение ингибиторы протонной помпы (способны вызвать ремиссию почти в половине случаев) и принимаемые перорально топические глюкокортикоиды флутикозон и будесонид, эффективность которых составляет 60–90% [2, 6].
Неконкурентный Н1-гистаминоблокатор и стабилизатор мембран тучных клеток кетотифен также нарушают хемотаксис эозинофилов в воспаленные области. В литературе имеются описания клинических случаев ЭГЭ, успешно пролеченных с помощью кетотифена, с многолетней ремиссией [4]. Описаны также случаи успешного применения другого стабилизатора тучных клеток — натрия кромогликата [9].
Селективный ингибитор лейкотриеновых D4 рецепторов монтелукаст также блокирует привлечение в ткани эозинофилов. Описанные клинические случаи показывают его эффективность как в терапии атак заболевания, так и в долгосрочном контроле тканевой эозинофилии.
Системные глюкокортикоиды в дозе 30–40 мг/сут перорально (в пересчете на преднизолон) — наиболее часто используемые препараты, назначаются либо при неэффективности терапии, либо при изначально тяжелой форме заболевания. Приблизительно в трети случаев удается достичь полного эффекта без последующих рецидивов, еще в трети случаев после достигнутой ремиссии вновь развиваются обострения при попытке их отмены [1].
Имеется также целый ряд методов, место которых в лечении ЭЗЖКТ точно не определено, хотя их эффективность предполагается на основании отдельных наблюдений. К ним относятся иммуносупрессоры (6-меркаптопурин и азатиоприн), внутривенный иммуноглобулин, меполизумаб (моноклональное антитело, блокирующее ИЛ-5), ингибиторы ФНО-α (инфликсимаб, адалимумаб, этанерцепт), макролиды (эритромицин и кларитромицин) [5, 10–14].
Заключение
Таким образом, в приведенном наблюдении ЭЗЖКТ в виде эозинофильного эзофагита, эозинофильного гастроэнтерита и эозинофильного колита имело характерные клинические проявления, типичную рентгенологическую картину (выраженное утолщение вовлеченных отделов ЖКТ, асцит), характерные эндоскопические признаки, было подтверждено обнаружением тканевой эозинофилии. Особенностью случая следует считать необычную распространенность процесса — от нижней трети пищевода до слепой кишки.
Интерес представляет также необычное осложнение в виде левостороннего надключичного лимфаденита, осложнившегося тромбофлебитом подключичной и внутренней яремной вены. С одной стороны, быстрое и значительное возрастание уровня СРБ, быстрый и полный ответ на лечение цефтриаксоном свидетельствуют о бактериальной природе лимфаденита. С учетом хорошо известного факта о связи лимфатических узлов левой надключичной области с органами ЖКТ и отсутствия местных источников воспаления можно предположить, что входными воротами инфекции послужила слизистая оболочка тонкой кишки, поврежденная основным заболеванием. Вследствие этого обсуждаемое наблюдение дает повод для настороженности в отношении бактериальных инфекций в активную фазу ЭЗЖКТ.
Список литературы Вы можете найти на сайте http://www.rmj.ru
.
Информация с rmj.ru






