Введение
Подагра — системное заболевание, характеризующееся отложением в различных тканях кристаллов моноурата натрия и развивающимся в связи с этим воспалением у лиц с гиперурикемией, обусловленной внешнесредовыми
и/или генетическими факторами [1]. По данным эпидемиологических исследований, ее распространенность во многих странах продолжает расти [2–6]. В Российской Федерации встречаемость подагры составляет 0,3% [7].
Нестероидные противовоспалительные препараты (НПВП) нашли широкое применение в лечении подагрического артрита (ПА). Всем пациентам с острым ПА в качес-тве терапии первой линии рекомендовано назначение НПВП, колхицина или глюкокортикостероидов (ГКС) [8–10]. Эффективность различных НПВП (как селективных, так и неселективных блокаторов циклооксигеназы (ЦОГ)) сопоставима [10]. Рекомендуют применять профилактическую противовоспалительную терапию (колхицин, или НПВП, или ГКС) в течение 3–6 мес. при назначении пациенту уратснижающей терапии [8, 10]. Ограничивают прием НПВП нежелательные реакции, обусловленные блокадой ЦОГ 1-го типа (ЦОГ-1). Использование селективных ингибиторов ЦОГ 2-го типа (ЦОГ-2) позволяет снизить число нежелательных реакций со стороны желудочно-кишечного тракта (ЖКТ) [11]. Одним из высокоселективных ингибиторов ЦОГ-2 является эторикоксиб (ЭК; 5-хлоро-3-(4-метансульфонилфенил)-6-метил-[2,3’]-бипиридинил), представляющий собой производное дипиридинила, содержащее (4-метилсульфонил) фенильную группу, связанную с центральным кольцом и обеспечивающую взаимодействие с ЦОГ-2 [12] примерно в 106 раз более мощное, чем с ЦОГ-1, и имеющий более выраженную ЦОГ-2-селективность, чем целекоксиб, рофекоксиб и вальдекоксиб [13]. При очевидной безопасности ЭК в отношении ЖКТ остается неизвестным, насколько безопасен препарат в отношении сердечно-сосудистой системы, особенно при условии многократно повторяющихся курсов его
приема.
Цель исследования: изучить частоту развития инфаркта миокарда (ИМ), артериальной гипертензии (АГ) и хронической болезни почек (ХБП) у пациентов с хроническим или рецидивирующим ПА на фоне применения ЭК повторными курсами.
Материал и методы
Анализ применения НПВП у пациентов с ПА проведен на основании данных Санкт-Петербургского городского регистра подагры и бессимптомной гиперурикемии за период с 2000 по 2019 г., сформированного на базе облачной электронной системы хранения данных GALENOS (OOO «TexЛаб»). Критерии включения в исследование: наличие информированного согласия пациента на участие в исследование, наличие ПА, возраст 18 лет и старше на момент включения в исследование. Критериями исключения служили беременность, вторичный генез подагры (опухоли и др.). Внесение данных пациентов в регистр проводилось в обезличенном виде, не позволяющем идентифицировать отдельного пациента как личность. Каждому пациенту присваивался индивидуальный номер. Исследование было одобрено локальным комитетом по этике ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России и СПб ГБУЗ «КРБ № 25» с соблюдением Федерального закона о персональных данных РФ с поправкой от 30.12.2017.
Регистр содержит сведения о числе пациентов, принимавших ЭК и другие НПВП, с указанием длительности приема и используемых дозировок препаратов. Рассчитывали индекс приема НПВП Дугадоса (относительное количество препарата, суммарно принятое пациентом за определенный период времени, рассчитанное относительно количества препарата, максимально разрешенного к приему за указанный период, и выраженное в процентах). На фоне приема ЭК оценивали возникновение de novo следующих коморбидных состояний: АГ, ИМ и ХБП.
Статистический анализ проводили с использованием пакета программного обеспечения STATISTICA 8.0 (StatSoftInc, США). Характер распределения данных оценивали графическим методом и с использованием критерия Шапиро — Уилка. В случае нормального распределения признака его описывали в виде среднее±стандартное отклонение (M±SD). При распределении данных, отличном от нормального, применяли критерий χ2. Рассчитывали относительный риск (ОР) развития событий и доверительный интервал (ДИ) для него. Различия и взаимосвязи считали статистически значимыми при p≤0,05.
Результаты исследования
Всего в регистр включены данные обследования и лечения 1725 пациентов с первичным ПА. ЭК принимали 315 (18,26%) пациентов, из них 209 — только ЭК, 106 человек чередовали прием ЭК и других НПВП. Повторные курсы (не менее двух) ЭК получили 118 пациентов (из них 75 (63,6%) мужчин), средний возраст которых составил 57,1±7,9 (24–89) года. Продолжительность каждого курса ЭК варьировала от 1 до 7 дней. Назначаемая доза ЭК составляла 120 мг/сут (доза могла быть снижена врачом ЛПУ по месту жительства при наличии коморбидности до 90 или 60 мг/сут). В группу сравнения включили 60 человек (из них 45 (75%) мужчин; средний возраст — 57,1±14,8 (17–88) года), принимавших другие НПВП без переключения на другие препараты этой группы. В исследование вошли пациенты, посетившие центр подагры не менее 2 раз с интервалом в год. Таким образом, в статистический анализ суммарно включены данные 178 пациентов с ПА.
Относительное количество принимаемых уратснижающих средств, уровень мочевой кислоты в сыворотке крови, индекс курения, сердечно-сосудистый риск в группах пациентов групп ЭК и других НПВП были сопоставимы.
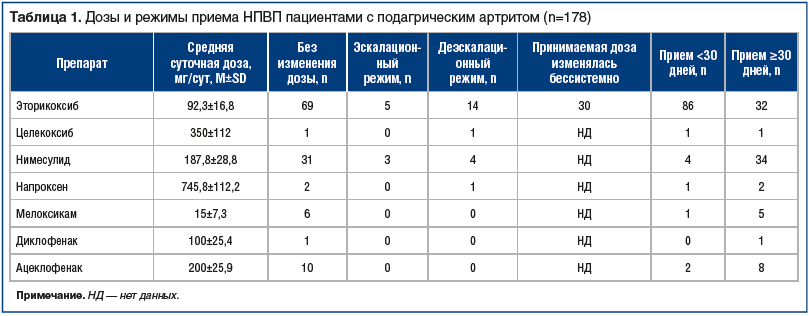
Средняя продолжительность приема ЭК составила 24,9±15,2 (8–87) дня, других НПВП из группы сравнения — 37,1±9,8 (21–74) дня (p<0,0001). В зависимости от длительности приема ЭК и других НПВП пациенты были разделены на 2 группы: в первую группу (кратковременного приема) включили пациентов, получавших терапию суммарно менее 30 дней, во вторую — 30 дней и более. Индекс приема НПВП (индекс Дугадоса) для ЭК составил 6,8%, для других НПВП — 10,2%, (p<0,05). Режимы приема НПВП и средние дозы НПВП представлены в таблице 1.
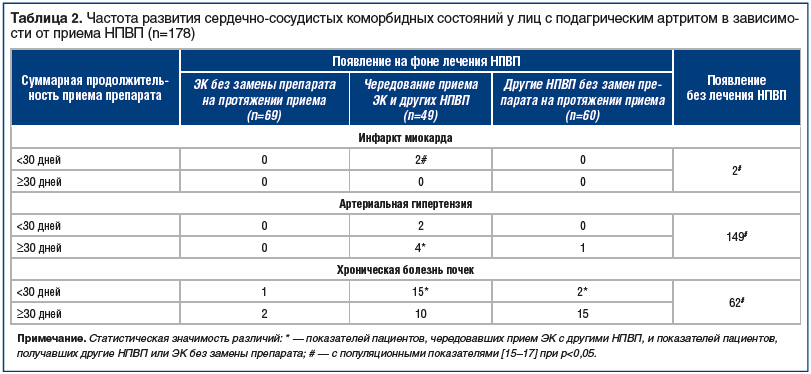
Согласно данным таблицы 2 из 178 пациентов с ПА у 7 (3,9%) на фоне приема НПВП зафиксировано формирование АГ de novo (распространенность в популяции — 60% [15]). ИМ (распространенность в общей популяции — 129 случаев на 100 тыс. населения [16]) развился у 2 (1,7%) пациентов с ПА на фоне приема НПВП (ОР=13,8, 95% ДИ 3,4–5,27, p=0,0005). У 45 (25,3%) пациентов с ПА на фоне приема НПВП отмечено формирование ХБП de novo (распространенность в популяции составляет 36% [17]) (ОР=0,7, 95% ДИ 0,48–1,0, p=0,0736).
Обсуждение
Изучение сердечно-сосудистых заболеваний на фоне приема НПВП представляется важной задачей клиники внутренних болезней, особенно в популяции лиц с высоким риском их развития [14]. Известно, что подагра и бессимптомная гиперурикемия являются независимыми факторами риска сердечно-сосудистых событий [14–16]. Настоящее исследование показало, что встречаемость сердечно-сосудистой патологии (АГ, ХБП, ИМ) у пациентов с ПА еще до приема первого НПВП превышает популяционные значения, что согласуется с нашими более ранними работами [17]. Интересным результатом настоящей работы явился тот факт, что на фоне лечения НПВП увеличение встречаемости сердечно-сосудистых событий отмечено только в группе пациентов с ПА, чередовавших прием ЭК с другими препаратами группы НПВП. В случае же приема только ЭК увеличения сердечно-сосудистой заболеваемости не отмечено. Указанный феномен можно объяснить тем, что ЭК в этих случаях применялся в меньших суммарных дозах и на протяжении меньшего времени (что косвенно свидетельствует о его высокой эффективности по сравнению с другими НПВП в лечении ПА). Нельзя исключить и способность разных НПВП потенцировать нефро- и кардиоповреждающее действие при последовательном их применении. Дозозависимый характер поражения сердечно-сосудистой системы и почек на фоне приема НПВП был показан в исследовании MEDAL при сравнении ЭК в суточных дозах 60 и 90 мг и диклофенака натрия в суточной дозе 150 мг (при объединении группы остеоартрита и ревматоидного артрита), но не в дозе 60 мг в сутки [18]. В метаанализе, объединившем 31 исследование, включавшее 116 429 пациентов и более 115 000 человеко-лет наблюдения, было показано, что все включенные в него препараты из группы НПВП ассоциируются с повышенным риском неблагоприятных исходов; при этом риск возникновения ИМ при применении ЭК не превышал таковой у диклофенака натрия и напроксена [19]. В нашем исследовании лишь 2 случая ИМ были связаны с приемом ЭК и других НПВП (пациенты до развития ИМ были переведены на другие препараты). Развитие АГ не было зафиксировано у пациентов, принимавших только ЭК. Прямая ассоциация развития ХБП с приемом ЭК была отмечена в 3 из 28 случаев развития ХБП. Полученные различия между группами свидетельствуют об увеличении частоты АГ и ХБП только при заменах ЭК (переключения как на ЭК, так и с ЭК) на другой НПВП, независимо от длительности их приема.
Следует отметить, что АГ, ИМ и ХБП способны взаимно потенцировать друг друга, формируя «порочные круги» (ХБП поддерживает АГ, а АГ усугубляет ХБП), как и сохраняющееся хроническое воспаление при подагре, в связи с не всегда достаточной коррекцией гиперурикемии у данной группы пациентов [16]. Неконтролируемое субклиническое воспаление на фоне гиперурикемии поддерживает высокую сердечно-сосудистую заболеваемость и смертность у пациентов с подагрой, не получающих НПВП. В то же время, по результатам нашего исследования, нельзя исключить, что адекватное и контролируемое уменьшение воспаления с применением современных НПВП из группы коксибов может улучшить сердечно-сосудистый прогноз у пациентов с ПА.
Заключение
Встречаемость ИМ, АГ и ХБП у пациентов с хроническим и рецидивирующим ПА, не принимающих НПВП, превышает популяционные значения. Применение повторных курсов ЭК для лечения хронического или рецидивирующего ПА не ассоциируется с увеличением рисков развития ИМ, АГ или ХБП при условии отсутствия переключения ЭК на другие НПВП, т. к. в этом случае достигаются наименьшие продолжительность приема и суммарная доза НПВП.
.
Информация с rmj.ru






