Введение
Тяжелая бронхиальная астма (ТБА) — форма трудно поддающейся лечению бронхиальной астмы (БА), которая остается неконтролируемой, несмотря на приверженность максимально оптимизированной терапии и лечению сопутствующих заболеваний, или ухудшается при снижении высоких доз глюкокортикостероидов (ГКС) [1].
Согласно рекомендациям Global Initiative for Asthma за 2022 г. (GINA 2022) предпочтительными препаратами для 5-й ступени терапии БА являются высокие дозы ингаляционных глюкокортикостероидов (ИГКС) и длительно действующих β2-агонистов (ДДБА) или тройных фиксированных комбинаций ИГКС/ДДБА с длительно действующими антихолинергическими (ДДАХ) препаратами [2]. Применение системных глюкокортикостероидов (СГКС) рекомендовано только в качестве альтернативы другим группам препаратов. GINA 2022 рекомендует проводить короткие (5–7 дней) курсы терапии СГКС только при обострениях БА. Длительное применение этих препаратов не рекомендуется из-за повышенного риска развития нежелательных явлений (НЯ). Однако, по данным литературы, порядка 15–57% пациентов с тяжелой или рефрактерной БА постоянно используют СГКС [3–6]. Так, в США примерно 15–22% пациентов с ТБА постоянно получают СГКС, в Европе — 46–57%, в частности в Италии — 62% [4–6].
Первые сообщения о повышенной частоте переломов, нарушениях углеводного обмена, желудочно-кишечных кровотечениях, инфекциях и нарушениях зрения у пациентов, длительно принимающих СГКС в дозах 20–60 мг/сут, появились в 1950-е годы [7]. Уже с 1990-х медицинские специалисты стремятся применять более низкие (5 мг/сут) дозы СГКС или использовать альтернативные лекарственные средства (ЛС) [7]. Однако даже низкая (0,5–1 г) кумулятивная доза СГКС может стать причиной серьезных неблагоприятных исходов [8]. Кроме того, риск НЯ повышается с увеличением накопительной дозы СГКС [8]. Применение СГКС ассоциировано со снижением качества жизни, увеличением затрат системы здравоохранения и показателей смертности [9]. Учитывая побочные эффекты, применение СГКС необходимо минимизировать. Снижению дозы СГКС и их последующей отмене способствует биологическая терапия моноклональными антителами. На данный момент отсутствует общепринятый алгоритм снижения дозы СГКС, несмотря на то что этот этап требует внимания как с точки зрения риска обострения БА, так и с точки зрения функционального состояния надпочечников. Развитие ТБА у большинства пациентов связано с активацией Т2-воспаления, в формировании которого участвуют эозинофилы, Th2-лимфоциты и врожденные лимфоидные клетки 2-го типа (ILC2), генерирующие цитокины Т2-профиля: интерлейкин (ИЛ) 4, ИЛ-5, ИЛ-13. В настоящее время таргетная терапия ТБА направлена на нейтрализацию циркулирующих ИЛ-5 (меполизумаб, реслизумаб), блокаду альфа-субъединицы рецептора ИЛ-5 (ИЛ-5Rα) (бенрализумаб) и альфа-субъединицы рецептора ИЛ-4, что нивелирует активность ИЛ-4 и ИЛ-13 (дупилумаб) [10].
Большинство (82%) пациентов с ТБА отнесены к эозинофильному фенотипу, который характеризуется более тяжелым течением, повышенной частотой обострений и резистентностью к стандартной противовоспалительной терапии [11]. Таким образом, подавление активности эозинофилов является перспективным направлением патогенетической терапии ТБА.
Одним из ЛС, подавляющих активность эозинофилов, является бенрализумаб. Препарат представляет собой моноклональное антитело, которое напрямую связывается с альфа-субъединицей рецептора ИЛ-5, индуцирует активный апоптоз эозинофилов за счет антителозависимой клеточно-опосредованной цитотоксичности, что приводит к быстрому и устойчивому, почти полному истощению эозинофилов в крови и тканях-мишенях [12].
Краткий обзор клинических исследований
Эффективность бенрализумаба и его влияние на контроль БА, частоту обострений, показатели функции внешнего дыхания (ФВД) были продемонстрированы в многоцентровых рандомизированных клинических исследованиях (РКИ) III фазы SIROCCO и CALIMA [13, 14]. Основная анализируемая популяция включала пациентов, получавших высокие дозы ИГКС в сочетании с ДДБА, с уровнем эозинофилов в крови ≥300 клеток/мкл. Пациенты были рандомизированы в 3 группы: 1-я группа — инъекции бенрализумаба в дозе 30 мг каждые 4 нед.; 2-я группа — инъекции бенрализумаба в дозе 30 мг каждые 4 нед. (первые 3 дозы) с последующим назначением бенрализумаба в дозе 30 мг каждые 8 нед.; 3-я группа — плацебо.
Активная фаза исследования SIROCCO продолжалась 48 нед., затем до 56-й недели длился период наблюдения без введения бенрализумаба. НЯ были зарегистрированы у 72% пациентов в группах бенрализумаба и у 76% в группе плацебо. Частота НЯ не зависела ни от дозы препарата, ни от уровня эозинофилов. Большая часть побочных эффектов не была связана с терапией бенрализумабом. В исследовании CALIMA длительность терапии бенрализумабом составила 56 нед. Post hoc анализ данных этих РКИ продемонстрировал статистически значимое снижение частоты обострений БА на 36% (p<0,001) и 42% (p<0,001) в исследованиях CALIMA и SIROCCO соответственно [15]. Также отмечалось улучшение ФВД: у пациентов с уровнем эозинофилов в крови ≥300 клеток/мкл показатель ОФВ1 увеличился на 159 мл через 4 нед. после введения первой дозы ЛС [13]. В результате терапии бенрализумабом был достигнут контроль БА и снижение количества эозинофилов в крови.
Пациенты, участвовавшие в РКИ CALIMA и SIROCCO, продолжили участие в расширенном исследовании по оценке безопасности и эффективности бенрализумаба — BORA [16]. Продолжительность исследования BORA составила 56 нед. у взрослых пациентов и 108 нед. у подростков. Результаты исследования показали, что на 2-й год наблюдения на фоне терапии 74% пациентов не имели обострений. Отмечено также увеличение ОФВ1 уже к 4-й неделе, которое сохранялось на протяжении 2 лет терапии у пациентов с числом эозинофилов >300 клеток/мкл. Профиль безопасности бенрализумаба был сопоставим с плацебо.
Продолжением исследования BORA стало другое расширенное исследование безопасности бенрализумаба — MELTEMI, — комплексный анализ результатов которого показал, что у пациентов с эозинофильной ТБА, получавших бенрализумаб в течение 5 лет, длительная деплеция эозинофилов не была связана с повышенным риском серьезной инфекции или какими-либо неизвестными ранее НЯ [17]. Эти результаты дополнительно подтвердили долгосрочную безопасность и эффективность бенрализумаба в достижении и поддержании контроля ТБА.
Результаты опорного исследования III фазы ZONDA показали, что бенрализумаб статистически значимо (p<0,001) снижает потребность в оральных глюкокортикостероидах (ОГКС) у пациентов с БА и эозинофилией крови, принимающих высокие дозы ИГКС/ДДБА и ОГКС: снижение потребности в ОГКС составило 75% и 25% для групп бенрализумаба и плацебо соответственно [18]. Вероятность снижения дозы ОГКС была более чем в 4 раза выше при использовании бенрализумаба в сравнении с плацебо. Две трети пациентов, получавших бенрализумаб, снизили дозу ОГКС на ≥50%. Порядка 50% пациентов, получавших преднизолон в дозе ≤12,5 мг, полностью прекратили использование ОГКС. При этом частота обострений БА была статистически значимо ниже при использовании бенрализумаба по сравнению с плацебо: до 70% снизилось общее число обострений (p<0,001), до 93% — число обострений, требующих обращения в отделение неотложной терапии или госпитализации. Помимо этого, у пациентов отмечено увеличение ОФВ1 уже после введения первой дозы бенрализумаба, которое сохранялось на протяжении всего периода лечения.
Возможность снижения дозы СГКС на фоне лечения бенрализумабом была подтверждена также в многоцентровом открытом клиническом исследовании PONENTE [19], которое включало 138 центров; исследуемая популяция включала 598 пациентов в возрасте ≥18 лет с эозинофильной ТБА (количество эозинофилов в крови ≥150 клеток/мкл на момент включения в исследование или ≥300 клеток/мкл в предыдущем году), которые получали СГКС в течение как минимум 3 мес. до включения в исследование. В рамках открытого когортного исследования IIIb фазы PONENTE пациенты получали бенрализумаб в дозе 30 мг каждые 4 нед. в течение 3 мес. и далее каждые 8 нед. Снижение дозы СГКС начиналось на 4-й неделе от начала терапии бенрализумабом на 1–5 мг каждые 1–4 нед. в зависимости от начальной дозы, контроля астмы и функционального состояния надпочечников (рис. 1).
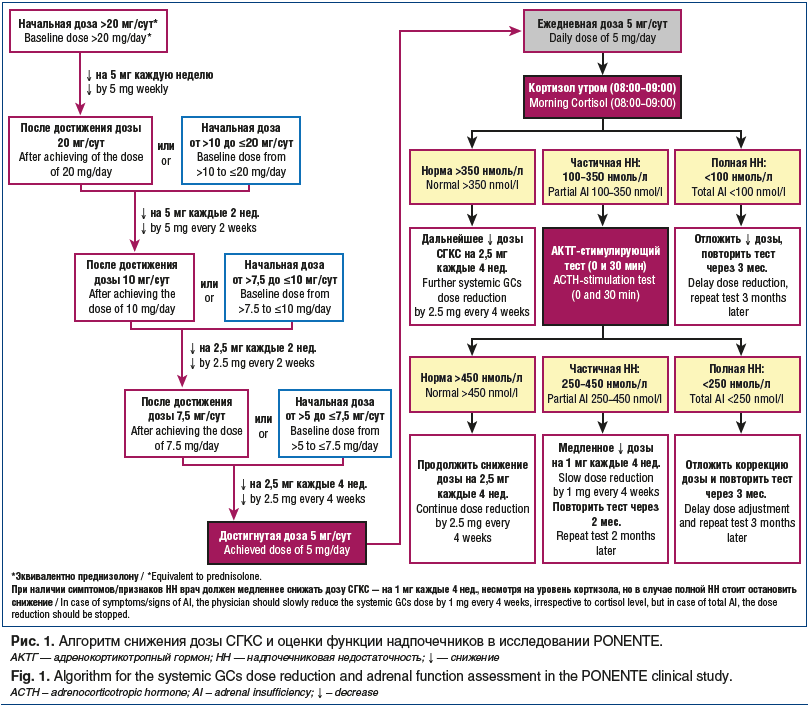
Если на старте пациент получал СГКС в дозе более 20 мг/сут, то снижение составляло 5 мг в неделю до первого промежуточного этапа — достижения дозы 20 мг/сут. Затем дозу СГКС снижали на 5 мг каждые 2 нед. до достижения дозы 10 мг/сут. После чего уменьшение СГКС проводилось на 2,5 мг каждые 2 нед. до достижения дозы 7,5 мг/сут. Далее снижение СГКС проводилось на 2,5 мг каждые 4 нед. до достижения дозы 5 мг/сут. Когда ежедневная доза СГКС достигала 5 мг/сут, проводился анализ крови на содержание утреннего (08:00–09:00) кортизола. Если уровень кортизола был в норме (>350 нмоль/л), дозу СГКС продолжали снижать на 2,5 мг каждые 4 нед. Если концентрация кортизола была <100 нмоль/л, что говорило о наличии полной надпочечниковой недостаточности (НН), снижение дозы СГКС откладывали на 3 мес. Содержание кортизола в диапазоне 100–350 нмоль/л свидетельствовало о наличии частичной НН, в этом случае проводился АКТГ-стимулирующий тест: после определения базального уровня кортизола пациенту внутривенно вводили 250 мкг 1–24-АКТГ и через 30 мин повторно исследовали уровень кортизола. Уровень кортизола >450 нмоль/л позволял рекомендовать дальнейшее снижение дозы СГКС на 2,5 мг каждые 4 нед. При уровне кортизола <250 нмоль/л снижение дозы СГКС не проводили, повторный анализ выполняли через 3 мес. Если концентрация кортизола была в диапазоне 250–450 нмоль/л, проводили медленное снижение дозы на 1 мг каждые 4 нед.; повторный тест выполняли через 2 мес.
Первичными конечными точками в исследовании PONENTE были процент пациентов, прекративших ежедневное применение СГКС в течение не менее 4 нед., и процент пациентов, достигших отмены приема преднизолона или снижения дозы до ≤5 мг/сут в течение не менее 4 нед. (если причиной отказа от дальнейшего снижения была НН). Прием СГКС прекратили 376 (62,88%; 95% ДИ 58,86–66,76) из 598 пациентов, 490 (81,94%; 95% ДИ 78,62–84,94) пациентов прекратили прием или достигли дозы ≤5 мг/сут (в случае НН) [20]. Анализ подгрупп показал, что снижение дозы было достигнуто независимо от исходного количества эозинофилов, базовой дозы СГКС или продолжительности лечения ОГКС. Бенрализумаб был эффективен у пациентов, принимавших ОГКС, в том числе со средним уровнем эозинофилии (≥150 клеток/мкл). Недостаточность функции надпочечников была выявлена у 321 (60%) из 533 пациентов при первом обследовании и у 205 (38%) через 2–3 мес. исследования. У большинства — 448 (75%) — пациентов не было обострений БА в период снижения дозы СГКС [20].
Данные проведенных РКИ подтверждают многочисленные публикации исследований реальной клинической практики [21–23]. В Городском пульмонологическом центре на базе ГБУЗ «Введенская городская клиническая больница» (Санкт-Петербург, Россия) также активно используются генно-инженерные биологические ЛС для лечения пациентов с ТБА, в том числе и бенрализумаб, неоднократно подтвердивший свою эффективность в достижении контроля БА, уменьшении числа обострений, улучшении ФВД и снижении дозы СГКС. Ниже приводится клиническое наблюдение больной ТБА, получавшей терапию бенрализумабом.
Клиническое наблюдение
Больная С., 48 лет, 18.04.2021 была доставлена в стационар каретой скорой медицинской помощи с диагнозом: бронхиальная астма, обострение. При поступлении пациентка предъявляла жалобы на одышку в покое, малопродуктивный кашель, приступы затрудненного дыхания до 8–10 раз в день, которые купировались ингаляцией двух доз комбинированного препарата ипратропия бромид/фенотерол. Ухудшение состояния отмечалось в течение последних 5 дней.
По результатам объективного осмотра у пациентки выявлена тахикардия (ЧСС 110 в минуту), увеличение частоты дыхания (ЧДД 28 в минуту), снижение сатурации (SpO2 92–93%), сухие свистящие хрипы над всей поверхностью легких. Со стороны других органов и систем патологии не выявлено. Оценка по опроснику контроля симптомов астмы ACQ-5 составила 1,9 балла.
Диагноз БА был установлен в 2000 г. Начиная с 2016 г. пациентка стала отмечать частые обострения заболевания, требующие стационарного лечения до 4–5 раз в год. Во время госпитализаций больная получала терапию ГКС в течение 10–14 дней (дексаметазон в дозе 16 мг с постепенным снижением дозировки), ингаляционную терапию (будесонид 4 г/сут, ипратропия бромид/фенотерол по потребности). При обострениях, не требующих госпитализаций (2–3 р/год), проходила короткие (7–10 дней) курсы терапии преднизолоном в дозе 30 мг/сут с постепенным снижением дозировки. С 2018 г. пациентка получала: комбинированное ЛС салметерол/флутиказон 50/500 мкг по 2 вдоха в сутки, тиотропия бромид 2,5 мкг по 2 вдоха в сутки, ипратропия бромид/фенотерол по потребности, преднизолон 10 мг/сут.
Пациентка никогда не курила. В анамнезе имела аллергическую реакцию на новокаин в виде отека Квинке. Работала менеджером, наличие профессиональных вредностей отрицала. Сопутствующие заболевания: хронический пиелонефрит, полипозный риносинусит, по поводу которого дважды проводилась полипотомия (в 1991 и 2015 гг.).
В клиническом анализе крови при поступлении в стационар обращала на себя внимание эозинофилия (814 клеток/мкл). В биохимическом анализе крови отмечалось незначительное повышение концентрации СРБ (6,75 мг/л). Содержание IgЕ не превышало нормальных значений (96 кЕ/л). Рентгенологическое обследование органов грудной клетки выявило повышение прозрачности легочной ткани. Спирометрия с бронхолитической пробой, выполненная при поступлении в стационар, выявила резкое снижение форсированной жизненной емкости легких (ФЖЕЛ) (35,34%) и проходимости дыхательных путей (ОФВ1 21,18%; ОФВ1/ФЖЕЛ 59,59%). Бронходилатационная проба отрицательная (прирост ОФВ1 +2,3%).
При поступлении был поставлен диагноз: ТБА, персистирующее течение, неаллергическая эозинофильная форма, неконтролируемая.
Пациентке были назначены ГКС внутривенно в течение 10 дней (дексаметазон 16 мг/сут с постепенным снижением дозы), эуфиллин, ингаляционная терапия (будесонид 4 г/сут, ипратропия бромид/фенотерол). На фоне проводимой терапии отмечалась положительная динамика в виде исчезновения приступов затрудненного дыхания, уменьшения потребности в скоропомощных препаратах (1 раз в 2 дня на фоне лечения), снижения баллов ACQ-5 (до 1,5), улучшения показателей ФВД (ОФВ1 66,31%), нормализации SpO2 (97%).
Пациентка была выписана через 12 дней, после купирования обострения БА, с диагнозом: ТБА, персистирующее течение, неаллергическая эозинофильная форма, частично контролируемая. Рекомендовано: ингаляционная терапия (салметерол/флутиказон 50/500 мкг по 1 вдоху 2 р/сут, тиотропия бромид 2,5 мкг по 2 вдоха 1 р/сут), преднизолон 10 мг/сут и бенрализумаб 30 мг подкожно каждые 4 нед. (первые 3 инъекции), в последующем 30 мг подкожно каждые 8 нед.
Терапия бенрализумабом была инициирована с июля 2021 г. Препарат вводился в виде инъекций в условиях дневного стационара. НЯ не отмечались. Через 1 мес. у пациентки выявлено: уменьшение содержания эозинофилов в клиническом анализе крови до 35 клеток/мкл; улучшение контроля БА по опроснику ACQ-5 (снижение до 0,95 балла); увеличение ОФВ1 до 77,52% по данным спирометрии. К моменту проведения 3-й инъекции препарата (сентябрь 2021 г.) был достигнут контроль над заболеванием (0,48 балла по ACQ-5) (рис. 2) и рекомендовано снижение текущей дозы СГКС (преднизолон 10 мг/сут) на 2,5 мг.
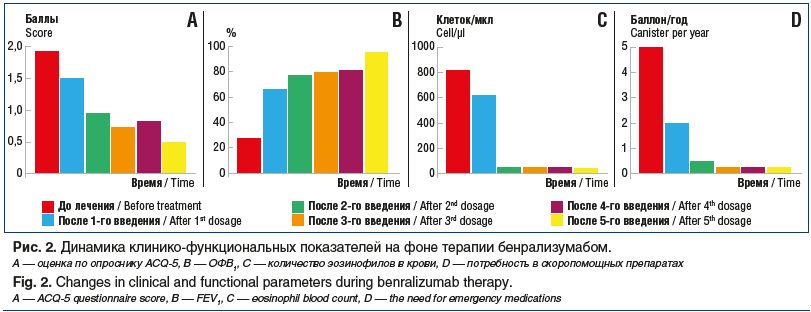
В течение двух последующих недель помимо базисной терапии БА пациентка получала преднизолон 7,5 мг/сут. Снижение ГКС не вызывало ухудшения клинической симптоматики, и через 2 нед. больной было рекомендовано уменьшить дозировку преднизолона до 5 мг/сут. Дальнейшее снижение дозы СГКС также не отразилось на контроле БА. Через 1 мес. был выполнен анализ крови на кортизол с целью решения вопроса о дальнейшей тактике снижения дозы СГКС. Содержание кортизола составило 320 нмоль/л, что свидетельствовало о наличии у больной частичной НН. Был проведен АКТГ-стимулирующий тест. Уровень кортизола в крови через 30 мин после инъекции АКТГ составил 450 нмоль/л. Было принято решение о продолжении снижения дозы СГКС на 2,5 мг каждые 4 нед. Через 2 мес. пациентке удалось полностью отказаться от приема преднизолона в соответствии с регламентированными сроками. Через 2 нед. после отмены СГКС была проведена 5-я инъекция бенрализумаба. Оценка по опроснику ACQ-5 — 0,5 балла — свидетельствовала о полном контроле над заболеванием; показатели вентиляционной функции легких достигли нормальных значений (ОФВ1 95%). За 6 мес. после начала биологической терапии не отмечалось ни одного обострения БА; пациентка переведена на терапию комбинацией беклометазона дипропионат/формотерол 100/6 мкг по 2 ингаляции в сутки. Основные этапы клинического наблюдения приведены на рис. 3.

В описанном клиническом наблюдении у пациентки был высокий исходный уровень эозинофилов периферической крови, однако необходимо отметить, что, по данным исследований, бенрализумаб демонстрирует свою эффективность при уровне эозинофилов начиная от 150 клеток/мкл [15].
Заключение
У пациентов с ТБА бенрализумаб улучшает контроль заболевания, показатели вентиляционной функции легких, снижает потребность в короткодействующих бронхолитиках, уменьшает количество эпизодов обострения заболевания. Бенрализумаб демонстрирует высокий уровень безопасности, сопоставимый с плацебо.
Результаты РКИ подтверждаются данными реальной клинической практики: использование бенрализумаба способствует отмене СГКС у пациентов с ТБА, что позволяет предотвратить развитие НЯ, обусловленных длительной терапией СГКС, при сохранении контроля заболевания.
Представленное клиническое наблюдение больной ТБА, получавшей терапию бенрализумабом, подтверждает результаты ранее проведенных многоцентровых РКИ.
Сведения об авторах:
Титова Ольга Николаевна — д.м.н., профессор, директор НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. акад. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0003-4678-3904.
Кузубова Наталия Анатольевна — д.м.н., заместитель директора по научной работе НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. акад. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0002-1166-9717.
Склярова Дарья Борисовна — к.м.н., старший научный сотрудник НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. акад. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Рентгена, д. 12; ORCID iD 0000-0001-7052-6903.
Контактная информация: Кузубова Наталия Анатольевна, e-mail: kuzubova@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах и методах.
Конфликт интересов отсутствует.
Статья поступила 04.07.2022.
Поступила после рецензирования 27.07.2022.
Принята в печать 19.08.2022.
About the authors:
Olga N. Titova — Dr. Sc. (Med.), Professor, Director of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 12, Roentgen str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0003-4678-3904.
Natalia A. Kuzubova — Dr. Sc. (Med.), Deputy Director for Science of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0002-1166-9717.
Daria B. Sklyarova — C. Sc. (Med.), Senior Researcher of the Research Institute of Pulmonology of the I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0001-7052-6903.
Contact information: Natalia A. Kuzubova, e-mail: kuzubova@mail.ru.
Financial Disclosure: no authors have no a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 04.07.2022.
Revised 27.07.2022.
Accepted 19.08.2022.
.
Информация с rmj.ru





