Содержание статьи
Введение
Проблема пренатальной диагностики врожденных пороков развития (ВПР) и хромосомной патологии плода в настоящее время остается актуальной, несмотря на повсеместное введение скрининговых программ для выявления данной патологии [1]. Заболеваемость детей первого года жизни, связанная с врожденными аномалиями (ВПР), деформациями и хромосомными нарушениями, за последние годы значительно выросла.
Так, если в 2005 г. данный показатель составил 84,7 тыс. (из зарегистрированных 3625,4), то в 2010 г. — 125,3 (из 4419,3), в 2017 г. — 139,7 (из 4454,7), в 2018 г. — 141,4 (из 4260,3) [2].
Значимость пренатальной диагностики хромосомных синдромов неоспорима, так как рождение ребенка с хромосомными аберрациями (ХА), не диагностированными пренатально, не только создает психоэмоциональные проблемы, но и сопровождается социально-экономическими потерями в семье и обществе [3]. В настоящее время в России проводится пренатальный скрининг беременных на наиболее частые ХА, такие как трисомия по хромосомам 21, 18, 13, который включает первый ультразвуковой (УЗ) скрининг в 11,0–13,6 нед на экспертном уровне с одновременным исследованием биохимических маркеров (ассоциированный с беременностью протеин А плазмы (PAPP-A) и свободная β-субъединица хорионического гонадотропина человека (β-ХГЧ)) [4, 5].
На сегодняшний день пренатальным скринингом охвачено около 83–88% беременных, несмотря на это, рождение детей с хромосомной патологией не имеет тенденции к снижению как в России, так и в мире в целом [6, 7].
Цель исследования: оценить эффективность пренатальной диагностики у женщин с постнатально диагностированными ХА у детей.
Материал и методы
Проведено описательное поперечное ретроспективное исследование с использованием данных медицинской документации, базы данных результатов пренатального скрининга 69 женщин, родивших детей с ХА за последние 3 года (2017–2019 гг.) в Алтайском крае Следует отметить, что диагнозы не были установлены на этапе пренатальной диагностики. Исследование проводилось на основании сведений, предоставленных Алтайской межрегиональной медико-генетической консультацией (г. Барнаул) и центром пренатальной диагностики КГБУЗ «АККПЦ» (г. Барнаул) за период 2017–2019 гг.
Проведен подробный анализ пренатальных факторов риска хромосомной патологии согласно общепринятым подходам к проведению пренатального обследования [4–7].
Обследование включало расчет индивидуального риска хромосомной патологии плода с помощью программного обеспечения Astraia на модуле, разработанном Фондом медицины плода (FMF) [5–7]. Риск определялся как высокий при пороговой отсечке 1:100 и выше, в дальнейшем в ходе медико-генетического консультирования решался вопрос о проведении инвазивных методов диагностики (биопсии ворсин хориона, кордоцентеза). В рамках автоматизированной программы Astraia расчет риска в I триместре проводится на основании анамнестических данных, результатов биохимического скрининга (PAPP-A и β-ХГЧ) и УЗ-маркеров ХА (расширение воротникового пространства, гипоплазия или отсутствие изображения носовых костей и др), установленных в 11,0–13,6 нед на экспертном уровне
Далее осуществлялось второе скрининговое УЗИ в сроке гестации 19,0–21,6 нед. При отсутствии первого пренатального скрининга и расчета риска или при наличии дополнительных показаний, которые определялись в рамках медико-генетического консультирования, рассчитывали индивидуальный риск по результатам обследования, проведенного во II триместре. Данное обследование включало второй биохимический скрининг в 16–18 нед. (α-фетопротеин, ХГЧ, эстриол) и УЗИ в 18–21 нед., с последующим программным комплексным расчетом индивидуального риска рождения ребенка с хромосомной патологией (PRISCA-2), и при наличии пороговой отсечки 1:250 рекомендовались инвазивные методы пренатальной диагностики Показанием к проведению инвазивных методов исследования также являлись ВПР, которые можно рассматривать как фенотипическое проявление ХА у плода, так и в качестве самостоятельной патологии.
Статистическую обработку данных проводили с использованием компьютерных программ Microsoft office (Word 2007, Excel 2007), пакета прикладных программ STATISTICA 7.0 (StatSoft Inc., США). Для расчета и анализа качественных показателей использовали абсолютное число и долю этих значений (отношение числа обследованных пациенток, обладающих изучаемым признаком, к общему числу пациенток). Значения долевых показателей представлены в виде доверительных интервалов.
Сравнительный анализ качественных переменных включал построение таблиц сопряженности 2×2 и оценку с помощью критерия Фишера или χ2 с поправкой Йетса на непрерывность
Результаты исследования
Всего за 3 года в Алтайском крае родилось 69 детей с ХА: 22 — в 2017 г., 29 — в 2018 г. и 18 — в 2019 г.
Ретроспективный анализ показал, что большинство детей с постнатально установленными ХА имели синдром Дауна (47, XX+21, 47, XY+21) — 63 (91,3±6,6%) ребенка. Существенно реже выявлялись синдром Эдвардса (47, XX+18, 47, XY±18) — у 2 (2,9±0,5%) детей, синдром Патау (47, XY+13) — у 1 (1,4±0,3%) и другие ХА —
у 3 (4,3±0,6%).
Среди всех родившихся детей с ХА девочек было в 1,7 раза больше, чем мальчиков: 62,3±1,4% и 37,7±1,4% соответственно (р=0,001). Сочетание хромосомной патологии и ВПР выявлено у 12 (17,4±1,2%) детей, из них у 50,0±6,1% отмечены врожденные пороки сердца (преобладают атриовентрикулярные септальные дефекты), на втором месте были пороки мочевыделительной системы — у 25,0±3,7%, пороки опорно-двигательной системы — у 8,3±2,7%, пороки ЖКТ — у 8,3±2,7%, пороки ЦНС — у 8,3±2,7%.
Возраст женщин, родивших детей с постнатально установленной хромосомной патологией, составил 35,0±2,3 года. При этом в 4,3% случаев возраст матери на момент рождения ребенка был 19–25 лет (в среднем 21,3±2,1 года), в 40,6% случаев — 26–34 года (в среднем 31,2±2,6 года). При этом каждая вторая женщина (55,1%) была старше 35 лет (средний возраст 39,0±2,1 года).
Анализ показал, что у 14 (20,3±1,1%) женщин отсутствовали эхографические маркеры ХА, ВПР, отклонения в биохимических показателях, поэтому пренатальная консультация генетика не проводилась. В 79,7±1,1% случаев имелись пренатальные маркеры ХА. Среди всех пренатальных факторов риска у 23,6±1,5% женщин присутствовали эхографические маркеры хромосомной патологии плода при первом и втором УЗ-cкринингах, у 21,8±1,5% — ВПР и у 40,0±1,7% — отклонения в биохимических маркерах I или II триместра, при этом в 14,5±1,3% случаев имелось сочетание эхо- и биохимических маркеров.
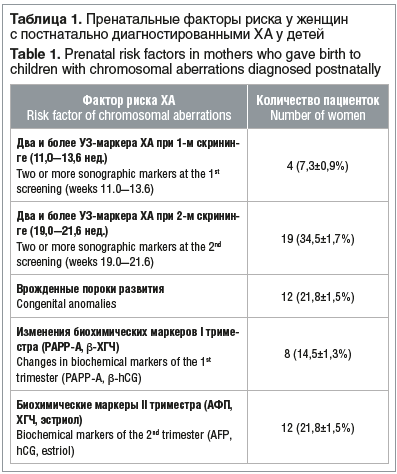
Среди обследованных женщин у каждой третьей (34,5%) при втором УЗ-скрининге (19,0–21,6 нед.) выявлялись два и более эхографических маркеров хромосомной патологии плода, такие как гипоплазия костей носа, вентрикуломегалия, пиелоэктазия, гиперэхогенный фокус в левом желудочке сердца, единственная артерия пуповины и др. ВПР, выявленные антенатально, наиболее часто ассоциированные с хромосомной патологией плода, также являлись показанием к проведению инвазивных методов обследования у 21,8% женщин В отличие от эхомаркеров II триместра изолированные эхографические маркеры I триместра имели меньшую прогностическую значимость и обнаруживались у 7,3% женщин. Биохимические маркеры I триместра показали свою чувствительность у 14,5% женщин, маркеры II триместра были изменены в 21,8% случаев (табл. 1).
Автоматизированная оценка риска хромосомной патологии плода показала, что высокий индивидуальный риск (Astraia, PRISCA) имели 43,5±1,4% женщин, средний риск — 18,8±1,1%, ВПР (наиболее часто ассоциированные с ХА) — 17,4±1,1%, следовательно, все эти пациентки нуждались в проведении пренатальной инвазивной диагностики, за исключением 20,3±1,1% женщин, у которых отсутствовали эхо- и биохимические маркеры ХА.
Необходимо отметить, что из всех женщин у каждой пятой (20,3±1,1%) был пропущен ранний пренатальный скрининг в связи с поздней явкой в женскую консультацию Ретроспективный анализ медицинской документации показал, что по результатам медико-генетического консультирования каждой второй беременной (38–55,1±1,4%) рекомендовано проведение инвазивной пренатальной диагностики с целью пренатального кариотипирования Все пациентки отказались от инвазивных манипуляций и оформили информированный отказ. Восьми (14,5%) беременным в связи с выявленными ВПР предлагалось прерывание беременности по медицинским показаниям со стороны плода, но от них также получен информированный отказ.
Обсуждение
Проведение массового раннего пренатального скрининга в 11,0–13,6 нед с использованием автоматизированного расчета индивидуального риска ХА с помощью программного модуля Фонда медицины плода показывает очень хорошие результаты и позволяет выявить женщин с высоким и средним риском хромосомной патологии плода, с последующим дообследованием и уточнением диагноза с помощью инвазивных методов [5]. В настоящее время всеобщие усилия врачей — генетиков, акушеров-гинекологов, врачей функциональной диагностики направлены на как можно более полное выявление плодов с ХА в 11,0–13,6 нед., в среднем этот показатель сейчас составляет 72,1% с некоторыми различиями на региональном уровне [6]. В то же время в нашей стране для оценки пренатального риска ХА у плода в основном используются эхографические и биохимические маркеры II триместра [6, 7]. В нашем исследовании, проведенном ретроспективно, уже по факту постнатально диагностированных ХА, установлено, что у каждой пятой женщины отсутствовали эхо- и биохимические маркеры ХА I и II триместров, у 20,3% женщин не проведен ранний пренатальный скрининг из-за поздней явки. В этой связи можно утверждать, что наибольшей эффективностью в группе с постнатально выявленными хромосомными синдромами у детей обладают маркеры II триместра, как эхографические, так и биохимические. Каждой второй женщине (55,1%) предлагалась инвазивная пренатальная диагностика для исследования кариотипа плода, но пациентки категорически отказались Полученные нами в ходе практической работы и настоящего исследования данные о причинах отказа от обследования согласуются с выводами других авторов Основной причиной отказа является страх осложнений инвазивной процедуры, некоторые пациентки не могли объяснить причины отказа или высказывали решимость родить ребенка, несмотря на риск. При этом нами, как и другими авторами [8], была четко установлена зависимость решения женщин от определенных установок врача-генетика, проводящего консультирование Коммуникация врача и пациентки при консультировании по поводу высокого риска ХА у плода требует определенной формы представления информации, в зависимости от социальных, моральных, религиозных установок конкретных женщин, при сохранении определенной нейтральности врача [8].
Перспективным неинвазивным методом более точного определения пренатального риска ХА в государственных учреждениях медико-генетического консультирования является неинвазивный пренатальный тест, который позволяет уменьшить количество инвазивных процедур и повысить эффективность пренатальной диагностики хромосомной патологии
Заключение
Соблюдение срока проведения оценки пренатального развития плода с использованием автоматизированного расчета индивидуального риска хромосомной патологии позволяет своевременно выявить группу высокого риска и провести необходимые диагностические мероприятия для уточнения диагноза и дальнейшей тактики ведения пациентки Ретроспективный анализ пренатальных факторов риска у детей с постнатально выявленной хромосомной патологией показал важность и необходимость своевременной дополнительной оценки эхографических и биохимических маркеров II триместра, недирективность медико-генетического консультирования Четкое соблюдение технологии антенатального обследования позволит своевременно установить диагноз, предоставляя семье право решать вопрос о целесообразности пролонгирования беременности
Сведения об авторах:
Дударева Юлия Алексеевна — д.м.н., доцент, профессор кафедры акушерства и гинекологии с курсом ДПО ФГБОУ ВО АГМУ Минздрава России; 656038, Россия, г. Барнаул, ул. Ленина, д. 40; ORCID iD 0000-0002-9233-7545.
Шипилов Александр Александрович — врач-генетик отделения лучевой и функциональной диагностики (пренатальной диагностики) КГБУЗ «АККПЦ»; 656045, Россия, г. Барна-
ул, ул. Фомина, д. 154; ORCID iD 0000-0001-8614-1725.
Контактная информация: Дударева Юлия Алексеевна, e-mail: iuliadudareva@yandex.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует Статья поступила 07.10.2020, поступила после рецензирования 30.10.2020, принята в печать 24.11.2020.
About the authors:
Yuliya A. Dudareva — Doct. of Sci. (Med.), Associate Professor, professor of the Department of Ophthalmology with the Course of the Additional Professional Education, Altay State Medical University; 40, Lenin str., Barnaul, 656038, Russian Federation; ORCID iD 0000-0002-9233-7545.
Aleksandr A. Shipilov — geneticist of the Department of Radiological & Functional Diagnostics, Altay Regional Clinical Perinatal Center; 154, Fomin str., Barnaul, 656045, Russian Federation; ORCID iD 0000-0001-8614-1725.
Contact information: Yuliya A. Dudareva, e-mail: iuliadudareva@yandex.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 07.10.2020, revised 30.10.2020, accepted 24.11.2020.
.
Информация с rmj.ru






